Unidades de concentracin Unidad 1 soluciones Objetivo de

Unidades de concentración Unidad 1 soluciones

Objetivo de la clase Aprender el cálculo en unidades de concentración químicas de una disolución

Concentración se define como la relación que existe entre la cantidad de soluto y la cantidad del disolvente en una disolución. Concentración La concentración de una disolución se puede determinar mediante distintos cálculos. 1. - Soluciones porcentuales (que requieren el peso molecular del soluto). a. Porciento peso/peso. b. Porciento volumen/volumen c. Porciento peso/volumen. 2. Molaridad 3. Molalidad 4. Fraccion molar
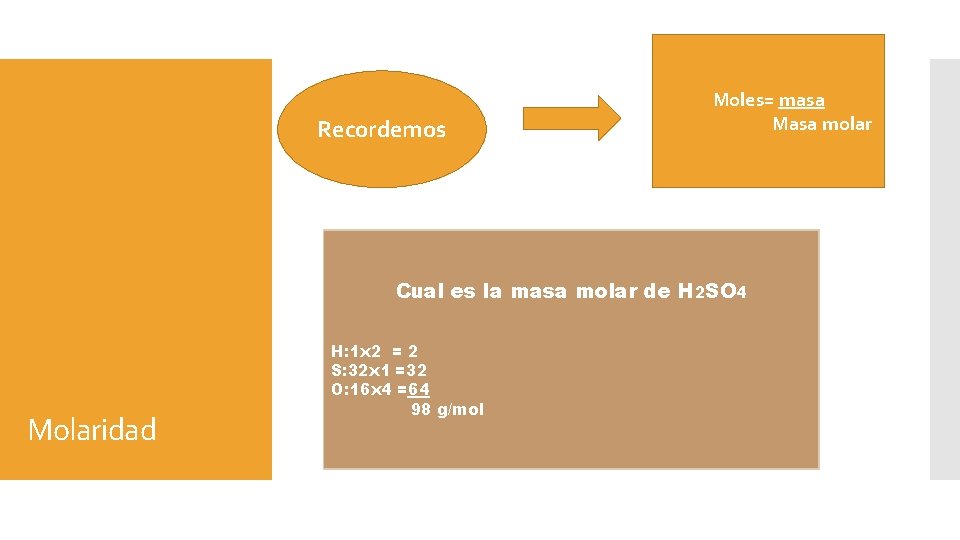
Recordemos Moles= masa Masa molar Cual es la masa molar de H 2 SO 4 Molaridad H: 1 x 2 = 2 S: 32 x 1 =32 O: 16 x 4 =64 98 g/mol
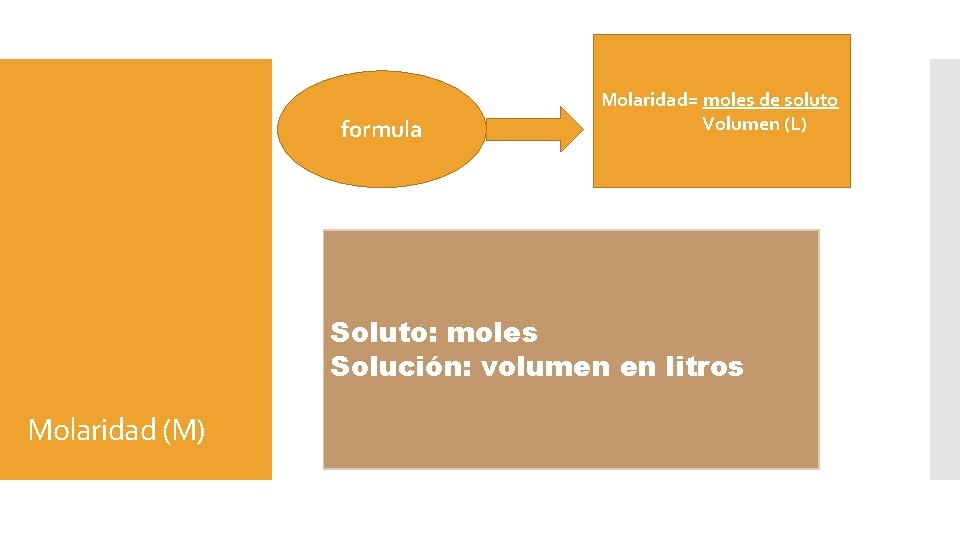
formula Molaridad= moles de soluto Volumen (L) Soluto: moles Solución: volumen en litros Molaridad (M)

Calcular la molaridad de una solución que contiene 33 gr de azúcar en 500 m. L de solución. (MM: 180 g/mol) Molaridad n=33 gr = 0, 18 moles de azúcar 180 g/mol D =M V M= n V M= 0, 18= 0, 36 M 0, 5 moles= masa Masa molar 1000 ml = 1 L 500 m. L = x X= 0, 5 L
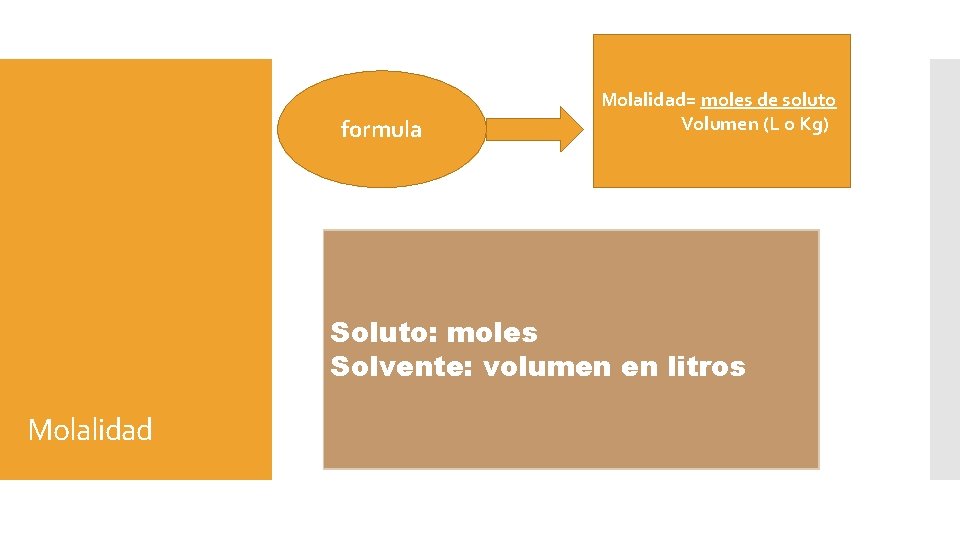
formula Molalidad= moles de soluto Volumen (L o Kg) Soluto: moles Solvente: volumen en litros Molalidad

Calcular la molaridad (M) y la molalidad (m) de una solución que contiene 33 gr de Na. Cl con 350 gr de agua. (densidad solución resultante: 1, 06 gr/m. L) Masa molar Na. Cl= 58, 5 g/mol Ejercitemos n= 33 gr = 0, 56 moles de sal 58, 5 g/mol Molalidad = 0, 56 = 1, 6 m 0, 35 Molalidad= moles de soluto Volumen (L o Kg) 1 kg > 1000 gr x Kg > 350 gr X= 0, 35 Kg
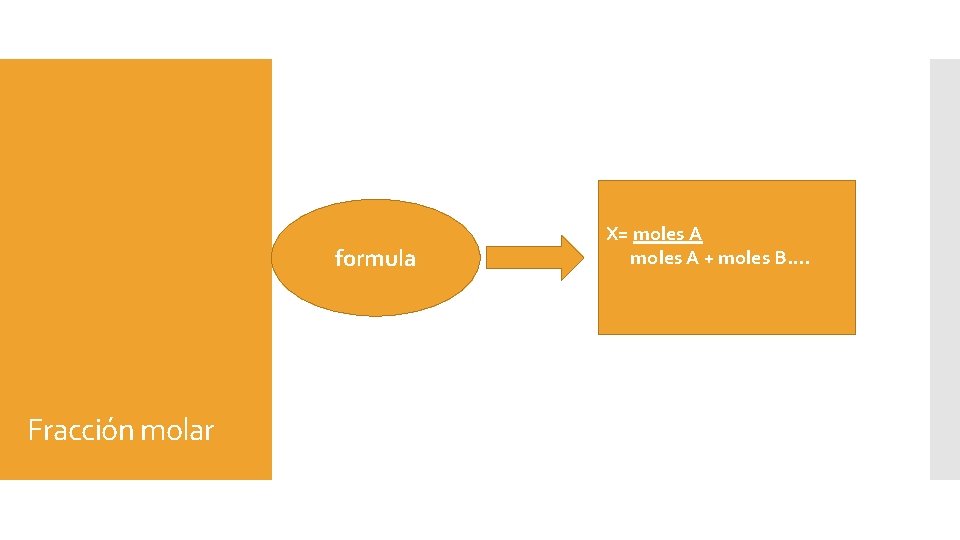
formula Fracción molar X= moles A + moles B….

Calcular la fracción molar de cloro de una mezcla de gases. Compuesto por 3 moles de cloro, 4 moles de oxigeno y 3 moles de nitrógeno. Ejercitemos Moles de cloro: Moles de oxigeno: Moles de nitrógeno: 3 moles 4 moles 3 moles Moles totales : 10 moles X cloro = 3 moles = 0, 33 10 moles X oxigeno= 4 moles = 0, 4 10 moles X= moles A + moles B….

Fin Recuerde que la practica hace al maestro
- Slides: 11