PESTICIDAS INTOXICACIONES POR PLAGUICIDAS INSECTICIDAS HERBICIDAS Y RODENTICIDAS

PESTICIDAS: INTOXICACIONES POR PLAGUICIDAS INSECTICIDAS, HERBICIDAS Y RODENTICIDAS. 2015 -16 ¤ PLAGUICIDAS (FAO): sustancia o mezcla de sustancias destinadas a prevenir, destruir o controlar cualquier plaga, incluyendo vectores de enfermedad humana o animal, especies indeseadas de plantas o animales capaces de causar daños DRA IGLESIAS LEPINE
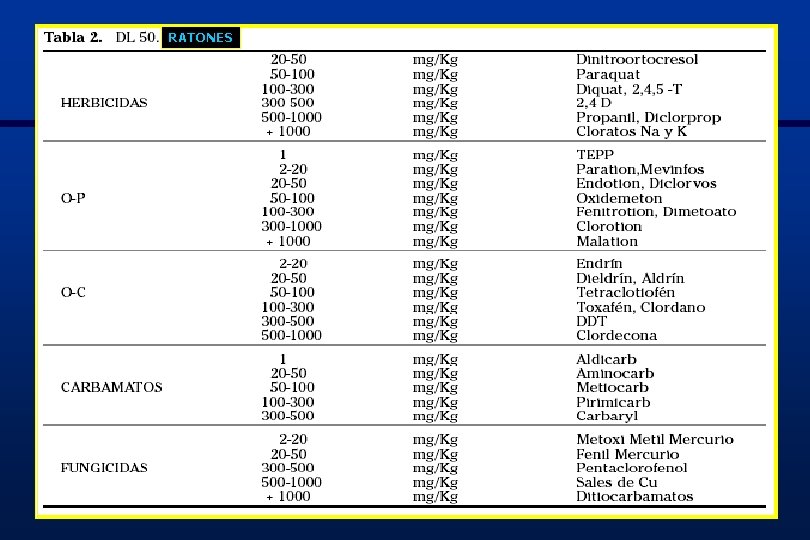
RATONES 2

COLOMBIA INSECTICIDAS: ORGANOFOSFORADOS (OF) Y CARBATOS ¤ Generalidades - Son las intoxicaciones más graves en toxicología - España: frecuentes zonas agrícolas de Almería, Levante, Islas Canarias y Baleares - Centros turísticos: cuidados de jardines de casas particulares (fácil accesibilidad). Ej. : Pollença - Sustancias muy liposolubles se absorben a través tracto GI, piel, mucosas y vía respiratoria se acumulan tejido adiposo, hígado, riñones, músculo y glándulas salivares - Tentativa autolítica o accidental, Ej. : perejil fumigado o ingesta de producto en envase inadecuado 3

NO SI SI

¤ Productos (España): formulación: polvo, granulado, aerosol o líquido - OF (compuestos derivados del ácido fosfórico): metamidofos, clorpirifos, carbofenotion, clorfenvinfos, disulfotón, fonofos, fosfamidón, mecarbam, metilparatión, etión, metidatión, triclorfón, malatión, ometoato, temefos, etc. - Carbamatos: aldicarb, baygon, bendiocarb, carbarilo, carbofurano, metiocarb, metomilo (Lannate®), oxamilo, promecarb y prosopur ¤ Clasificación según su inhibición sobre la ACh. E - Inhibidores directos: no necesitan activación para inhibir ACh. E - Inhibidores indirectos: necesitan activación metabólica para ejercer su acción. Ej. : paration se desulfura oxidativamente a paraoxon, que es el compuesto activo que se une ACh. E

¤ Fisiopatología 1. - Fosforilación de esterasas SN: inhibición acetilcolinesterasa (ACh. E) acumulación acetilcolina en la sinapsis cuando 50% actividad habitual ACh. E aparecen los síntomas ▪ Carbamatos: rápida reversión de unión tóxico-enzima en < 6 h ▪ Organofosforados: unión tóxico-enzima es irreversible Clasificación IOF según Repetto (1995) ▪ IOF Tipo I: inhibición ACh. E de forma reversible. La intoxicación se supera con facilidad ▪ IOF Tipo II: inhibición ACh. E más persistente. Los síntomas revierten con tratamiento. La actividad enzimática se restaura semanas/meses ▪ IOF Tipo III: exposición crónica inhibición ligeramente superior a la capacidad diaria de regeneración de la enzima lenta actividad ACh. E antes de manifestarse la intoxicación 2. - Acción tóxica directa sobre distintos parénquimas: crisis colinérgicas

¤ Clínica 1. - Carbamatos: solo provocan síntomas muscarínicos y nicotínicos periféricos pero no afectan SNC y no producen neurotoxicidad retardada 2. - OF: 8 -12 h triple cuadro clínico colinérgico y neurotoxicidad retardada ▪ Sintomatología leve: solo clínica muscarínica ▪ Sintomatología moderada/grave: clínica nicotínica y central predomina sobre la clínica muscarínica A. - Síndrome muscarínico (músculo liso y glándulas): miosis, visión borrosa, “SLUDGE” (salivación, lagrimeo, “urination”, diarrea, GI motilidad y emésis), “BBB” (bradicardia, broncorrea y broncoespasmo) hipotermia, hipotensión y shock B. - Síndrome nicotínico x estimulación neuromuscular: fasciculaciones musculares, calambres, debilidad sobre todo de extremidades inferiores, temblores, mialgias, taquicardia e HTA

C. - Síndrome neurológico ▪ Fase inicial estimulación: ansiedad, insomnio, pesadillas, confusión, neurosis e inestabilidad emocional ▪ Fase 2ª de depresión del SNC: convulsiones y coma D. - Síndrome intermedio: entre 1 -4 días deterioro pre y postsináptico de la transmisión neuromuscular debilidad y parálisis músculos proximales miembros y flexores del cuello, nervios craneales y músculos respiratorios E. - Complicaciones IOF ● Respiratorias: insuficiencia respiratoria x debilidad muscular neumonía. Muerte: fallo respiratorio x obstrucción respiratoria x secreciones bronquiales y broncoconstricción, parálisis musculatura respiratoria y depresión centro respiratorio ● Cardiológicas: inhibición bomba Na-K-ATPasa bradiarritmia sinusal, bloqueo AV completo y extrasístoles ventriculares ● Neurológicas: ataxia, parálisis flácida EEII y cuerdas vocales, AVC, etc.

● Alteraciones neuropsicológicas y neuroconductuales crónicas ● Hepatonecrosis, pancreatitis necrótica-hemorrágica aguda y diabetes insípida central F. - Debilidad muscular IOF ▪ Fase colinérgica: acetilcolina acumulada estimula receptores nicotínicos fasciculaciones musculares. La activación repetida desensibilización y bloqueo receptores neuromusculares debilidad muscular y parálisis. Recuperación según dosis y toxicocinética del producto en 48 h ▪ Segunda fase: entrada excesiva iones Ca en la célula muscular activación enzimas calcio-dependientes necrosis celular reversión en > 4 semanas

▪ Hacia 2ª-3ª semana (8 -21 días): puede aparecer neuropatía retardada desmielinizante (síndrome OPIDP) axonopatía distal sensitivo-motora calambres agudos, adormecimiento y debilidad EEII Dos teorías: Jonson (1982), por inhibición de una enzima axonal conocida como NTE (neurotóxicoesterasa). Abou-Donia y Lapadula (1990), producen fosforilación del citoesqueleto neuronal ¤ Diagnóstico a. - Fuerte olor a plaguicidas en la ropa de trabajo b. - Determinaciones seriadas de colinesterasa plasmática (N: 3500 -8000 U/l) o de colinesterasa en hematíes (N: 26 -43 U/g de Hb) c. - Estudio neurofisiológico extremidades inferiores (axonopatía distal) después del accidente y a las 2 semanas de la intoxicación
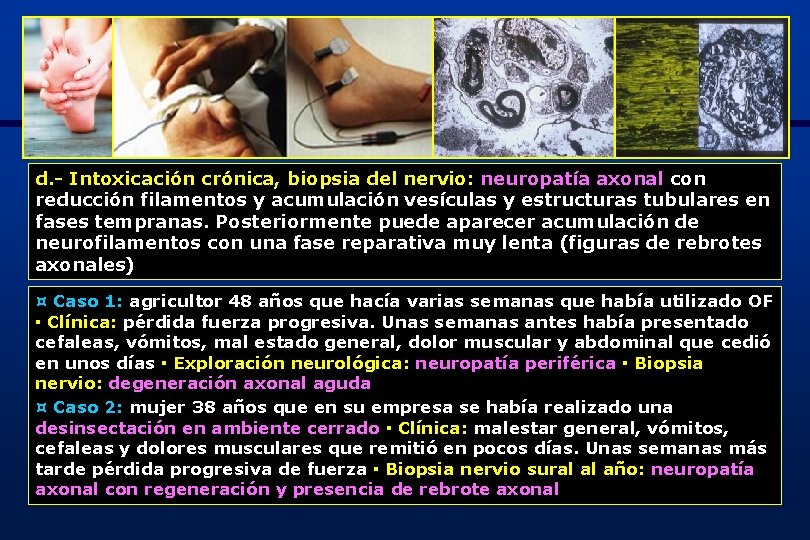
d. - Intoxicación crónica, biopsia del nervio: neuropatía axonal con reducción filamentos y acumulación vesículas y estructuras tubulares en fases tempranas. Posteriormente puede aparecer acumulación de neurofilamentos con una fase reparativa muy lenta (figuras de rebrotes axonales) ¤ Caso 1: agricultor 48 años que hacía varias semanas que había utilizado OF ▪ Clínica: pérdida fuerza progresiva. Unas semanas antes había presentado cefaleas, vómitos, mal estado general, dolor muscular y abdominal que cedió en unos días ▪ Exploración neurológica: neuropatía periférica ▪ Biopsia nervio: degeneración axonal aguda ¤ Caso 2: mujer 38 años que en su empresa se había realizado una desinsectación en ambiente cerrado ▪ Clínica: malestar general, vómitos, cefaleas y dolores musculares que remitió en pocos días. Unas semanas más tarde pérdida progresiva de fuerza ▪ Biopsia nervio sural al año: neuropatía axonal con regeneración y presencia de rebrote axonal

¤ Tratamiento: personal sanitario protegido a. - Absorción cutánea-inhalatoria: retirar ropa y lavado con alcohol etílico seguido de cantidades copiosas de agua y jabón graso alcalino b. - Toxicidad ocular: lavar con abundante agua limpia o SF durante 15 min e instilación local atropina/escopolamina oftalmólogo c. - Si ingesta VO: descontaminación digestiva con aspirado y lavado gástrico si < 60 min y administración carbón activo (25 g) si < 120 min d. - Contraindicada emesis por riesgo de convulsiones e. - Diuresis forzada alcalina: favorece hidrólisis de plaguicidas y eliminación de atropina f. - Medidas específicas ▪ Protección receptores de acetilcolina: ATROPINA: antídoto específico para IOF y carbamatos inhibidor competitivo acetilcolina receptores muscarínicos neutraliza sintomatología muscarínica 1. - Dosis de prueba: 1 mg EV atropina (ancianos, 0, 5 mg)

2. - Si a los 10 min aparecen signos atropinización (midriasis, FC > 120 lpm, piel seca y/o rojiza, fiebre e íleo) intoxicación leve y STOP 3. - Si no aparecen signos atropinización dosis repetidas hasta la desaparición hipersecreción pulmonar: 0, 02 -0, 04 mg/kg EV c/5 -10 min 4. - Perfusión continua 0, 08 mg/kg/h si fuera preciso durante 24 -48 h para mantener una FC: 80 -100 lpm ▪ Reactivación ACh. E inhibida: después de la atropinización en intoxicación moderada o grave OXIMAS: antídoto exclusivo IOF. El tiempo es crítico: la fosforilación ACh. E sólo es reversible en < 12 h y solo neutraliza síntomas nicotínicos (fasciculaciones y debilidad muscular) PRALIDOXIMA: 2 g en 30 min e infusión continúa 1 g en 1 h c/h durante 48 h o 15 -30 mg/Kg (1 -2 g) hasta 3 dosis seguidas en 15 -30 min cada una y seguir con 0, 5 g/h sin exceder 4 g/día -Infusión continua frente a bolus periódicos: IOT, duración soporte ventilatorio, neumonías, atropina en las 1ª 24 h y mortalidad Kristi L Koenig et al. Continuous pralidoxime infusion versus repeated bolus infection to treat organophosphorus pesticide poisoning: A randomized controlled trial. Lancet 2006; 368: 2136 -41 OBIDOXIMA: 250 mg EV lento y repetir 3 -4 h. Dosis máx. : 5 mg/kg - Efectos 2º oximas: dosis moderadas (sedación, alteraciones visuales, FC, náuseas e hiperventilación) y elevadas [bloqueo neuromuscular transitorio, TA y hepatotoxicidad (obidoxima)]

Pralidoxima presenta efectos 2ª más acentuados que obidoxima ▪ Protección del SNC: DIAZEPAM, dosis 5 -10 mg EV g. - Evitar el empleo fisostigmina, succinilcolina (para IOT) y opiáceos porque deprimen SNC h. - Broncoespasmo o broncorrea continúa: nebulización con atropina y bromuro de ipratropio

INSECTICIDAS PIRETROIDES ¤ Generalidades - Piretrinas: insecticidas origen natural obtenidos flor del crisantemo, inestable a luz y calor - Piretroides: insecticidas sintéticos, estructura química similar piretrinas, modificadas para mejorar su estabilidad en el ambiente - Los productos comerciales utilizan derivados petróleo como disolventes y algunos contienen compuestos organofosforados o cabarmatos NOMBRE GENÉRICO NOMBRE COMERCIAL Fenvalerato Belmark, Pydrin, Tribute Permetrina Ambush, Piretox, Pounce, Talcord Deltrametrina Decis, K-Ortine, K-Obicol 15

- Se usan en el terreno agrícola y doméstico (carcoma muebles, disoluciones antimosquitos enchufe o pulverizadores) - Se absorben bien tracto GI, respiratorio y a través piel intacta es relativamente baja su absorción - Su concentración es baja difícil alcanzar dosis tóxica humana Dosis letal estimada en humanos: 1 g/kg ¤ Clasificación - Tipo I (carecen grupo alfa-ciano): aletrina, permetrina, tetrametrina, cismetrina y d-fenotrina - Tipo II (contienen grupo alfa-ciano): cipermetrina, deltametrina, fenvalerato y fenpropatrin ¤ Fisiopatología: enlentecimiento del cierre canal del sodio en la membrana celular fallo repolarización células nerviosas ¤ Clínica - Irritantes locales: hormigueo en párpados y labios. Prurito conjuntival y estornudos - Mareos, cefaleas, anorexia y fatiga - Irritantes pulmonares: broncoespasmo - Dosis altas: convulsiones y coma, SDRA

USO DE ROTENONA Y PARAQUAT PODRÍA RIESGO PADECER PARKINSON, SEGÚN EL INSTITUTO NACIONAL CIENCIAS DE SALUD Y MEDIO AMBIENTE EEUU INSECTICIDA ACARICIDA PIRETRINA + ROTENONA INSECTICIDA ROTENONA ¤ Generalidades - Obtenido raíces de diversas especies plantas familia de las leguminosas (C 23 H 2206) - Su actividad biológica llega a durar una semana - Se puede obtener como insecticida doméstico de venta libre ¤ Fisiopatología: toxicidad mitocondrial x inhibición de la NADPH deshidrogenasa mitocondrial ¤ Curso clínico: shock con acidosis metabólica severa muerte por fracaso multiorgánico ¤ Tratamiento: ningún antídoto. Experimentación: N-acetilcisteína 17

PARAQUAT GRAMOXONE 20 -40% HERBICIDAS BIPIRIDÍLICOS: PARAQUAT Y DIQUAT ¤ Productos: Gramoxone y Dextrone X® (paraquat 20%), Gramoxone plus y Weedol® (paraquat 2, 5% y diquat), Reglone (diquat) ¤ Generalidades: herbicidas no selectivos que se utilizan para todo tipo de vegetación - Derivados bipiridílicos dicatiónicos en forma de sales (cloruro/bromuro) - Tentativa autolítica o accidental - En España, los preparados comerciales llevan un emético ¤ Toxicocinética ▪ Vías absorción: tópica tras contacto prolongado con piel y VO alcanza niveles plasmáticos máx. 2 h y se distribuye rápidamente en tejidos

▪ Distribución y eliminación Paraquat: se distribuye en pulmón donde se absorbe x neumocitos I y II, riñón, hígado y músculo. Semivida eliminación: 12 h (IRA: 120 h) y 90% dosis se elimina sin intercambiar - Dosis tóxica humanos: 10 -20 mg/kg y mortal 20 -40 mg/kg - DL 50 humanos: 3 -5 mg/kg, lo que se traduce 10 -15 m. L 20% Diquat: se distribuye en riñón y menor concentración en vesícula, hígado y músculo pero no se absorbe x neumocitos I y II del pulmón. Se elimina por vía renal y GI ”Cualquier exposición VO debe ser considerada peligrosa. La ausencia inicial de síntomas no excluye el diagnóstico” ¤ Fisiopatología: paraquat/diquat es reducido en el ciclo oxidaciónreducción a un radical monocatiónico libre por un electrón que cede el NADPH en presencia citocromo P 450 reductasa. El radical libre es reoxidado por acción del O 2 molecular originando un anión superóxido libre anión superóxido en los tejidos agotamiento del NADPH muerte celular DIQUAT PARAQUAT 19

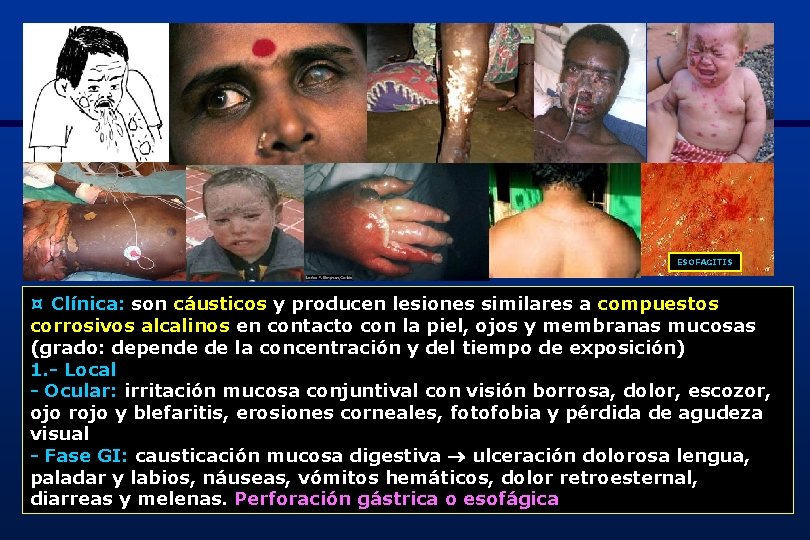
ESOFAGITIS ¤ Clínica: son cáusticos y producen lesiones similares a compuestos corrosivos alcalinos en contacto con la piel, ojos y membranas mucosas (grado: depende de la concentración y del tiempo de exposición) 1. - Local - Ocular: irritación mucosa conjuntival con visión borrosa, dolor, escozor, ojo rojo y blefaritis, erosiones corneales, fotofobia y pérdida de agudeza visual - Fase GI: causticación mucosa digestiva ulceración dolorosa lengua, paladar y labios, náuseas, vómitos hemáticos, dolor retroesternal, diarreas y melenas. Perforación gástrica o esofágica 21

PARAQUAT Y DIQUAT ESTÓMAGO: NECROSIS ESOFAGO: NECROSIS 2. - Sistémicos ▪ Fase hepatorrenal (2º y 5º día) - Necrosis centrolobulillar hepática, con destrucción células epiteliales de los conductos biliares (ictericia y transaminasas) - Necrosis tubular proximal y degeneración asa de Henle (IRA) - Miocarditis, hemorragia cerebral (crisis parciales/totales) y suprarrenal - En esta fase se puede producirse la muerte 22
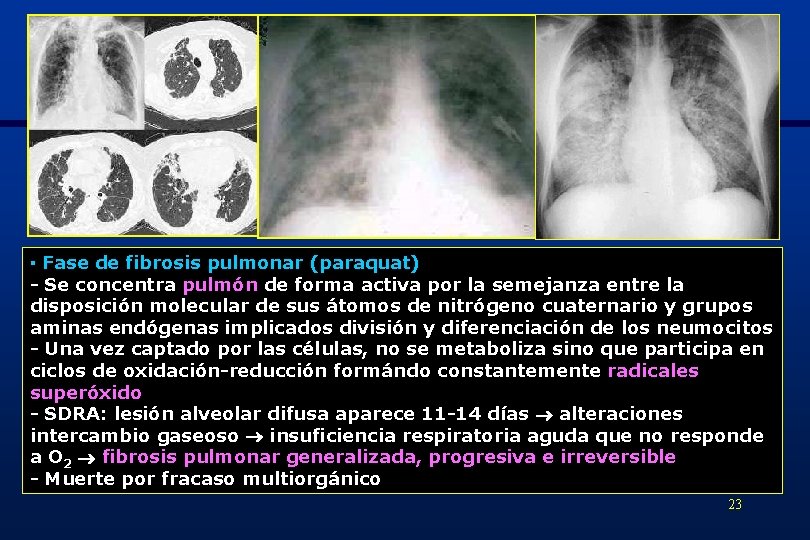
▪ Fase de fibrosis pulmonar (paraquat) - Se concentra pulmón de forma activa por la semejanza entre la disposición molecular de sus átomos de nitrógeno cuaternario y grupos aminas endógenas implicados división y diferenciación de los neumocitos - Una vez captado por las células, no se metaboliza sino que participa en ciclos de oxidación-reducción formándo constantemente radicales superóxido - SDRA: lesión alveolar difusa aparece 11 -14 días alteraciones intercambio gaseoso insuficiencia respiratoria aguda que no responde a O 2 fibrosis pulmonar generalizada, progresiva e irreversible - Muerte por fracaso multiorgánico 23

¤ Diagnóstico - No esperar la confirmación para iniciar el tratamiento - Confirmación cualitativa en orina o aspirado gástrico - Estimación cuantitativa en plasma NO 24

¤ Tratamiento local a. - Piel: quitar toda la ropa, lavar piel y cabello con agua abundante y jabón durante 10 min, dejando que el agua arrastre el producto y frotando suavemente b. - Ocular: lavar con abundante agua limpia/SF durante 15 min y añadir un colirio con corticoides y antibiótico oftalmólogo ¤ Si ingesta VO a. - Rescate material tóxico con aspirado y lavado gástrico (ingesta < 60 min). Pensar en la posibilidad de perforación gástrica por efecto cáustico b. - Descontaminación con carbón activo (< 120 min de la ingesta) c. - Soporte diurético d. - Acúmulo selectivo paraquat en tejido pulmonar es un proceso dependiente de energía daños semejos a los producidos x toxicidad del O 2 a elevadas concentraciones al producir radicales superóxidos O 2 solo el preciso. Realizar precozmente VMNI-BIPAP o VMET con PEEP e. - Si fallo renal agudo: hemodiálisis temprana o hemoperfusión con cartuchos carbón activo < 6 h ingestión paraquat buenos resultados 25

1. - RODENTICIDAS ¤ Generalidades - Conjunto de sustancias utilizadas para combatir y exterminar a roedores por lo que por extensión se añaden a los raticidas - Poco frecuentes: accidentales en niños y tentativas autolíticas adultos ¤ Clasificación ● Rodenticidas inorgánicos - Sales de talio (actualmente prohibidas en España) - Fósforo (Nogat®, Ibys), fosfuro de zinc y fosfuro de aluminio (Phostoxin®, Bhostoxin®, Celphos®, Quickphos®, Phosphume®, Phostek®) - Fluoroacetatos - Fluoruro de sodio ● Rodenticidas orgánicos - Cumarina (Racumin®, Bayer), dicumarol (Ratisin®, Camons) - Derivados de la urea: PNU (N-Piridinmetil-N´-p-nitofenilurea) y ANTU ( -Naftiltiourea) - Estricnina ● Otros rodenticidas: 0, 025 -0, 05% en las formulaciones comerciales - Warfarina (Raticida Ibys®) - Superwarfarinas [4 - hidroxicumarinas: brodifacoum (Klerat®, Zeneca) con t 1/2 de semanas a meses, difenacoum (Ratak®, ICI-Zeltia), bromadiolona y cumatetralito] y [indandionas: difacinona, clorofacinona (t 1/2 de 6 -23 días) y pindona] - Alfacloralosa (acción sedativa), carbonato de bario y scilirosida 26

TERRORISMO: "CORTINAS DE HUMO" 1. 1. - FOSFORO BLANCO ¤ Generalidades: es corrosivo efecto cáustico ¤ Fisiopatología: inhibe oxidación celular interfiriendo en la fase anaerobia respiración celular degeneración grasa citolisis en hígado, miocardio, riñón y músculo esquelético. Vasos sanguíneos degeneración de túnica muscular o media disminuye resistencia roturas vasculares: diátesis hemorrágica y hemorragias ¤ Clínica tópica o VO - GI: quemaduras, vómitos (fosforescentes y olor a ajo), diarreas y dolor abdominal, HDA y HDB - Arritmias o adinamia, insuficiencia hepato-renal aparece a la semana exposición (causa de muerte) y endocrino: hipo/hiperfosfatemia e hipocalcemia ¤ Diagnóstico: analítica completa (Ca y Mg), Rx tórax y ECG (monitorización) ¤ Tratamiento: aspirado y lavado gástrico con permanganato potásico 1: 5. 000/10. 000 o peróxido de hidrógeno (agua oxigenada 2%), seguido de lavado con bicarbonato sódico oxida fósforo dando lugar varios óxidos menos tóxicos Aunque tiene poca afinidad: carbón activo si < 120 min de ingesta y la emésis está contraindicada x efecto cáustico del fósforo 27

28

29

2. - FOSFURO DE ALUMINIO (FA) ¤ Generalidades - Pesticida sólido usado contra roedores e insectos para preservación del grano en espacios cerrados. Altamente tóxico y bajo coste - Más frecuente población rural. En Irán se utiliza con fines suicidas y en Inglaterra entre 1997 -2003, 93 casos la mayoría accidentales - Tabletas y comprimidos 0, 6, 1, 2 y 3 g (sobres 3 tabletas, tubo de 8 y 30 tabletas y frascos de 500 tabletas) o en forma de pasta 1 pastilla: 56% fosfuro aluminio. De color verde, gris o amarillo - DL 50: 70 Kg = 20 mg/Kg. Mortalidad: 37 -100% ▪ Productos: Gastoxin®, Phostek®, Gastion®, Tekphos®, Phosfino®, Fumigas®, Acostoxin®, Phostoxin®, Celfos®, Destia Gas® y Delicia® 30

¤ Fisiopatología - Principal vía de entrada: VO. Principal vía de absorción: vía respiratoria - Fosfuro zinc solo libera gas fosfina (PH 3) si contacta ácido o humedad - Ingestión VO: formación fosfina gaseosa INH respiratoria + absorción hepática. En contacto con piel intacta no se absorbe - Mecanismo: fosfina hidrolizada se une endotelios estimulando formación radicales libres degradación lípidos membrana celular alteración permeabilidad membrana con introducción Ca al interior célula y a nivel mitocondrial estimula formación citocromo-oxidasa inhibiendo respiración celular 31

- Eliminación: respiratoria (90%), 3 r-5º día y renal-digestiva (10%) ¤ Clínica - GI: vómitos (halitosis olor pescado/ajo), náuseas, dolor abdominal, epigastralgia y diarreas. HDA y HDB - Endocrino: hipo/hiperglicemia - Cardiovascular: hipotensión, pericarditis y miocarditis tóxica shock cardiogénico éxitus 1 -48 h ▪ ECG: alteraciones ST y T, ritmo (bradi/taqui, FV y EV), conducción y IAM - Respiratorias (24 h): tos, disnea, cianosis SDRA (muerte al 4º día) - SNC (infrecuentes): cefalea, vértigo, irritabilidad, somnolencia, convulsiones, ataxia, parestesias y coma - Insuficiencia hepática ¤ Diagnóstico - Analítica: hemograma, función hepática, renal y GSA - Niveles aire espirado o líquidos biológicos x cromatografía - Rx tórax 32

¤ Tratamiento - Protección personal: aislamiento cutáneo y aéreo - Descontaminación cutánea reglada - Descontaminación digestiva ● Contraindicada emésis x efecto cáustico fósforo x posibilidad de producir fosfina ● Aspirado y lavado gástrico con disolución permanganato potásico 1: 5. 000 o peróxido hidrógeno (agua oxigenada 2%) + lavado bicarbonato sódico oxida fósforo dando lugar varios óxidos menos tóxicos ● Carbón activo si < 120 min desde ingesta (poca afinidad) - Hipotensión: resucitación precoz del shock - Acidosis láctica x bloqueo fosforilación oxidativa - Broncoespasmo: agonistas 2, corticoides y oxígeno - Convulsiones: BDZ - Pericarditis y miocarditis: hidrocortisona 500 mg c/4 -6 h - Propiedades antioxidantes: n-acetilcisteína 33

3. - RODENTICIDAS ANTICOAGULANTES ¤ Generalidades: España están registrados 416 formulados. Más usados son anticoagulantes ▪ Clasificación según su composición química - Derivados cumarínicos (87, 4%): brodifacoum, bromadiolona, cumatetralilo, difenacoum, difetialona, flocoumafen y warfarina - Derivados indandiónicos (12, 6%): difacinona y clorofacinona ▪ Clasificación según semivida eliminación - 1ª generación o corta duración. Ej. : warfarina - 2ª generación o larga duración. Ej. : bromadiolona ¤ Fisiopatología: inhibe vitamina-K-reductasa e impide activación de los factores coagulación x inhibición síntesis hepática de factores complejo protrombínico (II, VII, IX y X) cuya correcta síntesis se realiza en presencia de Vk 34
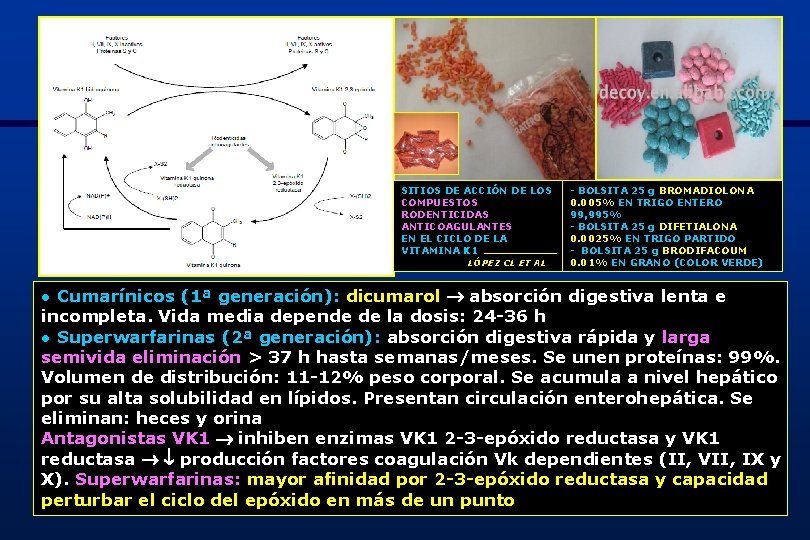
SITIOS DE ACCIÓN DE LOS COMPUESTOS RODENTICIDAS ANTICOAGULANTES EN EL CICLO DE LA VITAMINA K 1 LÓPEZ CL ET AL - BOLSITA 25 g BROMADIOLONA 0. 005% EN TRIGO ENTERO 99, 995% - BOLSITA 25 g DIFETIALONA 0. 0025% EN TRIGO PARTIDO - BOLSITA 25 g BRODIFACOUM 0. 01% EN GRANO (COLOR VERDE) ● Cumarínicos (1ª generación): dicumarol absorción digestiva lenta e incompleta. Vida media depende de la dosis: 24 -36 h ● Superwarfarinas (2ª generación): absorción digestiva rápida y larga semivida eliminación > 37 h hasta semanas/meses. Se unen proteínas: 99%. Volumen de distribución: 11 -12% peso corporal. Se acumula a nivel hepático por su alta solubilidad en lípidos. Presentan circulación enterohepática. Se eliminan: heces y orina Antagonistas VK 1 inhiben enzimas VK 1 2 -3 -epóxido reductasa y VK 1 reductasa producción factores coagulación Vk dependientes (II, VII, IX y X). Superwarfarinas: mayor afinidad por 2 -3 -epóxido reductasa y capacidad perturbar el ciclo del epóxido en más de un punto 35

● TÉCNICAS CROMATOGRÁFICAS han permitido identificar, cuantificar y describir modelos cinéticos superwarfarinas individualizar pauta de actuación en base a la variabilidad genética intrapoblacional ▪ Modelo cinético eliminación bromadiolona en sangre: bicompartimental, con fase inicial eliminación rápida (3, 5 días-plasma/6 días-sangre), seguida de fase terminal más lenta (10 -13 días-plasma/24 días-sangre) ▪ Modelo cinético eliminación brodifacoum en sangre: multicompartimental (20 -209 días). Si ingesta grande modelo cinético de 1 er orden (exponencial) modelo de orden cero (velocidad constante) ▪ Metabolización individual de cada producto marca pauta de actuación ▪ Valores 10 ng/m. L en plasma de bromadiolona y 4 -10 ng/m. L en suero del brodifacoum no precisa terapia con VK 1 36

¤ Clínica: coagulopatía 24 -72 h postingesta si la TP es < 20%: epistaxis, gingivorragias, hematuria, equimosis y petequias, hemoptisis, hemorragia vaginal, pulmonar, GI (brodifacoum no causa síntomas GI), epidural, adrenal, retroperitoneal y pericárdica. Gran parte de estas hemorragias debutan como dolor abdominal o lumbar ¤ Pauta de actuación a) Calcular dosis ingerida e interpretar si es tóxica para humanos - Brodifacoum: 0, 1 -0, 27 mg/Kg - Bromadiolona: 0, 17 mg/Kg - Difetialona: desconocida EEUU: test de screening de compuestos warfarínicos mediante técnicas cromatográficas (ratio VK 1 -2, 3 epóxido/K 1) b) Averiguar tiempo transcurrido desde última ingesta para prever las probables/posibles manifestaciones que aparecen 24 -48 h si la TP < 20% c) Se necesita ingesta importante para producir síntomas en humanos “solo se debe iniciar una actuación si la dosis es tóxica” d) Descontaminación digestiva: aspirado y lavado ( < 60 min) y carbón activo (< 120 min desde ingesta) 37
e) TP No presenta alteraciones significativas a las 48 h postingesta: no es necesario administrar VK 1 profiláctica 50 -80%: administrar 10 mg (1 ampolla) EV de VK 1 y control c/24 h Inicio acción: 1 -3 h (EV) y semivida eliminación: 8 -20 h. Tarda de 3 -5 h y retorna el 15 -25% TP ≤ 50% y el paciente sangra: administrar 3, 5 mg/kg/día c/6 h de VK 1 durante al menos 48 h EV f) Si riesgo vital: añadir complejo protrombínico y/o plasma fresco congelado g) Si el producto fuera brodifacoum: administrar fenobarbital (100 -180 mg/24 h) para metabolismo del producto (¿? ) h) Una vez estabilizado cuadro: administrar 10 mg VK 1 c/24 h VO durante semanas/meses (control TP semanal) 38

4. - ESTRICNINA ALEJANDRO MAGNO ¤ Generalidades - Alcaloide derivado semillas de la strychnos nux-vomica (nuez vómica) de la familia de las loganiáceas (Asia y Australia) - Polvo blanco, cristalino, inodoro y amargo que se absorbe rápidamente a través mucosas y tracto GI, INH, mezclado en solución o EV directo - Muy tóxico. Se han descrito muertes con dosis 16 mg en adulto, aunque cualquier dosis estricnina debe considerarse potencialmente mortal (1530 mg) - Utilizado para cebos para matar animales (Ej. : ratas) ¤ Fisiopatología: antagoniza competitivamente glicina, principal neurotransmisor inhibitorio de la médula espinal excitabilidad refleja médula espinal contracciones grupos musculares hasta el agotamiento 39

¤ Clínica - Aparece 15 -30 min postingesta y desaparecen 10 -24 h - Agitación, taquipnea (contractura musculatura respiratoria éxitus por insuficiencia respiratoria), bradicardia, HTA, mialgias, hiperreflexia, mioclonias y contracturas tetaniformes dolorosas (convulsiones tónicas y extensoras en paciente despierto, opistótonos y risa sardónica) que pueden durar 1 semana hipertermia, rabdomiolisis e insuficiencia renal ¤ Tratamiento ● Por contacto: retirar ropa contaminada con tijeras para evitar pasarla por cara; lavar piel con agua y jabón durante 15 min. Residuo tóxico ● Por VO: previo tto con BZD descontaminación digestiva (aspirado y lavado gástrico y carbón activo). Contraindicada la emesis por riesgo convulsiones. Minimizar al máximo estímulos externos - Convulsiones: BZD y agentes bloqueantes neuromusculares si procede (succinilcolina) - Alcalinizar la orina: riesgo asociado de rabdomiolisis 40

5. - TALIO DOSIS LETAL: 6 -8 mg/Kg 41
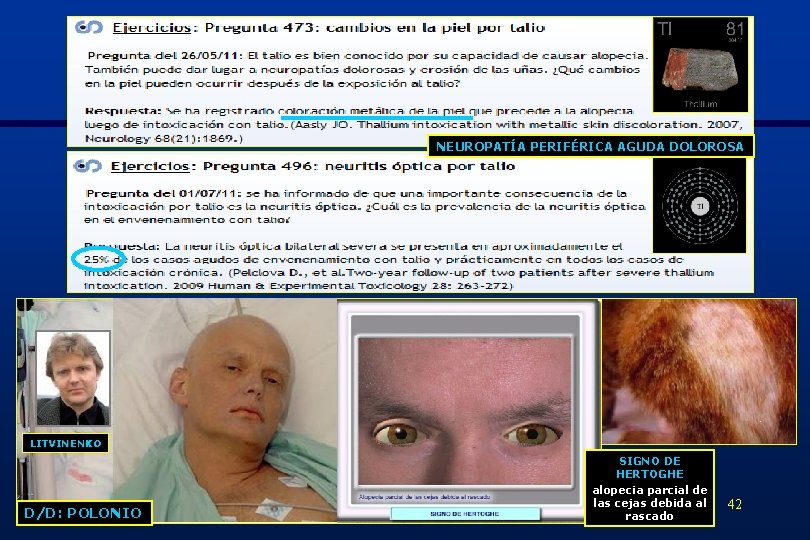
NEUROPATÍA PERIFÉRICA AGUDA DOLOROSA LITVINENKO D/D: POLONIO SIGNO DE HERTOGHE alopecia parcial de las cejas debida al rascado 42

Blau de Prússia (ferrocianur fèrric) Tal·li. Evidencia II - HEMODIÁLISIS INTERMITENTE/3 DÍAS VO: 10 g/8 h emulsionats en 50 m. L de mannitol al 20%, durant 10 dies. Medicació estrangera, difícil d’obtenir. Pot ésses substituït per carbó activat. Enfosqueix la femta. 43 Ghannoum M et al. Extracorporea treatment. Clin J Am Coc Nephrol 7: 1682 -90, October, 2012

BIBLIOGRAFÍA 1. - Symposium Internacional de Toxicología Clínica. Mojacar, 30 de Noviembre y 1 de Diciembre del 2000. 2. - Guía práctica: el tratamiento de la intoxicación por Paraquat. 1995, Zeneca Agro. 3. - Triguero de la Torre J et al. Intoxicación por herbicidas. En: Consejos de urgencia. Hospital Universitario "Virgen Macarena" de Sevilla. Roche Farma, 1999. 4. - Canto E. Intoxicación por paraquat. En: Sempere G et al. Manual de Diagnóstico y Tratamiento en Urgencias. Hospital Dr. Peset de Valencia. Barcelona, Sanofi-Winthrop, S. A. 5. - Barrios AM et al. Intoxicaciones. En: Acedo MS et al: Manual de Diagnóstico y Terapéutica Médica. Hospital 12 de Octubre. 4ª edición. MSD, 1998. 6. - Munné et al. Antídotos ¿cuando y como utilizarlos? . Edicomplet, 1996. 7. - Shannon BE et al. Intoxicaciones e ingestiones. En Jenkins JL y Loscalzo J. Manual de medicina de urgencia. Diagnóstico y tratamiento. Salvat, 1989. 8. - Dueñas A. Carbamatos (insecticidas). Paraquat y diquat. En: Dueñas A. Intoxicaciones agudas en medicina de urgencia y cuidados críticos. Ed. Masson, S. A. 9. - López AM, Rivero C, Galban C, Mariño A, Piñeiro A, Ferrer E. Envenenamiento por paraquat y hemoperfusión con carbón activado. An Med Interna (Madrid) 2002; 19: 310 -12. 10. - Repetto M. Toxicología de Postgrado. Ed. Área de Toxicología. Universidad de Sevilla. CD-ROM. Sevilla, 2004. 11. - Sogorb-Sánchez MA, Vilanova-Gisbert E, Carrera-González V. Nuevas perspectivas en los tratamientos de intoxicaciones por insecticidas organofosforados y agentes nerviosos de guerra. Rev Neurol 2004; 39: 739 -47. 12. - Rodenticidas. http: //www. viasalus. com 2004. 13. - Repetto M. Toxicología de Postgrado. Ed Área de Toxicología. Universidad de Sevilla. CD-ROM. Sevilla, 2004. 14. - Moreno J, López J, Jiménez R. El control de los roedores: revisión de los rodenticidas registrados en el ámbito de la sanidad ambiental en España. Rev Esp Salud Pública 2004; 78: 5 -16. 15. - Nelson AT, Hartzell JD, More K y Durming SJ. Ingestion of Superwarfarin Leading to Coagulopathy: A Case Report and Review of the literature. Med. Gen. Med 2006: 8; 41. http: //www. ncbi. nlm. nih. gov/pmc/articles/PMC 1868388/? tool=pubmed. 08 -04 -2010. 16. - Shu-Lei Z, Peng L, Ming J, Ye Z, Shu-Tian Z. Upper gastrointestinal hemorrhage caused by superwarfarin poisoning. Word J Gastroenterology 2010; 16: 1680 -82. 17. - Rodrigo P, Rodríguez V, García JM, Aguilera I. Intento autolítico con superwarfarinas. www. sedar. es/restringido/2005/8/cartas. pdf. 18 - López CM y Olmos V. Intoxicación con rodenticidas superwarfarínicos desde el laboratorio toxicológico. RETEL, Revista de Toxicología en Línea: 2006: 09; 1 -14. www. sertox. comar/retel/default. htm. 19. - Watt BE, Proudfoot AT, Bradberry SM, Vale JA. Anticoagulant rodenticides. Toxicol Rev 2005; 24: 259 -69. 20. - North Dakota Poison Center. Anticoagulantes Rodenticides. http: //www. ndpoison. org/index. asp? page. ID=150. 10 -04 -2011. 21. - Dolin EK, Baker DL, Buck SC. A 44 -year-old woman with hematemesis and cutaneous hemorrhages as a result f superwarfarin poisoning. J Am Osteopath Assoc 2006; 106: 280 -4. 22. - Lo VM, Ching CK, Chan AY, Mak TW. Bromadiolone toxicokinetics: diagnosis and treatment implications. Clin Toxicol (Phila) 2008; 46: 703 -10. 23. - Tsutaoka BT, Miller M, Fung SM, Patel MM, Olson KR. Superwarfarin and glass ingestion with prolonged coagulopathy requiring high-dose vitamin K 1 therapy. Pharmacotherapy 2003; 23: 1186 -9. 24. - Chua JD, Friedenberg WR. Superwarfarin Poisoning. Arch Intern Med 1998; 158: 1929 -32. 25. - Bruno GR, Howland MA, Mc. Meeking A, Hoffman R. Long-Acting Anticoagulant Overdose: Brodifacoum Kinetics and Optimal Vitamin K. Ann Emerg Med 2000; 36: 262: 67. 26. - Laposata M, Van Cott E, Lev MH. Case 1 -2007: A 40 years-Old Woman with Epixtasis, Hematemesis and Altered Mental Status. N Engl Med 2007; 356: 174 -82. 27. - Spahr JE, Maul JS, Rodgers GM. Superwarfarin poisoning: a report of two cases and review of the literature. Am J Hematol 2007; 82: 656 -60. 28. - Conte G, Torres C, Alfaro J, Marianela V. Intoxicación por rodenticida-superwarfarina: Descripción de un caso clínico. Revista Hospital Clínico Universidad de Chile 2004; 15: 209 -212. 29. - Olmos V, López CM. Brodifacoum poisoning with toxicokinetics data. Clin Toxicol (Phila) 2007; 45: 487 -9. 30. - Grobosch T, Angelow B, Schönberg L, Lampe D. Acute bromadiolone intoxication. J Anal Toxicol 2006; 30: 281 -6. 31. - Jin MC, Ren YP, Xu XM, Chen XH. Determination of bromadiolone in whole blood by high-performance liquid chromatography coupled with electrospray ionization tandem mass spectrometry. Forensic Sci Int 2007; 17: 52 -6. 32. - Vindenes V, Karinen R, Hasvoid I, Bernard HP, Morland JG, Christophersen AS. Bromadiolone poisoning: LC-MS method and pharmacokinetic data. Forensic Sci 2008; 53: 993 -6. 33. - Pavlu J, Harrington DJ, Voong K, Savidge GF, Jan-Mohamed S, Kaczmarski R. Superfarfaring poisoning. Lancet 2005; 365: 628. 34. - Eddleston M et al. Early management alter self-poisoning with an organophosphorus or carbamate pesticida: a protocol for junior doctors. Critical Care 2004: 8: 391 -7. 35. - Wood DM et al. Fatality after deliberate ingestion of the pesticide rotenone: a case report. Crit Care 2005; 9: R 280 -R 284: http: //ccforum. com/content/9/3/R 280 36. - Suárez ML, González-Delgado ML, Rubio F, Hardisson A. Estudio de seis suicidios consumados por ingestión de carbamatos en el partido judicial de La Laguna (Tenerife) durante el período de 1998 -2002. Rev Toxicol 2004; 21: 108 -112. 37. - Pawar KS, Bhoite RR, Pillay CP, Chavan SC, Malshikare DS, Garab SG. Continuous pralidoxime infusión versus repeated bolus injection to treta organophosphorus pseticide poisoning: a randomised controlled trial. Lancet 2006; 368: 2136 -41. 39. - Datos sobre la estricnina. CDC. Emergencias causadas por agentes químicos. Emergenvy. cdc. gov/agent/strychnine/espanol/pdf. 2003. 40. - Estricnina: www. hiperactivos. com/estricnina. shtlm 2007. 41. - Piretrinas y piretroides: wwww. agroinfomacion. com/leer-contenidos. aspx? . . . 2007. 42. - Abizanda I. Jornadas sobre neurotoxicología laboral: neuroradiologiadeltrabajo. sen. es/jorneurotox 99_ponencia 3_nt. htm 1999. 43. - Bloomquist JR. Insecticidas: Químicas y características: ipmworl. umn. edu/…/Spchapters/Bloomquistsp. htm 2003 44. - Ferrer A. Intoxicación por plaguicidas. www. cfnavarra, es/. . . /vol 26/sup 1/suple 9 a. htm 2003 45. - Barco JC, Oma C, Puiguriguer J, Coll I, Barceló B, Castanyer T. Revisión de las intoxicaciones graves por insecticidas organofosforados atendidos en un período de 11 años (1996 -2006). Emergencias 2008; 20: 207 -11. 46. - Roberts DM and Aaron CK. Management of acute organophosphate pesticide poisoning. Br Med J 2007; 334: 629 -34. 47. - Iraola Ferrer M et al. Suicidio con fosfuro de aluminio: presentación de un caso. Emergencias 2009; 21: 228 -31. 48. - Weselak M et al. Pesticide exposures and developmental outcomes: the epidemiological evidence. Journal of Toxicology and Environmental Health 2007; Part B: 41 -80. 49. - Toxicología-Sustancias: fosfuro de aluminio. http: //www. estrucplan. com. ar/Producciones/entrega. asp? Id. Entrega=788. 14/08/2009. 50. - Fosfuro de aluminio. http: //es. wikipedia. org/wiki/Fosfuro_de_aluminio. 14/08/09. 51. - Riesgo químico-Accidentes gravas. Fosfuro de aluminio. Región de Murcia. Consejaría de Sanidad. Dirección General de Salud Pública. Octubre 2008. 52. - Hernández-Hernández N et al. Intoxicación por paraquat. Salud en Tabasco 2000; 6: 300 -5. http: //redalyc. uaemex. mx/redalyc/htlm/48760104/4876104_1. html 53. - Hernández J et al. Intoxicación por paraquat: descripción de un caso clínico lieth 1. Acta toxicológica argentina 2008; 6: 1. Versión On-line http: //www. scielo. org. ar/scielo. php? script=sci_arttext&pid=S 1851 -37432008000100002
- Slides: 44