glkozidz aktivits mrse talajban Enzimek globulris fehrjk jellegzetes

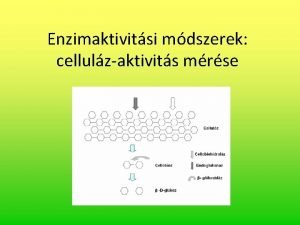
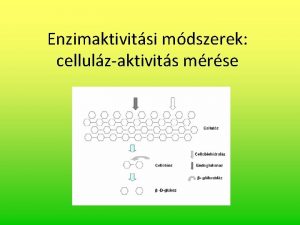
β-glükozidáz aktivitás mérése talajban

Enzimek • globuláris fehérjék • jellegzetes térszerkezet specifikusság • biológiai katalizátorok: vagy egy reakciótípust vagy egy bizonyos anyag átalakulását katalizálják • a reakciók lebonyolításában az aminosavoldalláncok által kialakított aktív centrum vesz részt

Az enzimek működése • egy enzimkatalizált reakcióban az enzim aktív centrumában ideiglenesen megköti a szubsztrátot és létrejön egy enzim-szubsztrát komplex • a reakció lejátszódásával termék keletkezik, amely leválik az enzimről, majd az enzim visszakerül eredeti állapotába • függ: kémhatás, hőmérséklet
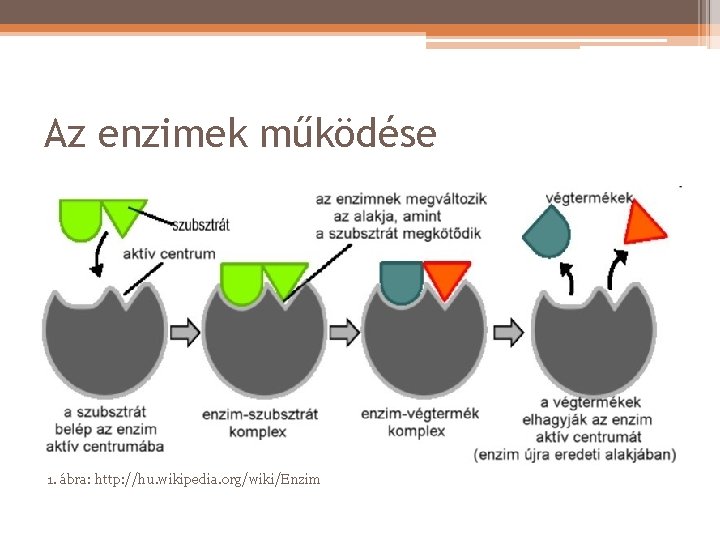
Az enzimek működése 1. ábra: http: //hu. wikipedia. org/wiki/Enzim

Enzimaktivitás • az enzim mennyiségét az enzimaktivitással szokták jellemezni • tulajdonképpen reakciósebességet jelent, vagyis azt jelenti, hogy a jelen levő enzimmennyiség szigorúan meghatározott szubsztrát koncentráció mellett, időegység alatt, mennyi szubsztrát átalakulását katalizálja • egysége: 1 µmol/perc, catal

Enzimaktivitást befolyásoló tényezők • • • enzimkoncentráció szubsztrátkoncentráció kémhatás hőmérséklet inhibitorok, aktivátorok

β-glükozidáz • mikroorganizmusokban, növényekben és állatokban is egyaránt megtalálható • hidroláz enzim • a cellulózt hidrolitikusan hasítja glükóz molekulákká • a diszacharidokat hidrolizáló glükozidázok csoportjába tartozik • a talajban sokkal nagyobb jelentőségű, mint az ugyanebbe a csoportba tartozó α- glükozidáz és α - és β-galaktozidáz

Hidrolízis 2. ábra: Alef K. and Nannipieri P. : Methods in Applied Soil Microbiology and Biochemistry • a hidrolizáló enzimek víz belépésével két részre hasítják a szubsztrátmolekulákat • a szubsztrátmolekulák egy részét az OHcsoportra viszik át, míg a víz protonja a szubsztrátmolekula másik részére kerül

β-glükozidáz aktivitás mérése • leggyakrabban p-Nitrofenil-β-D-glükozidot használnak szubsztrátként • ennél a szubsztrátnál Km értéke általában 1, 3 -2, 4 m. M (Michaelis-állandó (Km): az a szubsztrátkoncentráció, amelynél a maximális ( vmax) felét éri el a reakciósebesség) • 70°C-on inaktiválódik és jelentős összefüggést mutat a talaj szeversanyagával

β-glükozidáz aktivitás vizsgálata (Tabatabai 1982; Eivazi és Tabatabai 1988) • alapja a p-nitrofenol csökkenésének meghatározása, a talaj p-nitrofenil glükozid oldat inkubációja után • az inkubáció időtartama 1 óra; hőmérséklet: 37 °C 3. ábra: Alef K. and Nannipieri P. : Methods in Applied Soil Microbiology and Biochemistry

Szükséges eszközök és anyagok Eszközök • • Spektrofotométer Erlenmeyer lombik (50 ml) 37°C –os vízfürdő, rázató Szűrőpapír Anyagok • Toluol • MUB (modified universal buffer) puffer (p. H=6) • 0, 5 M Ca. Cl 2 • 0, 1 M TRIS puffer (p. H=12 és 10) • Standard p-Nitrofenol oldat • 25 m. M p-Nitrofenil-β-Dglükozid (PNG) oldat (0, 377 g PNG-t 40 ml MUB pufferben oldva, 50 ml-re hígitva)

A mérés metodikája • 1 g nedves talajt Erlenmeyer lombikba helyezünk, majd hozzáadunk 0, 25 ml toluolt, 4 ml MUB oldatot és 1 ml PNG oldatot • lezárva 1 órán keresztül 37°C-os rázatóban inkubáljuk • az inkubáció után hozzáadunk 1 ml Ca. Cl 2 oldatot , 4 ml TRIS puffert (p. H=12), összekeverjük a lombikban és szűrőpapírral azonnal leszűrjük a szuszpenziót • spektrofotométerrel 400 nm-en megmérjük az intenzitást (ha túl magas, azaz nem fér bele a mérhető tartományba, akkor p. H=10 -es TRIS pufferrel hígítani kell a szűrletet) • vakoldat készítése • mérés megismétlése 3 x (ugyanahhoz a vakoldathoz)

β-glükozidáz aktivitás vizsgálata (Hoffmann és Dedeken 1965) • alapja a salignin (2 -oxymetil-fenol) csökkenésének meghatározása salicin 2 -( hidroximetil)fenil –β-Dglükopiranozid (β-glükozid salignin) talajban történő inkubálása után • az inkubálás időtartama 3 óra; hőmérséklet: 37 °C

Szükséges anyagok és eszközök Anyagok Eszközök • 2 M acetát puffer (p. H=6, 2) • Borát puffer (p. H=9, 6) • Dibróm-kinon -klórimid oldat (200 mg 100 1/ml etanol) • 2, 306 g β-glükozid salignin oldat • Standard salignin oldat (0, 1 mg/ml) • toluol • • Spektrofotométer Mérőlombik (50 ml) 37 °C-os vízfürdő, rázató Szűrőpapír

A mérés metodikája • mérőlombikba 5 g nedves talajt helyezünk, majd hozzáadunk 1 ml toluolt és 15 percig állni hagyjuk, szobahőmérsékleten • ezután hozzáadunk 10 ml-t a szubsztrát oldatból és 20 ml acetát puffert, majd 3 órán keresztül 37°C-on inkubáljuk • az inkubálás után desztillált vízzel 50 ml-re hígitjuk, összekeverjük és leszűrjük • a szűrletből 1 -3 ml-t mérőlombikba pipettázunk és hozzáadunk 20 ml acetát puffert, 2 ml borát puffert és 0, 5 ml dibróm-kinon-klórimid oldatot • desztillált vízzel 50 ml-re töltjük és 90 perc után, 578 nm-en mérjük az abszorbanciát • a vakoldat elkészítéséhez 10 ml desztillált vizet adunk a szubsztrát helyett • a mérést háromszor megismételjük (ugyanazzal a vakoldattal)

Felhasznált irodalom: • Alef K. and Nannipieri P. (Editors): Methods in Applied Soil Microbiology and Biochemistry. Academic Press Limited. London. 1995 • Boross László, Sajgó Mihály: A biokémia alapja. Mezőgazda Kiadó Kft. 2003 • Ádám Veronika: Orvosi biokémia. Medicina. 2004 • Sarkadi Lívia: Biokémia mérnök szemmel. Typotex. 2007 • http: //hu. wikipedia. org/wiki/Enzim
- Slides: 16