Urez aktivits mrse Ksztette Majoros Katalin Bevezets p

Ureáz aktivitás mérése Készítette: Majoros Katalin
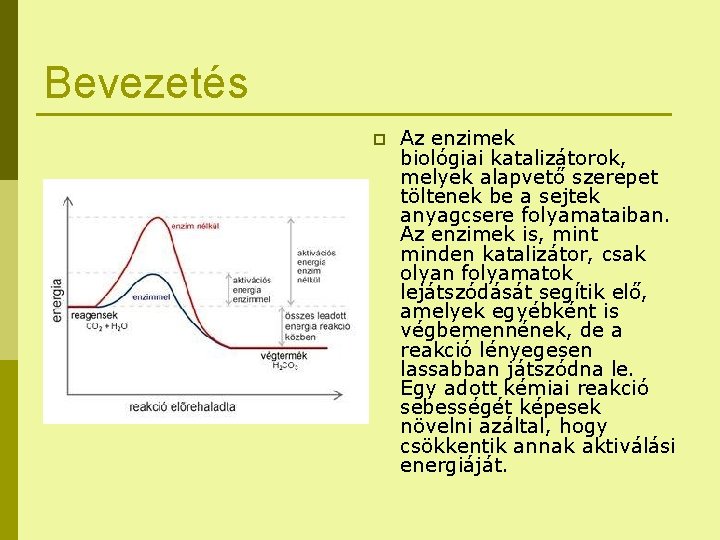
Bevezetés p Az enzimek biológiai katalizátorok, melyek alapvető szerepet töltenek be a sejtek anyagcsere folyamataiban. Az enzimek is, mint minden katalizátor, csak olyan folyamatok lejátszódását segítik elő, amelyek egyébként is végbemennének, de a reakció lényegesen lassabban játszódna le. Egy adott kémiai reakció sebességét képesek növelni azáltal, hogy csökkentik annak aktiválási energiáját.
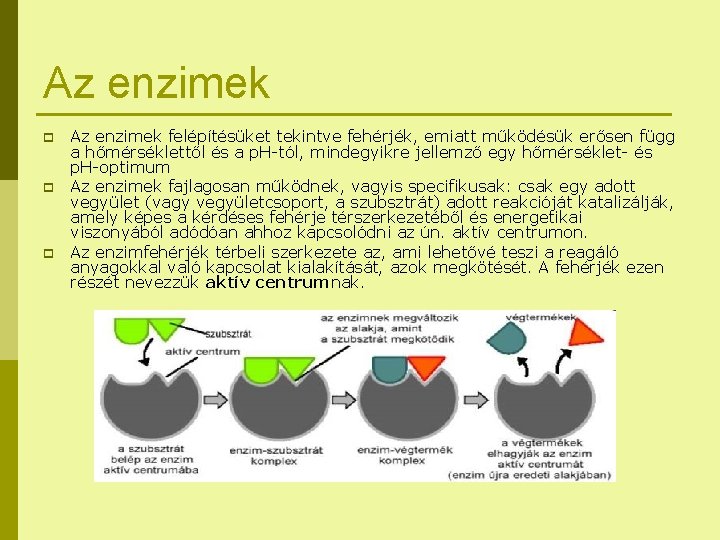
Az enzimek p p p Az enzimek felépítésüket tekintve fehérjék, emiatt működésük erősen függ a hőmérséklettől és a p. H-tól, mindegyikre jellemző egy hőmérséklet- és p. H-optimum Az enzimek fajlagosan működnek, vagyis specifikusak: csak egy adott vegyület (vagy vegyületcsoport, a szubsztrát) adott reakcióját katalizálják, amely képes a kérdéses fehérje térszerkezetéből és energetikai viszonyából adódóan ahhoz kapcsolódni az ún. aktív centrumon. Az enzimfehérjék térbeli szerkezete az, ami lehetővé teszi a reagáló anyagokkal való kapcsolat kialakítását, azok megkötését. A fehérjék ezen részét nevezzük aktív centrumnak.

Ureáz p p Az ureáz a karbamid hidrolízisét katalizáló enzim. Megtalálható magasabb rendű növényekben és mikroorganizmusokban. Jelenléte teszi lehetővé a karbamidnak, mint nitrogénforrásnak a felhasználását. Csak bizonyos környezeti feltételek mellett működik hatékonyan. Aktivitását befolyásolja a hőmérséklet és a kémhatás. Optimális p. H tartománya 8, 5 -9 közötti. A baktériumok az ureáz enzim segítségével bontják a húgysavat, miközben ammóniát szabadítanak fel.

Az ureáz működése és aktivitásmérése p p p p Mint már említettem, az ureáz katalizálja a húgysav hidrolízisét szén-dioxidra és ammóniára, karbamid képződése közben. A reakció egyenlete: H 2 NCONH 2 + H 2 O =2 NH 3 + CO 2 Sokféle módszert fejlesztettek ki az ureáz aktivitásának mérésére talajmintákból Legtöbbjük magában foglalja a toluollal kezelt, pufferelt húgysavoldattal átitatott talajmintából felszabaduló ammónia mennyiségének mérését Más módszerek inkább a felszabaduló szén-dioxid mennyiségéből következtetnek a talajmintában történő húgysavhidrolízis mértékére Megint mások sem toluolt, sem puffereket nem alkalmaznak a mérésekhez

Nehézségek a meghatározásban p p p A sokféle módszer miatt eltérőek a vélemények a p. Hoptimumot, illetve az optimális hőmérséklettartományt tekintve is: p. H-ra a semlegestől a 6 -7 tartományon át, a 8. 8 -10 -es értékekig találhatók irodalmi adatok Optimális hőmérsékletre 60°C adódott, de az ureáz általában 70°C-on denaturálódik, a talajminták inkubációjának hőmérséklete 15 -40°C tartományban végezhető ( a 30°C az ideális) Ráadásul az ureáz aktivitás nem arányos a mikrobiális biomasszával, és hatását a nehézfémek, az oxigén koncentráció, a bontható nitrogénmennyiség mind-mind befolyásolja A továbbiakban két meghatározási módszert vizsgálunk részletesebben, melyek eltérő módon juttatnak (remélhetőleg) ugyanahhoz az eredményhez.

Tabatabi és Bremner ureáz aktivitás meghatározási módszere (1972) I. p A módszer lényege: n p Az ammóniafelszabadulás mértékének meghatározásán alapul, miután a talajmintákat 2 órán keresztül 37°C-on, húgysavoldattal inkubáltuk Eszközök: n n n Gőzdesztillációs berendezés 37°C-ra állítható inkubátor p. H mérő Mérőlombikok (50, 1000, 2000 ml) Automata titráló berendezés Erlenmeyer lombik (100 ml)

Tabatabai-Bremner (1972) II. vegyszerek és oldatok p p Toluol Hidroxi-metil-amino-metán puffer n p Ebből 6. 1 g-ot 700 ml desztillált vízben oldunk, majd addig adagolunk hozzá H 2 SO 4 -ot (0. 2 M), amíg el nem érjük a 9. 0 p. H -t. Ezután desztillált vízzel 1000 ml térfogatúra töltjük fel Húgysavoldat (200 m. M) n p (50 m. M, p. H 9) 1. 2 g húgysavat 80 ml pufferoldatban oldunk, majd ugyanezzel a pufferrel 100 ml-re töltjük fel. Minden nap friss oldatot kell készíteni és 4°C-on kell tárolni Kálium-klorid (2. 5 M)- ezüst-szulfát (100 mg/l) oldat n Feloldunk 100 mg Ag 2 SO 4 -ot 700 ml desztillált vízben, majd 188 g KCl-ot ebben az oldatban és desztillált vízzel 1000 ml-re töltjük fel.

Tabatabai-Bremner III. - Az NH 4 -N meghatározás reagensei p p H 2 SO 4 (0. 005 M) Indikátor oldat n p Bórsavas indikátor oldat n p A 2 l-es mérőlombikba pipettázunk 40 ml-t az indikátor oldatból, és 400 ml-t a 95%-os etanolból. 40 g bórsavat 1400 ml meleg desztillált vízzel keverünk. Hűtés után ezt is a 2 l-es mérőlombikba öntjük. Ezután addig pipettázunk hozzá Na. OH-ot (0. 05 M), amíg 1 ml oldat színe rózsaszínről zöldre változik 1 ml desztillált víz hozzáadásakor. Végül mindezt 2000 ml-re töltjük fel desztillált vízzel. Mg. O n p Feloldunk 0. 66 g brómkrezol zöldet és 0. 33 g metilvöröst 95%-os etanolban, és szintén etanollal 1000 ml-re töltjük fel 600 -700°C-on hőkezelünk hőstabil Mg. O-ot 2 órán keresztül, majd hűtjük és kiszárítjuk Na. OH-on vagy szilikagélen exikátorban. Ammóniastandard oldat n Feloldunk 0. 234 g ammónium-szulfátot desztillált vízben, majd 1000 ml -re töltjük fel szintén desztillált vízzel

Tabatabai-Bremner IV. – A meghatározás menete p p p 5 g nedves talajmintát helyezünk az 50 ml-es mérőlombikba, majd hozzáadunk 0. 2 ml toluolt és 9 ml pufferoldatot, ezt összekeverjük, és hozzáadunk 1 ml húgysavoldatot, majd ismét keverjük néhány másodpercig. Ezután az edényt inkubátorba helyezzük ás 2 órán át 37°C-on inkubáljuk. Ezt követően hozzáadunk a mintához kb. 35 ml KCl-Ag 2 SO 4 oldatot, összerázzuk, majd hagyjuk a lombik tartalmát szobahőmérsékletűre hűlni. Miután lehűlt, feltöltjük a káliumos oldattal 50 ml-re, és jól elkeverjük az összetevőket. Ajánlott legalább 3 ismétlést csinálni. Az ammóniameghatározás menete: n 5 ml bórsav indikátort pipettázunk egy Erlenmeyer lombikba, és 20 ml talajminta szuszpenziót egy 100 ml-es desztilláló lombikba. Ehhez hozzáadunk 0. 2 g Mg. O-ot és gőzdesztilláljuk, amíg össze nem gyűlik 30 ml desztillátum. Ezt öntjük majd az Erlenmeyer lombikba az indikátorra. n A desztillátumot ezután 0. 005 M-os H 2 SO 4 oldattal titráljuk. 1 ml H 2 SO 4 70 μg NH 4 -N-nek felel meg.

Tabatabai-Bremner V. Számítás p Miután a standardokkal ellenőriztük a mérési eredményeink helyességét, a következőképpen számolunk: p ureáz aktivitás (μg NH 4 -N g-1 dwt*2 h-1)= (C× 50)/(dwt× 5) p Ahol C: a mért NH 4 -N koncentráció (1 ml talajszuszpenzióban), dwt: 1 g nedves talajminta száraz tömege, 5: a méréshez használt talajtömeg, 50: a talaj-szuszpenzió teljes térfogata p p p

Kandeler és Gerber módszere (1988) I. p A módszer lényege: n p Az ammónia kolorimetriás meghatározása a talajminta és a húgysavoldat 37°C-on, 2 órán át tartó inkubálása után. Szükséges eszközök: n n n 37°C-ra állítható inkubátor Rázó Szűrőpapír Spektrofotométer Mérőlombikok (100, 500, 1000, 2000 ml) Erlenmeyer lombik (50, 100 ml)

Kandeler-Gerber II. - Vegyszerek és oldatok 1. p Húgysavoldat n p KCl oldat n p 12 g Na. OH-ot oldunk desztillált vízben, majd szintén desztillált vízzel 1000 ml-re töltjük fel. Nátrium-szalicilát oldat n p 74. 6 g KCl-ot feloldunk desztillált vízben, majd hozzáadunk 10 ml 1 M-os HCl-ot, és desztillált vízzel feltöltjük 1000 ml-re. Na. OH (0. 3 M) n p Oldjunk fel 2. 4 g húgysavat 400 ml desztillált vízben, majd töltsük fel 500 ml-ig desztillált vízzel (naponta újat készítünk belőle) 17 g Na-szalicilátot és 120 mg nitroprusszid-nátriumot oldunk desztillált vízben, majd 100 ml-re töltjük desztillált vízzel. Na-szalicilát/Na. OH oldat n Egyenlő mennyiségű Na. OH oldatot, Na-szalicilát oldatot és desztillált vizet keverünk össze. (naponta újat kell belőle készíteni)

Kandeler-Gerber III. – Vegyszerek és oldatok 2. p Nátrium-diklór-izocianid oldat (0. 1%) n p Borát puffer (p. H 10) n p 0. 1 g nátrium-diklór-izocianátot oldunk 100 ml desztillált vízben (közvetlenül használat előtt készítjük el) 56. 85 g dinátrium-tetraborátot, vagy 30 g vízmentes dinátriumtetraborátot oldunk 1500 ml meleg desztillált vízben. Hűlés után annyi 20%-os Na. OH-t adunk hozzá, hogy p. H-ja 10 legyen, majd 2000 ml-re töltjük fel desztillált vízzel Ammónium-standard oldat n I. oldat: p p n 3. 82 g ammónium-kloridot oldunk desztillált vízben, majd 1000 ml -re töltjük (1000μg NH 4 -N/ml) Az oldat 4°C-on tárolva több hétig stabil marad II. oldat: p 0. 0, 1. 5, 2. 0, 2. 5 ml I. oldatot pipettázunk 100 ml-es mérőlombikokba, majd KCl oldattal 100 ml-re töltjük őket.

Kandeler-Gerber III. – A meghatározás menete: a nem pufferelt módszer p p 5 g nedves talajmintát helyezünk a 100 ml-es Erlenmeyer lombikba, és hozzáadunk 2. 5 ml húgysavoldatot. Ezt 2 órán át 37°C-on inkubáljuk, majd 50 ml KCl oldat hozzáadása után az egész lombikot 30 percen keresztül rázatjuk. A kapott szuszpenzió szűrése után, a szűrlet ammóniumtartalma mérhető. Ammónia-meghatározás: n 1 ml tiszta szűrletet pipettázunk az 50 ml-es Erlenmeyer lombikba, majd hozzáadunk 9 ml desztillált vizet, 5 ml Na-szalicilát/Na. OH oldatot és 2 ml nátrium-diklórizocianát oldatot, majd 30 percig szobahőmérsékleten állni hagyjuk, majd a 690 nm-en mérjük az optikai denzitást.

Kandeler-Gerber III. – A meghatározás menete: a pufferelt módszer - Kalibrálás p p p 5 g nedves talajmintát helyezünk 100 ml-es Erlenmeyer lombikba, és hozzáadunk 2. 5 ml húgysavat és 20 ml borát puffert. A további lépések megegyeznek a nem pufferelt változat lépéseivel, de a végén 30 ml KCl-ot adunk hozzá az inkubáció után. Kalibrálás: n 1 ml ammónium standard II. oldatot pipettázunk a kémcsövekbe és 9 ml desztillált vízzel hígítjuk, majd meghatározzuk az ammónium koncentrációkat (0, 1, 1. 5, 2, 2. 5 μg NH 4 -N/ml)

Kandeler-Gerber IV. - Számítás p Számolás: n Ureáz aktivitás (μg NH 4 -N g-1 dwt*2 h-1)= ((μg NH 4 -N/ml) × V × 10)/(dwt × 5) n Ahol dwt: 1 g nedves talaj száraz tömege V: 52. 5 ml, a minta teljes térfogata 10: a hígítási arány 5: a meghatározáshoz használt talaj tömege n n n

Megjegyzések p p p p Tabatabaiék módszerében a puffer megakadályozza a NH 4+ ionok kötődését a talajban, így a pufferelt közegben nagyobb ureáz aktivitás adódik, mint a nem pufferelt közegben. A KCl-Ag 2 SO 4 oldat készítésekor fontos, hogy a KCl-ot oldjuk az ezüst-szulfátban, mert az ezüst szulfát nem oldódik a káliumkloridban. Erre az oldatra azért van szükség, hogy megakadályozza az enzimreakciót, így a szuszpenzió tud 2 órát állni ammónium felszabadulása nélkül. Kandelerék módszerében nem használunk ilyen inhibítort, de a KCl itt is lelassítja a reakciót. A szűréskor ügyelni kell, hogy a szűrőpapír nitrogénmentes legyen, hogy megelőzzük a nitrogénmegkötődést a szűrletben. Az ammónium vizsgálathoz előállított színreakció szobahőmérsékleten 8 óráig stabil marad. A kolorimetriás meghatározás nem ajánlott a sok nehézség miatt, mint a reagensek vagy a színes vegyületek instabilitása, a nehézkes ismételhetőség, az alacsony érzékenység, az alacsony húgysav-koncentrációk, stb.

Köszönöm a figyelmet!

Források: p p p Alef K. and Nannipieri P. (Editors): Methods in Applied Soil Microbiology and Biochemistry, Academic Press Limited, London, 1995 http: //hu. wikipedia. org/wiki/Enzim : enzimműködés képek, bevezető az enzimekről http: //taplalkozas. bioenergetikus. hu/enzimek. ht ml : bevezető az enzimekről http: //160. 114. 99. 91/astrojan/protein/pictures/u rease. jpg : ureáz képe http: //www. vilaglex. hu/Kemia/Html/Ureaz. htm bevezető az ureázról
- Slides: 20