Enzimaktivitsi mdszerek cellulzaktivits mrse Enzimek a talajban Enzimek
Enzimaktivitási módszerek: celluláz-aktivitás mérése

Enzimek a talajban • Enzimek: biológiai folyamatokat katalizáló biomolekulák • Enzimek nevezéktana: hagyományosan az általuk lebontott vagy felépített vegyület neve -áz végződéssel; újabban azonban új nevezéktan készült, amely pontosabban kategorizálja őket a katalizált reakció típusa alapján • Elhelyezkedésük a talajban: élő vagy elhalt sejtek, sejttöredékek citoplazmájában vagy azok külső felületéhez kötődve, vagy sejten kívül mint oldott molekula, vagy agyagásványokhoz adszorbeálódva, vagy kolloid rendszerekben

Enzimek mennyiségének mérése a talajban • Mintavétel • A méréshez meg kell akadályozni, hogy a mintavétel után a mintában további enzim- vagy a reakciótermékek fogyása játszódjon le • A leggyakrabban toluolt adnak a mintához, így a lebontó mikrobák ezt bontják és nem a talajba került enzimet; segíti a sejten belüli enzimek kibocsátását is • A talaj sterilizálásához nagy energiájú elektron-nyalábokat vagy gammasugárzást használnak: így ki lehet szűrni az élő sejtek által folyamatosan végzett enzimtermelést • Analitikai elemzés

Mérési eredmények kiértékelése • Nem lehet megkülönböztetni kísérleti úton, hogy a minta enzimtartalmának mekkora része milyen módon volt kötve • Nem a tényleges talajban lévő enzim-aktivitást mutatja meg, inkább egy potenciális maximumot: a valós aktivitást a szubsztrát p. H-tól és hőmérséklettől függő koncentrációja befolyásolja • Mindezen hibákkal azonban a többi mikrobiológiai elemzési módszer is rendelkezik, ezzel viszont mennyiségi meghatározás is végezhető és jól kombinálható más módszerekkel

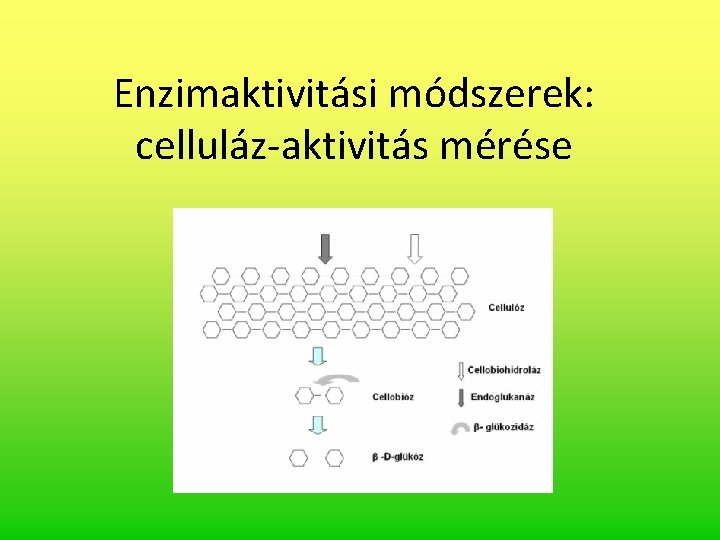
Cellulóz és celluláz I. • Cellulóz: növényi sejtfalak alkotóeleme, egy D-glükózból β (14) glikozidos kötéssel képződött polimer, vízben oldhatatlan • A természetben nagy mennyiségben fordul elő, így bontása létfontosságú • Cellulóz bontása a celluláz enzimmel történik: ez 3 enzimből áll: az exo- β-1, 4 -glükanáz a kristályos cellulózt, az endo- β-1, 4 -glükanáz a nem-kristályos cellulózt hasítja oligoszacharidokká, a β-glükozidáz pedig ezeket bontja egyszerű glükózzá • A bontás lassú, az avar típusától, a szubsztrát- és vízkoncentrációtól, p. H-tól, hőmérséklettől erősen függ

Cellulóz és celluláz II. • A talajba kijutva celluláz enzimei más-más elhalt növényi alkotóelemeken adszorbeálódnak és eltérő ütemben szabadulnak fel • Bontás optimuma: p. H=5 -6, 30 -50 °C • Főleg a rhizoszómában zajlik • Talajszárítás erősen visszaveti a folyamatot • A talajban lévő cellulázt nagyrész gombák termelik (Actinomyces képes megélni csak cellulózon mint szénforrás, anaerob körülmények között Clostridium) • Celluláz-aktivitás mérése a talajban a szubsztrát talajmintához adagolás hatására felszabaduló glükóz és szén-dioxid mennyisége alapján történik • Szubsztrát: gyapot-szálak, nyomjelzett cellulóz, karboxi-metil cellulóz (CMC), Avicel (savval részben hidrolizált mikrokristályos cellulóz)

Schinner és Von Mersi módszere (1990. ) • Segédanyagok: 2 M, p. H 5, 5 acetát-pufferoldat, 0, 7% Na-CMC sóoldat, a cukor meghatározásához 4 féle reagens: – A: Vízmentes Na 2 CO 3 és KCN keverékének vizes oldata – B: Kálium-vas-hexacianid vizes oldata – C: Vas-ammónium-szulfát, nátrium-dodecil-szulfát és kénsav keverékének vizes oldata – glükóz-monohidrát oldat • Mérés menete: 10 g szántóföldi vagy 5 g erdei talajmintát (2 mm vízzel nedvesítve), 15 ml puffert és 15 ml CMC-oldatot kevertek egy Erlenmayer-lombikban, majd lefedve inkubálták 50 °C-on 24 órát • Belső standardnak 15 ml CMC-t kevertek hozzá szűrés előtt, majd leszűrték, a szűrletet hígítva mintát vettek • 1 -1 ml A, B reagenst hozzáadva 15 percet forralták 100 °C-on, majd 5 perc 20°C-os hűtőfürdő után C reagensből adtak hozzá 5 ml-t és egy órát állni hagyták 20°C-on • Megmérték a fényáteresztő-képességét 690 nm-en

Az oldatok részletes receptje • Ecetsavas puffer: 164, 08 g nátrium-acetátot oldottak 700 ml desztillált vízben, 5, 5 -re állították a p. H-t ecetsavval és 1000 ml-re hígították • 0, 7 %-os CMC-só-oldat: 7 g CMC-t oldottak 1000 ml ecetsavas pufferben és 2 órára 45 o. C-on inkubálták, 4 o. Con egy hétig tárolható • A reagens: 16 g vízmentes Na 2 CO 3 -ot és 0, 9 g KCN-ot oldottak 1000 ml desztillált vízben • B reagens: 0, 5 g kálium-vas-hexacianidot oldottak 1000 ml desztillált vízben; barna üvegekben tartandó! • C reagens: 1, 5 g vas-ammónium-szulfátból, 1 g nátriumdodecil-szulfátból és 4, 2 ml cc. kénsavból 50 o. C-on desztillált vizes oldatot készítettek és 1000 ml-re hígították • glükóz-monohidrát oldat: 28 mg glükóz-monohidrátot oldottak 1000 ml desztillált vízben

A módszerről levont következtetések • Csak az endoglükanáz és a β-glükozidáz mennyisége mérhető így, az exoglükanázé nem • A módszer főleg a nedves erdőtalajok mérésére adott jó eredményt • A bomlás sebessége az időtől nem lineárisan függ • A bontást zavaró más vegyületek: nagy koncentrációban jelenlévő sók, ezüst, ammónium-ion, oxalátok stb. , a talaj egyéb mikrobiális paraméterei viszont nem befolyásolják • Toluolos kezelés nem változtatta meg az eredményt számottevően • A p. H kontrollja fontos: A és B oldatok hozzáadása után p. H>10, 5, C oldat hozzáadása után p. H<2 legyen • A cianid alkalmazása kiváltható hidrogén-peroxidos, savas közegben történő oxidációval

Hope és Burns módszere (1987. ) • Segédanyagok: azidos, 0, 1 M, p. H 5, 5 acetát-pufferoldat, Avicel (por), a cukor meghatározására 7 féle reagens: – – – I. oldat: Na és K borkősavval alkotott sója, Na 2 CO 3 és Na. HCO 3 vizes oldata II. oldat: Na 2 SO 4 vizes oldata III. oldat: az első kettő keveréke IV. oldat: Cu. SO 4*5 H 2 O és Na 2 SO 4 vizes oldata V. oldat: a III. és a IV. keveréke – glükóz-monohidrát oldat – arzenát-molibdát oldat • Mérés menete: Erlenmeyer-lombikba mértek 1 g nedves talajt, 5 ml acetát-puffert és 0, 5 g Avicelt, lezárva 16 órát inkubálták 40°c-on, majd belső standardnak Avicelt hozzáadva, centrifugálták. • 1 ml mintát véve, azt 1 ml V. oldattal 20 percet forralva, majd lehűtve és 1 ml arzenát-molibdát oldatot, majd 3 ml desztillált vizet hozzáadva megmérték a fényáteresztőképességét 520 nm-en.

Az oldatok részletes receptje • Azidos acetát-puffer: 13, 6 g nátrium-acetát-tetrahidrátot oldottak 700 ml desztillált vízben, majd a p. H-t 5, 5 -re állították ecetsavval. Hoozáadtak 2 g nátrium-azidot és 1000 ml-re hígították az egészet. • I. oldat: 15 g-ot Na és K borkősavval alkotott sójából, 30 g Na 2 CO 3 -ból 300 ml desztillált vízben oldatot készítettek, és ebben 20 g Na. HCO 3 ot oldottak fel • II. oldat: 180 g Na 2 SO 4 oldata 500 ml desztillált vízben; kiforralták belőle az oldott oxigént, majd hagyták lehűlni • III. oldat: az első kettő keveréke 1000 ml-re hígítva • IV. oldat: 5 g Cu. SO 4*5 H 2 O és 45 g Na 2 SO 4 oldata 250 ml desztillált vízben • V. oldat: a III. és a IV. 1: 1 arányú keveréke (frissen keverték) • glükóz-monohidrát oldat: 79 mg glükóz-monohidrátot oldottak 1000 ml desztillált vízben • arzenát-molibdát oldat: 25 g ammónium-molibdátot oldottak 450 ml desztillált vízben és 21 ml cc. kénsavat adtak hozzá kevergetés mellett. 25 ml NA 2 HAs. O 4 * 7 H 2 O oldatot adtak hozzá (3 g só 25 ml vízben). 2 nap 37 o. C-on történő állás után barna üvegekbe töltötték. Használat előtt egységnyi ilyen oldattal 2 egységnyi 0, 75 M kénsavat kevertek.

A módszerről levont következtetések • Az enzimreakció lineáris volt 16 órán keresztül • Az azid inhibitorként működött: megakadályozta a keletkezett cukrok baktériumok általi elfogyasztását, de hatását minden talajtípusnál külön ellenőrizni kell, mert nem univerzális • A módszer nem különbözteti meg a különböző cellulázenzimeket • Magas glükóz-oxidáz koncentráció a talajban meghamisítja ennek a mérési módszernek az eredményét

Alternatív módszerek • A szubsztrátként szolgáló cellulóz lehet szűrőpapír, cellubióz, HEC (hidroxi-etilcellulóz) stb. is; lehet oldott (Avicel) vagy oldahtatatlan (szűrőpapír) formában a mérés során • Citromsavas pufferoldatokat is szokás alkalmazni • A keletkezett cukor mennyisége dinitroszalicilsav alkalmazásával is megbecsülhető • Az egyes mikroba-fajok egész celluláz enzimrendszerekkel rendelkeznek, amelyekben az említett 3 enzim működését más enzimek is segítik; ezekre is vannak mérési módszerek • Az egész téma, mind a talaj celluláz-aktivitásának megmérése, mind a celluláz-enzimrendszer működése és a talajban történő cellulóz-lebontás sebessége erősen kutatott téma, ahol még sok megoldandó problémával néznek szembe a kutatók.

Források • Methods in Applied Soil Miccrobiology and Biochemistry, Chapter 7: Enzime activities (a bevezető: 311 -312. oldal és K. Alef és P. Nannipieri cikke a 345 -349. oldalon) (1995, Academic Press Ltd. ) • Az Avicelről: http: //www. answers. com/topic/avicel • T. K. GHOSE (INTERNATIONAL UNION OF PURE AND APPLIED CHEMISTRY): MEASUREMENT OF CELLULASE ACTIVITIES • Kép forrása: http: //akciospotencial. blog. hu/2007/10/21/title_13504
- Slides: 14