Estado Gasoso LEIS VOLUMTRICAS DAS REAES QUMICAS Se






- Slides: 13

Estado Gasoso

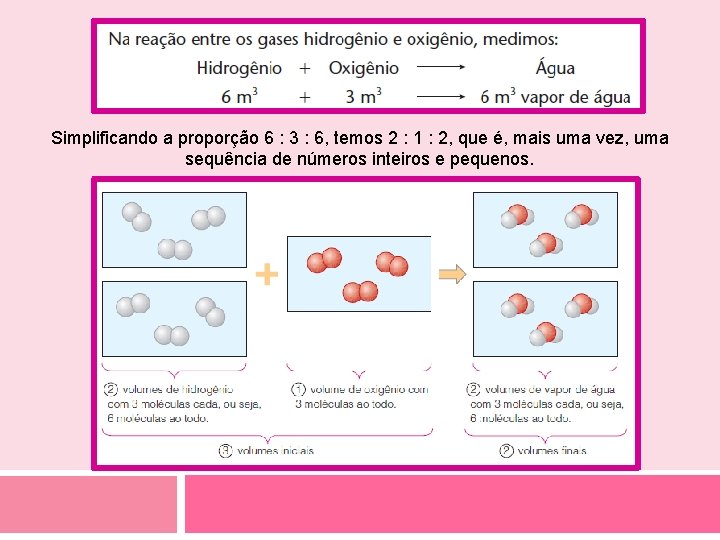
LEIS VOLUMÉTRICAS DAS REAÇÕES QUÍMICAS Se referem aos volumes dos gases que participam de uma reação química Lei volumétrica de Gay-Lussac Quando medidos nas mesmas condições de pressão e temperatura, os volumes dos reagentes e dos produtos gasosos formam uma proporção constante, de números inteiros e pequenos. Simplificando esses números, temos 1 : 2, que é uma proporção de números inteiros e pequenos

Simplificando a proporção 6 : 3 : 6, temos 2 : 1 : 2, que é, mais uma vez, uma sequência de números inteiros e pequenos.

Hipótese ou lei de Avogadro Volumes iguais de diferentes gases, a uma mesma temperatura e pressão, contêm igual número de moléculas.

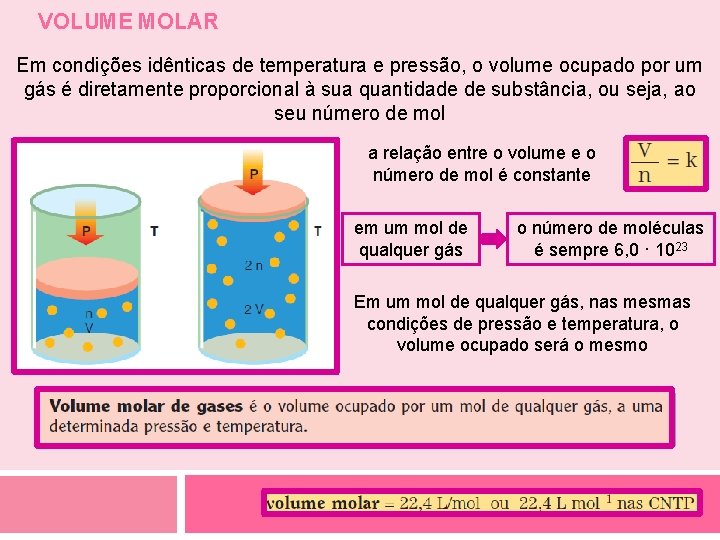
VOLUME MOLAR Em condições idênticas de temperatura e pressão, o volume ocupado por um gás é diretamente proporcional à sua quantidade de substância, ou seja, ao seu número de mol a relação entre o volume e o número de mol é constante em um mol de qualquer gás o número de moléculas é sempre 6, 0 · 1023 Em um mol de qualquer gás, nas mesmas condições de pressão e temperatura, o volume ocupado será o mesmo

EQUAÇÃO DE ESTADO DOS GASES PERFEITOS Para uma massa constante de um mesmo gás, a relação é sempre válida: Isso significa que, por mais que variem o volume (V ), a pressão (P ) e a temperatura absoluta (T ), a fração PV/T permanece constante Supondo que tivéssemos 1 mol de gás nas condições normais de pressão (P = 1 atm) e temperatura (T = 273 K). Sabemos que 1 mol de qualquer gás, nessas condições, ocupa o volume molar (V= 22, 4 litros/mol). constante universal dos gases perfeitos

Equação de Estado dos Gases Perfeitos ou Equação de Clapeyron. Qualquer gás que obedeça a essa lei será considerado um gás perfeito ou ideal

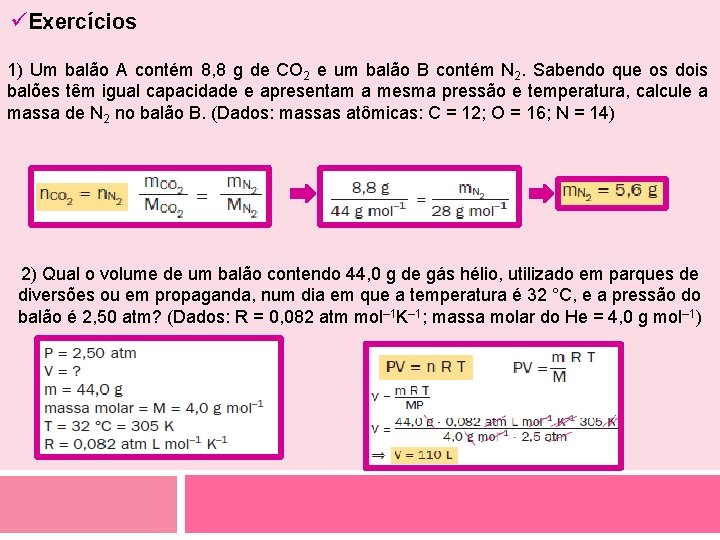
üExercícios 1) Um balão A contém 8, 8 g de CO 2 e um balão B contém N 2. Sabendo que os dois balões têm igual capacidade e apresentam a mesma pressão e temperatura, calcule a massa de N 2 no balão B. (Dados: massas atômicas: C = 12; O = 16; N = 14) 2) Qual o volume de um balão contendo 44, 0 g de gás hélio, utilizado em parques de diversões ou em propaganda, num dia em que a temperatura é 32 °C, e a pressão do balão é 2, 50 atm? (Dados: R = 0, 082 atm mol– 1 K– 1; massa molar do He = 4, 0 g mol– 1)

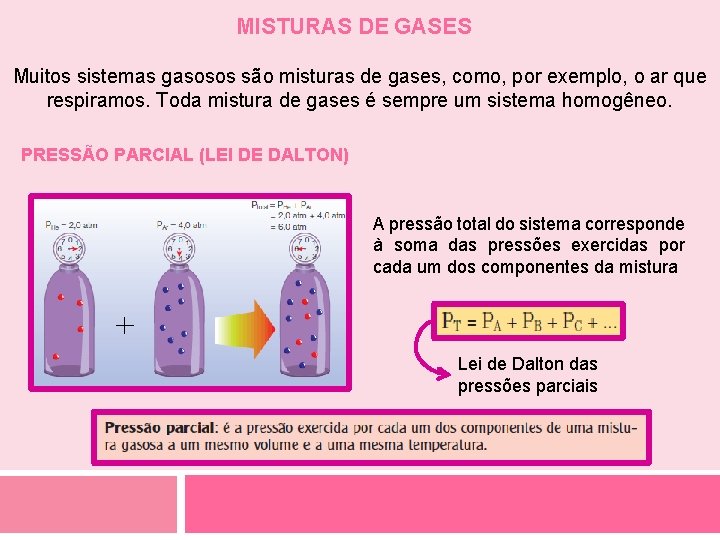
MISTURAS DE GASES Muitos sistemas gasosos são misturas de gases, como, por exemplo, o ar que respiramos. Toda mistura de gases é sempre um sistema homogêneo. PRESSÃO PARCIAL (LEI DE DALTON) A pressão total do sistema corresponde à soma das pressões exercidas por cada um dos componentes da mistura Lei de Dalton das pressões parciais

A pressão parcial exercida por cada gás é diretamente proporcional ao número de mol do gás. A pressão total é diretamente proporcional ao número total de mol VOLUME PARCIAL (LEI DE AMAGAT) Fração Molar : relação entre o número de mol de um gás e o número total de mol da mistura.

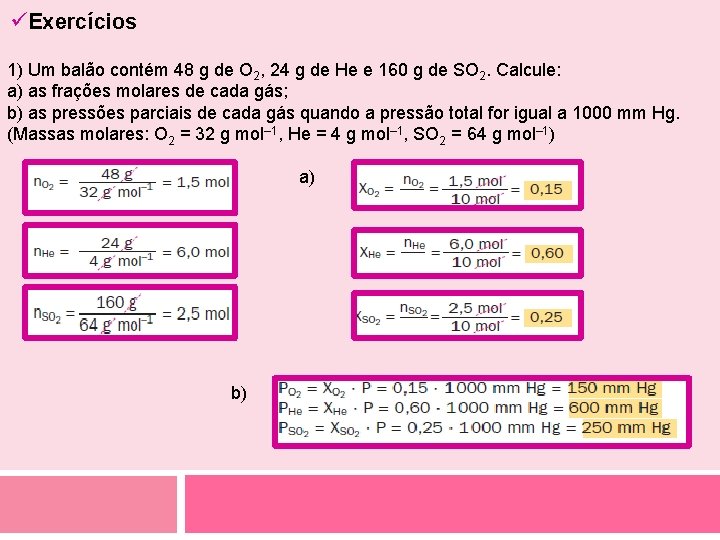
üExercícios 1) Um balão contém 48 g de O 2, 24 g de He e 160 g de SO 2. Calcule: a) as frações molares de cada gás; b) as pressões parciais de cada gás quando a pressão total for igual a 1000 mm Hg. (Massas molares: O 2 = 32 g mol– 1, He = 4 g mol– 1, SO 2 = 64 g mol– 1) a) b)

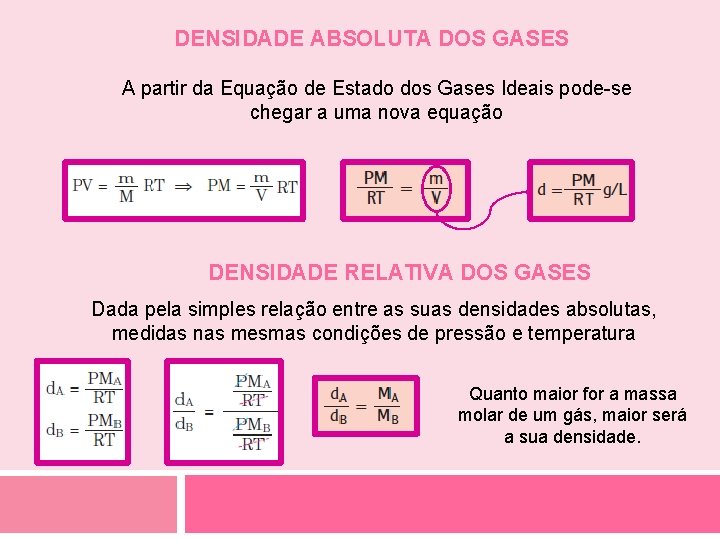
DENSIDADE ABSOLUTA DOS GASES A partir da Equação de Estado dos Gases Ideais pode-se chegar a uma nova equação DENSIDADE RELATIVA DOS GASES Dada pela simples relação entre as suas densidades absolutas, medidas nas mesmas condições de pressão e temperatura Quanto maior for a massa molar de um gás, maior será a sua densidade.

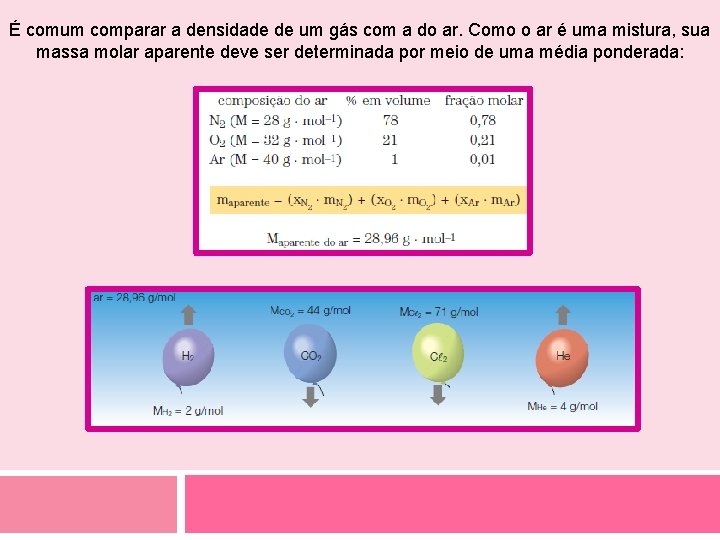
É comum comparar a densidade de um gás com a do ar. Como o ar é uma mistura, sua massa molar aparente deve ser determinada por meio de uma média ponderada: