LEIS DAS REAES QUMICAS Prof Agamenon Roberto As

LEIS DAS REAÇÕES QUÍMICAS Prof. Agamenon Roberto

As leis das reações químicas podem ser divididas em dois grupos: LEIS PONDERAIS LEIS VOLUMÉTRICAS São as leis relativas às São as leis relativas aos massas das substâncias que participam das reações químicas volumes das substâncias que participam das reações químicas Prof. Agamenon Roberto

As principais leis ponderais são: Lei da conservação das massas ou Lei de Lavoisier Lei das proporções constantes ou Lei de Proust Lei das proporções múltiplas ou Lei de Dalton Prof. Agamenon Roberto
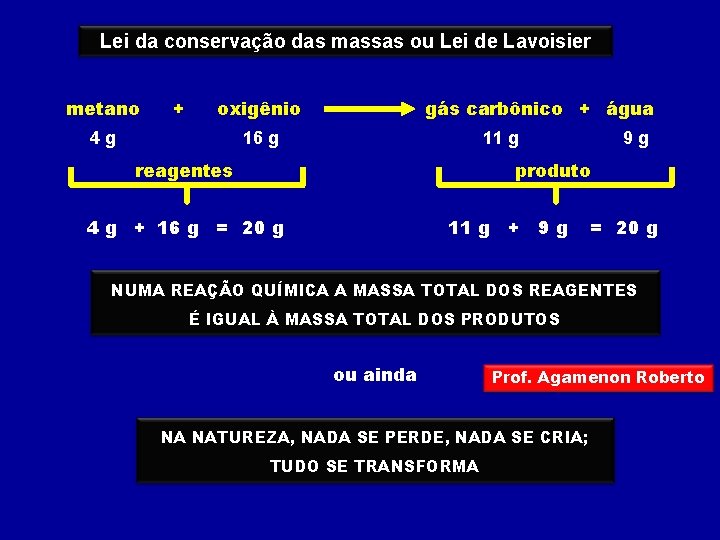
Lei da conservação das massas ou Lei de Lavoisier metano + gás carbônico + água oxigênio 4 g 16 g 11 g reagentes 9 g produto 11 g + 9 g 4 g + 16 g = 20 g NUMA REAÇÃO QUÍMICA A MASSA TOTAL DOS REAGENTES É IGUAL À MASSA TOTAL DOS PRODUTOS ou ainda Prof. Agamenon Roberto NA NATUREZA, NADA SE PERDE, NADA SE CRIA; TUDO SE TRANSFORMA
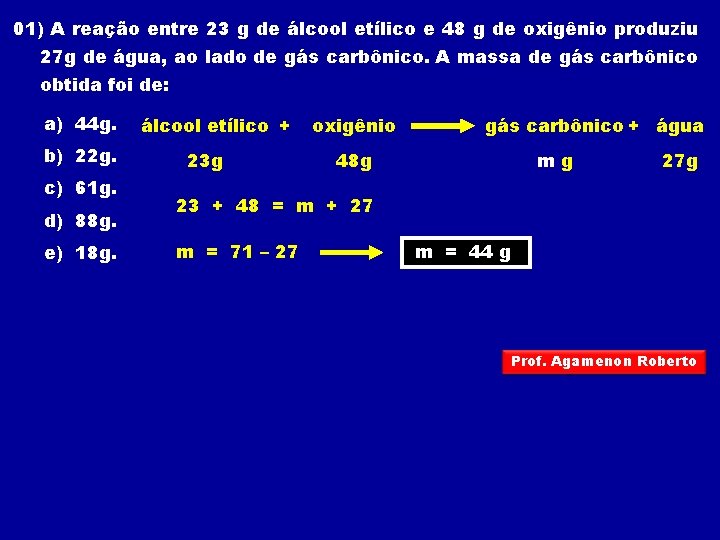
01) A reação entre 23 g de álcool etílico e 48 g de oxigênio produziu 27 g de água, ao lado de gás carbônico. A massa de gás carbônico obtida foi de: a) 44 g. b) 22 g. c) 61 g. d) 88 g. e) 18 g. álcool etílico + 23 g oxigênio gás carbônico + água 48 g mg 27 g 23 + 48 = m + 27 m = 71 – 27 m = 44 g Prof. Agamenon Roberto
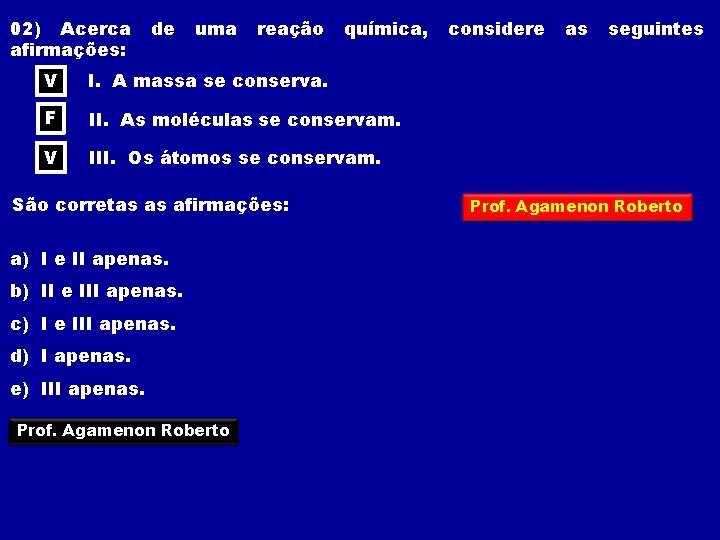
02) Acerca afirmações: de uma reação química, V I. A massa se conserva. F II. As moléculas se conservam. V III. Os átomos se conservam. São corretas as afirmações: a) I e II apenas. b) II e III apenas. c) I e III apenas. d) I apenas. e) III apenas. Prof. Agamenon Roberto considere as seguintes Prof. Agamenon Roberto

Lei das proporções constantes ou Lei de Proust hidrogênio + oxigênio água 1ª experiência: 2 g 16 g 18 g 2ª experiência: 4 g 32 g 36 g 1ª experiência: massa de hidrogênio massa de oxigênio 2ª experiência: massa de hidrogênio massa de oxigênio = = 2 g = 1 g 16 g 8 g 4 g 1 g 32 g = 8 g QUALQUER QUE SEJA O MÉTODO DE OBTENÇÃO DE UMA SUBST NCIA, ELA É SEMPRE FORMADA PELOS MESMOS ELEMENTOS QUÍMICOS COMBINADOS NUMA MESMA PROPORÇÃO Prof. Agamenon Roberto

CONSEQÜÊNCIAS DA LEI DE PROUST CÁLCULO ESTEQUIOMÉTRICO É o cálculo pelo qual prevemos as quantidades das substâncias que participarão de uma reação química Prof. Agamenon Roberto

01) Sabemos que 7 g de nitrogênio reagem todo com 1, 5 g de hidrogênio, produzindo gás amônia. A massa de gás amoníaco que iremos obter nessa reação quando misturamos 2, 1 g de nitrogênio com uma quantidade suficiente de hidrogênio é: a) 8, 1 g. b) 10, 2 g. c) 2, 55 g. nitrogênio + hidrogênio gás amoníaco 7 g d) 4, 00 g. 2, 1 g e) 3, 60 g. 7 2, 1 = 1, 5 g 8, 5 g mg 8, 5 m 7 x m = 2, 1 x 8, 5 7 x m = 17, 85 Prof. Agamenon Roberto m = 17, 85 7 m = 2, 55 g
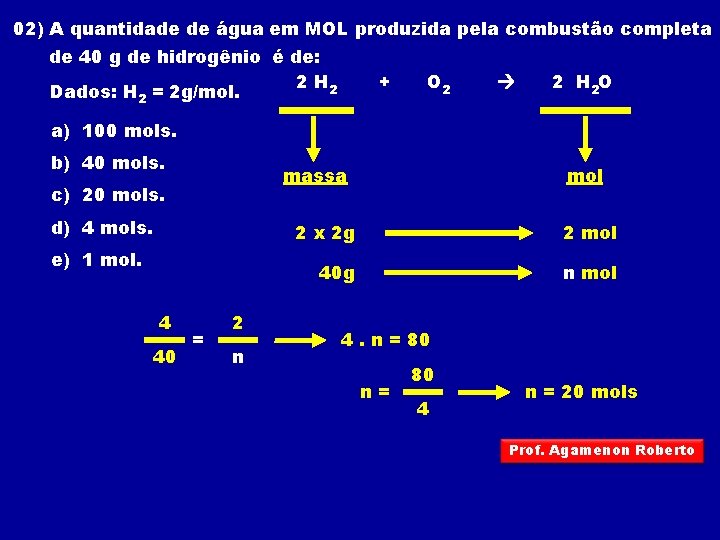
02) A quantidade de água em MOL produzida pela combustão completa de 40 g de hidrogênio é de: 2 H 2 Dados: H 2 = 2 g/mol. + O 2 2 H 2 O a) 100 mols. b) 40 mols. massa c) 20 mols. d) 4 mols. e) 1 mol. 4 40 = 2 n mol 2 x 2 g 2 mol 40 g n mol 4. n = 80 n= 80 4 n = 20 mols Prof. Agamenon Roberto

03) O mármore (Ca. CO 3) reage com o ácido sulfúrico formando o gesso (Ca. SO 4), de acordo com a equação balanceada: H 2 SO 4(aq) + Ca. CO 3(s) Ca. SO 4(s) + H 2 O(l) + CO 2(g) A massa de gesso formada pela reação de 25 g de mármore com H 2 SO 4 suficiente será: Prof. Agamenon Roberto Dados: Ca. CO 3 = 100 u; Ca. SO 4 = 136 u a) 5 g. . + Ca. CO 3(s) b) 17 g. e) 100 g. Ca. SO 4(s) +. . . 100 g c) 34 g. d) 68 g. 136 g 25 g 100 25 m= = 136 m 3400 100 mg m= 25 x 136 m = 34 g 100

04) Quantos gramas de H 2 são liberados na reação completa de 1 mol de cálcio metálico com ácido clorídrico ? Dado: H 2 = 2 g/mol a) 1 g. Ca + 2 HCl Ca. Cl 2 + H 2 b) 2 g. c) 3 g. d) 4 g. e) 5 g. mol massa 1 mol 12 mol g Prof. Agamenon Roberto

05) O brometo de cálcio encerra 20% de cálcio em massa. Juntando-se 4 g de cálcio e 4 g de bromo teremos, no máximo: a) 8 g de brometo de cálcio. b) 7 g de brometo de cálcio. Prof. Agamenon Roberto c) 6 g de brometo de cálcio. d) 5 g de brometo de cálcio. e) 4 g de brometo de cálcio + 20 g bromo brometo de cálcio 80 g 100 g ou 1 g 4 g 5 g 1 4 g g 4 g xg 1 g + 4 g = x x = 5 g
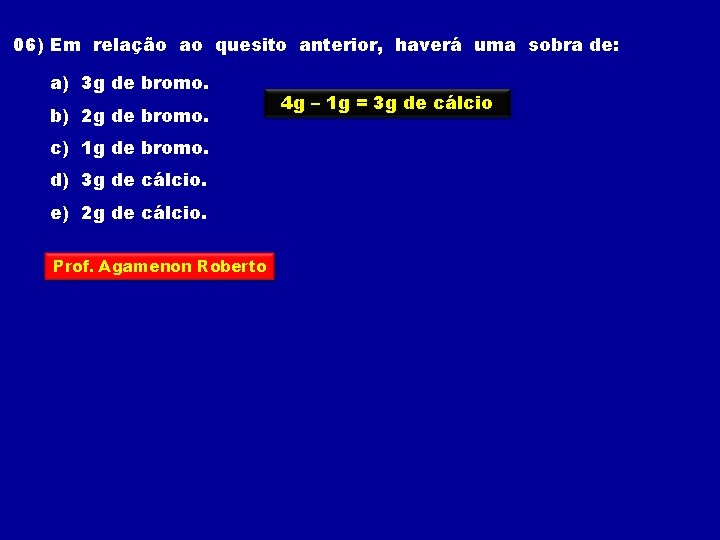
06) Em relação ao quesito anterior, haverá uma sobra de: a) 3 g de bromo. b) 2 g de bromo. c) 1 g de bromo. d) 3 g de cálcio. e) 2 g de cálcio. Prof. Agamenon Roberto 4 g – 1 g = 3 g de cálcio

COMPOSIÇÃO CENTESIMAL São as porcentagens, em massa, dos elementos formadores de uma substância Prof. Agamenon Roberto
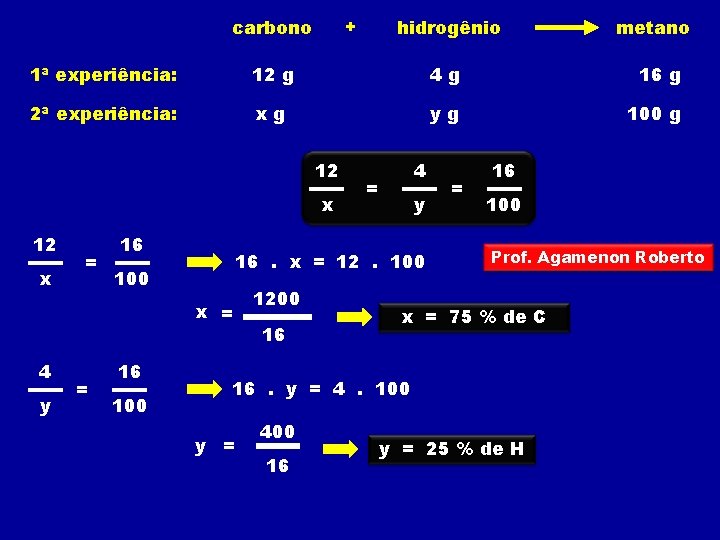
+ carbono hidrogênio metano 1ª experiência: 12 g 4 g 16 g 2ª experiência: xg yg 100 g 12 x = 16 100 y = 16 100 = y 16. x = 12. 100 x = 4 4 1200 16 = 16 100 Prof. Agamenon Roberto x = 75 % de C 16. y = 4. 100 y = 400 16 y = 25 % de H
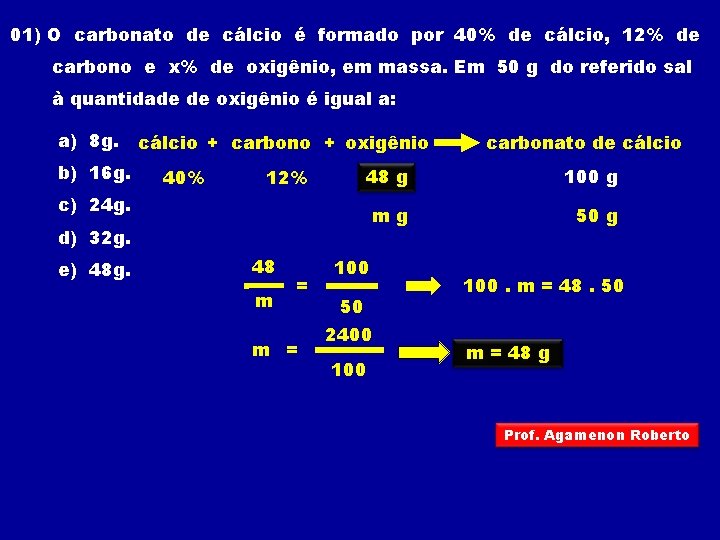
01) O carbonato de cálcio é formado por 40% de cálcio, 12% de carbono e x% de oxigênio, em massa. Em 50 g do referido sal à quantidade de oxigênio é igual a: a) 8 g. b) 16 g. cálcio + carbono + oxigênio 40% 12% 48 g x% 100 g mg 50 g c) 24 g. d) 32 g. e) 48 g. 48 m = carbonato de cálcio 100 50 2400 100. m = 48. 50 m = 48 g Prof. Agamenon Roberto

02) A porcentagem em massa do carbono no CHCl 3 (clorofórmio) é: Dados: H = 1 u; C = 12 u; Cl = 35, 5 u a) 1%. b) 10%. c) 12%. d) 24%. e) 50%. carbono + hidrogênio 12 g + cloro 1 g 106, 5 g xg 12 x = 119, 5 g 100 g = x clorofórmio 119, 5 100 1200 119, 5. x = 12. 100 = 10% Prof. Agamenon Roberto

LEI DAS PROPORÇÕES MÚLTIPLAS ou LEI DE DALTON Quando dois elementos reagem formando substâncias diferentes, se a massa de um dos dois permanecer constante, a massa do outro irá variar segundo valores múltiplos ou submúltiplos 1ª experiência: + oxigênio hidrogênio 4 g 2ª experiência: 32 g + oxigênio hidrogênio 4 g 32 g 64 g = 32 g : 32 64 g : 32 = 64 g 1 2 água 36 g água oxigenada 68 g A proporção é de 1 : 2 Prof. Agamenon Roberto

LEIS VOLUMÉTRICAS São as leis relativas aos volumes das substâncias que participam de uma reação As relações entre os volumes dos gases que reagem foram determinadas por GAY-LUSSAC Prof. Agamenon Roberto

Estas leis podem ser resumidas em um único enunciado “ Quando medidos nas mesmas condições de temperatura e pressão, os volumes reagentes e dos produtos gasosos formam uma proporção constante, de números inteiros e pequenos “ Prof. Agamenon Roberto

Na reação entre os gases hidrogênio e cloro, foram medidos os seguintes volumes: hidrogênio 15 L + cloro gás clorídrico 15 L 30 L Simplificando-se esses valores teremos a seguintes relação 1: 1: 2 que é uma relação de números inteiros e pequenos Prof. Agamenon Roberto

Na reação entre os gases hidrogênio e oxigênio foi medidos os seguintes volumes: hidrogênio 6 L + oxigênio água 3 L 6 L Simplificando-se esses valores teremos a seguintes relação 2: 1: 2 que é uma relação de números inteiros e pequenos Prof. Agamenon Roberto

HIPÓTESE DE AVOGADRO Volumes iguais de gases quaisquer, medidos nas mesmas condições de temperatura e pressão encerram o mesmo número de moléculas Prof. Agamenon Roberto

01)Um balão A contém 8, 8 g de CO 2 e um balão B contém N 2. Sabendo que os dois balões têm igual capacidade e apresentam a mesma pressão e temperatura, calcule a massa de N 2 no balão B. Dados: C = 12 g/mol; O = 16 g/mol; N = 14 g/mol. m CO 2 n CO 2 == M CO 2 m N 2 n N 2 M N 2 8, 8 44 = m 28 44. m = 8, 8. 28 CO 2 1. 12 + 2. 16 = 44 g/mol N 2 2. 14 = 28 g/mol m = 246, 4 = 5, 6 g 44 Prof. Agamenon Roberto

02)(Covest – 90) Como produto da eletrólise da água, recolhe-se gás oxigênio no eletrodo positivo (ânodo) e gás hidrogênio no eletrodo negativo (cátodo). Assinale que afirmativa representa a razão entre os volumes dos gases recolhidos, nas mesmas condições de temperatura e pressão. 2 H 2 O 1 O 2 + 2 H 2 a) 1 volume de oxigênio para 1 volume de hidrogênio. b) 2 volumes de oxigênio para 1 volume de hidrogênio. c) 1 volume de oxigênio para 3/2 volumes de hidrogênio. d) 1 volume de oxigênio para 2 volumes de hidrogênio. e) 3/2 volumes de oxigênio para 1 volume de hidrogênio. Prof. Agamenon Roberto
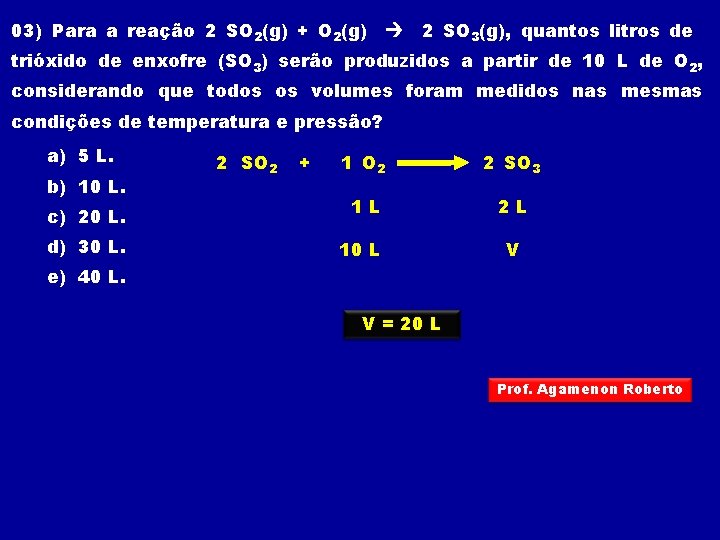
03) Para a reação 2 SO 2(g) + O 2(g) 2 SO 3(g), quantos litros de trióxido de enxofre (SO 3) serão produzidos a partir de 10 L de O 2, considerando que todos os volumes foram medidos nas mesmas condições de temperatura e pressão? a) 5 L. b) 10 L. c) 20 L. d) 30 L. 2 SO 2 + 1 O 2 2 SO 3 1 L 2 L 10 L V e) 40 L. V = 20 L Prof. Agamenon Roberto

DETERMINAÇÃO DE FÓRMULAS As substâncias podem ser representadas pelas fórmulas CENTESIMAL MÍNIMA e MOLECULAR Prof. Agamenon Roberto

FÓRMULA CENTESIMAL É a fórmula que indica os elementos químicos e as porcentagens, em massa, de cada átomo que forma a substância METANO C 75% H 25% Prof. Agamenon Roberto Indica que: O metano é constituído por carbono e hidrogênio Em 100 g de metano existem 75 g de carbono e 25 g de hidrogênio

Podemos calcular a FÓRMULA CENTESIMAL partindo da fórmula molecular, fórmula mínima ou das massas que participam da reação Determine a fórmula centesimal do metano sabendo que 12 g do carbono reagem com 4 g de hidrogênio para a produção de 16 g de metano. + carbono hidrogênio metano 1ª experiência: 12 g 4 g 16 g 2ª experiência: xg yg 100 g 12 12 x = 4 y = 16 x 100 4 y = = 16 100 x = 75 % de C y = 25 % de H Prof. Agamenon Roberto

FÓRMULA MOLECULAR É a fórmula que indica os elementos químicos que constituem a substância e o número de átomos de cada elemento na molécula GLICOSE C 6 H 12 O 6 Prof. Agamenon Roberto Indica que: A glicose é constituída por carbono, hidrogênio e oxigênio Em uma molécula de glicose existem 6 átomos de carbono, 12 átomos de hidrogênio e 6 átomos de oxigênio

FÓRMULA MÍNIMA Prof. Agamenon Roberto É a fórmula que indica os elementos químicos que constituem a substância e a proporção em número de átomos desses elementos, expressa em números inteiros e os menores possíveis GLICOSE fórmula molecular GLICOSE fórmula mínima C 6 H 12 O 6 CH 2 O Indica que: A glicose é constituída por carbono, hidrogênio e oxigênio Em uma molécula de glicose existe uma proporção de 1 átomo de carbono, 2 átomos de hidrogênio e 1 átomo de oxigênio

Podemos calcular a fórmula mínima partindo da fórmula molecular, fórmula centesimal ou das massas que participam da reação 01) (Covest – 2005) Uma substância pura foi analisada em laboratório e foram obtidos os seguintes resultados: Teor de H = 0, 4 g, teor de C = 2, 4 g e teor de O = 3, 2 g. Sendo a fórmula mínima desta substância HℓCm. On, calcule a soma ℓ + m + n. Dados H (A = 1 u. ), C (A = 12 u. ), O (A = 16 u. ). H: C: O: 0, 4 1 2, 4 12 3, 2 16 = 0, 4 mol : 0, 2 = 2 mol = 0, 2 mol : 0, 2 = 1 mol Prof. Agamenon Roberto = 0, 2 mol : 0, 2 = 1 mol fórmula mínima soma: H 2 C 1 O 1 ℓ + m + n = 2 + 1 = 04

02) (Modificado) Uma substância pura foi analisada em laboratório e foram obtidos os seguintes resultados: Teor de H = 0, 4 g, teor de C = 2, 4 g, teor de O = 3, 2 g e massa molar 90 g/mol. A fórmula mínima desta substância é HℓCm. On, escreva a fórmula molecular da substância. Dados H (A = 1 u. ), C (A = 12 u. ), O (A = 16 u. ). H: C: O: n = 0, 4 1 2, 4 12 3, 2 16 = 0, 4 mol : 0, 2 = 2 mol fórmula mínima H 2 C 1 O 1 = 0, 2 mol : 0, 2 = 1 mol fórmula molecular = 0, 2 mol : 0, 2 = 1 mol (H 2 C 1 O 1)n massa molar massa da fórmula mínima fórmula molecular: = 90 30 = 3 H 6 C 3 O 3 Prof. Agamenon Roberto

03)(Mackenzie-SP) Ao se analisar um óxido de elemento não metálico Y, encontrou-se a proporção de 1, 5 mols de átomos de oxigênio para 1 mol de átomos de Y. A fórmula desse óxido pode ser: a) OF 2. b) SO 3. (Y 1 O 1, 5) x 2 = Y 2 O 3 c) CO 2. d) Fe 2 O 3. e) N 2 O 3. Prof. Agamenon Roberto

04) A combustão realizada em altas temperaturas é um dos fatores da poluição do ar pelos óxidos de nitrogênio, causadores de afecções respiratórias. A análise de 0, 5 mol de um desses óxidos apresentou 7, 0 g de nitrogênio e 16 g de oxigênio. Qual a sua fórmula molecular? Em 0, 5 mol do óxido temos. . . Prof. Agamenon Roberto N: O: Em 1, 0 mol do óxido teremos. . . 7, 0 14 16 16 = 0, 5 mol = 1, 0 mol de nitrogênio e 2, 0 mol de oxigênio A fórmula molecular será NO 2

05) Em 0, 5 mol de quinina, substância utilizada no tratamento da malária há 120 g de carbono, 12 g de hidrogênio, 1 mol de átomos de nitrogênio e 1 mol de átomos de oxigênio. Determine a fórmula molecular da quinina. Em 0, 5 mol de quinina temos. . . C: H: 120 12 12 1 Prof. Agamenon Roberto Em 1, 0 mol de quinina teremos. . . = 10 mol C: 20 mol = 12 mol H: 24 mol N: 1, 0 mol N: 2, 0 mol O: 1, 0 mol O: 2, 0 mol A fórmula molecular será C 20 H 24 N 2 O 2
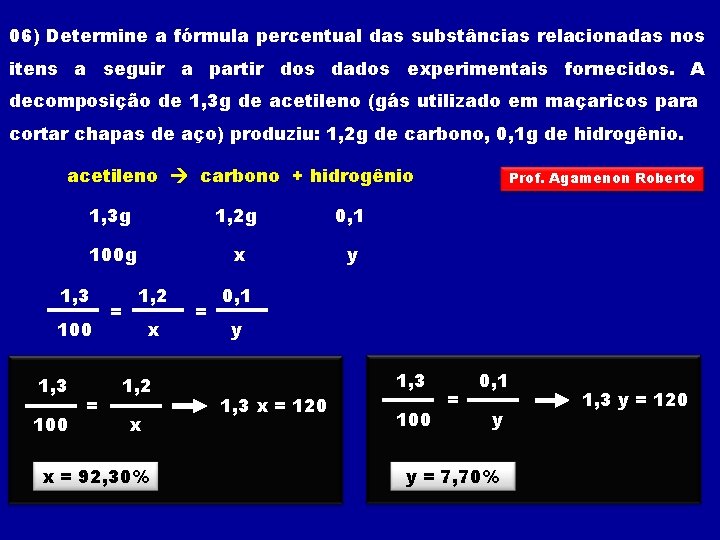
06) Determine a fórmula percentual das substâncias relacionadas nos itens a seguir a partir dos dados experimentais fornecidos. A decomposição de 1, 3 g de acetileno (gás utilizado em maçaricos para cortar chapas de aço) produziu: 1, 2 g de carbono, 0, 1 g de hidrogênio. acetileno carbono + hidrogênio 1, 3 g 1, 2 g 0, 1 100 g x y 1, 3 100 = = 1, 2 x x = 92, 30% = Prof. Agamenon Roberto 0, 1 y 1, 3 x = 120 1, 3 100 = 0, 1 y y = 7, 70% 1, 3 y = 120
- Slides: 38