FSICA PTICA AULA 14 MUDANAS DE FASES FASES























- Slides: 25

FÍSICA ÓPTICA AULA 14 – MUDANÇAS DE FASES

FASES DA MATÉRIA Ø As substâncias, dependo da temperatura e da pressão em que se encontram podem mudar a organização de suas moléculas. Ø Estas diferentes formas de organização geram uma mudança no comportamento das moléculas, principalmente na força de ligação entre elas. Ø A esta mudança de comportamento molecular se dá o nome “fases da matéria” Ø Assim sendo, dependo da temperatura e pressão que uma substância se encontra estas podem estar em três diferentes fases. A fase sólida, líquida ou gasosa.

FASES DA MATÉRIA Ø Primeiramente vamos considerar que a pressão na qual a substância está submetida seja constante, ou seja, não varie. Ø Assim sendo, vamos mudar apenas a temperatura na qual a substância em questão está submetida. P=K T

FASES DA MATÉRIA Fase sólida Ø As partículas que compõem a substância, na fase sólida estão fortemente ligadas entre si, ocorrendo uma rígida e organizada disposição das partículas (retículo cristalino)

FASES DA MATÉRIA Fase sólida Ø A fase sólida apresenta as seguintes características: • Forma e volume bem definidos; • Partículas próximas umas das outras e ligadas por forças elétricas intensas; • Devido as fortes ligações, não há movimentação das partículas uma em relação às outras no interior do corpo (a movimentação de cada partícula se deve a agitação térmica)

FASES DA MATÉRIA Fase líquida Ø Na fase líquida as partículas também estão ligadas entre si, porém com uma intensidade bem menor do que na fase sólida, sendo que nesta fase não existe a mesma disposição organizada das moléculas como na fase sólida.

FASES DA MATÉRIA Ø As características da fase líquida são: • Volume bem definido; • A forma da massa líquida é a mesma do recipiente que a contém; • Partículas mais dispersas porém ainda há forças entre elas; • Há a movimentação das partículas no interior dos líquidos.

FASES DA MATÉRIA Fase gasosa Ø Na fase gasosa as partículas que compõem a substâncias praticamente não possuem mais nenhuma ligação, ou seja, a força de atração entre elas é praticamente nula. Estas partículas estão livres uma das outras, de forma que possuem grande mobilidade.

FASES DA MATÉRIA Fase gasosa Ø Esta fase apresenta as seguintes características • Volume e forma do recipiente que contém a massa gasosa; • Partículas praticamente livres uma das outras; • Movimentação desorganizadas partículas.

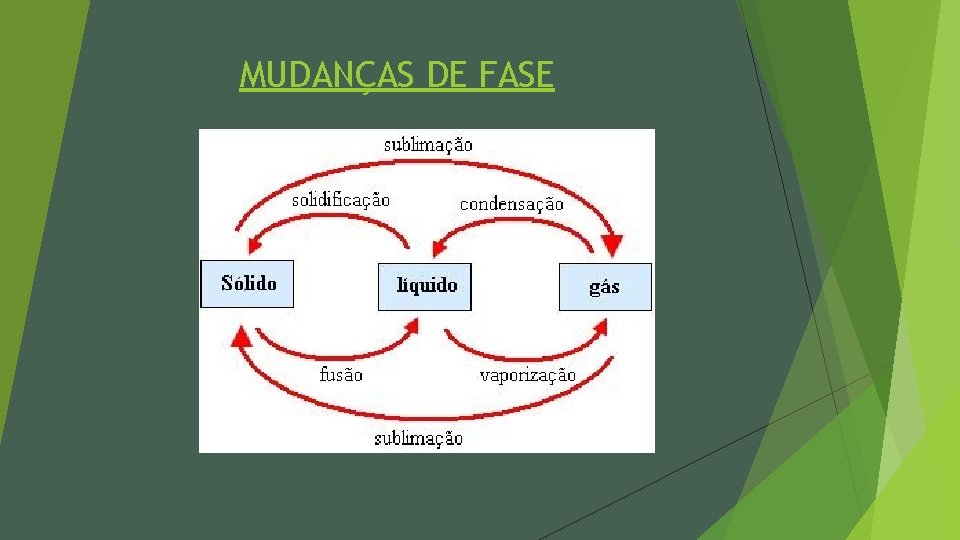
MUDANÇAS DE FASE Ø Dessa forma, já conhecendo as fases e como elas se comportam podemos estudar agora como se dá a passagem da substância para as fases apresentadas. § Fusão: Passagem da substância para do estado sólido para o estado líquido. § Solidificação: Passagem da substância do estado líquido para o estado sólido. § Vaporização: Passagem da substância do estado líquido para o estado gasoso. § Condensação ou liquefação: Passagem da substância do estado gasoso para o líquido. § Sublimação: Passagem da substância do estado gasoso para o estado sólido ou vice e versa.

MUDANÇAS DE FASE

MUDANÇAS DE FASE Tipos de vaporização Ø A vaporização, conforme a maneira que ela acontece, recebe nomes diferentes, sendo eles: Evaporação Ebulição Calefação

MUDANÇAS DE FASE Tipos de vaporização Ø Evaporação: A evaporação é a passagem da substância do estado líquido pra o estado gasoso de forma lenta e gradual, acontecendo na superfície do líquido. Ø Exemplos: • A roupa no varal. • A água na bacia. • Um lago.

MUDANÇAS DE FASE Tipos de vaporização Ø Ebulição: É a passagem da substância do estado líquido para o estado gasoso perante um processo tumultuoso que se estende por toda a massa líquida, sendo um processo previsível que ocorre a uma dada pressão e temperatura. Ø Exemplos: § A água que ferve a pressão de 1 atm e temperatura de 100 ºC!

MUDANÇAS DE FASE Tipos de vaporização Ø Calefação: É a passagem da substância do estado líquido para o estado gasoso após um aquecimento muito rápido, ou seja, é a mudança brusca da fase líquida para a fase de vapor. Ø Exemplos: § Quando uma porção de água é jogada em um chapa quente!

TEMPERATURA E MUDANÇA DE ESTADO Ø É importante saber que a fusão e a solidificação se processam na mesma temperatura, conhecida como ponto de fusão ou ponto de fusão. θF = θ S Temperatura de fusão e solidificação Ø Por exemplo, água se funde a 0ºC e se solidifica a 0ºC.

TEMPERATURA E MUDANÇA DE ESTADO Ø Da mesma forma que a temperatura em que se processa a ebulição também é a temperatura que ocorre a condensação. θV = θ C Temperatura de ebulição e condensação Ø Por exemplo, a água se vaporiza por ebulição à 100ºC e se condensa a 100ºC.

ENERGIA E MUDANÇA DE ESTADO Ø Vimos que o calor é definido como a energia térmica em trânsito de um corpo para o outro. Ø Assim, ao fornecer calor para um pedaço de gelo através de uma chama sabe-se que este derrete (se funde). Ø Ao fornecer calor para um pedaço de ferro nota-se que este se aquece (Varia a temperatura)

ENERGIA E MUDANÇA DE ESTADO Ø Calor sensível: É o calor que provoca apenas variação de temperatura, sem mudar a fase da substância, ou seja, é a quantidade de calor trocada por uma substância enquanto esta estiver na mesma fase. Ø No caso, seria fornecer calor através de uma chama para a chapa de ferro, onde esta varia sua temperatura, mas não seu estado físico. Ø O calor sensível é calculado a partir da equação fundamental da calorimetria. Q = m. c. ∆θ Q = Quantidade de calor sensível; (Cal) m = Massa da substância; (g) c = Calor específico; ( cal/g. ºC) ∆θ = Cº

ENERGIA E MUDANÇA DE ESTADO Ø Calor latente: Quando o efeito do calor gera apenas mudança de estado e a temperatura não varia, ou seja, é a quantidade de calor trocada por uma unidade de massa da substância para que ela mude de fase à temperatura constante. Ø No caso, seria o calor fornecido através de uma chama para o gelo que muda seu estado. Ø O quantidade de calor latente é calculada pela expressão: QL = m. L QL – Quantidade calor latente [Cal] m – Massa da substância [g] L – Calor específico latente [ cal/g]

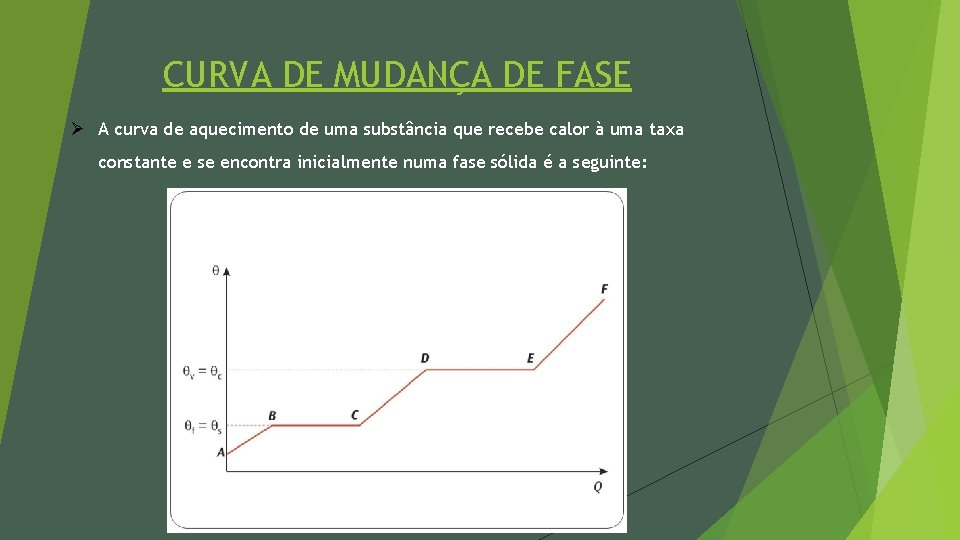
CURVA DE MUDANÇA DE FASE Ø A curva de aquecimento de uma substância que recebe calor à uma taxa constante e se encontra inicialmente numa fase sólida é a seguinte:

CURVA DE MUDANÇA DE FASE Ø AB – Aquecimento da substância na fase sólida. (Variação da Temperatura – Calor sensível). Ø BC – Fusão Da Substância. (Não tem variação da temperatura – Calor Latente). Ø CD – Aquecimento da substância na fase líquida. (Variação da temperatura – Calor sensível). Ø DE – Ebulição da substância. (Não tem variação da temperatura – Calor Latente). Ø EF – Aquecimento da substância na fase gasosa. (Variação de temperatura – calor sensível)

EXERCÍCIOS 1) Qual a quantidade de calor sensível, em Kcal, para aquecer uma barra de ferro de 5 Kg de 10ºC para 100ºC ? Dado calor especifico do ferro = 0, 119 Cal/g. ºC. Resposta : 53, 55 Kcal

EXERCÍCIOS 2) (UNIP) O calor específico latente de fusão do gelo é de 80 cal/g. Para fundir uma massa de gelo de 80 g, sem variação de temperatura, a quantidade de calor latente necessária é de: a) 1, 0 Cal b) 6, 4 Cal c) 6, 4. 103 Cal d) 1, 0 Kcal e) 64 Kcal Resposta: C

EXERCÍCIOS 3) Defina o estado físico em que a frase se refere: a) Esta fase contém Forma bem definida, alta força de atração entre as moléculas e não há movimentação das moléculas. b) Esta fase contém volume bem definido, a forma é a mesma do recipiente que a contém, existe a movimentação de partículas estando essas mais dispersas. c) Esta fase contém forma e volume do recipiente que a contém, partículas dispersas e grande agitação das moléculas. Respostas: a) Sólido b) Líquido c) Gasoso