Dipl kol Nina Harsch Fachbereich Chemie und Pharmazie

Dipl. Ökol. Nina Harsch Fachbereich Chemie und Pharmazie – Institut für Didaktik der Chemie Westfälische Wilhelms-Universität Münster Lehrerfortbildung Luft und Luftbelastung: Experimente zu den Themen Luft, Treibhauseffekt, Ozon und Saurer Regen Eine Zusammenstellung von Nina Harsch Universität Münster Deutschland 2011
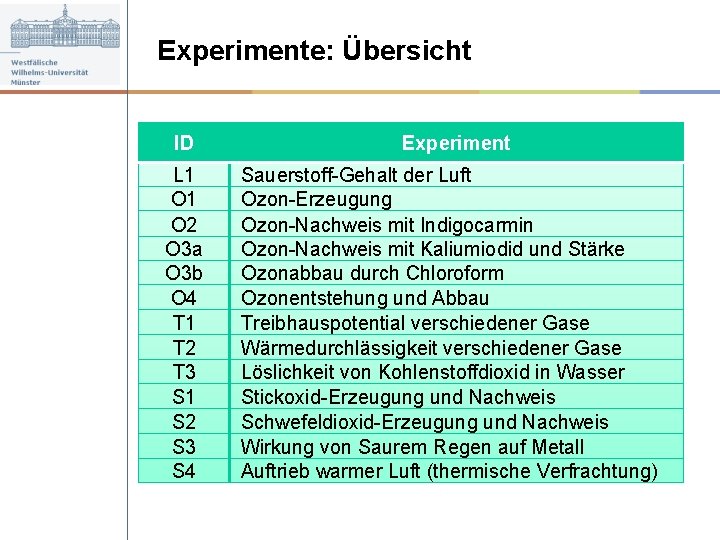
Experimente: Übersicht ID L 1 O 2 O 3 a O 3 b O 4 T 1 T 2 T 3 S 1 S 2 S 3 S 4 Experiment Sauerstoff-Gehalt der Luft Ozon-Erzeugung Ozon-Nachweis mit Indigocarmin Ozon-Nachweis mit Kaliumiodid und Stärke Ozonabbau durch Chloroform Ozonentstehung und Abbau Treibhauspotential verschiedener Gase Wärmedurchlässigkeit verschiedener Gase Löslichkeit von Kohlenstoffdioxid in Wasser Stickoxid-Erzeugung und Nachweis Schwefeldioxid-Erzeugung und Nachweis Wirkung von Saurem Regen auf Metall Auftrieb warmer Luft (thermische Verfrachtung)

Experimente: Luft L 1 Durchführung: 1. Weißen Phosphor auf Verbrennungslöffel entzünden 2. Verbrennungslöffel per Zapfen auf Glasrohr befestigen 3. Glasrohr in wassergefüllte Wanne stellen Beobachtung: Wasser steigt auf 1/5 des Glasrohrvolumens Deutung: Unterdruck bewirkt Aufstieg des Wassers - Weißer Phosphor verbrennt unter Sauerstoffverbrauch zu Rotem Phosphor: P 4 + 5 O 2 → P 4 O 10 - Sauerstoffgehalt im Glasrohr: a) Vor Verbrennung: 21 % Sauerstoff b) Nach Verbrennung: – 21 % Sauerstoff Die Verbrennungswärme bewirkt eine Gasausdehnung im Rohr. Der finale Wasserstand im Rohr wird somit erst nach Abkühlung erreicht. Die Luft, Versuch 2, Educa (2005). Sauerstoff-Gehalt der Luft
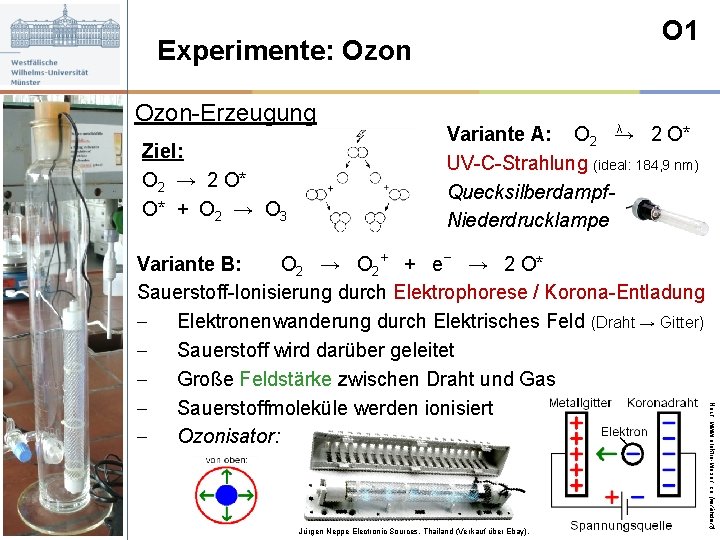
O 1 Experimente: Ozon-Erzeugung Ziel: O 2 → 2 O* O* + O 2 → O 3 λ Variante A: O 2 → 2 O* UV-C-Strahlung (ideal: 184, 9 nm) Quecksilberdampf. Niederdrucklampe Jürgen Neppe Electronic Sources, Thailand (Verkauf über Ebay). Nach: www. elektro-wissen. de (verändert) Variante B: O 2 → O 2+ + e– → 2 O* Sauerstoff-Ionisierung durch Elektrophorese / Korona-Entladung - Elektronenwanderung durch Elektrisches Feld (Draht → Gitter) - Sauerstoff wird darüber geleitet - Große Feldstärke zwischen Draht und Gas - Sauerstoffmoleküle werden ionisiert - Ozonisator:
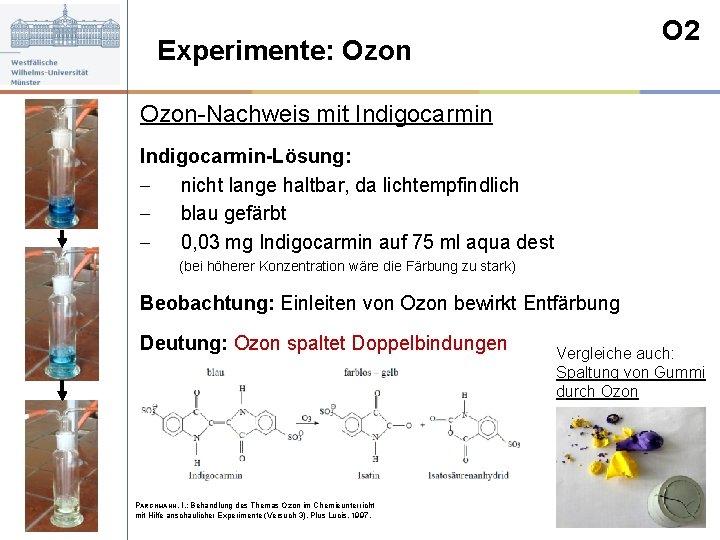
O 2 Experimente: Ozon-Nachweis mit Indigocarmin-Lösung: - nicht lange haltbar, da lichtempfindlich - blau gefärbt - 0, 03 mg Indigocarmin auf 75 ml aqua dest _____(bei höherer Konzentration wäre die Färbung zu stark) Beobachtung: Einleiten von Ozon bewirkt Entfärbung Deutung: Ozon spaltet Doppelbindungen PARCHMANN, I. : Behandlung des Themas Ozon im Chemieunterricht mit Hilfe anschaulicher Experimente (Versuch 3). Plus Lucis, 1997. Vergleiche auch: Spaltung von Gummi durch Ozon

Experimente: Ozon-Nachweis mit Kaliumiodid und Stärke Variante A: Filterpapier (angefeuchtet) Lehrmittel Reinhold, Art. Nr. 5801285 vorher: O 3 a Variante B: Lösung (lagerbar) 1. 0, 5 g Stärke in 100 ml Wasser aufkochen und abkühlen 2. 0, 5 g Kaliumiodid hinzugeben, abfiltrieren Beobachtung: Kontakt mit Ozon bewirkt Blaufärbung nachher: Deutung: Ozon ist ein starkes Oxidationsmittel und oxidiert Iodid zu Iod bildet zusammen mit Stärke einen blau-braunen Komplex. O 3 + H 2 O → H 2 O 2 + O 2 2 I– + H 2 O 2 → I 2 + 2 OH–

O 3 b Experimente: Ozonabbau durch Chloroform 1 Chlor-Radikal kann bis zu 100. 000 Ozonmoleküle spalten! λ CHCl 3 → Cl + CHCl 2 ● ● Cl + O 3 → O 2 + Cl. O ● Cl. O + O* → O 2 + Cl ● Durchführung: 2 Kolben (O 3, CHCl 3), Nachweisreagenz 1. Ozonnachweis positiv: Kaliumiodid-Stärke-Lösung blau 2. Chloroform: Erwärmung (Föhn) flüssig → gasförmig 3. Chloroform + Ozon: Ozonabbau durch Chlor-Radikale 4. Ozonnachweis negativ: Kaliumiodid-Stärke-Lösung farblos
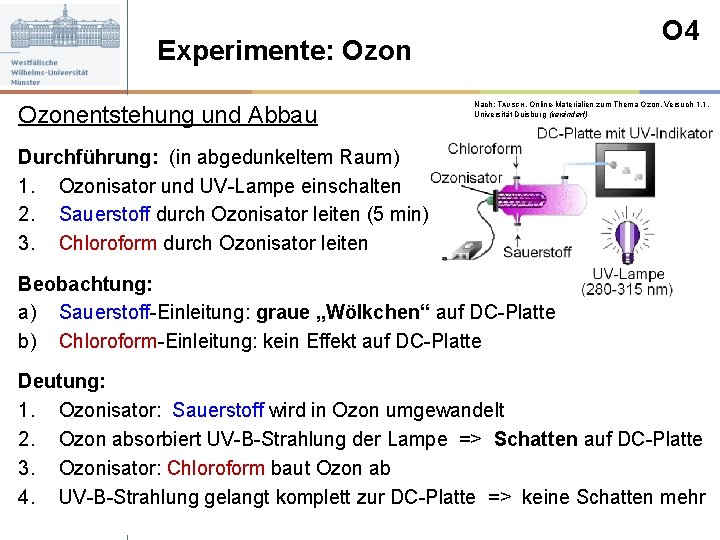
O 4 Experimente: Ozonentstehung und Abbau Nach: TAUSCH, Online-Materialien zum Thema Ozon, Versuch 1. 1, Universität Duisburg (verändert) Durchführung: (in abgedunkeltem Raum) 1. Ozonisator und UV-Lampe einschalten 2. Sauerstoff durch Ozonisator leiten (5 min) 3. Chloroform durch Ozonisator leiten Beobachtung: a) Sauerstoff-Einleitung: graue „Wölkchen“ auf DC-Platte b) Chloroform-Einleitung: kein Effekt auf DC-Platte Deutung: 1. Ozonisator: Sauerstoff wird in Ozon umgewandelt 2. Ozon absorbiert UV-B-Strahlung der Lampe => Schatten auf DC-Platte 3. Ozonisator: Chloroform baut Ozon ab 4. UV-B-Strahlung gelangt komplett zur DC-Platte => keine Schatten mehr

Experimente: Treibhauseffekt T 1 Treibhauspotential verschiedener Gase Durchführung: 1. Mehrere Rundkolben mit verschiedenen Gasen befüllen z. B. : N 2, O 2, CO 2, O 3, NOx, SO 2, Luft (normal / gesättigt) → wasserdampfgesättigte Luft: einige Tropfen H 2 O in Kolben geben und schütteln 2. 3. Kolben verschließen und mit Infrarotlampen bestrahlen Temperaturverläufe in den Kolben über 5 min messen Beobachtung: Temperaturänderung je Gas unterschiedlich Deutung: Treibhausgase absorbieren Wärmestrahlung. Dadurch erhöht sich die Temperatur in den jeweiligen Kolben um bis zu 5 °C.

Experimente: Treibhauseffekt T 2 Wärmedurchlässigkeit verschiedener Gase Aufbau: - Papprohr beidseitig dicht mit Frischhaltefolie verschließen - Oberseite: Evtl. Löcher für Gas -Einlass und Gas-Auslass - Heizplatte: Volle Leistung Durchführung: 1. Blindprobe: IR-Messung mit und ohne Rohr (50 cm Distanz) Ø Beide Werte liegen bei rund 70°C, Rohr und Folie haben somit keinen störenden Einfluss 2. 3. Rohr mit jeweils zu testendem Gas befüllen Rohr verschließen und IR-Durchlässigkeit je Gas messen Beobachtung: IR-Durchlässigkeit je Gas unterschiedlich Deutung: Treibhausgase absorbieren Wärmestrahlung. Dadurch fällt die IR-Messung hinter dem Rohr bei Treibhausgasen geringer aus. Beispiel CO 2: ΔT = 10°C

Experimente: Treibhauseffekt T 3 Löslichkeit von Kohlenstoffdioxid in Wasser Durchführung: 1. Wassergefüllten Messkolben mit Öffnung nach unten in wassergefüllten Behälter hängen (kein Bodenkontakt) 2. Brausetablette unter Kolbenöffnung legen 3. Nach Verbrauch: Weitere Brausetablette Beobachtung: - Tablette 1: Wasserstand im Kolben sinkt kaum - Tablette 2: Wasserstand im Kolben sinkt stark Deutung: Kohlenstoffdioxid löst sich in Wasser: CO 2 + H 2 O → H 2 CO 3 Tablette 1: Es kann noch viel CO 2 im Wasser gelöst werden Tablette 2: Wasser ist weitgehend gesättigt, d. h. kaum Lösung Variante: Unterschiedliche Temperaturen. Wärmeres Wasser: Weniger CO 2 in Lösung.
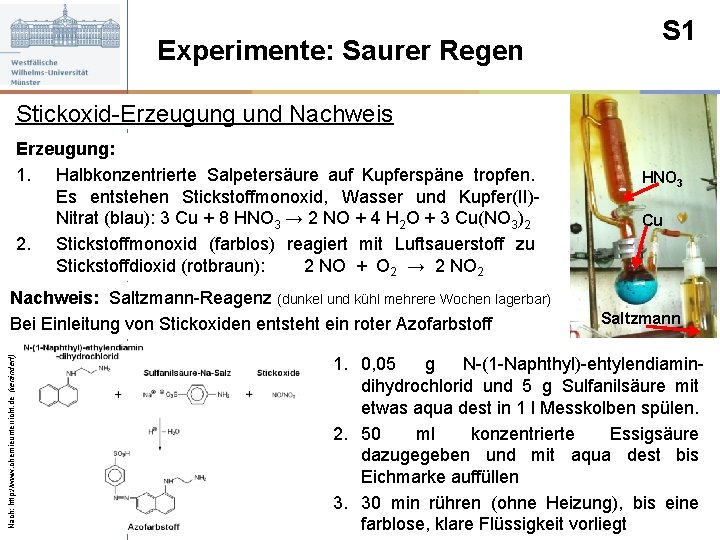
Experimente: Saurer Regen S 1 Stickoxid-Erzeugung und Nachweis Erzeugung: 1. Halbkonzentrierte Salpetersäure auf Kupferspäne tropfen. Es entstehen Stickstoffmonoxid, Wasser und Kupfer(II)Nitrat (blau): 3 Cu + 8 HNO 3 → 2 NO + 4 H 2 O + 3 Cu(NO 3)2 2. Stickstoffmonoxid (farblos) reagiert mit Luftsauerstoff zu Stickstoffdioxid (rotbraun): 2 NO + O 2 → 2 NO 2 Nach: http: //www. chemieunterricht. de (verändert) Nachweis: Saltzmann-Reagenz (dunkel und kühl mehrere Wochen lagerbar) Bei Einleitung von Stickoxiden entsteht ein roter Azofarbstoff HNO 3 Cu Saltzmann 1. 0, 05 g N-(1 -Naphthyl)-ehtylendiamindihydrochlorid und 5 g Sulfanilsäure mit etwas aqua dest in 1 l Messkolben spülen. 2. 50 ml konzentrierte Essigsäure dazugegeben und mit aqua dest bis Eichmarke auffüllen 3. 30 min rühren (ohne Heizung), bis eine farblose, klare Flüssigkeit vorliegt
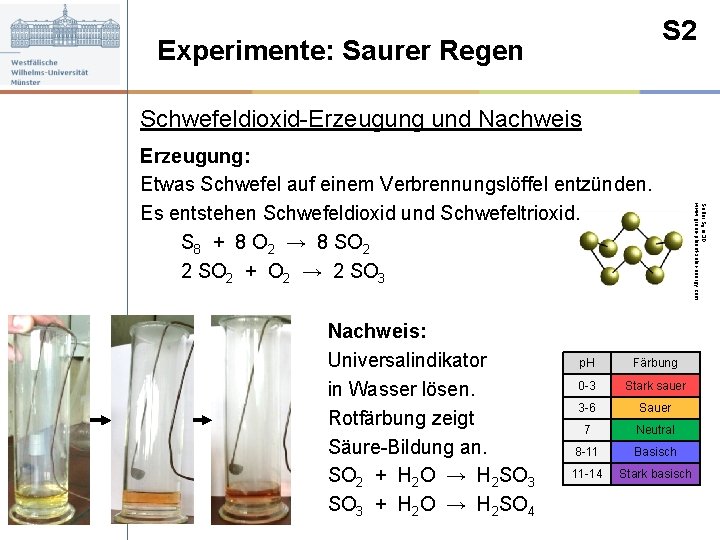
S 2 Experimente: Saurer Regen Schwefeldioxid-Erzeugung und Nachweis: Universalindikator in Wasser lösen. Rotfärbung zeigt Säure-Bildung an. SO 2 + H 2 O → H 2 SO 3 + H 2 O → H 2 SO 4 p. H Färbung 0 -3 Stark sauer 3 -6 Sauer 7 Neutral 8 -11 Basisch 11 -14 Stark basisch Sulfur S 8 in 3 D. www. green-planet-solar-energy. com Erzeugung: Etwas Schwefel auf einem Verbrennungslöffel entzünden. Es entstehen Schwefeldioxid und Schwefeltrioxid. S 8 + 8 O 2 → 8 SO 2 2 SO 2 + O 2 → 2 SO 3

Experimente: Saurer Regen S 3 Wirkung von Saurem Regen auf Metall Durchführung: 1. Schwefelsäure auf Watte geben, Eisenteile darauf legen 2. Einige Tage verschlossen im Einmachglas stehen lassen Beobachtung: Bildung einer rot-braunen Oxidschicht (Rost) Deutung: Säurekorrosion. Die Protonen der Säure entziehen dem Metall Elektronen: Fe + 2 H 3 O+ Fe 2+ + 2 H 2 O + H 2 Das Metall wird oxidiert. 0, 1 -molar 0, 5 -molar

Experimente: Saurer Regen S 4 Auftrieb warmer Luft (thermische Verfrachtung) Durchführung: 1. Teebeutel aufschneiden, entleeren und auffalten 2. Mit Öffnung nach oben aufstellen und oben anzünden Beobachtung: Nach kurzer Zeit steigt der Beutel auf Deutung: Warme Luft (Beutel) hat eine geringere Dichte, als kalte Luft (Umgebung). Es entsteht ein natürlicher Auftrieb. Aufstieg des Beutels: Auftriebskraft > Gravitationskraft
- Slides: 15


























