BIOLOGIE A BIOCHEMIE BUKY ENZYMY RNDr Lenka Pavlasov

BIOLOGIE A BIOCHEMIE BUŇKY ENZYMY RNDr. Lenka Pavlasová, Ph. D.

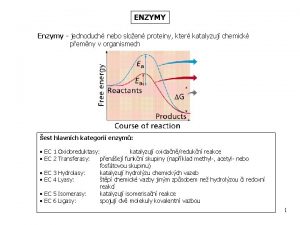
Enzymy jsou bílkovinné povahy V organismech jsou téměř všechny reakce řízeny soubory enzymů – biokatalyzátorů. Vyskytují se u všech živých organismů – od virů až po člověka. Enzymy zvyšují rychlost reakcí, nemění složení vznikajících reakčních směsí. Biochemické reakce probíhají cíleně podle geneticky určeného plánu (struktura enzymů je zapsána v DNA).

Specifita enzymu 1. Reakční (účinková) – podle typu reakce, kterou enzym katalyzuje (např. oxidaci). 2. Substrátová – podle substrátu, který enzym přeměňuje. - absolutní - skupinová

Názvy enzymů 1. Triviální – pepsin, trypsin, amylasa, hydrolasa (koncovka –in nebo –asa) 2. Systémové – složité, vypovídají o substrátu i katalyzované reakci, koncovka –asa, nejsou vhodné pro běžné použití

Klasifikace enzymů Enzymy se dělí do 6 tříd podle povahy chemické reakce, kterou katalyzují. Každý enzym je označen dvěma názvy a čtyřmi čísly. EC 1. 1. Alkoholdehydrogenasa (ADH) Alkohol: NAD+ - oxidoreduktasa

Stavba molekuly enzymu Bílkovinná část (jedna nebo více podjednotek). Nebílkovinná část = kofaktor. Kofaktor – kovové ionty (Zn++) nebo organické molekuly (koenzymy). Kofaktor může být vázán kovalentně nebo nekovalentně.

Koenzymy účastnící se enzymových reakcí se v těchto reakcích chemicky mění. Aby se uzavřel katalytický cyklus, musí se koenzymy regenerovat často další enzymovou reakcí. Např. oxidovaná a redukovaná forma NAD (NAD+, NADH + H+)
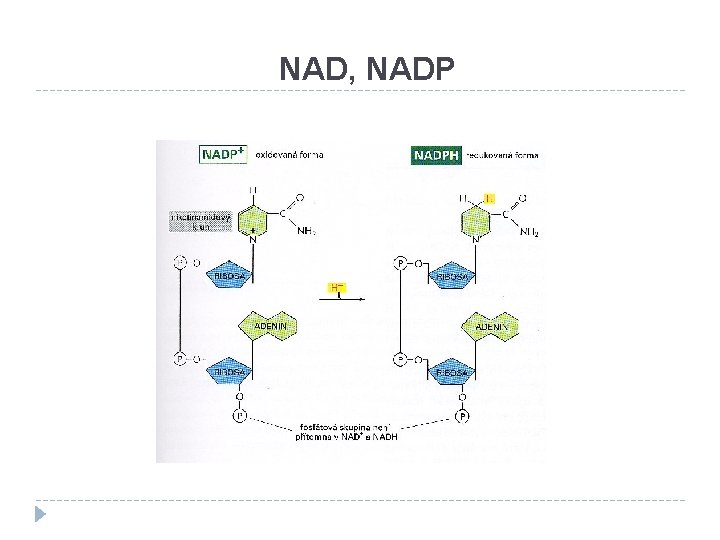
NAD, NADP
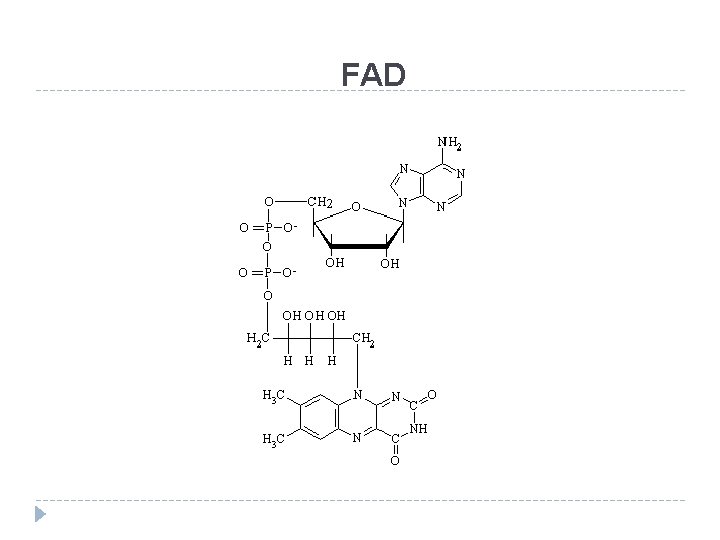
FAD

Mnoho organismů postrádá schopnost syntetizovat určité části koenzymů a vyžadují tyto látky v potravě – stávají se z nich vitaminy.

Katalytická aktivita Charakterizuje katalytickou účinnost enzymu. 1 katal (kat) = množství enzymu, které přemění za standardních podmínek 1 mol substrátu za 1 sekundu.
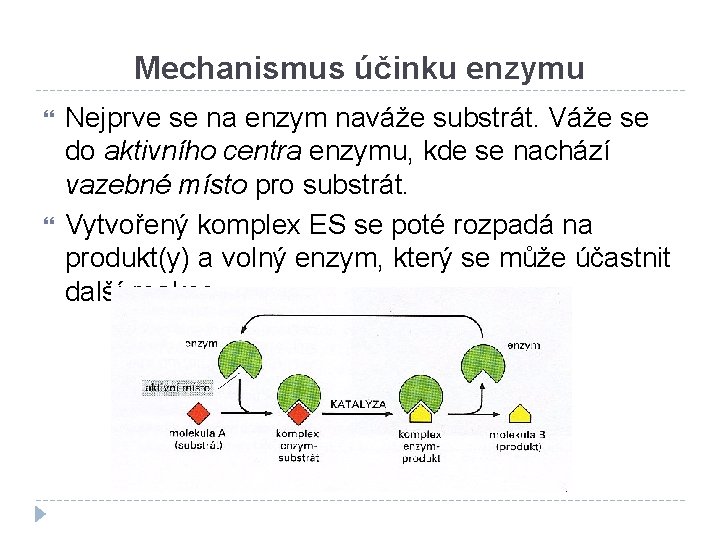
Mechanismus účinku enzymu Nejprve se na enzym naváže substrát. Váže se do aktivního centra enzymu, kde se nachází vazebné místo pro substrát. Vytvořený komplex ES se poté rozpadá na produkt(y) a volný enzym, který se může účastnit další reakce.
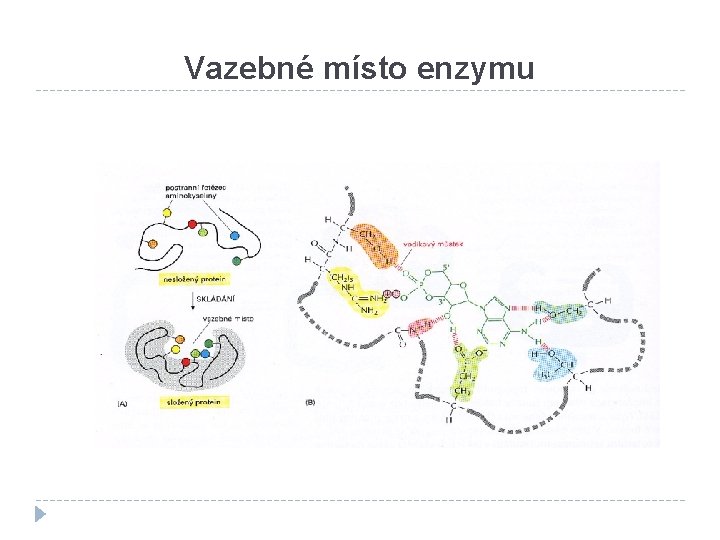
Vazebné místo enzymu

Enzymová kinetika Zkoumá rychlost enzymových reakcí, která závisí na řadě faktorů, např. : 1. na koncentraci přeměňované látky (substrátu) 2. na množství enzymu 3. na teplotě 4. na p. H
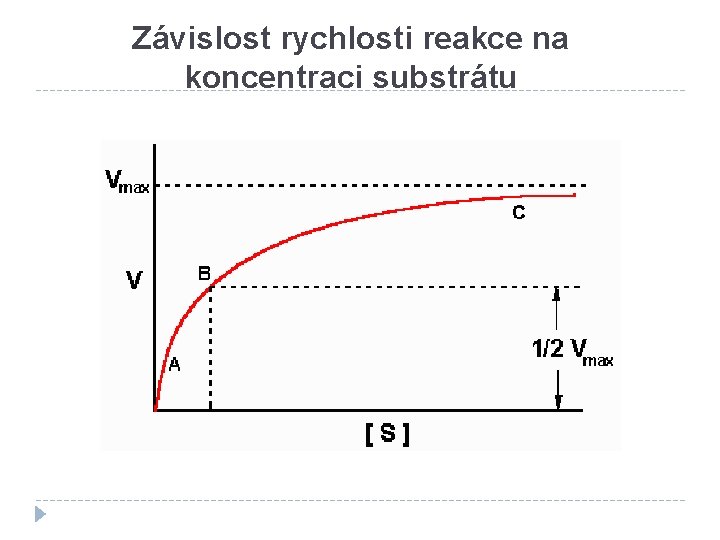
Závislost rychlosti reakce na koncentraci substrátu

Inhibitory enzymů Snižují aktivitu enzymu (opak jsou aktivátory). Použití inhibitorů v praxi: - chemoterapeutika - cytostatika - imunosupresiva - látky hubící plevel, hmyz, jedy

Mechanismus účinku inhibitoru 1. 2. 3. Inhibitor soutěží se substrátem o vazebné místo enzymu (kompetitivní inhibice) Inhibitor se váže na komplex ES, ne na volný enzym (akompetitivní inhibice) Inhibitor se váže jak na volný enzym, tak na komplex ES (smíšená inhibice) …. a tím je znemožněna přeměna substrátu na produkt(y)!

Regulace činnosti enzymů 1. 2. 3. Vhodnou organizací živého systému Inhibicí, aktivací, chemickou modifikací (fosforylace, přeměna proenzymu na aktivní enzym) Zvyšováním nebo snižováním množství enzymu v organismu regulací jeho syntézy nebo odbourávání

Metabolické funkce eukaryotních organel Mitochondrie: citrátový cyklus, oxidační fosforylace, oxidace mastných kyselin Cytosol: glykolýza, pentosový cyklus, syntéza mastných kyselin Jádro: replikace a transkripce DNA, opracování RNA Golgiho aparát: posttranslační opracování membránových a sekrečních proteinů, tvorba membrány a sekrečních váčků

Metabolické funkce eukaryotních organel Drsné endoplazmatické retikulum: syntéza membránově vázaných a sekrečních proteinů Hladké endoplazmatické retikulum: syntéza lipidů a steroidů Lysosomy: enzymové trávení buněčných složek a pohlcených látek Glyoxysomy (u rostlin): reakce glyoxylátového cyklu
- Slides: 20