Biologie Biochemie Chemie M Kresken 1 Biologie Naturwissenschaft

Biologie – Biochemie – Chemie M. Kresken 1

Biologie • Naturwissenschaft, die sich mit den lebenden Wesen, d. h. Mensch (Anthropologie), Tier (Zoologie), Pflanze (Botanik) und Mikroorganismus (Mikrobiologie) sowie mit ihrem Stoffwechsel und ihrem Verhalten auf Reize, beschäftigt. M. Kresken 2

Chemie • Naturwissenschaft, die sich mit Substanzen und ihren Eigenschaften sowie mit Substanzveränderungen befasst: Analysen und Synthesen, Strukturaufklärung, Reaktionen… • Anorganische Chemie, Organische Chemie, Physikalische Chemie, Lebensmittelchemie, Petrochemie, Technische Chemie, Umweltchemie… M. Kresken 3

Biochemie • Lehre von den chemischen Vorgängen bei der Atmung, Verdauung, Fortpflanzung, Bewegung. . . in Lebewesen • Untersucht den chemischen Aufbau und die Stoffwechselvorgänge in pflanzlichen, tierischen und menschlichen Zellen M. Kresken 4

Leben • „dynamisches Fließgleichgewicht“ (Zitat: Lehninger, Biochemie) • Der Organismus stellt kein „geschlossenes Reaktionsgefäß“ dar, sondern ist „im Fluss der Stoffe“ nach zwei Seiten offen: Nahrung + O 2 → ▓ → CO 2 + Abfallprodukte M. Kresken 5

Verflechtung der organischen Chemie M. Kresken 6

Von der Zelle zum Atom M. Kresken 7

Größen • • • • 10 1 m (10 m) = mittlere Höhe von Bäumen 10 0 m (1 m) = Höhe eines Tisches 10 -1 m (1 dm) = Länge einer Hand 10 -2 m (1 cm) = Breite eines Fingernagels 10 -3 m (1 mm) = Durchmesser von Wassertropfen 10 -4 m (100 µm) = Dicke eines Haares 10 -5 m (10 µm) = Dicke von Blattgold 10 -6 m (1 µm) = Durchmesser von Bakterien 10 -7 m (100 nm) = Durchmesser von Viren 10 -9 m (1 nm) = Durchmesser von Molekülen 10 -10 m (100 pm) = Durchmesser des Wasserstoffatoms 10 -14 m = mittlerer Durchmesser von Atomkernen 10 -15 m = theoretischer Durchmesser des Elektrons M. Kresken 8

Größen • 1 Å (10 -10 m) = Durchmesser des Wasserstoffatoms • 10 000 Å (10 -6 m) = Durchmesser von Bakterien M. Kresken 9
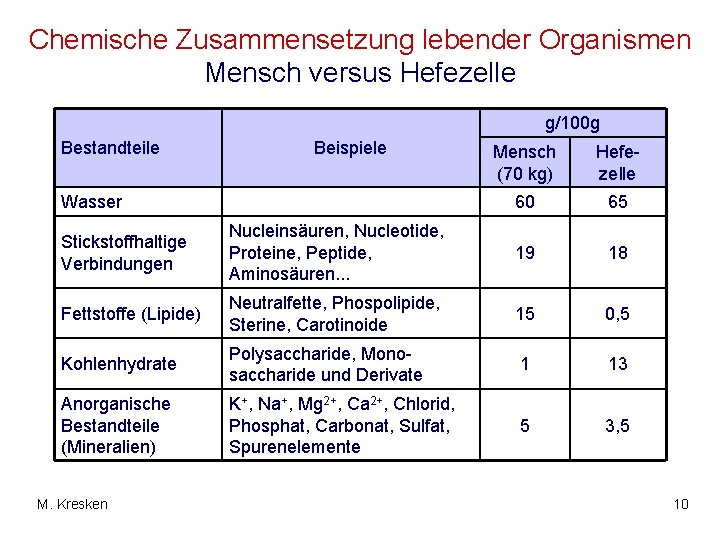
Chemische Zusammensetzung lebender Organismen Mensch versus Hefezelle g/100 g Bestandteile Beispiele Wasser Mensch (70 kg) Hefezelle 60 65 Stickstoffhaltige Verbindungen Nucleinsäuren, Nucleotide, Proteine, Peptide, Aminosäuren. . . 19 18 Fettstoffe (Lipide) Neutralfette, Phospolipide, Sterine, Carotinoide 15 0, 5 Kohlenhydrate Polysaccharide, Monosaccharide und Derivate 1 13 Anorganische Bestandteile (Mineralien) K+, Na+, Mg 2+, Ca 2+, Chlorid, Phosphat, Carbonat, Sulfat, Spurenelemente 5 3, 5 M. Kresken 10
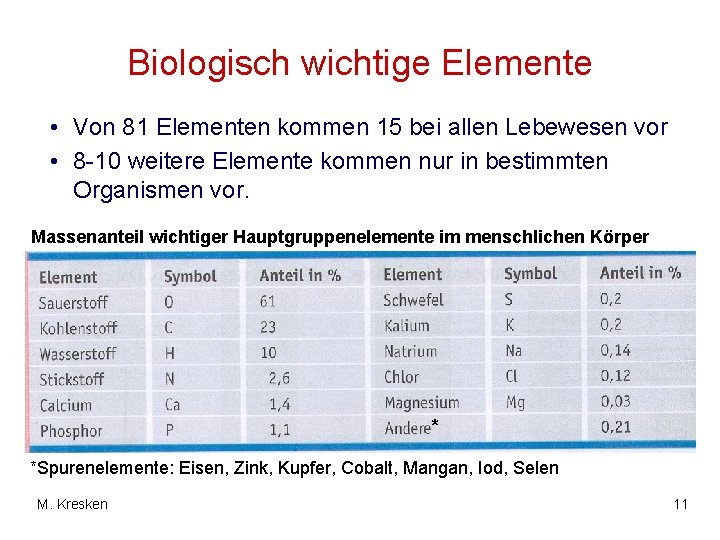
Biologisch wichtige Elemente • Von 81 Elementen kommen 15 bei allen Lebewesen vor • 8 -10 weitere Elemente kommen nur in bestimmten Organismen vor. Massenanteil wichtiger Hauptgruppenelemente im menschlichen Körper * *Spurenelemente: Eisen, Zink, Kupfer, Cobalt, Mangan, Iod, Selen M. Kresken 11

Biologisch wichtige Elemente • Über 99% der Atome im tierischen Organismus entfallen auf nur vier Elemente: Wasserstoff (H), Sauerstoff (O), Kohlenstoff (C), Stickstoff (N). • Diese Atome sind auch Hauptbestandteile der organischen Verbindungen. • Viele Biomoleküle enthalten zusätzlich Schwefel (S) oder Phosphor (P) M. Kresken 12
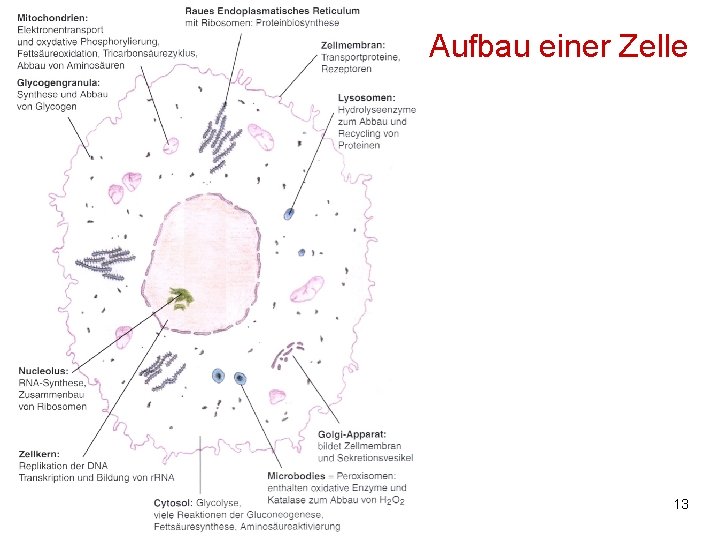
Aufbau einer Zelle M. Kresken 13
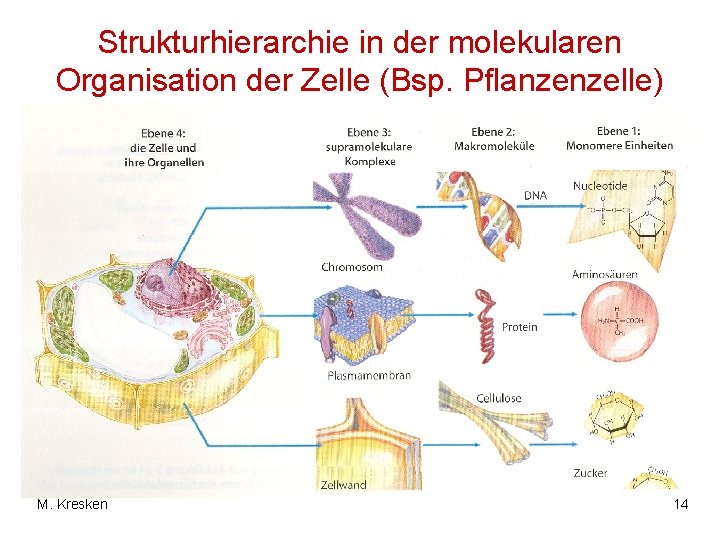
Strukturhierarchie in der molekularen Organisation der Zelle (Bsp. Pflanzenzelle) M. Kresken 14
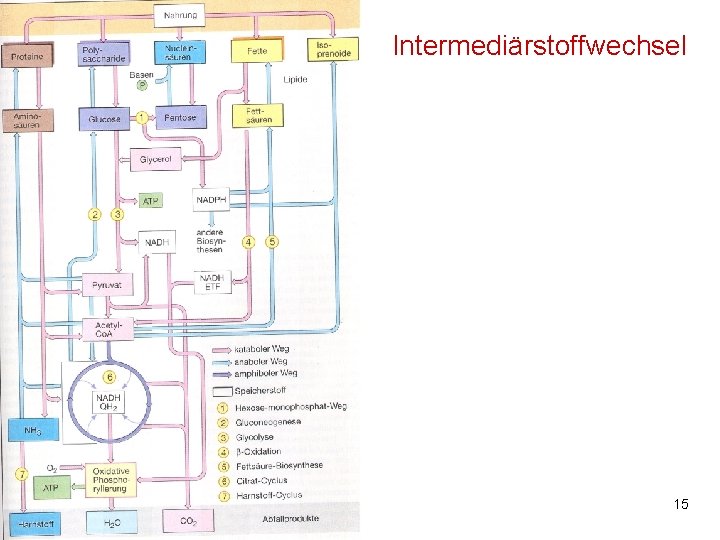
Intermediärstoffwechsel M. Kresken 15

Grundlagen der Chemie M. Kresken 16

Aufbau der Atome M. Kresken 17

Aufbau der Atome • Die Eigenschaften aller Stoffe gehen auf die Struktur und die Anordnung der kleinsten Teilchen zurück, aus dem diese Stoffe bestehen. • Die kleinsten Teilchen, die chemisch zugänglich sind, sind Atome. Þ griechisch atomos: unteilbar Þ Daltons Atommodell 1808: Atome werden als winzig kleine Kugeln betrachtet. • Mit physikalischen Methoden können Atome weiter zerlegt werden. Þ Rutherfordsche Streuversuche: Kern-Hülle-Modell 1911 - Das Atom besteht aus einem winzigen, positiv geladenen Atomkern und der Atomhülle, in der sich kugelförmige Elektronen befinden. M. Kresken 18
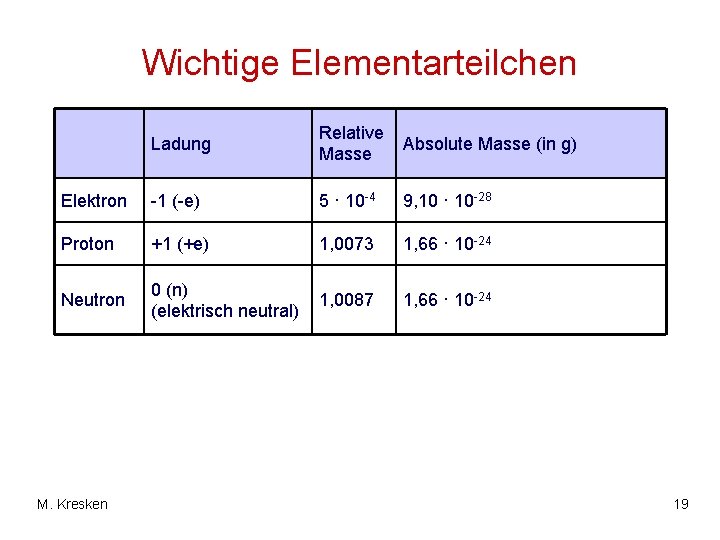
Wichtige Elementarteilchen Ladung Relative Masse Absolute Masse (in g) Elektron -1 (-e) 5 · 10 -4 9, 10 · 10 -28 Proton +1 (+e) 1, 0073 1, 66 · 10 -24 Neutron 0 (n) (elektrisch neutral) 1, 0087 1, 66 · 10 -24 M. Kresken 19
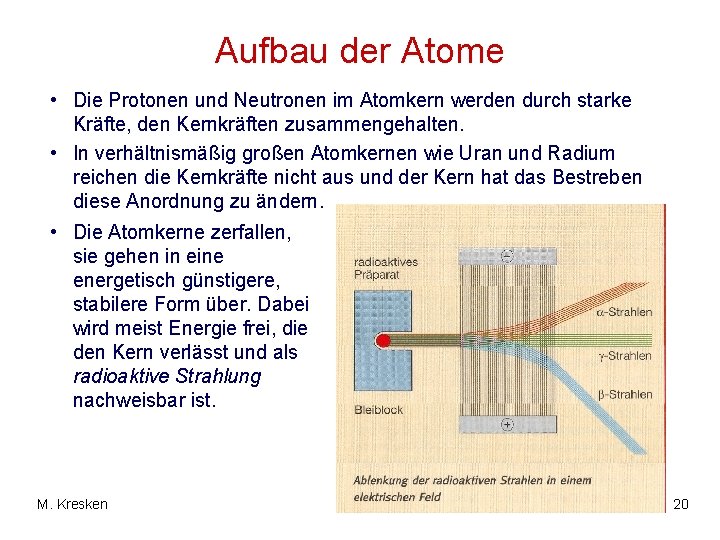
Aufbau der Atome • Die Protonen und Neutronen im Atomkern werden durch starke Kräfte, den Kernkräften zusammengehalten. • In verhältnismäßig großen Atomkernen wie Uran und Radium reichen die Kernkräfte nicht aus und der Kern hat das Bestreben diese Anordnung zu ändern. • Die Atomkerne zerfallen, sie gehen in eine energetisch günstigere, stabilere Form über. Dabei wird meist Energie frei, die den Kern verlässt und als radioaktive Strahlung nachweisbar ist. M. Kresken 20

Aufbau der Atome • Isotope: Atomsorten eines Elementes mit gleicher Protonen-Anzahl, jedoch unterschiedlicher Neutronen. Anzahl (Nuclide) - griechisch iso: gleich, topo: Ort • Natürlicher Kohlenstoff (6 Protonen) ist aus 12 C (6 n), 13 C (7 n) und 14 C* (8 n) gemischt und weist die Atommasse 12, 011 auf. M. Kresken 21

Elektronenhülle • Die Wechselwirkungen zwischen Atomen beruhen auf Wechselwirkungen zwischen ihren Elektronenhüllen. • Die Zahl, die räumliche Anordnung und die Energie der Elektronen in der Atomhülle prägen das chemische Verhalten, die chemischen Eigenschaften der Stoffe. M. Kresken 22

Elektronenhülle • Bohrsches Atommodell von 1913: Elektronen als punktförmige Ladungen umkreisen den Atomkern in bestimmten dünnen Schichten (Schalen) M. Kresken 23

Elektronenverteilung • Jede Schale kann maximal nur eine bestimmte Anzahl an Elektronen aufnehmen: - Zahl der Elektronen = 2 x Schalennummer 2 - 2 x 12 = 2, 2 x 22 = 8, 2 x 32 = 18 usw. • Die Besetzung der Schalen mit Elektronen erfolgt von innen nach außen. • Jede Schale entspricht einer bestimmten Energiestufe. Die innerste Schale weist die niedrigste Energie auf. M. Kresken 24

Darstellung der Aufenthaltswahrscheinlichkeitsdichte der ersten (2 Elektronen) und zweiten (8 Elektronen) Elektronenschale Atomorbitale sind Elektronen-Wellenfunktionen M. Kresken 25
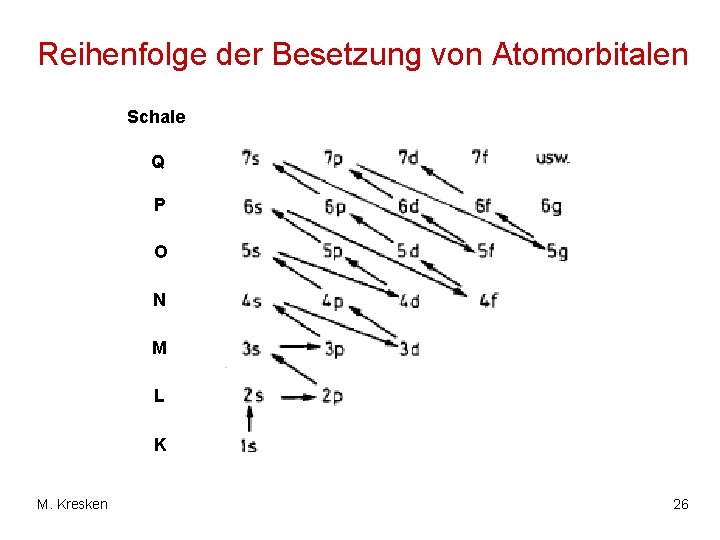
Reihenfolge der Besetzung von Atomorbitalen Schale Q P O N M L K M. Kresken 26

Besetzung von Atomorbitalen M. Kresken 27

Periodensystem der Elemente M. Kresken 28
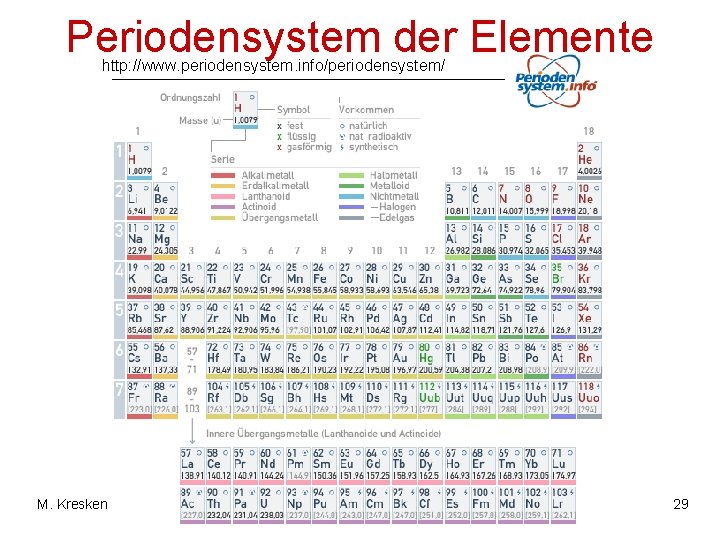
Periodensystem der Elemente http: //www. periodensystem. info/periodensystem/ M. Kresken 29
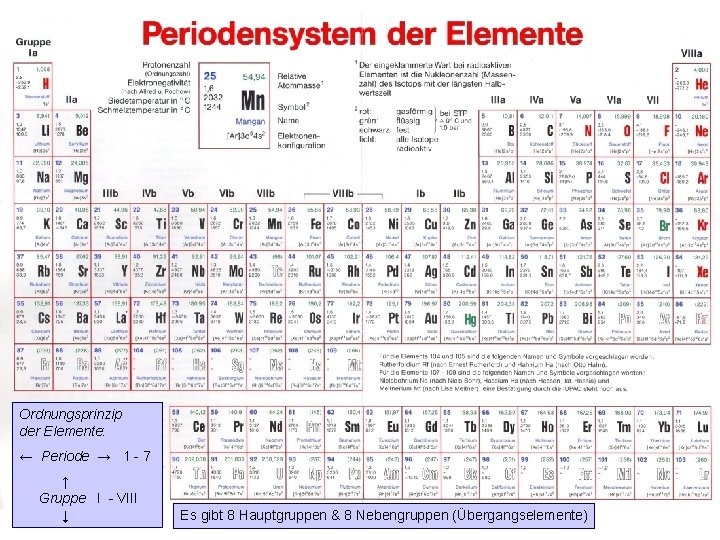
Ordnungsprinzip der Elemente: ← Periode → 1 - 7 ↑ Gruppe I - VIII M. Kresken ↓ Es gibt 8 Hauptgruppen & 8 Nebengruppen (Übergangselemente) 30

Periodensystem der Elemente (alte Nomenklatur) • Ordnungszahl: Anzahl der Protonen bzw. Anzahl der Elektronen • Nucleonenzahl (Massenzahl): Anzahl der Protonen plus Anzahl der Neutronen* • Hauptgruppennummer: Anzahl der Außenelektronen • Periodennummer: Anzahl der besetzten Schalen 2 3 M. Kresken *Chlor kommt in der Natur mit zwei Atomarten (Nucliden) vor, die 18 bzw. 20 Neutronen neben jeweils 17 Protonen im Kern enthalten. 31

Periodensystem der Elemente • Edelgase: Bei den Edelgasen sind die äußersten Elektronenschalen voll besetzt: He 1 s 2, Ne 2 s 2 p 6, Ar 3 s 2 p 6 usw. Sie sind daher extrem reaktionsträge. M. Kresken 32

Periodensystem der Elemente (alte Nomenklatur) • Biochemisch wichtige Hauptgruppenelemente sind - 1. Gruppe: Wasserstoff (H), Natrium (Na), Kalium (K) - 2. Gruppe: Magnesium (Mg), Calcium (Ca) - 4. Gruppe: Kohlenstoff (C) - 5. Gruppe: Stickstoff (N), Phosphor (P) - 6. Gruppe: Sauerstoff (O), Schwefel (S) - 7. Gruppe: Fluor (F), Chlor (Cl), Iod (I) • Biochemisch wichtige Nebengruppenelemente sind - Eisen (Fe), Cobalt (Co), Kupfer (Cu), Zink (Zn), Chrom (Cr), Molybdän (Mo), Mangan (Mn) M. Kresken 33

Valenzelektronenzahl • Die Elektronen in der äußersten Schale der Elemente sind für ihre chemischen und z. T. physikalischen Eigenschaften verantwortlich. • Mit Hilfe dieser Elektronen können Elemente verknüpft werden, d. h. Bindungen (Valenzen) ausbildet werden. • Man nennt diese Außenelektronen auch Valenzelektronen. • Die Valenzelektronen bestimmen somit das chemische Verhalten der Elemente. M. Kresken 34

Oxidationsstufen • Wird einem neutralen chemischen Element ein Valenzelektron entrissen, wird es einfach positiv geladen. - Es entsteht einwertiges Kation. - Das Element wird oxidiert, seine Oxidationsstufe ist +1. • Die Oxidationszahl -1 erhält man, wenn einem neutralen Element ein Valenzelektron zusätzlich hinzugefügt wird. - Es entsteht ein Anion. M. Kresken 35

Ionen • Als Ionen bezeichnet man geladene Teilchen (Atome, Moleküle): - Ionen mit Elektronenmangel sind Kationen, - Ionen mit Elektronenüberschuss sind Anionen. • Die jeweilige Ladung wird mit dem entsprechenden Vorzeichen oben rechts an dem Element, Molekül etc. angegeben, z. B. 23+ Cl , SO 4 , Cr M. Kresken 36

Metalle und Nichtmetalle • Die meisten Elemente sind Metalle. • Metalle haben hohe elektrische Leitfähigkeit, metallischen Glanz, kleine Elektronegativitäten, Ionisierungspotentiale und Elektronenaffinitäten. - Sie können in Säuren den Wasserstoff ersetzen und Oxide bilden. - Innerhalb einer Gruppe nimmt der metallische Charakter von oben nach unten zu. - Innerhalb einer Periode nimmt der metallische Charakter von links nach rechts ab. - Eine „Trennungslinie“ bilden die sogenannten Halbmetalle B, Si, Ge, As, Te M. Kresken 37

Metalle und Nichtmetalle (alte Nomenklatur) • Die Metalle der 1. Gruppe werden auch Alkalimetalle genannt. • Die Metalle der 2. Gruppe werden auch Erdalkalimetalle genannt. • Die Elemente der 6. Gruppe sind die sogenannten Chalkogene. • Die Elemente der 7. Gruppe sind die sogenannten Halogene. • In der 8. Gruppe stehen die Edelgase. M. Kresken 38
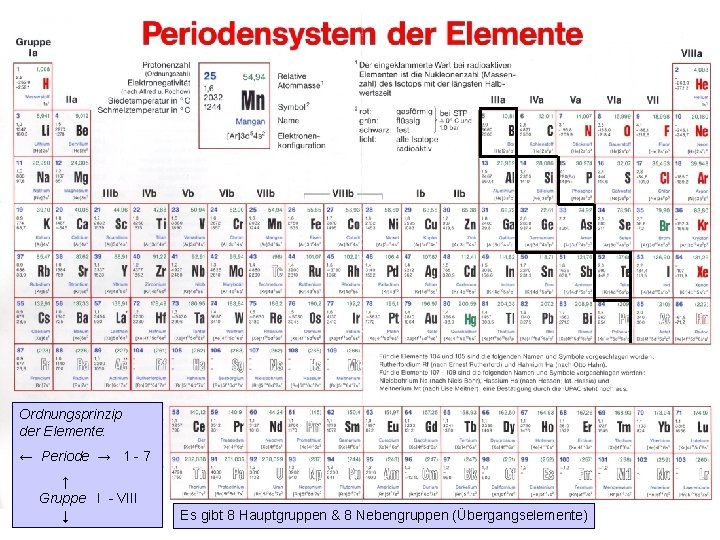
Ordnungsprinzip der Elemente: ← Periode → 1 - 7 ↑ Gruppe I - VIII M. Kresken ↓ Es gibt 8 Hauptgruppen & 8 Nebengruppen (Übergangselemente) 39

Metalle und Nichtmetalle • Nichtmetalle stehen mit Ausnahme des Wasserstoffs im Periodensystem eine bis vier Positionen vor einem Edelgas. - Sie haben relativ hohe Ionisierungspotentiale, relativ große Elektronenaffinitäten (für die einwertigen Anionen) und große Elektronegativitätswerte (außer den Edelgasen). - Sie können untereinander typisch kovalente Verbindungen bilden wie CO 2, SO 2, NO 2 M. Kresken 40
- Slides: 40