WACIWOCI I KLASYFIKACJA ENZYMW ENZYMY Substancje penice w

WŁAŚCIWOŚCI I KLASYFIKACJA ENZYMÓW

ENZYMY Substancje pełniące w komórkach funkcję katalizatora, czyli związku, który przyspiesza reakcje biochemiczne, obniżając ich energię aktywacji

ENERGIA AKTYWACJI Ilość energii potrzebna do zapoczątkowania reakcji
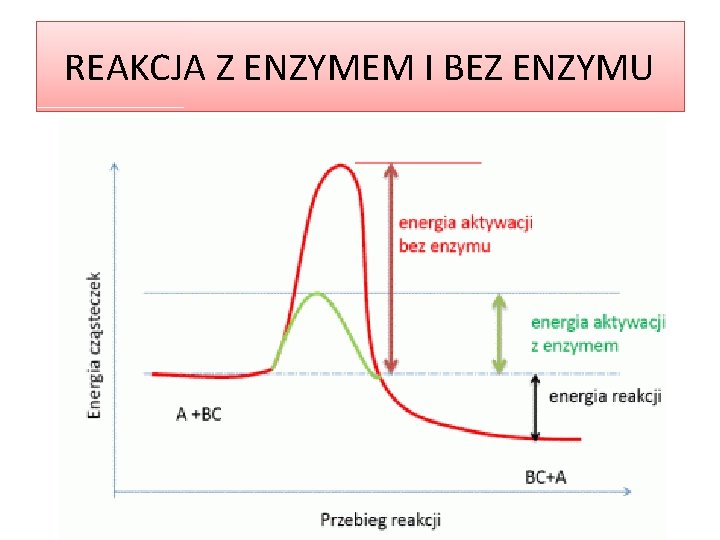
REAKCJA Z ENZYMEM I BEZ ENZYMU

NAZEWNICTWO I KLASYFIKACJA • Nazwy enzymów tworzy się przez dodanie końcówki „-aza” do nazw ich substratów lub katalizowanych przez nie reakcji, np. : sacharaza, syntaza ATP • Klasyfikacja: - Oksydoreduktazy (reakcje utleniania i redukcji) - Transferazy (przenoszenie grup funkcyjnych) - Hydrolazy (rozkład z udziałem wody) - Liazy (rozkład bez udziału wody) - Izomerazy (reakcje izomeryzacji) - Ligazy (synteza zw. chem. sprzężona z hydrolizą ATP)

BUDOWA ENZYMÓW • Z białek: amylaza, trypsyna, pepsyna • Z części białkowej – APOENZYM + z części niebiałkowej – KOFAKTOR (metale, grupy prostetyczne, koenzymy) • W części białkowej wyróżnia się centrum aktywne, czyli miejsce przyłączenia substratu

WŁAŚCIWOŚCI ENZYMÓW SĄ SWOISTE WZGLĘDEM SUBSTRATU łączą się wyłącznie z określonym substratem KATALIZUJĄ SWOISTE REAKCJE pojedynczy enzym katalizuje zestaw reakcji jednego typu lub tylko jedną, określoną reakcję NIE ZUŻYWAJĄ SIĘ W PRZEBIEGU REAKCJI mogą być wielokrotnie wykorzystywane
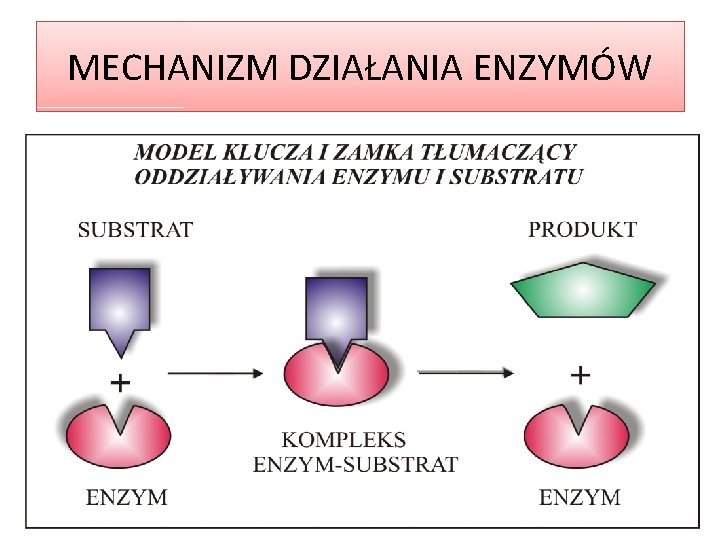
MECHANIZM DZIAŁANIA ENZYMÓW
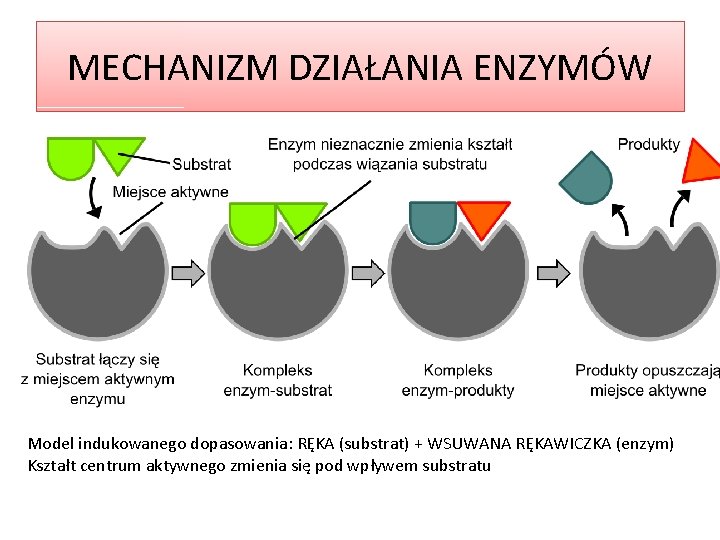
MECHANIZM DZIAŁANIA ENZYMÓW Model indukowanego dopasowania: RĘKA (substrat) + WSUWANA RĘKAWICZKA (enzym) Kształt centrum aktywnego zmienia się pod wpływem substratu

CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI ENZYMATYCZNEJ Stężenie substratu Temperatura Wartość p. H Stężenie soli Aktywatory (substancje podwyższające aktywność enzymu) • Inhibitory (substancje hamujące aktywność) • • •
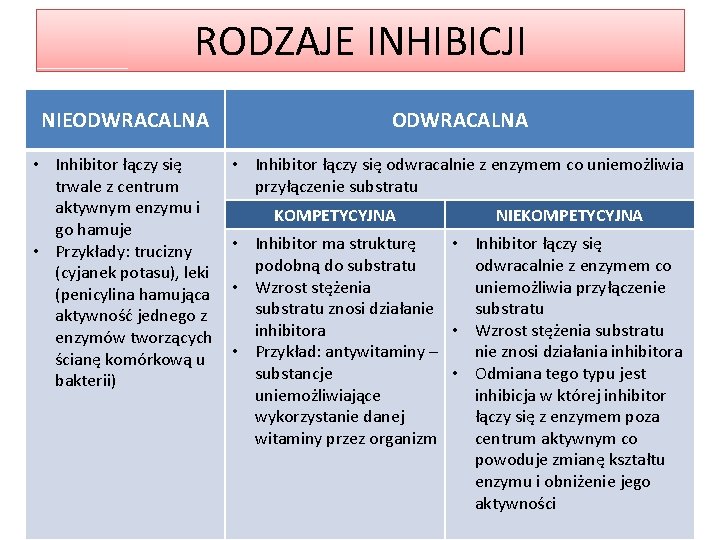
RODZAJE INHIBICJI NIEODWRACALNA • Inhibitor łączy się trwale z centrum aktywnym enzymu i go hamuje • Przykłady: trucizny (cyjanek potasu), leki (penicylina hamująca aktywność jednego z enzymów tworzących ścianę komórkową u bakterii) • Inhibitor łączy się odwracalnie z enzymem co uniemożliwia przyłączenie substratu KOMPETYCYJNA NIEKOMPETYCYJNA • Inhibitor ma strukturę • Inhibitor łączy się podobną do substratu odwracalnie z enzymem co • Wzrost stężenia uniemożliwia przyłączenie substratu znosi działanie substratu inhibitora • Wzrost stężenia substratu • Przykład: antywitaminy – nie znosi działania inhibitora substancje • Odmiana tego typu jest uniemożliwiające inhibicja w której inhibitor wykorzystanie danej łączy się z enzymem poza witaminy przez organizm centrum aktywnym co powoduje zmianę kształtu enzymu i obniżenie jego aktywności

Zadania

Rozwiązanie Zad. 3. 1 A Przykładowe uzasadnienie: • Ponieważ metanol i etanol konkurują o centrum aktywne tego enzymu. • Oba alkohole mają podobną budowę i przyłączają się do centrum aktywnego dehydrogenazy alkoholowej, która katalizuje ich utlenianie. Zad. 3. 2 Przykładowe uzasadnienie: • Cząsteczki etanolu łączące się z dehydrogenazą alkoholową zmniejszają możliwość przyłączenia do niego metanolu, ograniczając w ten sposób ilość powstających szkodliwych produktów utleniania metanolu. • Po spożyciu etanolu zmniejsza się tempo wytwarzania silnie toksycznego aldehydu i kwasu mrówkowego, gdyż cząsteczki etanolu łączą się z dehydrogenazą alkoholową, ograniczając przyłączanie się metanolu.
- Slides: 13