AMINOKYSELINY PEPTIDY BLKOVINY STRUKTURA VLASTNOSTI Mgr Jaroslav Najbert

AMINOKYSELINY, PEPTIDY, BÍLKOVINY – STRUKTURA, VLASTNOSTI Mgr. Jaroslav Najbert
Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Název školy Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Adresa školy IČO Operační program Registrační číslo Označení vzdělávacího materiálu Vzdělávací oblast Vzdělávací obor Tematický okruh Sokolovská 1638 Zhotoveno Ročník červenec, srpen 2012 Anotace Materiál je určen jako studijní v předmětu biochemie, který integruje vzdělávací obory biologie a chemie. Je zaměřen na obecnou charakteristiku, fyzikální a chemické vlastnosti uvedené skupiny látek. Předpokládá zvládnutí učiva obecné chemie, reakčních mechanismů a základy optiky. 620 330 26 Operační program Vzdělávání pro konkurenceschopnost CZ. 1. 07/1. 1. 28/01. 0050 K_INOVACE_1. CH. 36 Člověk a příroda Chemie Přírodní látky Vyšší stupeň osmiletého gymnázia a čtyřleté gymnázium (RVP – G)

Obecná charakteristika Dusíkaté substituční deriváty karboxylových kyselin, obsahují skupinu NH 2. Tvoří homologickou řadu aminokyseliny – peptidy – bílkoviny podle počtu aminokyselin, které molekulu tvoří. aminokyseliny peptidy bílkoviny 2 -100 aminokyselin olygopeptidy 2 – 10 aminokyselin dipeptid tripeptid >100 aminokyselin polypeptidy 11 – 100 aminokyselin tetrapeptid…. .
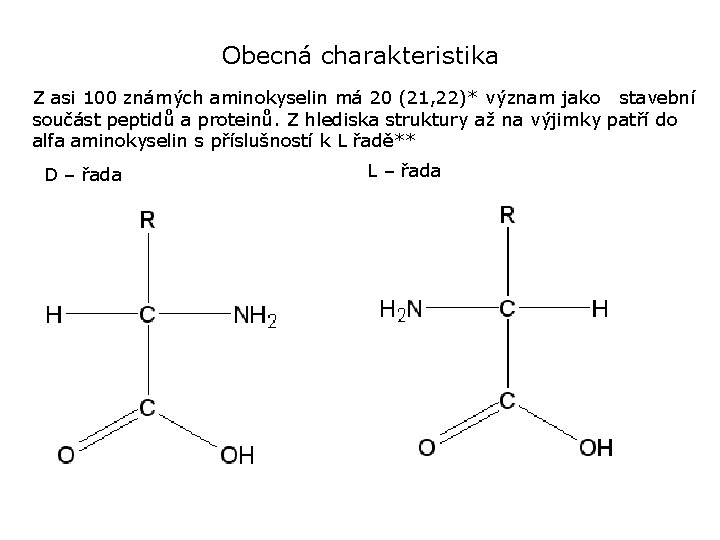
Obecná charakteristika Z asi 100 známých aminokyselin má 20 (21, 22)* význam jako stavební součást peptidů a proteinů. Z hlediska struktury až na výjimky patří do alfa aminokyselin s příslušností k L řadě** D – řada L – řada
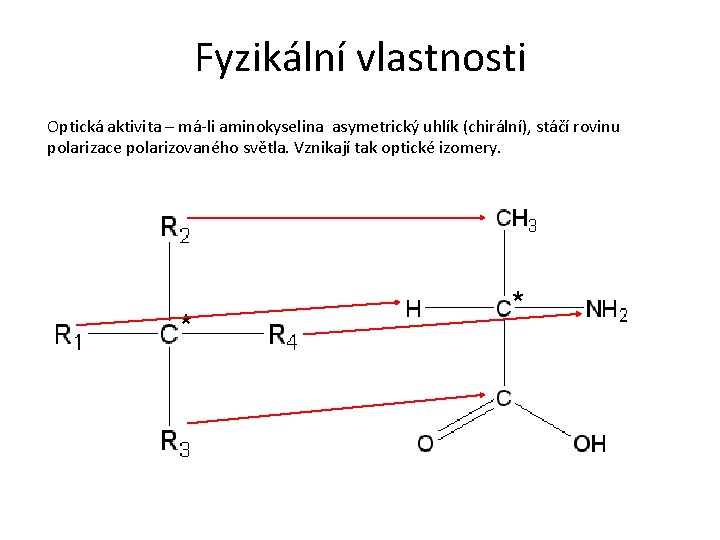
Fyzikální vlastnosti Optická aktivita – má-li aminokyselina asymetrický uhlík (chirální), stáčí rovinu polarizace polarizovaného světla. Vznikají tak optické izomery. * *
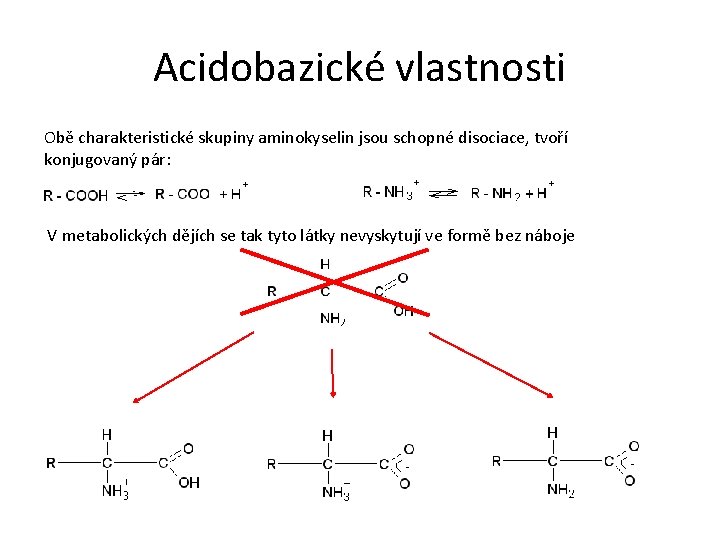
Acidobazické vlastnosti Obě charakteristické skupiny aminokyselin jsou schopné disociace, tvoří konjugovaný pár: V metabolických dějích se tak tyto látky nevyskytují ve formě bez náboje
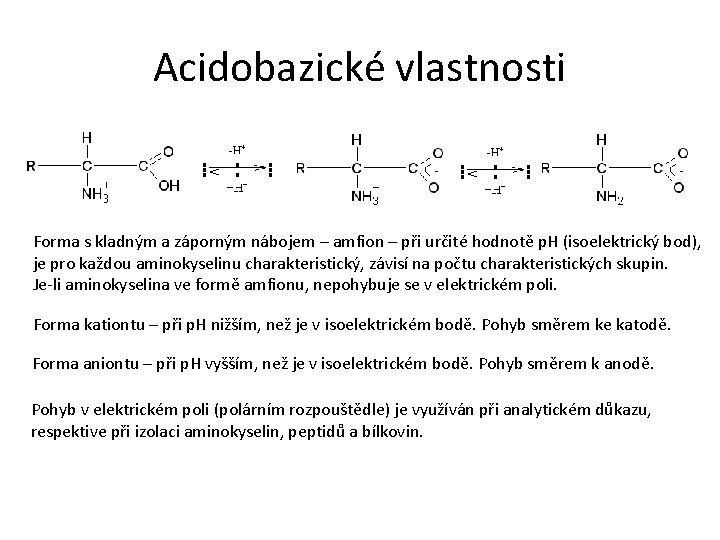
Acidobazické vlastnosti Forma s kladným a záporným nábojem – amfion – při určité hodnotě p. H (isoelektrický bod), je pro každou aminokyselinu charakteristický, závisí na počtu charakteristických skupin. Je-li aminokyselina ve formě amfionu, nepohybuje se v elektrickém poli. Forma kationtu – při p. H nižším, než je v isoelektrickém bodě. Pohyb směrem ke katodě. Forma aniontu – při p. H vyšším, než je v isoelektrickém bodě. Pohyb směrem k anodě. Pohyb v elektrickém poli (polárním rozpouštědle) je využíván při analytickém důkazu, respektive při izolaci aminokyselin, peptidů a bílkovin.
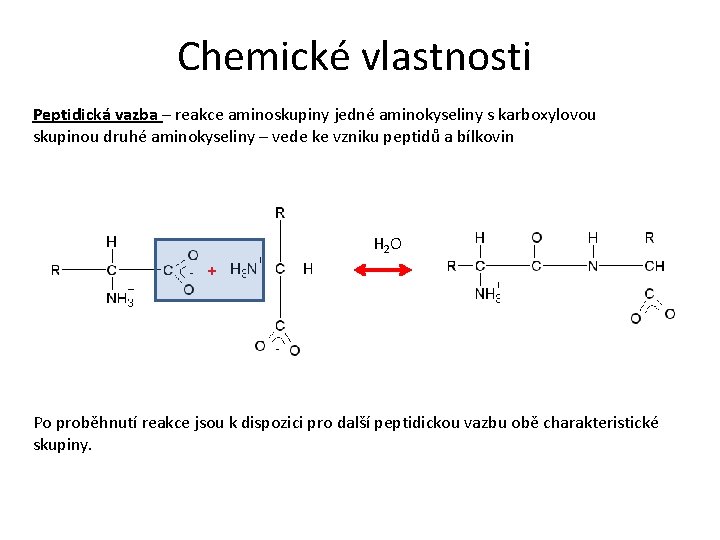
Chemické vlastnosti Peptidická vazba – reakce aminoskupiny jedné aminokyseliny s karboxylovou skupinou druhé aminokyseliny – vede ke vzniku peptidů a bílkovin H 2 O + Po proběhnutí reakce jsou k dispozici pro další peptidickou vazbu obě charakteristické skupiny.
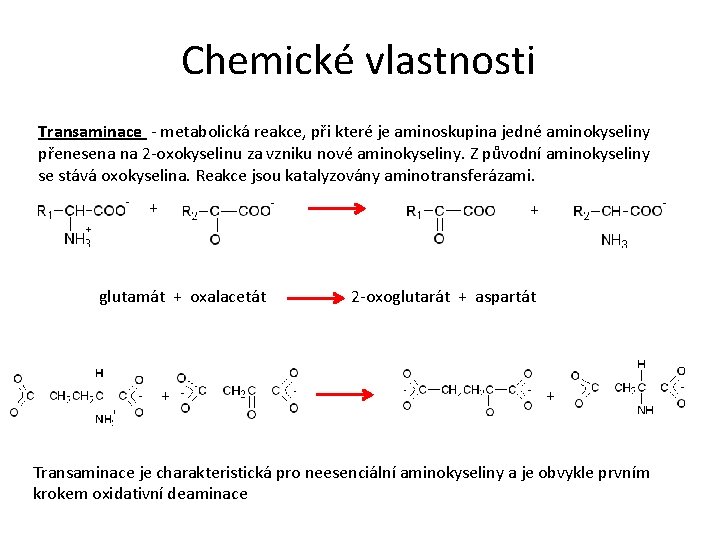
Chemické vlastnosti Transaminace - metabolická reakce, při které je aminoskupina jedné aminokyseliny přenesena na 2 -oxokyselinu za vzniku nové aminokyseliny. Z původní aminokyseliny se stává oxokyselina. Reakce jsou katalyzovány aminotransferázami. + + glutamát + oxalacetát 2 -oxoglutarát + aspartát + + Transaminace je charakteristická pro neesenciální aminokyseliny a je obvykle prvním krokem oxidativní deaminace
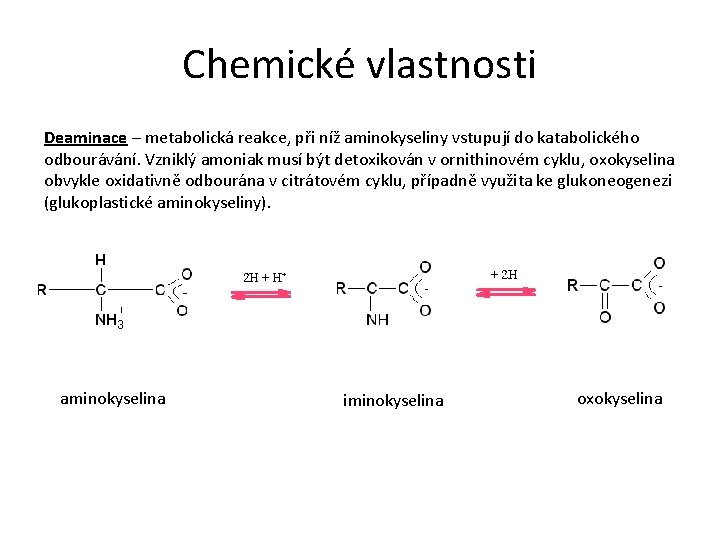
Chemické vlastnosti Deaminace – metabolická reakce, při níž aminokyseliny vstupují do katabolického odbourávání. Vzniklý amoniak musí být detoxikován v ornithinovém cyklu, oxokyselina obvykle oxidativně odbourána v citrátovém cyklu, případně využita ke glukoneogenezi (glukoplastické aminokyseliny). aminokyselina iminokyselina oxokyselina
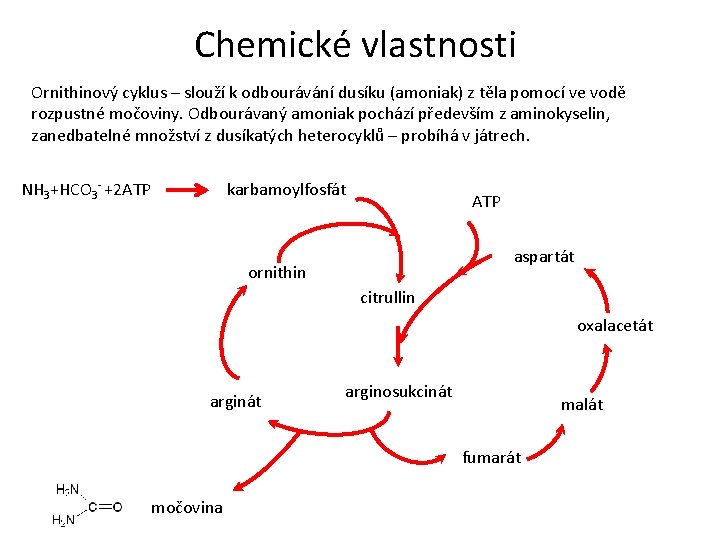
Chemické vlastnosti Ornithinový cyklus – slouží k odbourávání dusíku (amoniak) z těla pomocí ve vodě rozpustné močoviny. Odbourávaný amoniak pochází především z aminokyselin, zanedbatelné množství z dusíkatých heterocyklů – probíhá v játrech. karbamoylfosfát NH 3+HCO 3 - +2 ATP aspartát ornithin citrullin oxalacetát arginosukcinát malát fumarát močovina
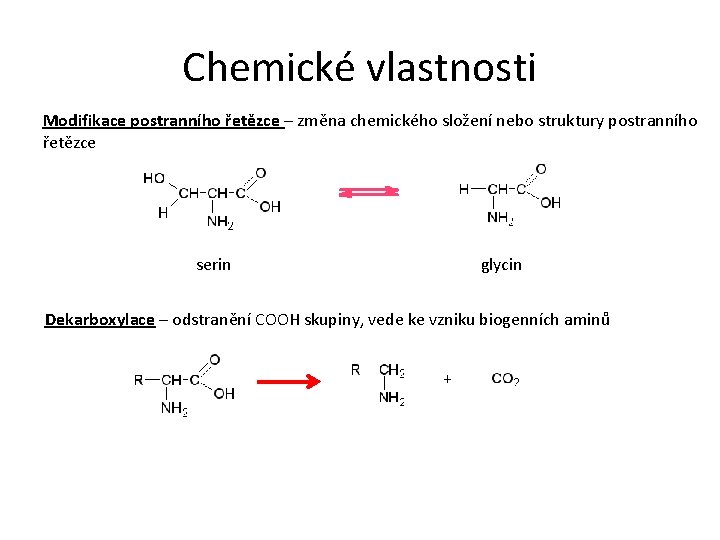
Chemické vlastnosti Modifikace postranního řetězce – změna chemického složení nebo struktury postranního řetězce serin glycin Dekarboxylace – odstranění COOH skupiny, vede ke vzniku biogenních aminů +
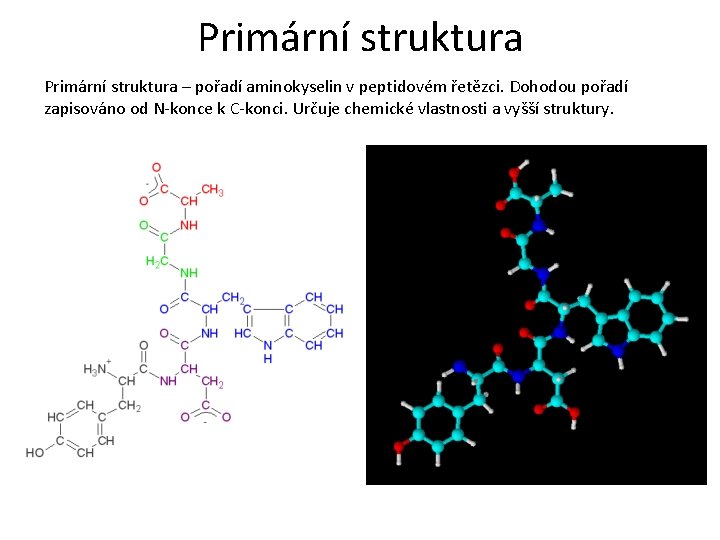
Primární struktura – pořadí aminokyselin v peptidovém řetězci. Dohodou pořadí zapisováno od N-konce k C-konci. Určuje chemické vlastnosti a vyšší struktury.
Primární struktura

Sekundární struktura – alfa helix Alfa-helix má tvar pravotočivé šroubovice, při pohledu shora tvoří šroubovici bílkovinná kostra, zatímco aminokyselinové zbytky směřují ven. Mezi jednotlivými patry šroubovice vznikají vodíkové můstky (a to konkrétně mezi C=O skupinou a N–H skupinou o čtyři aminokyseliny dál). Typickými aminokyselinami vyskytujícími se v alfa-helixu je zejména alanin, kyselina glutamová, leucin a methionin http: //cs. wikipedia. org/wiki/ Soubor: H%C 3%A 9 lice_Alpha. svg
Sekundární struktura – beta skládaný list Skládá se z několika aminokyselinových řetězců (peptidů), které jsou uspořádány vzájemně rovnoběžně a dochází mezi nimi ke vzniku vodíkových můstků (konkrétně mezi C=O skupinou a N–H skupinou. Paralelní skládaný http: //cs. wikipedia. org/wiki/Soubor: Beta_sheet_bonding_parallel-color. svg Antiparalelní skládaný http: //cs. wikipedia. org/wiki/Soubor: Beta_sheet_bonding_antiparallel-color. svg

Denaturace Ztráta sekundární struktury, vede ke ztrátě funkce. Může být reverzibilní nebo ireverzibilní. Teplota – u enzymů vede ke ztrátě funkce už teplota nad 43°C, termofylní – snesou i nad 100°C p. H – změna p. H ovlivňuje iontovou stabilitu – vnitřní prostředí ≤ 7, 28; 7, 42≥, trávicí trakt výrazně nižší. Detergenty – interakce s charakteristickými skupinami v postranních řetězcích Ionty – kationty i anionty – vysolení z roztoku ve formě sraženiny Mechanická energie – šlehání bílku Elektromagnetické záření

Terciární struktura Uspořádání jednotlivých sekundárních struktur v prostoru, vzniká mezi postranními řetězci aminokyselin. Je stabilizována: Vodíkovými můstky Elektrostatickými interakcemi Hydrofobními interakcemi Disulfidovými můstky cysteinů Podle terciární struktury rozlišujeme Globulární - kulovité Fibrilární - vláknité http: //cs. wikipedia. org/wiki/ Soubor: 3 D_protein. jpg

Kvarterní struktura Struktura oligomeru tvořeného asociací 2 nebo více polypeptidových řetězců, tzv. podjednotek. Stabilizována nekovalentními interakcemi. http: //cs. wikipedia. org/wiki/Soubor: Hemoglobin. jpg

Procvičení - rozpustnost Vyber správná tvrzení Aminokyseliny jsou rozpustné ve vodě, protože mají polární charakter ☺ Aminokyseliny nejsou rozpustné ve vodě, protože nemají polární charakter Aminokyseliny jsou rozpustné v nepolárních rozpouštědlech, protože mají polární charakter Aminokyseliny nejsou rozpustné v nepolárních rozpouštědlech, protože mají polární charakter ☺
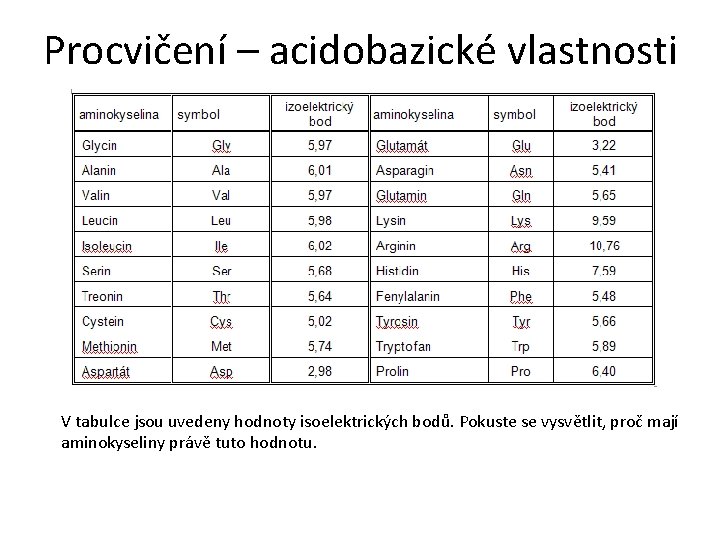
Procvičení – acidobazické vlastnosti V tabulce jsou uvedeny hodnoty isoelektrických bodů. Pokuste se vysvětlit, proč mají aminokyseliny právě tuto hodnotu.
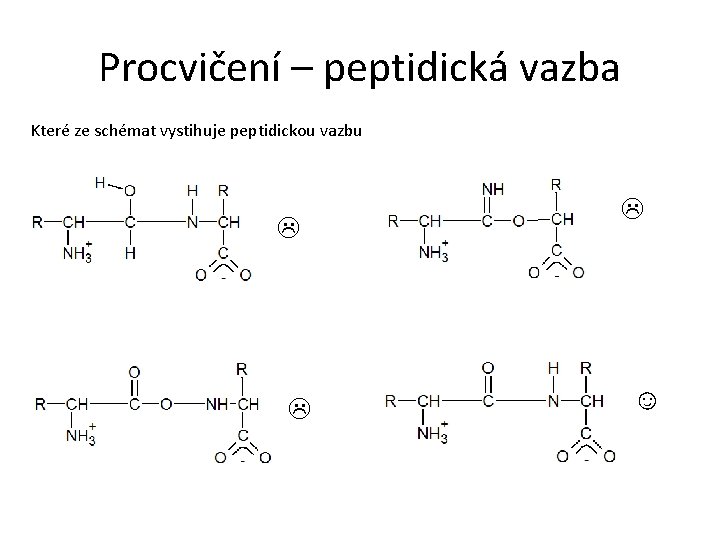
Procvičení – peptidická vazba Které ze schémat vystihuje peptidickou vazbu ☺

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Zdroje a použitá literatura 1. PACÁK, Josef. Stručné základy organické chemie. 1. vydání. Praha: SNTL-Nakladatelství technické literatury, 1975. Řada chem. literatury. 2. JAN MUSIL. Biochemie v obrazech a schématech. II. , zcela přepracované vydání. Praha: Avicenum, 1990. 3. Fotografie a vzorce z vlastní databáze autora. Vytvořeny programy ACD FREE 12, Snagit 4. MURRAY, Robert K. <i>Harperova biochemie</i>. 23. vyd. Jinočany: H H, 2002, ix, [3], 872 s. ISBN 80 -731 -9013 -3. 5. Aminokyselina. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001[cit. 2012 -11 -10]. Dostupné z: http: //cs. wikipedia. org/wiki/Aminokyseliny Materiál je určen pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízeních. Jakékoliv další využití podléhá autorskému zákonu.

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Zdroje a použitá literatura 6. Peptid. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 - [cit. 2012 -1110]. Dostupné z: http: //cs. wikipedia. org/wiki/Peptid 7. Bílkovina. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 - [cit. 201211 -10]. Dostupné z: http: //cs. wikipedia. org/wiki/B%C 3%ADlkoviny Materiál je určen pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízeních. Jakékoliv další využití podléhá autorskému zákonu.
- Slides: 24