DCHAC ETZEC Mgr Jaroslav Najbert Gymnzium a Jazykov

DÝCHACÍ ŘETĚZEC Mgr. Jaroslav Najbert
Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Název školy Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Adresa školy IČO Operační program Registrační číslo Označení vzdělávacího materiálu Vzdělávací oblast Vzdělávací obor Tematický okruh Sokolovská 1638 620 330 26 Operační program Vzdělávání pro konkurenceschopnost CZ. 1. 07/1. 1. 28/01. 0050 K_INOVACE_1. CH. 44 Člověk a příroda Chemie Metabolismus Zhotoveno Ročník Vyšší stupeň osmiletého gymnázia a čtyřleté gymnázium (RVP – G) Anotace Materiál je určen jako studijní v předmětu biochemie, který integruje vzdělávací obory biologie a chemie. Je zaměřen na metabolické přeměny látek v citrátovém cyklu. Předpokládá zvládnutí učiva reakčních mechanismů vzdělávacího oboru chemie.

Obecná charakteristika dýchacího řetězce Je lokalizován na vnitřní mitochondriální membráně. Pro průběh dějů je důležitá vnitřní membrána a mezimembránový prostor. http: //cs. wikipedia. org/wiki/Soubor: Animal_mitochondrion_diagram_cs. svg http: //cs. wikipedia. org/wiki/Soubor: Mitochondrion. CAM. jpg Sled oxidačně redukčních dějů, kdy systém redoxních enzymů odnímá substrátům (konečný příjemce NADH+H+, FADH 2) elektron a proton (H꞊H++e-). Energie, uvolněná přenosem e- mezi enzymy, je využita pro přenos H+ do mezimembránového prostoru. Tím je vytvořen koncentrační gradient H+, který je následně využit pro tvorbu ATP. Konečným příjemcem elektronu je kyslík ve formě aniontu O 2 -, který následně se dvěma H+ tvoří molekulu vody. Elektrochemický gradient, vytvořený odlišnou koncentrací protonů, označujeme jako protonmotorickou (protonmotivní) sílu.

Přenos redukčních ekvivalentů β-oxidace mastných kyselin – probíhá v matrix mitochondrií – FADH 2 a NADH+H+ - ihned k dispozici. Odbourávání aminokyselin – probíhá v matrix mitochondrií a cytoplazmě – produkty z cytoplasmy přenášeny do mitochondrií, vstupují do citrátového cyklu. S výjimkou pyruvátu jsou ostatní produkty přenášeny do mitochondrií přes specifické přenašeče Pyruvát (glukoplastické aminokyseliny) – alanin, valin, cystein, glycin, serin, threonin – nejsou-li využity pro glukoneogenezi, přes acetyl-Co. A do citrátového cyklu. Acetyl-Co. A (acetyl-Co. A, ketoplastické aminokyseliny) – leucin, lysin, tryptofan, částečně fenylalanin a tyrosin. 2 -oxoglutarát – prolin, histidin, arginin, glutamát. Sukcinát – methionin, valin, isoleucin. Fumarát – část molekuly fenylalaninu a tyrosinu Oxalacetát – aspartát a asparagin
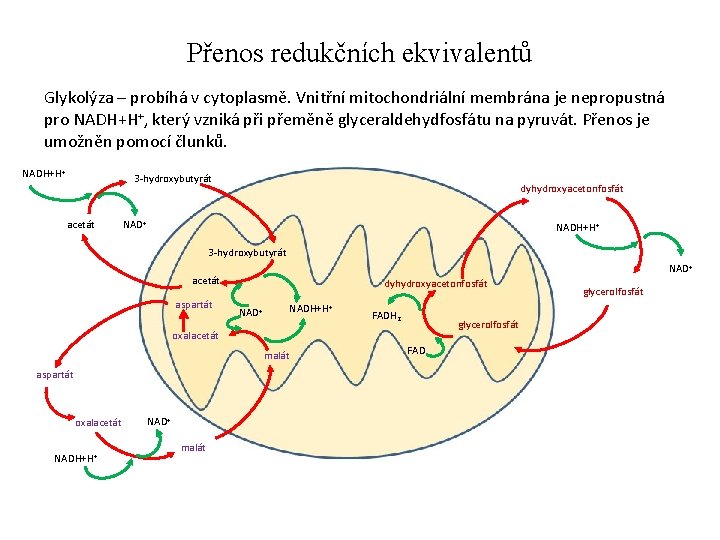
Přenos redukčních ekvivalentů Glykolýza – probíhá v cytoplasmě. Vnitřní mitochondriální membrána je nepropustná pro NADH+H+, který vzniká při přeměně glyceraldehydfosfátu na pyruvát. Přenos je umožněn pomocí člunků. NADH+H+ 3 -hydroxybutyrát acetát dyhydroxyacetonfosfát NAD+ NADH+H+ 3 -hydroxybutyrát NAD+ acetát aspartát dyhydroxyacetonfosfát NADH+H+ NAD+ FADH 2 glycerolfosfát oxalacetát malát aspartát oxalacetát NADH+H+ NAD+ malát FAD glycerolfosfát
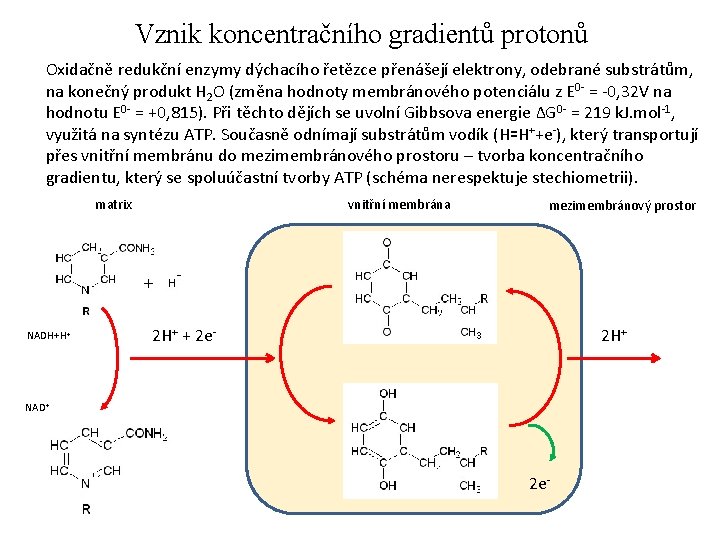
Vznik koncentračního gradientů protonů Oxidačně redukční enzymy dýchacího řetězce přenášejí elektrony, odebrané substrátům, na konečný produkt H 2 O (změna hodnoty membránového potenciálu z E 0 - = -0, 32 V na hodnotu E 0 - = +0, 815). Při těchto dějích se uvolní Gibbsova energie ∆G 0 - = 219 k. J. mol-1, využitá na syntézu ATP. Současně odnímají substrátům vodík (H꞊H++e-), který transportují přes vnitřní membránu do mezimembránového prostoru – tvorba koncentračního gradientu, který se spoluúčastní tvorby ATP (schéma nerespektuje stechiometrii). matrix NADH+H+ vnitřní membrána mezimembránový prostor 2 H+ + 2 e- 2 H+ NAD+ 2 e-

Oxidačně redukční enzymy Komplex I – NADH ubichinon-oxidoreduktáza (NADH dehydrogenáza) – složen z více jak 30 ti bílkovinných podjednotek, z FMN a několika Fe. S center. Komplex III – cytochrom bc 1 (QH 2 -cytochrom-c-oxidoreduktáza, ubichinol-cytochrom-c-oxidoreduktáza) – obsahuje 11 polypeptidů, cytochrom b 562, cytochrom b 566, cytochrom c 1, koenzym Q (ubichinon), Rieskeho protein – (Fe 2 S 2). Komplex IV - cytochrom aa 3 (Cytochrom c oxidáza) – skládá se z 8 - 13 podjednotek, cytochrom c 1, cytochrom a 3, měďnaté komplexy. Komplex II – sukcinát-ubichinon-oxidoreduktáza – cyklus, umožňující vstup substrátů přes sukcinát (FADH 2) – 4 podjednotky (FAD, FADH), Fe. S protein a cytochromy. Elektrony jsou přenášeny na komplex III.
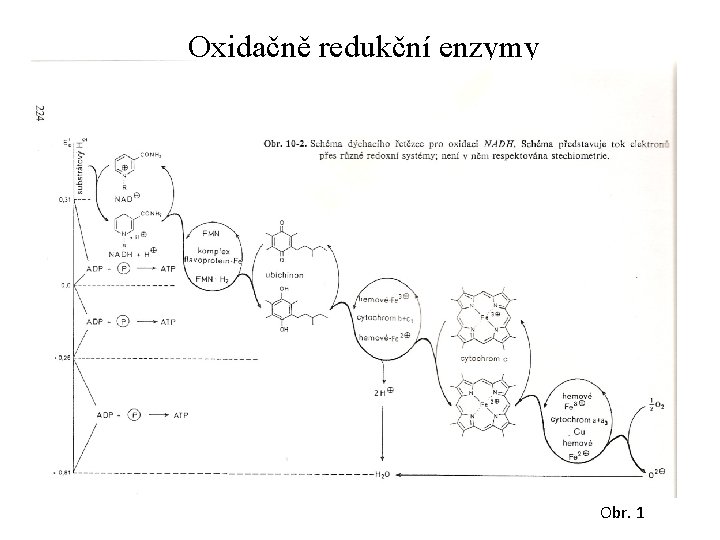
Oxidačně redukční enzymy Obr. 1
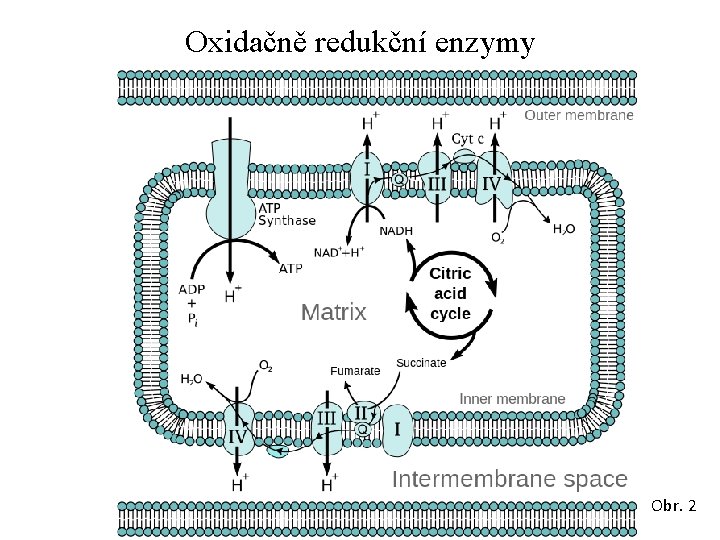
Oxidačně redukční enzymy Obr. 2
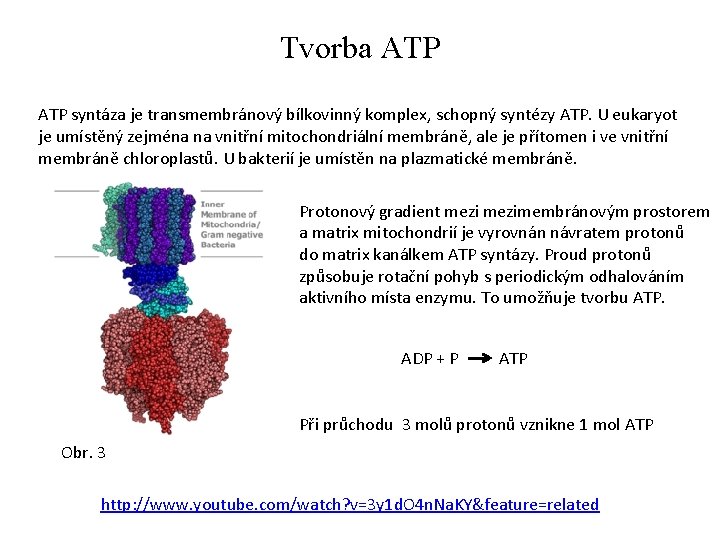
Tvorba ATP syntáza je transmembránový bílkovinný komplex, schopný syntézy ATP. U eukaryot je umístěný zejména na vnitřní mitochondriální membráně, ale je přítomen i ve vnitřní membráně chloroplastů. U bakterií je umístěn na plazmatické membráně. Protonový gradient mezimembránovým prostorem a matrix mitochondrií je vyrovnán návratem protonů do matrix kanálkem ATP syntázy. Proud protonů způsobuje rotační pohyb s periodickým odhalováním aktivního místa enzymu. To umožňuje tvorbu ATP. ADP + P ATP Při průchodu 3 molů protonů vznikne 1 mol ATP Obr. 3 http: //www. youtube. com/watch? v=3 y 1 d. O 4 n. Na. KY&feature=related

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Zdroje a použitá literatura Obrázky: 1. KARLSON, Peter. Základy biochemie, str. 224. 2. (doplněné) vydání. Praha: Academia, 1971. 2. FVASCONCELLOS. Mitochondrial electron transport chain—Etc 4. svg. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 - [cit. 2013 -05 -26]. Dostupné z: http: //cs. wikipedia. org/wiki/Soubor: Mitochondrial_electron_transport_chain%E 2%80%94 Etc 4. svg 3. ALEX. X. Atp synthase. PNG. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 - [cit. 2013 -05 -26]. Dostupné z: http: //cs. wikipedia. org/wiki/Soubor: Atp_synthase. PNG Materiál je určen pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízeních. Jakékoliv další využití podléhá autorskému zákonu.

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Zdroje a použitá literatura Publikace: 1. JAN MUSIL. Biochemie v obrazech a schématech. II. , zcela přepracované vydání. Praha: Avicenum, 1990. 2. Neoznačené obrázky a vzorce z vlastní databáze autora. Vytvořeny programy ACD FREE 12, Snagit 3. MURRAY, Robert K. <i>Harperova biochemie</i>. 23. vyd. Jinočany: H H, 2002, ix, [3], 872 s. ISBN 80 -731 -9013 -3. 4. KARLSON, Peter. Základy biochemie. 2. (doplněné) vydání. Praha: Academia, 1971. 5. Dýchací řetězec. Wikiskripta [online]. [cit. 2013 -06 -24]. Dostupné z: http: //www. wikiskripta. eu/index. php/D%C 3%BDchac%C 3%AD_%C 5%99 et%C 4%9 Bzec Materiál je určen pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízeních. Jakékoliv další využití podléhá autorskému zákonu.
- Slides: 12