ALDEIDI E CHETONI Sono composti caratterizzati dalla presenza






- Slides: 14

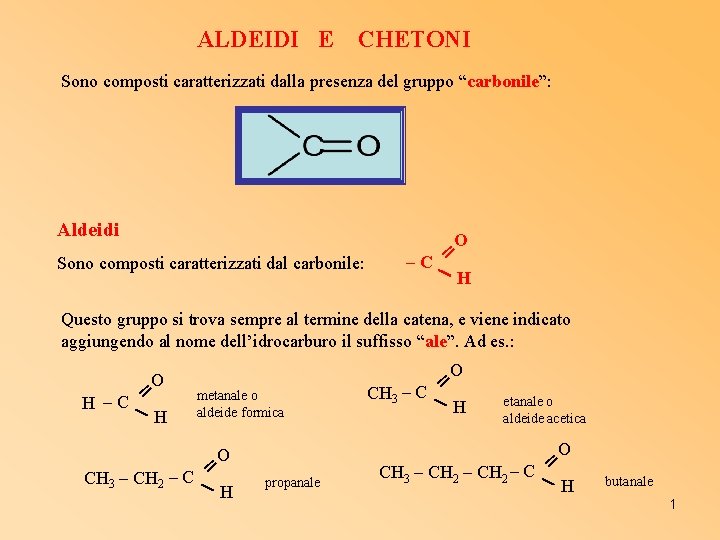
ALDEIDI E CHETONI Sono composti caratterizzati dalla presenza del gruppo “carbonile”: Aldeidi Sono composti caratterizzati dal carbonile: O ═ –C H Questo gruppo si trova sempre al termine della catena, e viene indicato aggiungendo al nome dell’idrocarburo il suffisso “ale”. Ad es. : O ═ H –C H metanale o aldeide formica O ═ CH 3 – CH 2 – C H propanale O ═ CH 3 – C H etanale o aldeide acetica O ═ CH 3 – CH 2 – C H butanale 1

Nella nomenclatura IUPAC il gruppo aldeidico non è numerato poiché è sempre terminale. L’aldeide formica è l’unica aldeide gassosa, le altre sono liquide, e quelle a catene lunga sono solide. SOLUBILITÀ delle Aldeidi Le aldeidi sono composti molto poco solubili in H 2 O, e la loro solubilità diminuisce con l’aumentare del numero di atomi di C. Se confrontiamo l’aldeide acetica e l’etanolo: CH 3 – CH 2 – OH bolle a 78°C O ═ CH 3 – C H bolle a 20°C La grande differenza nella temperatura di ebollizione è dovuta al fatto che essendo composti poco polari hanno legami idrogeno molto più deboli degli alcoli. 2

Chetoni Sono composti caratterizzati dal carbonile: ═ O C Questo gruppo non si trova mai al termine della catena, e viene indicato aggiungendo al nome dell’idrocarburo il suffisso “one”. Ad es. : ═ O CH 3 – CH 3 propanone o acetone E’ un chetone simmetrico, ed è il più semplice chetone ═ O CH 3 – CH 2 – CH 3 butanone O CH 3 – CH 2 – CH 3 2 pentanone ═ ═ O CH 3 – CH 2 – CH 3 3 pentanone 3

Nella nomenclatura IUPAC il composto carbonilico ha sempre la precedenza nella dizione. SOLUBILITÀ dei Chetoni I chetoni sono relativamente poco solubili in H 2 O, e come per le aldeidi la loro solubilità diminuisce mano che aumenta il n° di atomi di C della catena. I chetoni che hanno un numero di atomi di C > 4 non sono solubili in H 2 O. 4

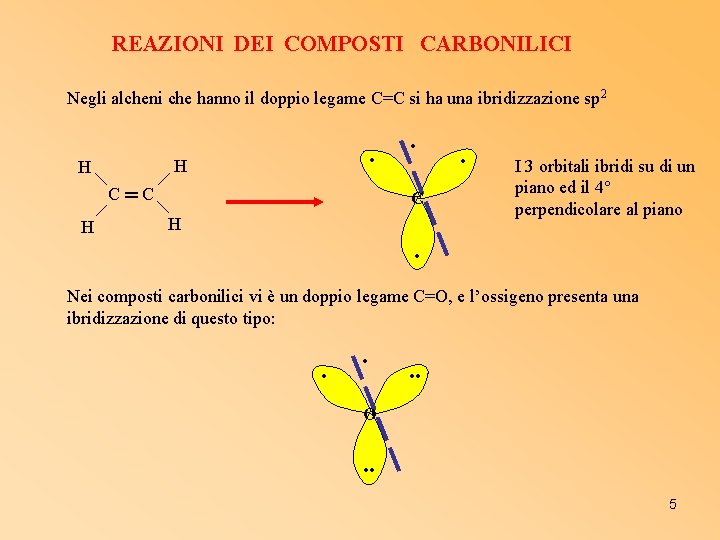
REAZIONI DEI COMPOSTI CARBONILICI Negli alcheni che hanno il doppio legame C=C si ha una ibridizzazione sp 2 • H H C═C H • I 3 orbitali ibridi su di un piano ed il 4° perpendicolare al piano • Nei composti carbonilici vi è un doppio legame C=O, e l’ossigeno presenta una ibridizzazione di questo tipo: • • • • O • • 5

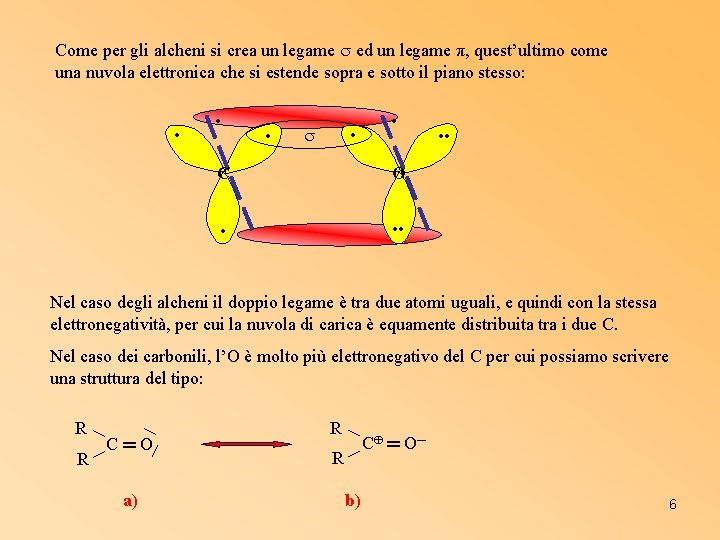
Come per gli alcheni si crea un legame ed un legame π, quest’ultimo come una nuvola elettronica che si estende sopra e sotto il piano stesso: • • • C O • • • Nel caso degli alcheni il doppio legame è tra due atomi uguali, e quindi con la stessa elettronegatività, per cui la nuvola di carica è equamente distribuita tra i due C. Nel caso dei carbonili, l’O è molto più elettronegativo del C per cui possiamo scrivere una struttura del tipo: R R C═O a) R C ═ O─ R b) 6

In questo caso dunque il gruppo carbonilico è rappresentato da entrambe le strutture. Sono due strutture limite: a) indica che gli elettroni sono a metà tra O e C b) indica che gli elettroni sono sull’O In realtà dobbiamo parlare di polarizzazione, ossia il legame in questo caso è fortemente polarizzato: R R + C═O Un tale composto allora potrà reagire sia con elettrofili che con nucleofili, ed in particolare gli elettrofili reagiranno con l’O─ (nucleofilo) mentre i nucleofili reagiranno con il C (elettrofilo). 7

Sia le aldeidi chetoni danno reazioni di ADDIZIONE NUCLEOFILA: O─ O ═ R –C H + N─ R–C–H N Il nucleofilo attacca il C sia da sopra che da sotto il piano, e l’O richiama su di sé gli e- del = legame In questo meccanismo il C passa da una ibridizzazione sp 2 ad una ibridizzazione sp 3. La reazione dipenderà dalla forza del nucleofilo. Caso A O ═ R –C H + H 2 O R–O–H Cl-, Br- + R – ONH 3, R – NH 2 OH- Caso B O R –C ═ H 8

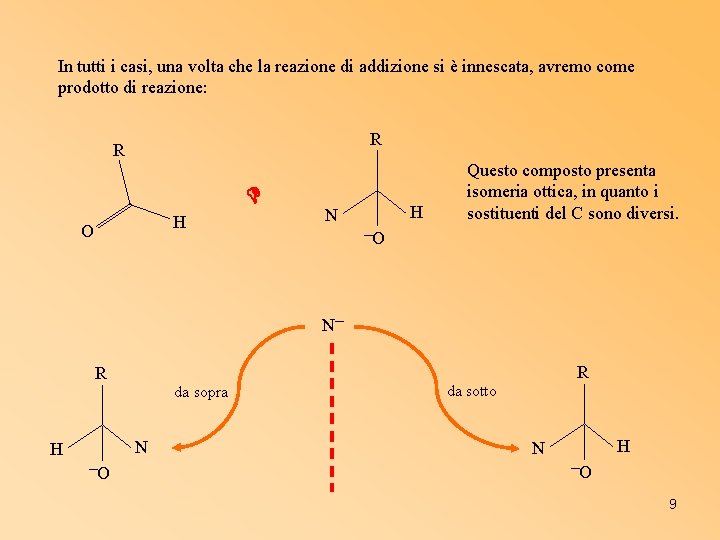
In tutti i casi, una volta che la reazione di addizione si è innescata, avremo come prodotto di reazione: R R H O H N Questo composto presenta isomeria ottica, in quanto i sostituenti del C sono diversi. ─O N─ R R da sopra N H ─O da sotto H N ─O 9

R R N H ─O Le due strutture sono enantiomeri, e si formano in uguale quantità. H N ─O NOTA: Quando una reazione porta alla scomparsa di un C sp 2 ed alla formazione di un C sp 3 il meccanismo comporta la formazione di un C asimetrico (chirale) e il prodotto sarà un RACEMO. Il racemo è una miscela di enantiomeri in uguale quantità per cui il potere ottico rotatorio è zero (l’angolo di rotazione = 0). Se si forma una quantità diversa dei due enentiomeri la reazione viene detta “ENANTIO-SELETTIVA”. In natura le reazione sono quasi sempre enantio-selettive, come ad es. nella sintesi degli Amminoacidi. 10

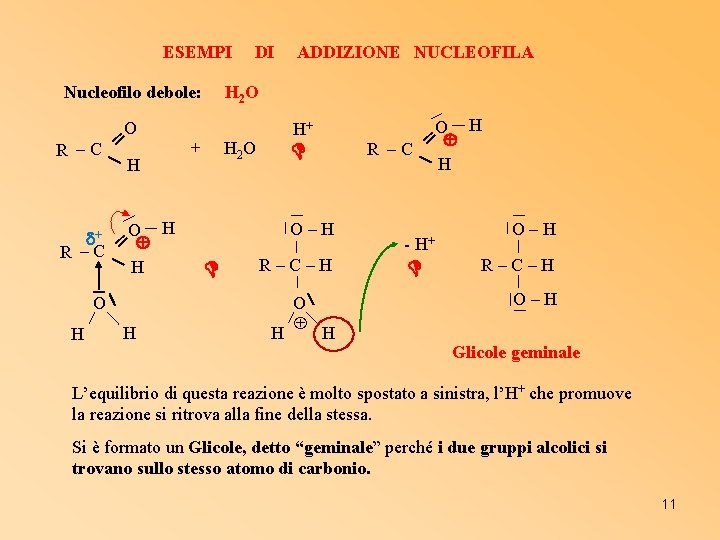
ESEMPI Nucleofilo debole: O ═ R –C H H + ═O R –C H DI H 2 O + H O H R –C ═ H H+ H 2 O O–H R–C–H O H ADDIZIONE NUCLEOFILA H O - H+ O–H R–C–H O–H H Glicole geminale L’equilibrio di questa reazione è molto spostato a sinistra, l’H+ che promuove la reazione si ritrova alla fine della stessa. Si è formato un Glicole, detto “geminale” perché i due gruppi alcolici si trovano sullo stesso atomo di carbonio. 11

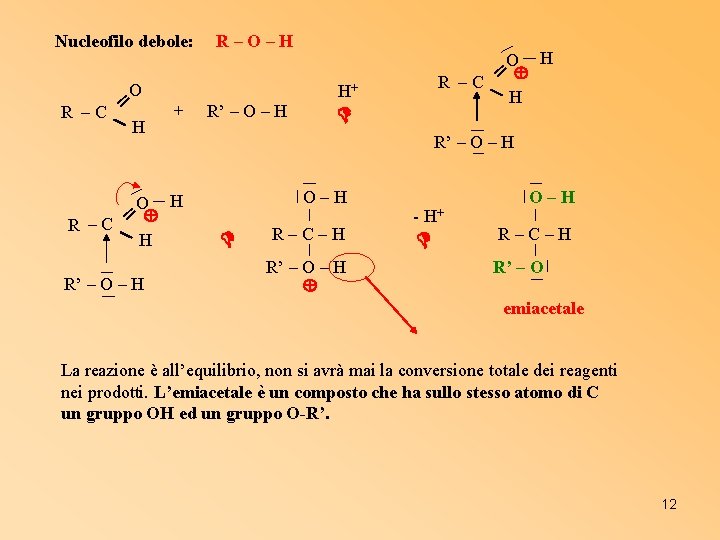
Nucleofilo debole: O R –C ═ H + O H R –C ═ H R’ – O – H R–O–H R’ – O – H O H ═ R –C H H+ R’ – O – H O–H R–C–H R’ – O – H - H+ O–H R–C–H R’ – O emiacetale La reazione è all’equilibrio, non si avrà mai la conversione totale dei reagenti nei prodotti. L’emiacetale è un composto che ha sullo stesso atomo di C un gruppo OH ed un gruppo O-R’. 12

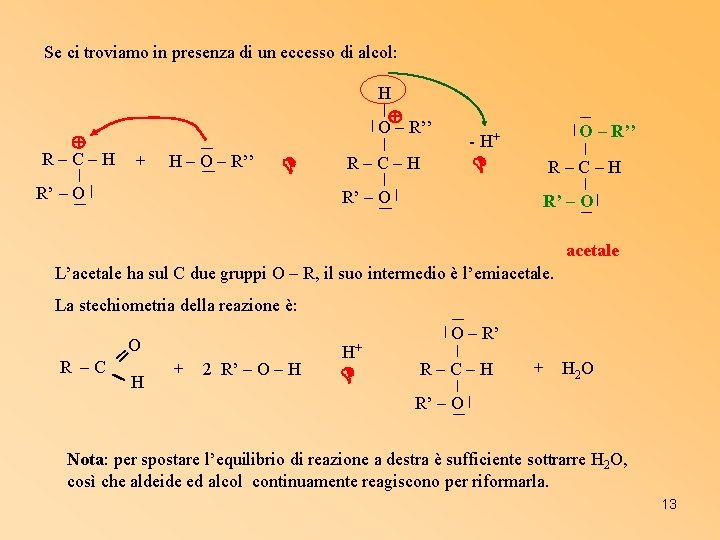
Se ci troviamo in presenza di un eccesso di alcol: R–C–H H O – R’’ + H – O – R’’ R’ – O O – R’’ - H+ R–C–H R’ – O acetale L’acetale ha sul C due gruppi O – R, il suo intermedio è l’emiacetale. La stechiometria della reazione è: O R –C ═ H + 2 R’ – O – H H+ O – R’ R–C–H + H 2 O R’ – O Nota: per spostare l’equilibrio di reazione a destra è sufficiente sottrarre H 2 O, così che aldeide ed alcol continuamente reagiscono per riformarla. 13

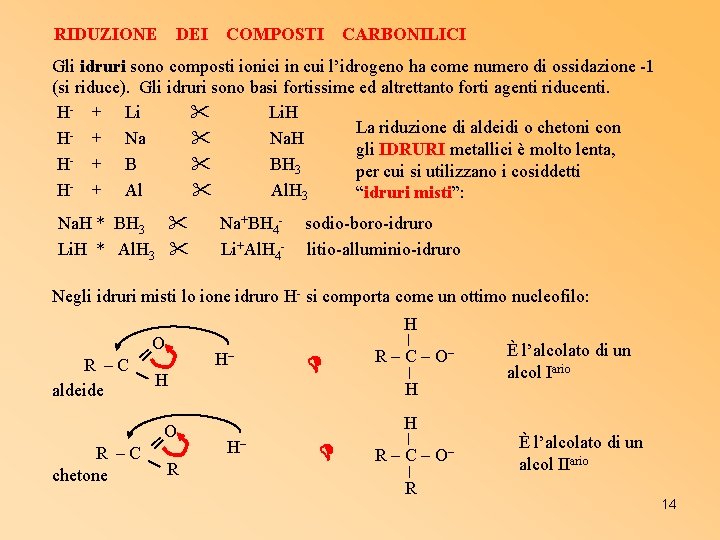
RIDUZIONE DEI COMPOSTI CARBONILICI Gli idruri sono composti ionici in cui l’idrogeno ha come numero di ossidazione -1 (si riduce). Gli idruri sono basi fortissime ed altrettanto forti agenti riducenti. H- + Li Li. H La riduzione di aldeidi o chetoni con H- + Na Na. H gli IDRURI metallici è molto lenta, H + B BH 3 per cui si utilizzano i cosiddetti H + Al Al. H 3 “idruri misti”: Na. H * BH 3 Li. H * Al. H 3 Na+BH 4 Li+Al. H 4 - sodio-boro-idruro litio-alluminio-idruro Negli idruri misti lo ione idruro H- si comporta come un ottimo nucleofilo: O ═ R –C H aldeide O ═ R –C R chetone H H– R – C – O– H H H– R – C – O– R È l’alcolato di un alcol Iario È l’alcolato di un alcol IIario 14