ACCOPPIAMENTO DI SPIN ACCOPPIAMENTO INDIRETTO SCALARE Interazione magnetica














- Slides: 39

ACCOPPIAMENTO DI SPIN

ACCOPPIAMENTO INDIRETTO (SCALARE) § Interazione magnetica fra nuclei § Mediato dagli elettroni di legame § Misurato dalla J (Hz) costante di accoppiamento MECCANISMO: Termine di contatto di Fermi

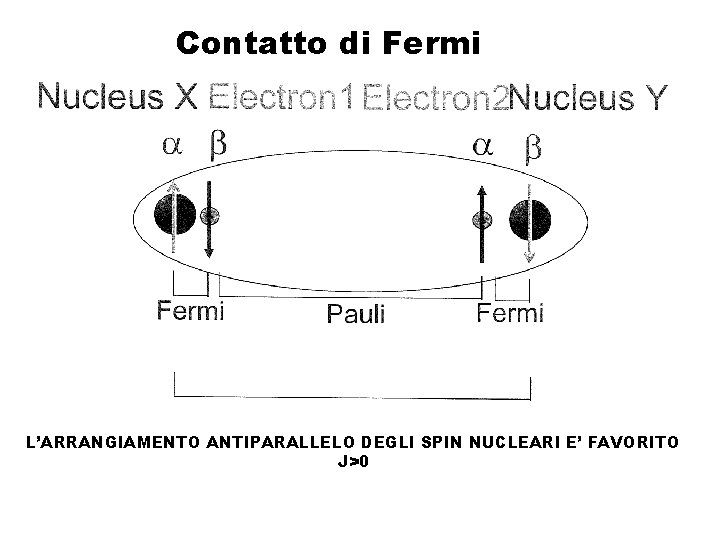
Contatto di Fermi L’ARRANGIAMENTO ANTIPARALLELO DEGLI SPIN NUCLEARI E’ FAVORITO J>0

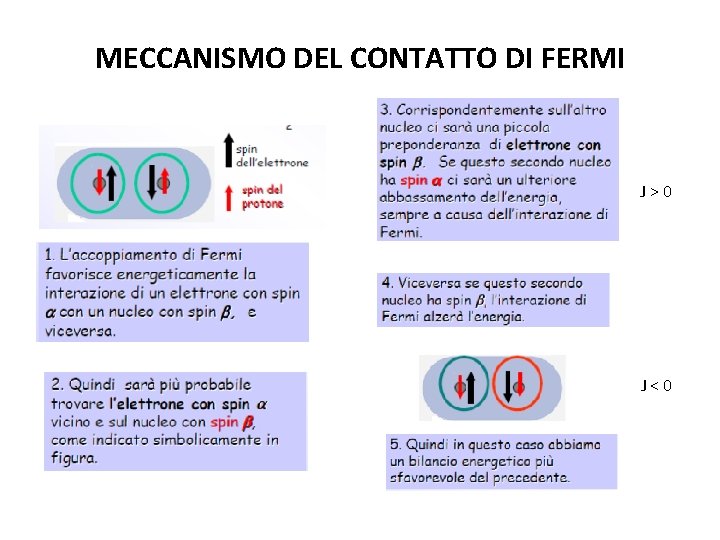
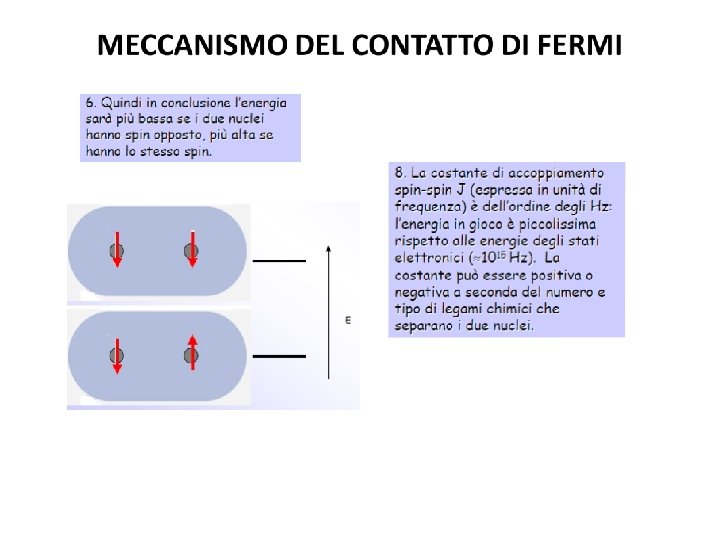
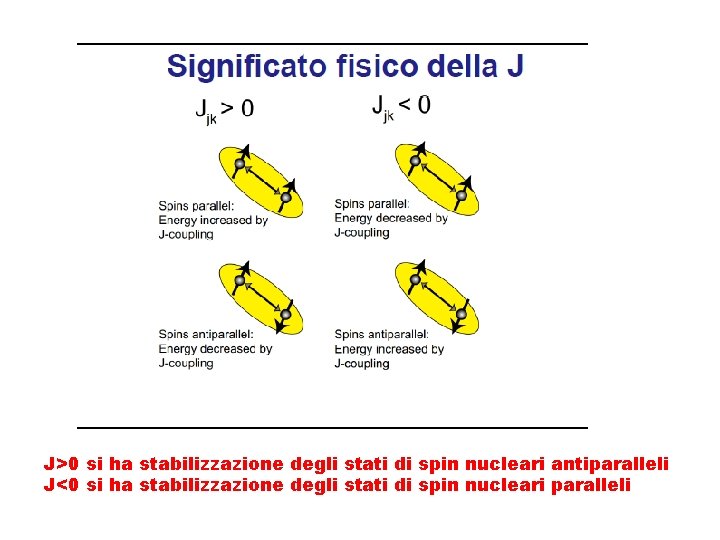
MECCANISMO DEL CONTATTO DI FERMI J>0 J<0


Contatto di Fermi Regola di Pauli: spin elettronici antiparalleli nello stesso orbitale Regola di Hund: massima molteplicità degli spin elettroni in orbitali atomici diversi L’ARRANGIAMENTO PARALLELO DEGLI SPIN NUCLEARI E’ FAVORITO J<0

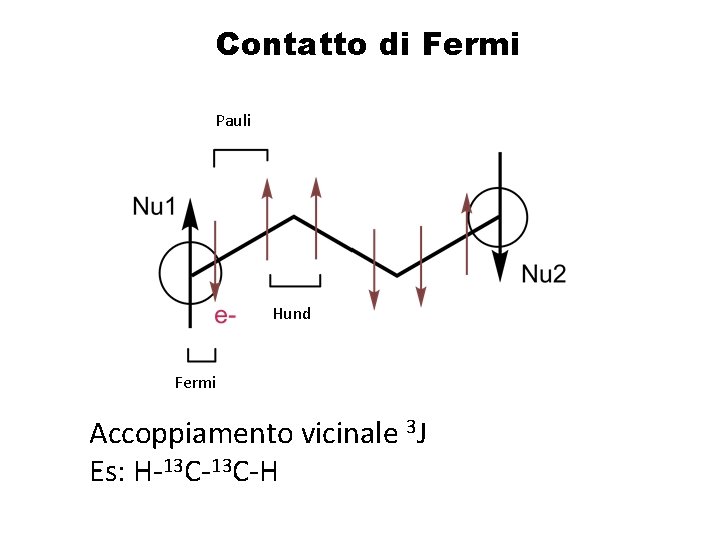
Contatto di Fermi Pauli Hund Fermi Accoppiamento vicinale 3 J Es: H-13 C-H

J>0 si ha stabilizzazione degli stati di spin nucleari antiparalleli J<0 si ha stabilizzazione degli stati di spin nucleari paralleli

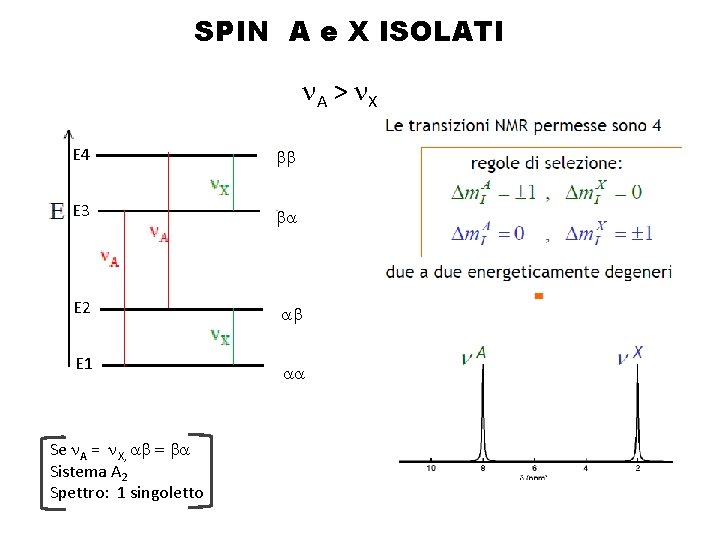
SPIN A e X ISOLATI n. A > n. X E 4 bb E 3 ba E 2 ab E 1 aa Se n. A = n. X, ab = ba Sistema A 2 Spettro: 1 singoletto

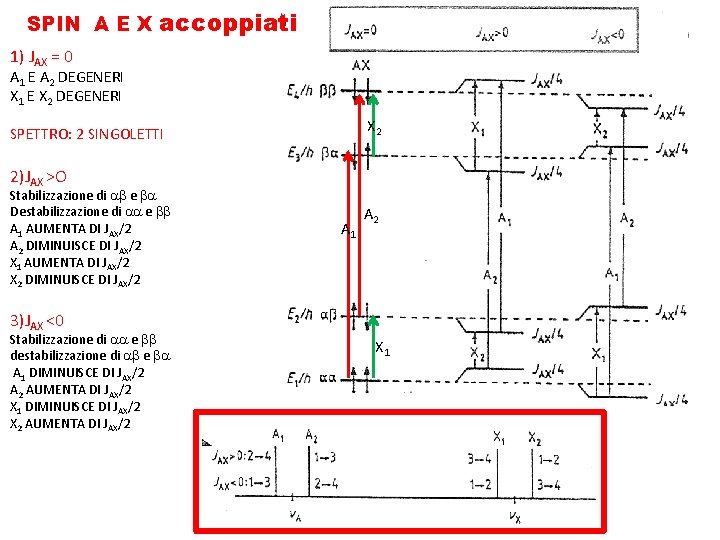
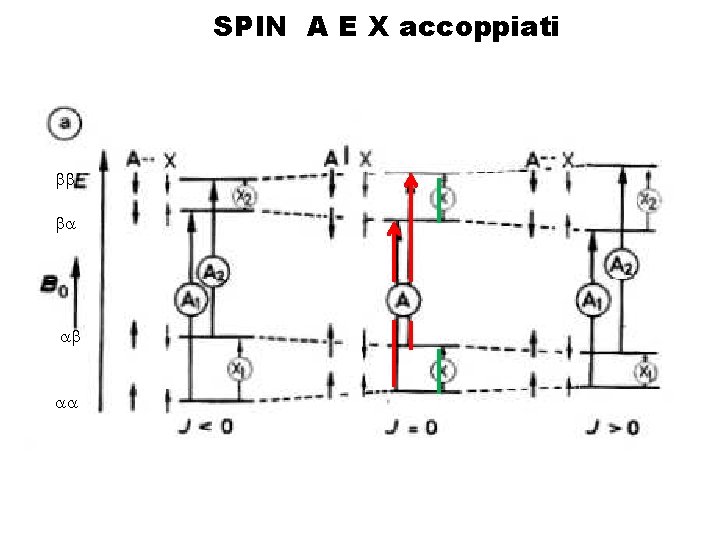
SPIN A E X accoppiati 1) JAX = 0 A 1 E A 2 DEGENERI X 1 E X 2 DEGENERI X 2 SPETTRO: 2 SINGOLETTI 2)JAX >O Stabilizzazione di ab e ba Destabilizzazione di aa e bb A 1 AUMENTA DI JAX/2 A 2 DIMINUISCE DI JAX/2 X 1 AUMENTA DI JAX/2 X 2 DIMINUISCE DI JAX/2 A 1 A 2 3)JAX <0 Stabilizzazione di aa e bb destabilizzazione di ab e ba A 1 DIMINUISCE DI JAX/2 A 2 AUMENTA DI JAX/2 X 1 DIMINUISCE DI JAX/2 X 2 AUMENTA DI JAX/2 X 1

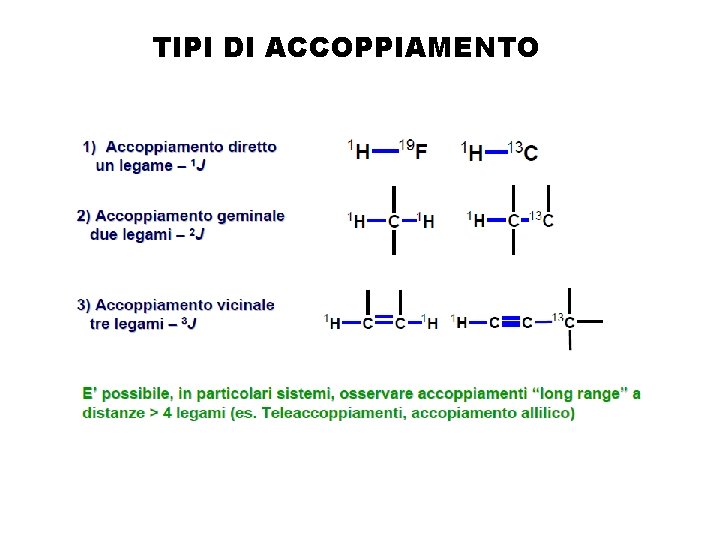
TIPI DI ACCOPPIAMENTO

EQUIVALENZA CHIMICA E MAGNETICA 1. EQUIVALENZA CHIMICA: DUE NUCLEI i E k SONO CHIMICAMENTE EQUIVALENTI QUANDO SONO SCAMBIABILI DA OPERAZIONI DI SIMMETRIA, O PER ROTAZIONE RAPIDA O PER COINCIDENZA. ni = nk. 3. EQUIVALENZA MAGNETICA: DUE NUCLEI i E k SONO MAGNETICAMENTE EQUIVALENTI QUANDO SONO CHIMICAMENTE EQUIVALENTI E HANNO LA STESSA COSTANTE DI ACCOPPIAMENTO CON UN TERZO NUCLEO ni = nk. e Jil = Jkl NUCLEI CHIMICAMENTE EQUIVALENTI SONO ISOCRONI (EQUIVALENZA DI CHEMICAL SHIFT) MA NON SEMPRE VALE IL CONTRARIO

EQUIVALENZA CHIMICA 1. Analizzare la simmetria della molecola 2. Determinare le relazioni stereochimiche (TOPICITA’) dei nuclei 3. Valutare la presenza di eventuali processi dinamici

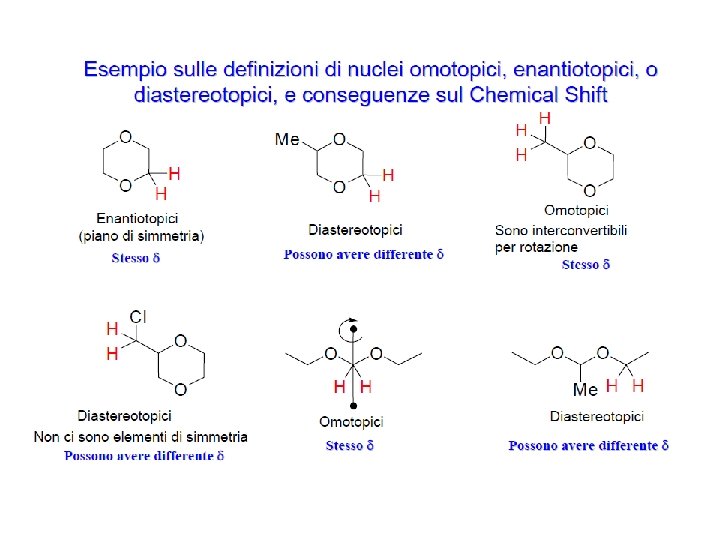
EQUIVALENZA CHIMICA 1. Analizzare la simmetria della molecola Nuclei scambiabili da operazioni di simmetria (assi > C 1 o piani) sono chimicamente equivalenti 2. Determinare le relazioni stereochimiche (TOPICITA’) dei nuclei La topicità descrive le relazioni stereochimiche fra atomi (o gruppi) identici in una molecola, (ad esempio i due idrogeni di un CH 2 o i due metili di un isopropile) Essi possono essere 1. Omotopici 2. Enantiotopici 3. Diastereotopici

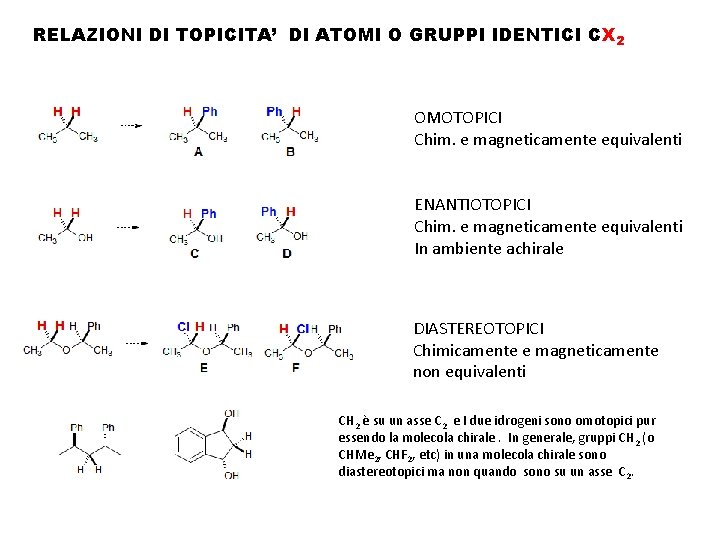
RELAZIONI DI TOPICITA’ DI ATOMI O GRUPPI IDENTICI CX 2 OMOTOPICI Chim. e magneticamente equivalenti ENANTIOTOPICI Chim. e magneticamente equivalenti In ambiente achirale DIASTEREOTOPICI Chimicamente e magneticamente non equivalenti CH 2 è su un asse C 2 e I due idrogeni sono omotopici pur essendo la molecola chirale. In generale, gruppi CH 2 (o CHMe 2, CHF 2, etc) in una molecola chirale sono diastereotopici ma non quando sono su un asse C 2.


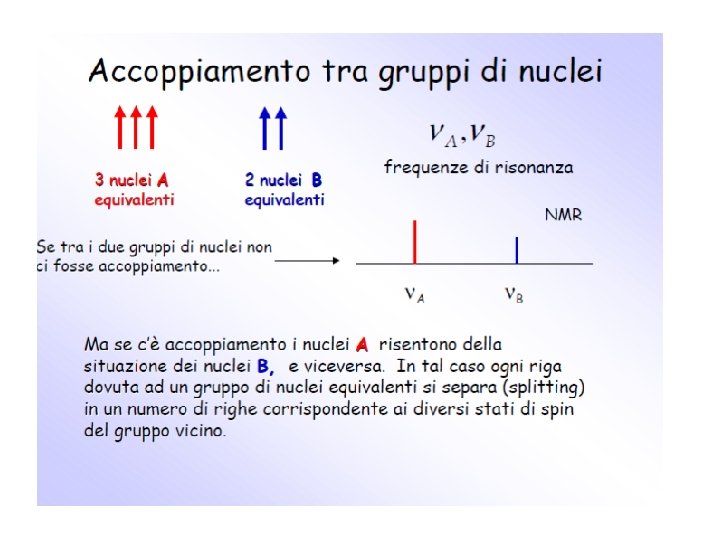
NOTAZIONE DI POPLE PER SISTEMI DI SPIN q I nuclei chimicamente e magneticamente equivalenti sono denominati utilizzando GRUPPI DI LETTERE MAIUSCOLE ABC, M, N, X, Y, Z e PEDICI NUMERICI. (An, Bm, Cp, …). I pedici indicano il numero di nuclei magneticamente equivalenti che costituiscono il gruppo. q Gruppi di protoni fortemente accoppiati vengono indicati con lettere dell’alfabeto consecutive (A, B, C…) andando da sinistra a destra dello spettro q Gruppi di protoni debolmente accoppiati vengono indicati con lettere dell’alfabeto lontane (A, M, X…) q Nuclei chimicamente equivalenti ma non equivalenti magneticamente vengono distinti tramite un apice (A, A’)

ESEMPI A 2 Due nuclei chimicamente e magneticamente equivalenti AX Due nuclei non chimicamente equivalenti debolmente accoppiati AB Due nuclei non chimicamente equivalenti fortemente accoppiati AA’ Due nuclei chimicamente ma non magneticamente equivalenti AMX tre nuclei chimicamente non equivalenti accoppiati debolmente ABX tre nuclei ch. non equivalenti di cui due accoppiati fortemente

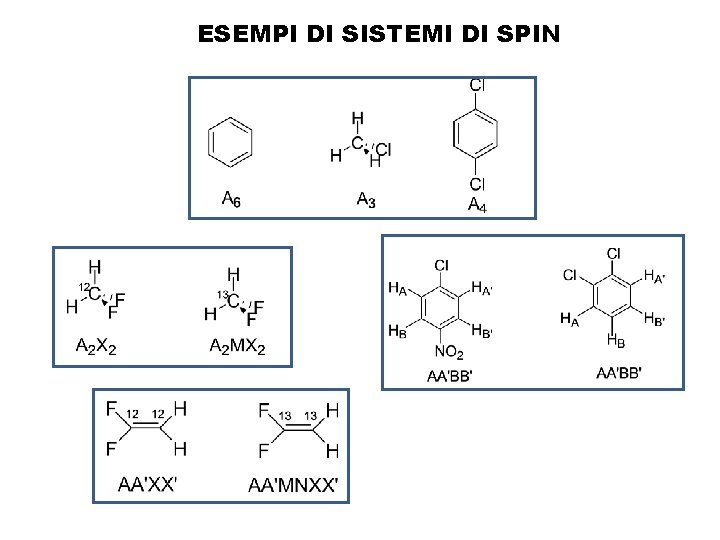
ESEMPI DI SISTEMI DI SPIN

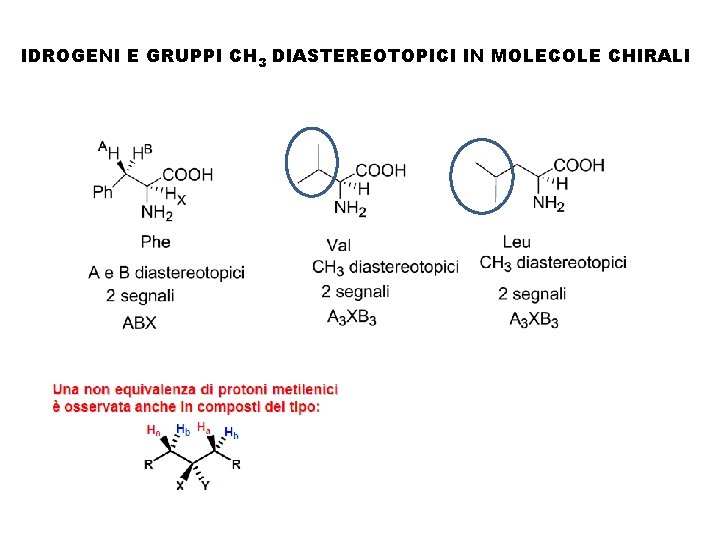
IDROGENI E GRUPPI CH 3 DIASTEREOTOPICI IN MOLECOLE CHIRALI

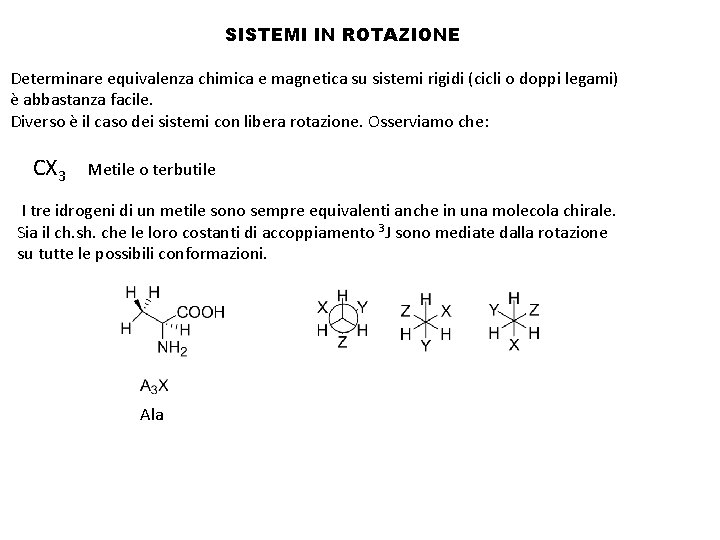
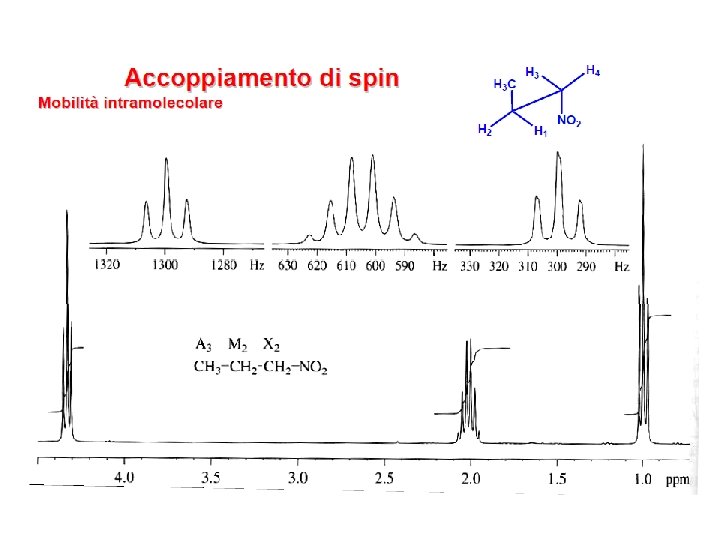
SISTEMI IN ROTAZIONE Determinare equivalenza chimica e magnetica su sistemi rigidi (cicli o doppi legami) è abbastanza facile. Diverso è il caso dei sistemi con libera rotazione. Osserviamo che: CX 3 Metile o terbutile I tre idrogeni di un metile sono sempre equivalenti anche in una molecola chirale. Sia il ch. sh. che le loro costanti di accoppiamento 3 J sono mediate dalla rotazione su tutte le possibili conformazioni. Ala

ORDINE DEGLI SPETTRI 1° ORDINE: SPETTRI DEBOLMENTE ACCOPPIATI Dn/J > 10 I parametri chemical shift e J sono ricavabili dagli spettri 2° ORDINE: SPETTRI FORTEMENTE ACCOPPIATI Dn/J < 7 I parametri chemical shift e J NON sono tutti ricavabili dagli spettri, sono richiesti calcoli


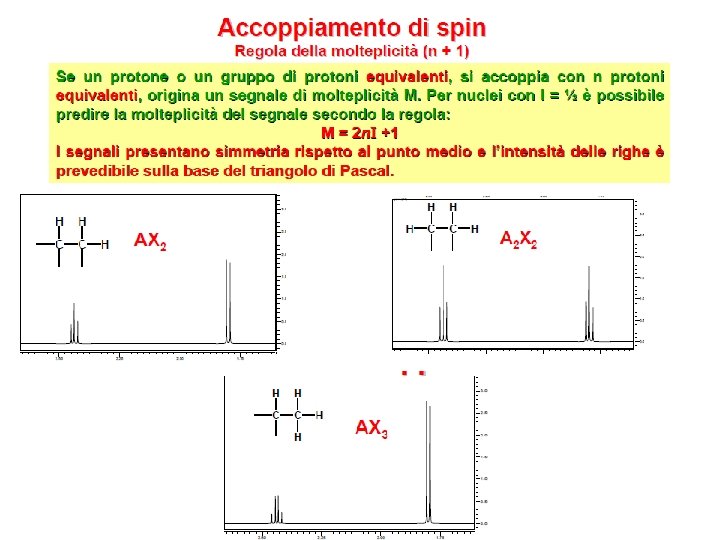
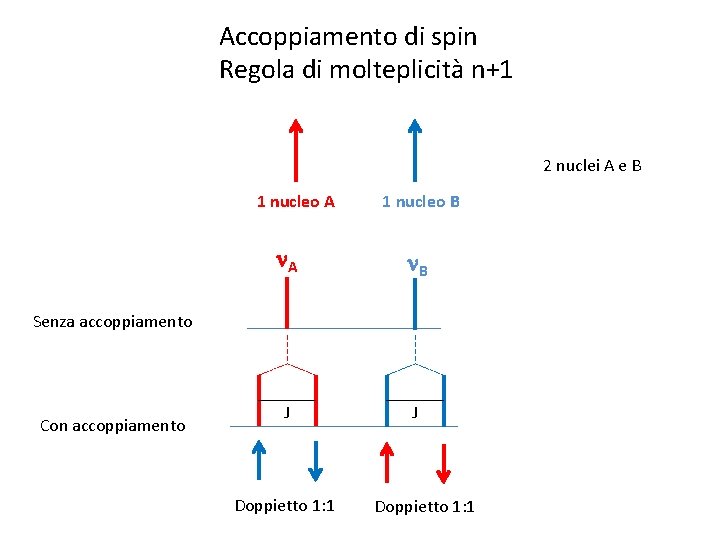
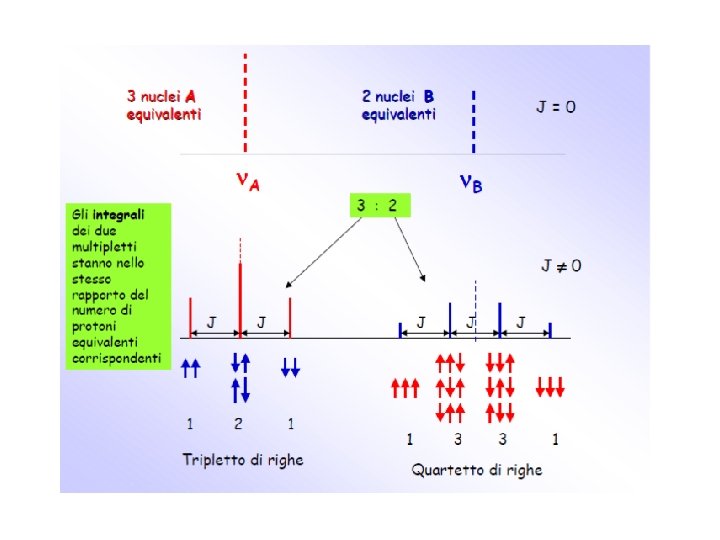
Accoppiamento di spin Regola di molteplicità n+1 2 nuclei A e B 1 nucleo A 1 nucleo B n. A n. B J J Senza accoppiamento Con accoppiamento Doppietto 1: 1



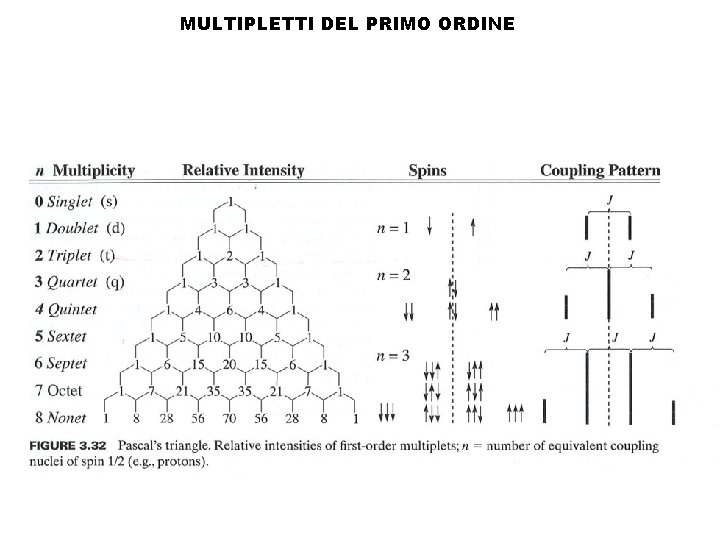
MULTIPLETTI DEL PRIMO ORDINE


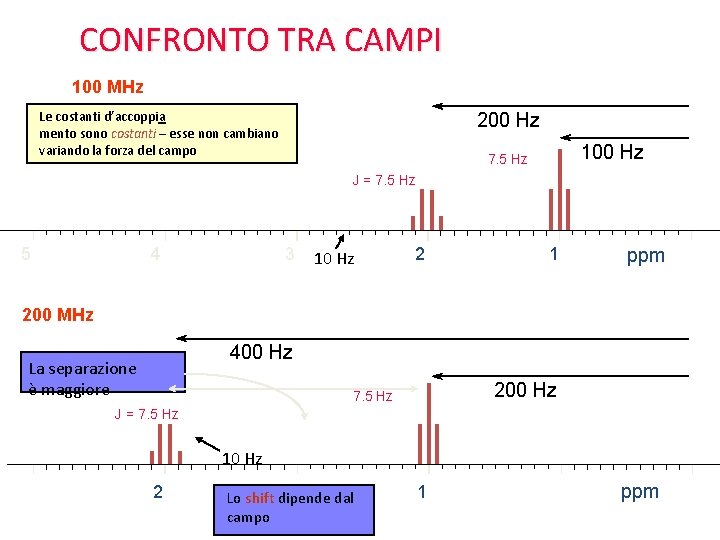
CONFRONTO TRA CAMPI 100 MHz Le costanti d’accoppia mento sono costanti – esse non cambiano variando la forza del campo 200 Hz 100 Hz 7. 5 Hz J = 7. 5 Hz 5 4 3 10 Hz 2 1 ppm 200 MHz 400 Hz La separazione è maggiore 200 Hz 7. 5 Hz J = 7. 5 Hz 10 Hz 2 Lo shift dipende dal campo 1 ppm

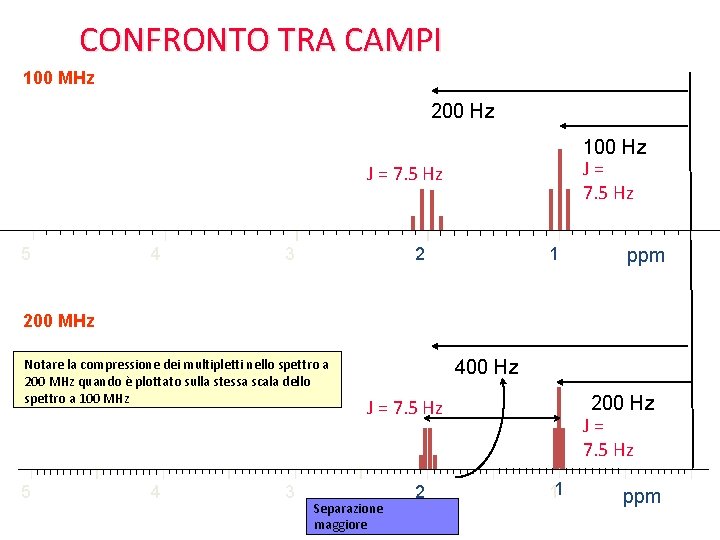
CONFRONTO TRA CAMPI 100 MHz 200 Hz 100 Hz J= 7. 5 Hz J = 7. 5 Hz 5 4 3 2 1 ppm 200 MHz Notare la compressione dei multipletti nello spettro a 200 MHz quando è plottato sulla stessa scala dello spettro a 100 MHz 5 4 3 400 Hz 200 Hz J= 7. 5 Hz J = 7. 5 Hz Separazione maggiore 2 11 ppm

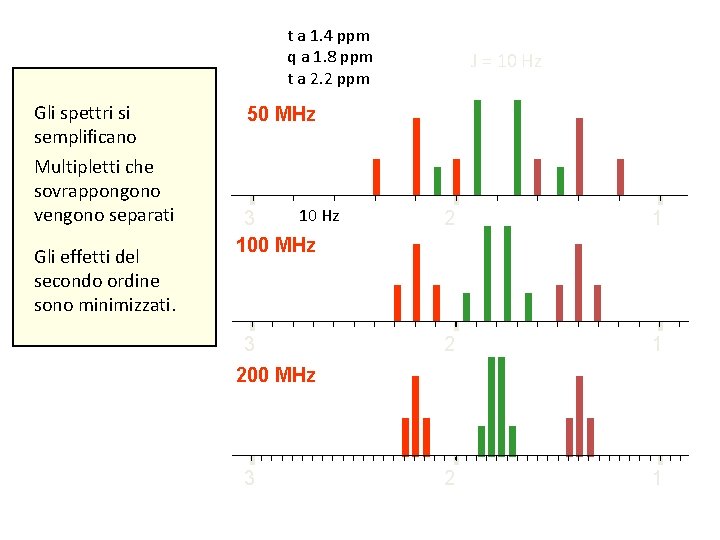
t a 1. 4 ppm q a 1. 8 ppm t a 2. 2 ppm Gli spettri si semplificano Multipletti che sovrappongono vengono separati Gli effetti del secondo ordine sono minimizzati. J = 10 Hz 50 MHz 10 Hz 3 100 MHz 3 2 1 2 1 200 MHz 3

ANALISI DEI SISTEMI DI SPIN


Sistemi di spin – Notazione di Pople

SPIN A E X accoppiati bb ba ab aa


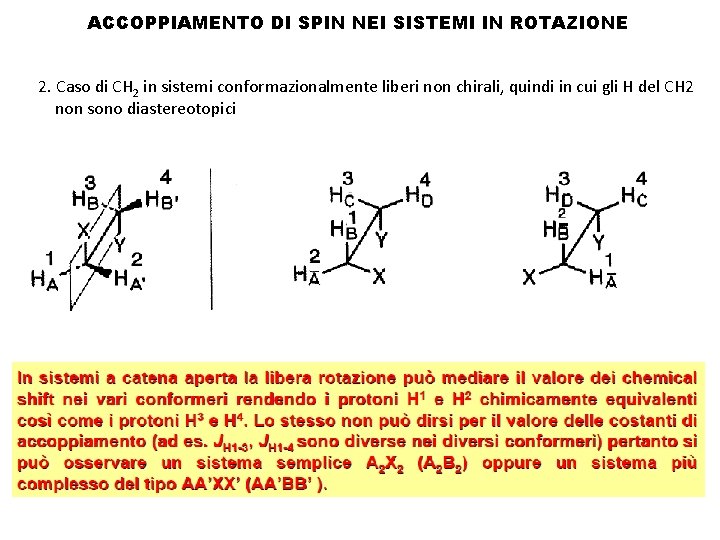
ACCOPPIAMENTO DI SPIN NEI SISTEMI IN ROTAZIONE 2. Caso di CH 2 in sistemi conformazionalmente liberi non chirali, quindi in cui gli H del CH 2 non sono diastereotopici

