UNIVERSIDAD DE LAS FUERZAS ARMADAS ESPE DEPARTAMENTO DE











- Slides: 27

UNIVERSIDAD DE LAS FUERZAS ARMADAS “ESPE” DEPARTAMENTO DE CIENCIAS DE LA VIDA Y LA AGRICULTURA CARRERA DE INGENIERÍA EN BIOTECNOLOGÍA PROYECTO DE TITULACIÓN PREVIO A LA OBTENCION DEL TÍTULO DE INGENIERA EN BIOTECNOLOGÍA “Síntesis y caracterización de nanopartículas de plata a partir del extracto de fruto de carrasquilla (Berberis hallii) y evaluación de su actividad fotocatalítica” AUTORA: GEOVANNA VICTORIA ARROYO PARDO DIRECTOR: ING. CUMBAL, LUIS. Ph. D. SANGOLQUÍ 2018

“Síntesis y caracterización de nanopartículas de plata a partir del extracto de fruto de carrasquilla (Berberis hallii) y evaluación de su actividad fotocatalítica” INTRODUCCIÓN MATERIALES Y MÉTODOS RESULTADOS Y DISCUCIÓN CONCLUSIONES Y RECOMENDACIONES AGRADECIMIENTOS

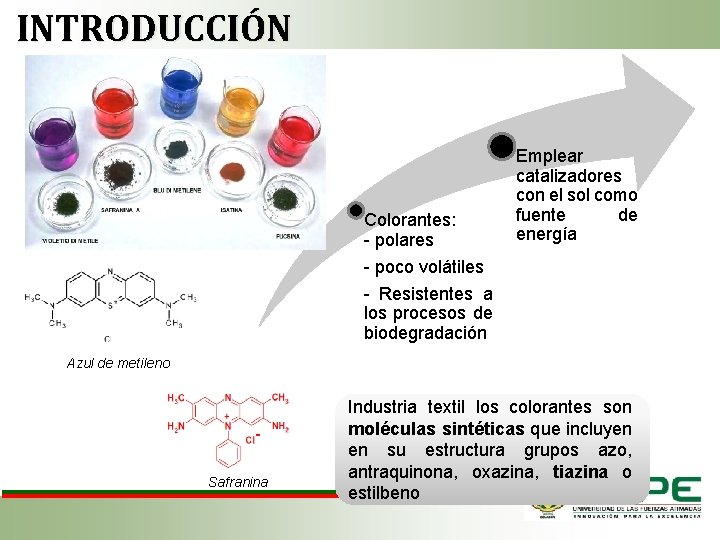
INTRODUCCIÓN Colorantes: - polares - poco volátiles - Resistentes a los procesos de biodegradación Emplear catalizadores con el sol como fuente de energía Azul de metileno Safranina Industria textil los colorantes son moléculas sintéticas que incluyen en su estructura grupos azo, antraquinona, oxazina, tiazina o estilbeno

• escala nano (10 -9 m). • Los metales en forma de nanomateriales exhiben propiedades físico químicas Metabolitos secundarios Nanotecnología INTRODUCCIÓN • Compuestos fenólicos: Antocianinas: protección de planta y coloración

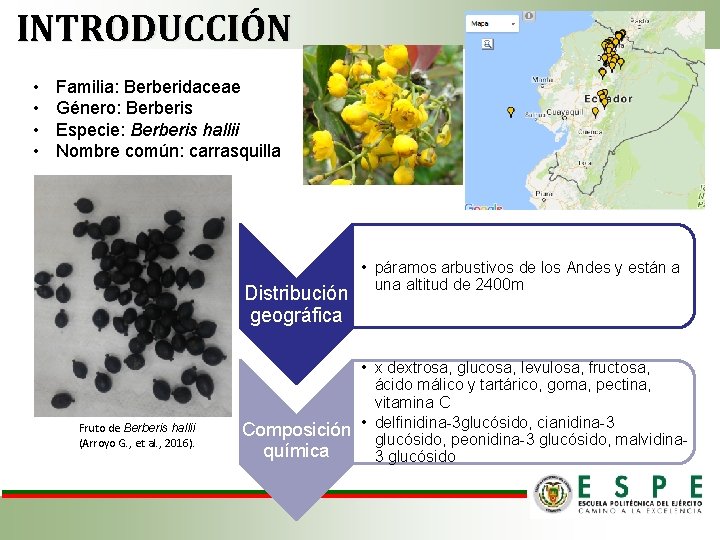
INTRODUCCIÓN • • Familia: Berberidaceae Género: Berberis Especie: Berberis hallii Nombre común: carrasquilla Distribución geográfica Fruto de Berberis hallii (Arroyo G. , et al. , 2016). • páramos arbustivos de los Andes y están a una altitud de 2400 m • x dextrosa, glucosa, levulosa, fructosa, ácido málico y tartárico, goma, pectina, vitamina C Composición • delfinidina-3 glucósido, cianidina-3 glucósido, peonidina-3 glucósido, malvidinaquímica 3 glucósido

INTRODUCCIÓN Objetivos Sintetizar y caracterizar nanopartículas de plata a partir de extracto de Carrasquilla (Berberis hallii) y evaluación de su actividad fotocatalítica en tintes textiles Obtener el extracto pigmentado de carrasquilla mediante maceración con un solvente polar. Establecer las condiciones óptimas para la síntesis de nanopartículas usando el pigmento de carrasquilla. Caracterizar las muestras obtenidas utilizando técnicas espectroscópicas, microscópicas, de difracción y con pruebas electroquímicas. Evaluar el porcentaje de degradación fotocatalítica de colorantes sintéticos asistida por nanopartículas de plata.

MATERIALES Y MÉTODOS Preparación del material vegetal Berberis hallii Licuado en el solvente Muestra filtrada Concentrar el extracto Extracción de grasas T: 40 °C P: 61 -70 mbar V: 125 rpm rotavapor, marca Buchi R-210 profesional Filtración al vacío

MATERIALES Y MÉTODOS Evaluación de la estabilidad en el tiempo del material vegetal Muestra homogénea Alícuota de muestra Conservació n de la solución Actividad antioxidante del extracto Ensayo TCP Ensayo DPPH 765 nm 517 nm 2, 2 -difenil-1 -picrilhidracilo

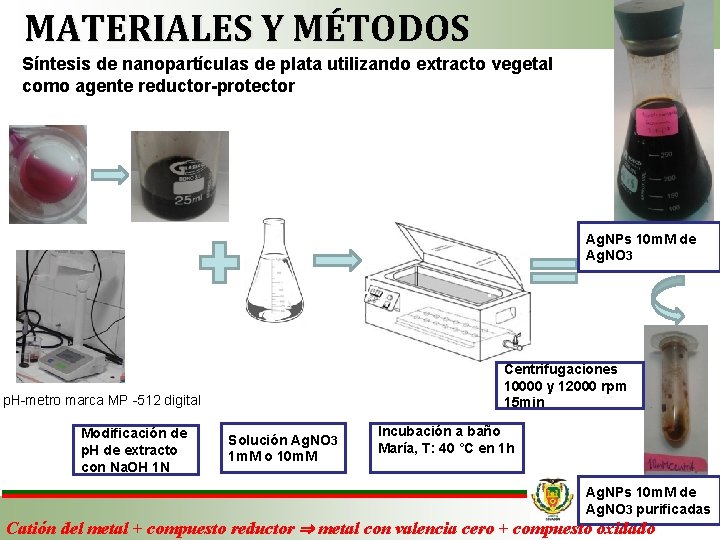
MATERIALES Y MÉTODOS Síntesis de nanopartículas de plata utilizando extracto vegetal como agente reductor-protector Ag. NPs 10 m. M de Ag. NO 3 Centrifugaciones 10000 y 12000 rpm 15 min p. H-metro marca MP -512 digital Modificación de p. H de extracto con Na. OH 1 N Solución Ag. NO 3 1 m. M o 10 m. M Incubación a baño María, T: 40 °C en 1 h Ag. NPs 10 m. M de Ag. NO 3 purificadas Catión del metal + compuesto reductor ⇒ metal con valencia cero + compuesto oxidado

MATERIALES Y MÉTODOS Técnicas de Caracterización espectroscópicas Espectroscopia ultravioleta-visible espectroscopia de emisión de fotones 300 -800 nm Dynamic Light Scattering Tamaño de partícula en suspensión acuosa Técnicas de Caracterización microscópicas Microscopio electrónico de barrido en modo de transmisión STEM tensión 30 k. V, modo de escaneo resolution, WD: 5, 8 nm

MATERIALES Y MÉTODOS Técnicas de Caracterización de difracción Difracción de rayos X Interpretación de difractogramas Pruebas electroquímicas de extracto y agnps Voltametría cíclica Respuesta corriente-potencial. 4 números de cruces de parada y que corra de -1, 2 a 1, 2 e. V el rango de SHE vs SCE. A una velocidad de 0, 05 V/s.

MATERIALES Y MÉTODOS Degradación de colorantes asistido por nanopartículas de plata Liofilizador frezze dryer Porcentaje de degradación de colorantes Lámpara simulador solar 30 cm de distancia muestrarayo de luz y potencia de 387 W.

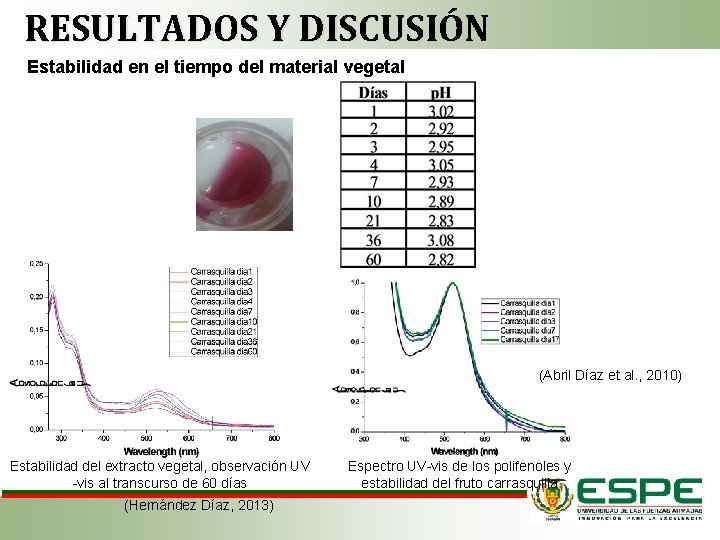
RESULTADOS Y DISCUSIÓN Estabilidad en el tiempo del material vegetal (Abril Díaz et al. , 2010) Estabilidad del extracto vegetal, observación UV -vis al transcurso de 60 días (Hernández Díaz, 2013) Espectro UV-vis de los polifenoles y estabilidad del fruto carrasquilla

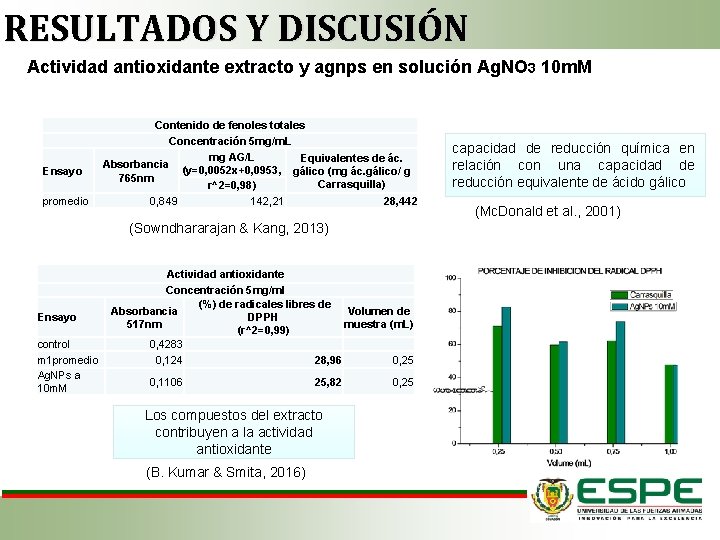
RESULTADOS Y DISCUSIÓN Actividad antioxidante extracto y agnps en solución Ag. NO 3 10 m. M Ensayo promedio Contenido de fenoles totales Concentración 5 mg/m. L mg AG/L Equivalentes de ác. Absorbancia (y=0, 0052 x+0, 0953, gálico (mg ác. gálico/ g 765 nm Carrasquilla) r^2=0, 98) 0, 849 142, 21 28, 442 (Sowndhararajan & Kang, 2013) Ensayo control m 1 promedio Ag. NPs a 10 m. M Actividad antioxidante Concentración 5 mg/ml (%) de radicales libres de Absorbancia Volumen de DPPH 517 nm muestra (m. L) (r^2=0, 99) 0, 4283 0, 124 28, 96 0, 25 0, 1106 25, 82 Los compuestos del extracto contribuyen a la actividad antioxidante (B. Kumar & Smita, 2016) 0, 25 capacidad de reducción química en relación con una capacidad de reducción equivalente de ácido gálico (Mc. Donald et al. , 2001)

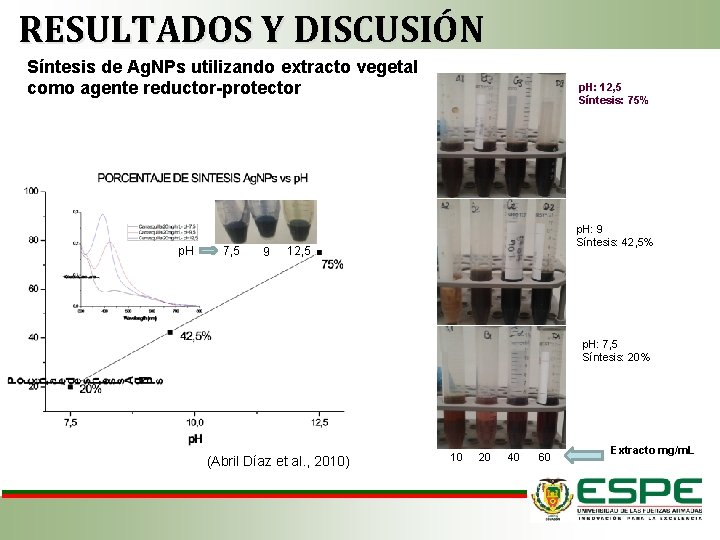
RESULTADOS Y DISCUSIÓN Síntesis de Ag. NPs utilizando extracto vegetal como agente reductor-protector p. H 7, 5 9 p. H: 12, 5 Síntesis: 75% p. H: 9 Síntesis: 42, 5% 12, 5 p. H: 7, 5 Síntesis: 20% (Abril Díaz et al. , 2010) 10 20 40 60 Extracto mg/m. L

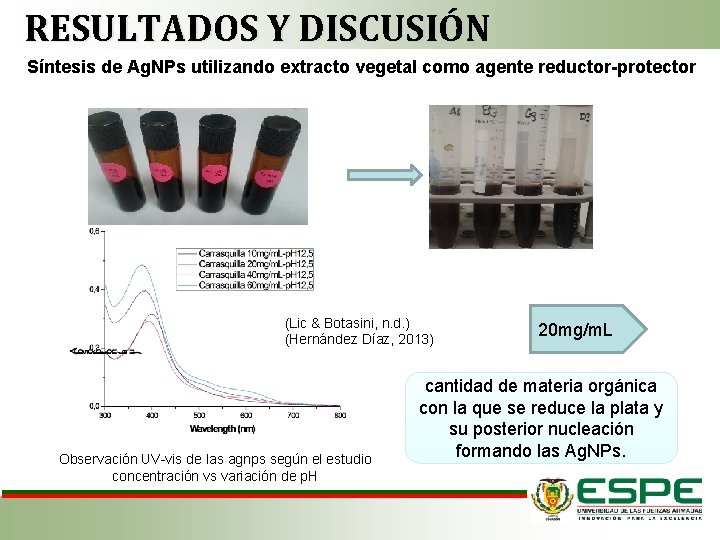
RESULTADOS Y DISCUSIÓN Síntesis de Ag. NPs utilizando extracto vegetal como agente reductor-protector (Lic & Botasini, n. d. ) (Hernández Díaz, 2013) Observación UV-vis de las agnps según el estudio concentración vs variación de p. H 20 mg/m. L cantidad de materia orgánica con la que se reduce la plata y su posterior nucleación formando las Ag. NPs.

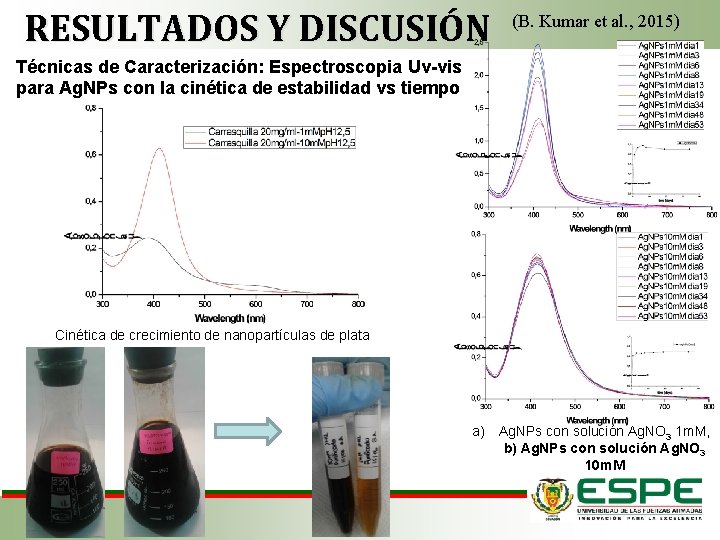
RESULTADOS Y DISCUSIÓN (B. Kumar et al. , 2015) Técnicas de Caracterización: Espectroscopia Uv-vis para Ag. NPs con la cinética de estabilidad vs tiempo Cinética de crecimiento de nanopartículas de plata a) Ag. NPs con solución Ag. NO 3 1 m. M, b) Ag. NPs con solución Ag. NO 3 10 m. M

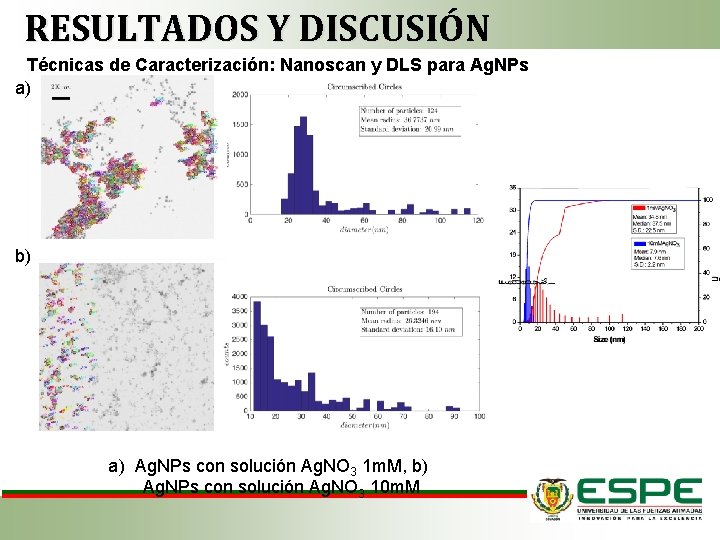
RESULTADOS Y DISCUSIÓN Técnicas de Caracterización: Nanoscan y DLS para Ag. NPs a) b) a) Ag. NPs con solución Ag. NO 3 1 m. M, b) Ag. NPs con solución Ag. NO 3 10 m. M

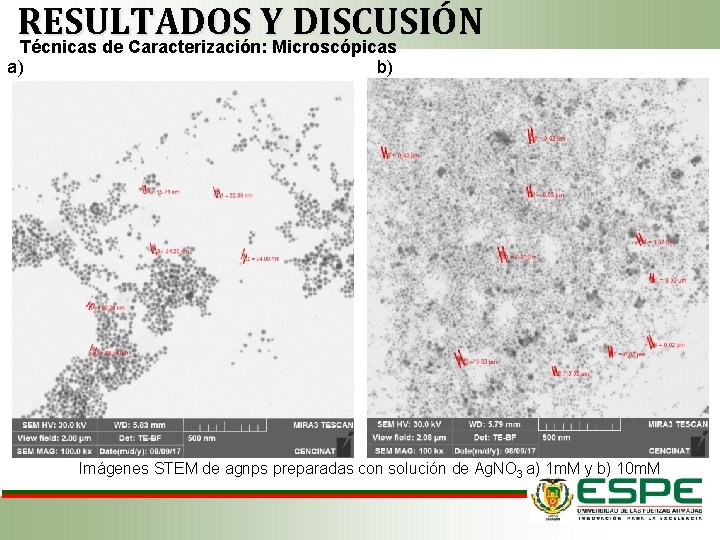
RESULTADOS Y DISCUSIÓN Técnicas de Caracterización: Microscópicas a) b) Imágenes STEM de agnps preparadas con solución de Ag. NO 3 a) 1 m. M y b) 10 m. M

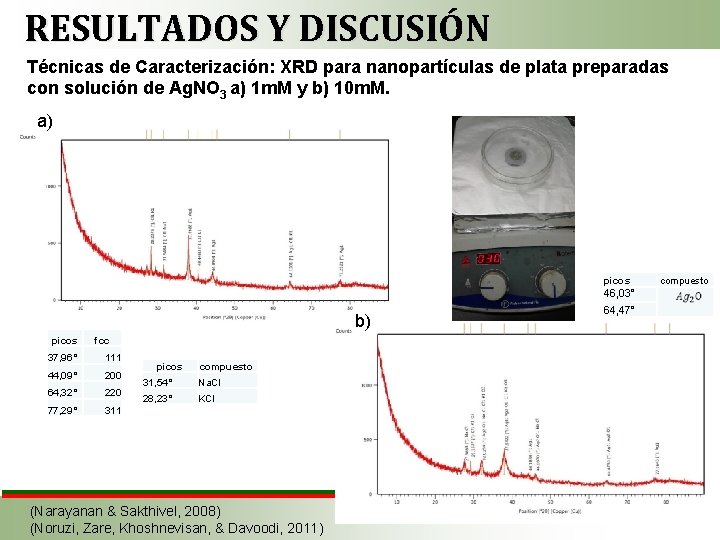
RESULTADOS Y DISCUSIÓN Técnicas de Caracterización: XRD para nanopartículas de plata preparadas con solución de Ag. NO 3 a) 1 m. M y b) 10 m. M. a) picos 46, 03° b) picos fcc 37, 96° 111 44, 09° 200 64, 32° 220 77, 29° 311 picos compuesto 31, 54° Na. Cl 28, 23° KCl (Narayanan & Sakthivel, 2008) (Noruzi, Zare, Khoshnevisan, & Davoodi, 2011) 64, 47° compuesto

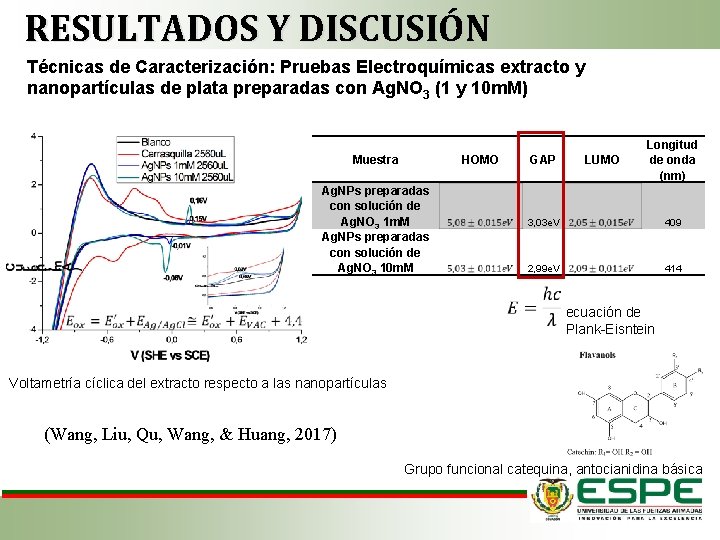
RESULTADOS Y DISCUSIÓN Técnicas de Caracterización: Pruebas Electroquímicas extracto y nanopartículas de plata preparadas con Ag. NO 3 (1 y 10 m. M) Muestra HOMO GAP Ag. NPs preparadas con solución de Ag. NO 3 1 m. M Ag. NPs preparadas con solución de Ag. NO 3 10 m. M LUMO Longitud de onda (nm) 3, 03 e. V 409 2, 99 e. V 414 ecuación de Plank-Eisntein Voltametría cíclica del extracto respecto a las nanopartículas (Wang, Liu, Qu, Wang, & Huang, 2017) Grupo funcional catequina, antocianidina básica

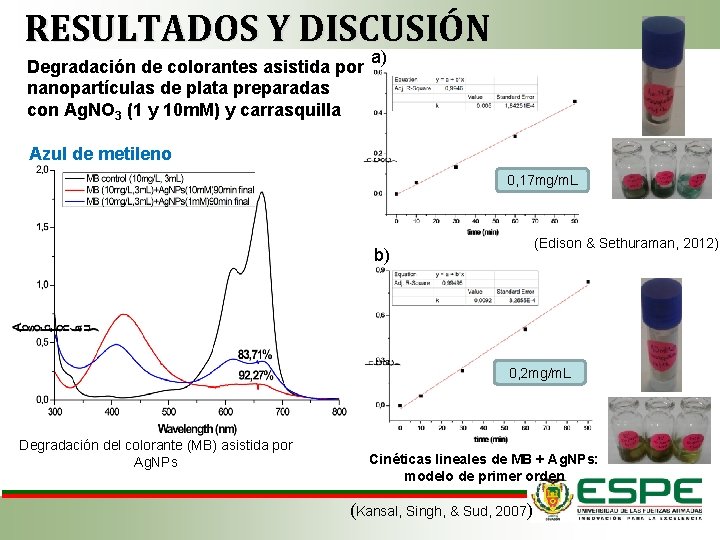
RESULTADOS Y DISCUSIÓN Degradación de colorantes asistida por nanopartículas de plata preparadas con Ag. NO 3 (1 y 10 m. M) y carrasquilla a) Azul de metileno 0, 17 mg/m. L (Edison & Sethuraman, 2012) b) 0, 2 mg/m. L Degradación del colorante (MB) asistida por Ag. NPs Cinéticas lineales de MB + Ag. NPs: modelo de primer orden (Kansal, Singh, & Sud, 2007)

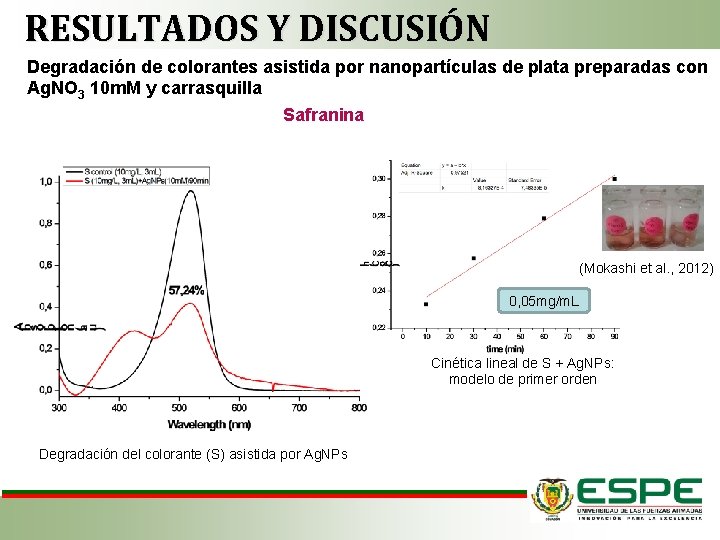
RESULTADOS Y DISCUSIÓN Degradación de colorantes asistida por nanopartículas de plata preparadas con Ag. NO 3 10 m. M y carrasquilla Safranina (Mokashi et al. , 2012) 0, 05 mg/m. L Cinética lineal de S + Ag. NPs: modelo de primer orden Degradación del colorante (S) asistida por Ag. NPs

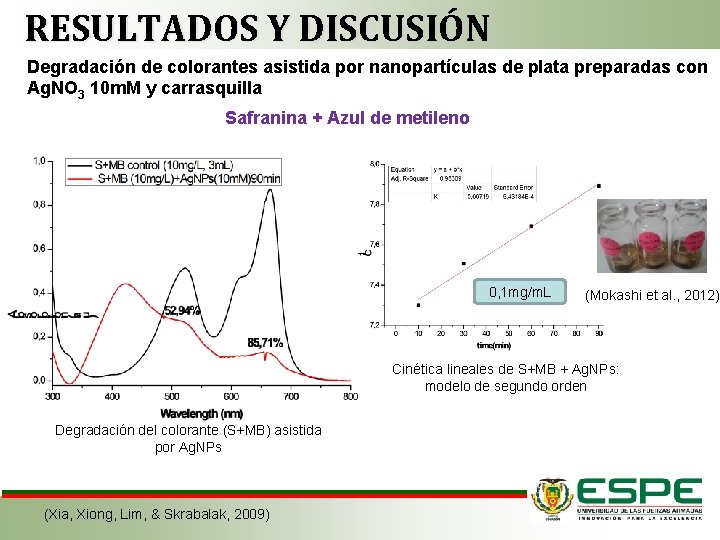
RESULTADOS Y DISCUSIÓN Degradación de colorantes asistida por nanopartículas de plata preparadas con Ag. NO 3 10 m. M y carrasquilla Safranina + Azul de metileno 0, 1 mg/m. L (Mokashi et al. , 2012) Cinética lineales de S+MB + Ag. NPs: modelo de segundo orden Degradación del colorante (S+MB) asistida por Ag. NPs (Xia, Xiong, Lim, & Skrabalak, 2009)

CONCLUSIONES • La obtención del extracto pigmentado de carrasquilla mediante maceración con un solvente polar, permitió mantenerlo a p. H ácido y conservarlo seco como materia prima para la síntesis de Ag. NPs. • Excelente la estabilidad y actividad antioxidante del extracto asegura la síntesis de Ag. NPs. • Se estableció que las condiciones óptimas para realizar la síntesis de las nanopartículas fueron: concentración de extracto, 20 mg/m. L; p. H~12, 5; tiempo de temperatura de incubación de 1 h; proceso de purificación, con centrifugaciones a 10000 y 12000 rpm por 15 min y posterior liofilización. • Hubo diferencias de porcentaje de remoción del colorante azul de metileno utilizando distintas Ag. NPs. • La safranina se degrado alrededor del 50%, conservando su coloración al finalizar el ensayo. • La actividad catalítica de las Ag. NPs depende del método de síntesis de nanopartículas, ya que relaciona el tamaño y morfología resultantes. Además, la estructura cristalina, el área superficial específica.

RECOMENDACIONES • Para realizar una caracterización completa de las Ag. NPs y del extracto vegetal se recomienda emplear otras técnicas, como FTIR, que permita identificar las biomoleculas del extracto que interactúan con las Ag. NPs. • En el proceso de optimizar la síntesis de Ag. NPs, se requiere un control del tamaño de Ag. NPs para evitar un valor alto de desviación estándar, por ejemplo aumentar la concentración del precursor o el volumen de extracto. • En cada ensayo de degradación se recomienda hacer la acción catalítica de Ag. NPs y S, con el fin de obtener la molécula de mineralización y comprobar si no afecta al ambiente.

AGRADECIMIENTOS § Universidad de las Fuerzas Armadas – ESPE § Centro de Nanociencia y nanotecnología Ing. Luis Cumbal, Ph. D. § Investigadora en nanomateriales orgánicos e híbridos Yolanda Angulo, Ph. D. § Jefe del Laboratorio de Caracterización de Nanomateriales Alexis Debut, Ph. D § Técnico del laboratorio de Caracterización de Nanomateriales Ing. Karla Vizuete § Técnico del centro de Nanociencia y nanotecnología Ing. Carina Stael