Termokimia Perubahan kimia suhu endapan warna gelembung Taukah

Termokimia
Perubahan kimia suhu endapan warna gelembung

Taukah kamu? ? Berasal dari mana energi yang kita gunakan sehari-hari? Contohnya: berlari, bermain, berkuda, belajar. Berasal dr rx dalam tubuh Bahan makanan masuk ke tubuh terjadi rangkaian reaksi kimia energi Energi
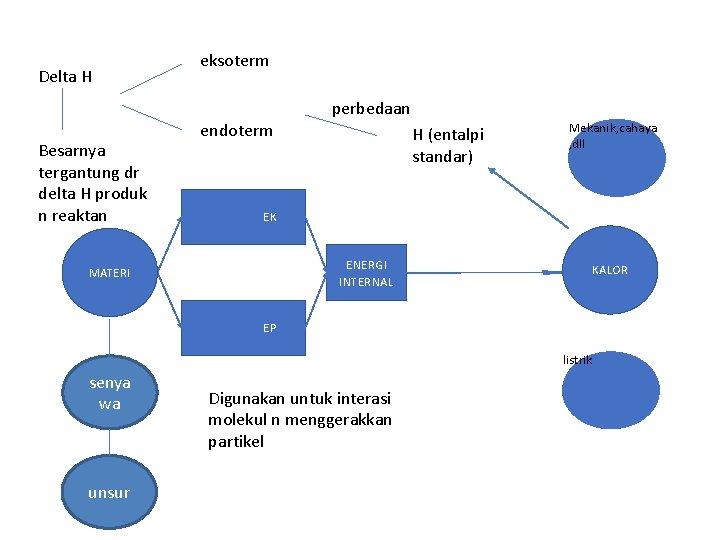
Delta H eksoterm perbedaan Besarnya tergantung dr delta H produk n reaktan endoterm H (entalpi standar) Mekanik, cahaya , dll EK ENERGI INTERNAL MATERI KALOR EP listrik senya wa unsur Digunakan untuk interasi molekul n menggerakkan partikel

Bahan Kajian Termokimia • Bahan kajian termokimia adalah penerapan hukum kekekalan energi dan hukum termodinamika I dalam bidang kimia. Hukum kekekalan energi berbunyi : 1. Energi tidak dapat diciptakan dan tidak dapat dimusnahkan. 2. Energi dapat berubah bentuk menjadi energi lain.
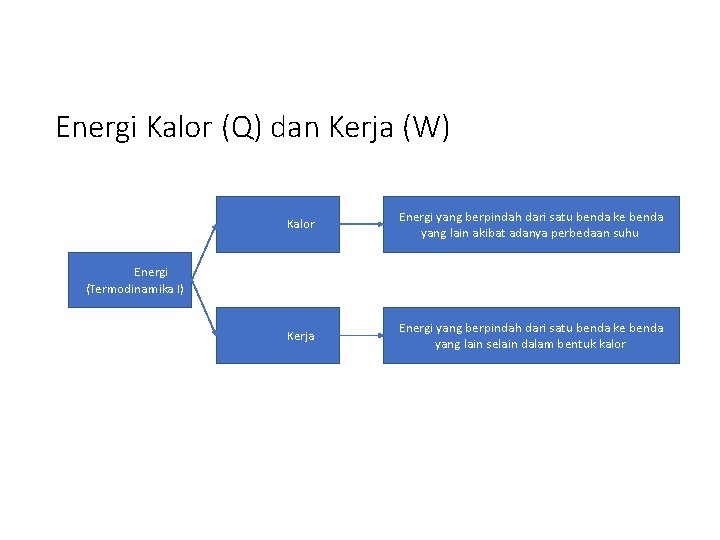
Energi Kalor (Q) dan Kerja (W) Kalor Energi yang berpindah dari satu benda ke benda yang lain akibat adanya perbedaan suhu Kerja Energi yang berpindah dari satu benda ke benda yang lain selain dalam bentuk kalor Energi (Termodinamika I)
Energi Termokimia Bahasan Ilmu kimia yang berhubungan dengan energi Jika energi yang terkadung dari materi berubah, perubahan energi ini dinamakan dengan kalor. Jika ada perubahan kalor pada tekanan tetap, kita namakan sebagai perubahan entalpi/ ∆H. Tidak semua materi dapat dihitung, materi hanya dapat dihitung dengan kecepatan cahaya. Rumus eistein E=MC 2. Kita tidak bs mengukur energi dalam materi, jadi yang bisa diukur adalah perubahannya.

Energi Kalor (q) • Kapasitas kalor adalah banyaknya energi kalor yang dibutuhkan untuk meningkatkan suhu zat 1 o. C. • Kapasitas kalor spesifik (kalor jenis) adalah banyaknya energi kalor yang dibutuhkan untuk meningkatkan suhu 1 o. C zat sebesar 1 gram. • Kalor jenis molar adalah banyaknya energi kalor yang dibutuhkan untuk meningkatkan suhu 1 mol zat sebesar 1 o. C.



Pengertian Termokimia adalah cabang dari ilmu kimia yang mempelajari hubungan antara reaksi kimia dengan panas.

Proses Perpindahan energi Energi berpindah : Dari lingkungan sistem Sistem lingkungan Sistem : segala sesuatu yang kita pelajari perubahan energinya reaksi. Sesuatu yang bereaksi Lingkungan : segala sesuatu yang mengelilingi sistem dan terpengaruh oleh sistem. Segala sesuatu di luar reaksi. Contoh: gelas kimia yang terpengaruhi oleh zat yang bereaksi.
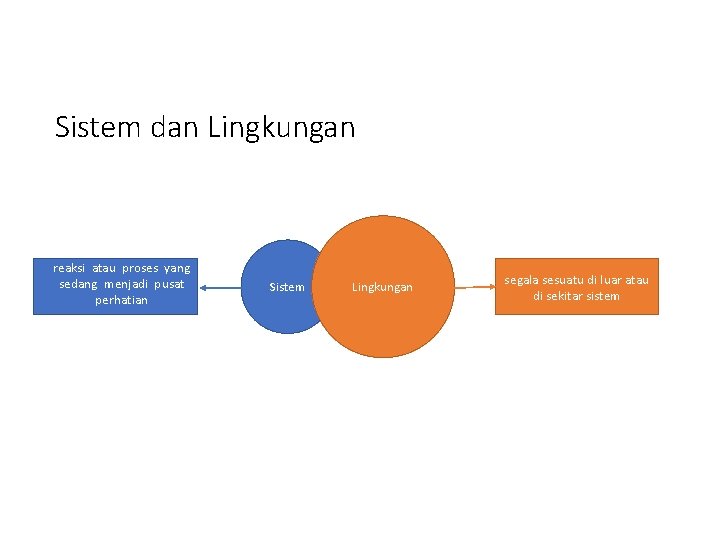
Sistem dan Lingkungan reaksi atau proses yang sedang menjadi pusat perhatian Sistem Lingkungan segala sesuatu di luar atau di sekitar sistem

Sistem • Berdasarkan interaksinya dengan lingkungan, sistem dibedakan menjadi tiga macam, yaitu :
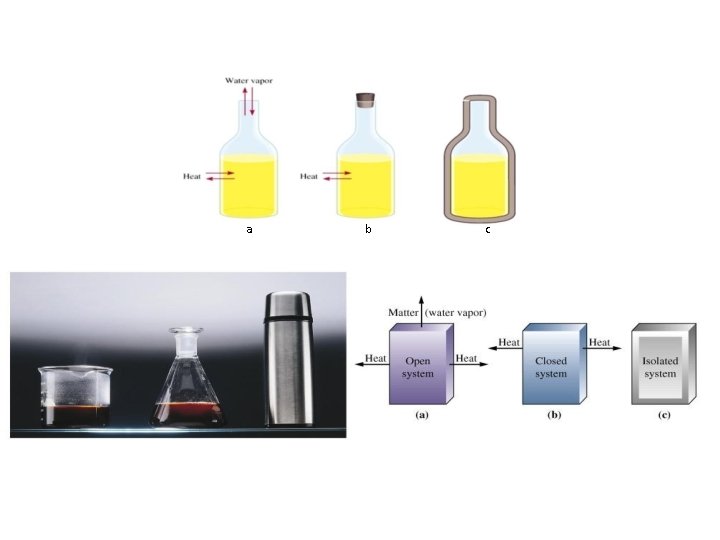
a b c

Reaksi Eksoterm dan Endoterm • Dalam konsep termokimia, reaksi terbagi menjadi dua, yaitu reaksi eksoterm dan reaksi endoterm. • Reaksi eksoterm, yaitu reaksi yang sistemnya membebaskan/ melepas energi, sehingga lingkungan menjadi naik temperaturnya. Contoh: reaksi diatas suhu kamar (pembakaran), pelarutan Na. OH, reaksi Mg dengan HCl. • Reaksi endoterm, yaitu reaksi yang sistemnya menyerap/menerima energi, sehingga lingkungan menjadi turun temperaturnya. • Contoh: reaksi Ba(OH)2 dengan NH 4 Cl
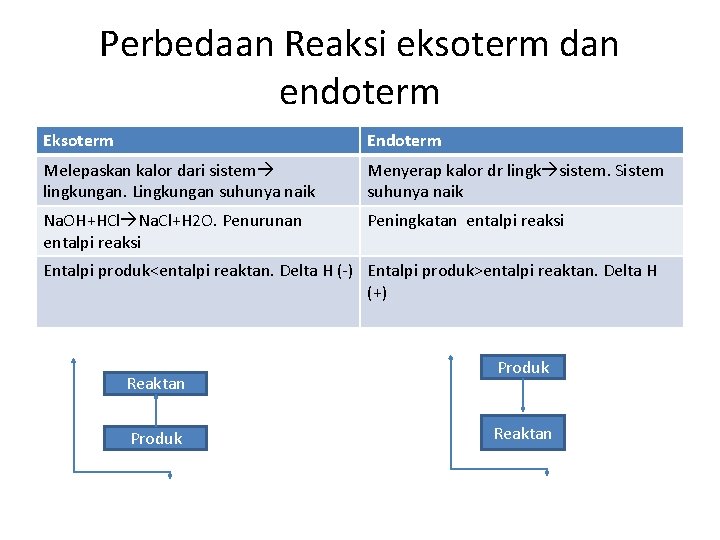
Perbedaan Reaksi eksoterm dan endoterm Eksoterm Endoterm Melepaskan kalor dari sistem lingkungan. Lingkungan suhunya naik Menyerap kalor dr lingk sistem. Sistem suhunya naik Na. OH+HCl Na. Cl+H 2 O. Penurunan entalpi reaksi Peningkatan entalpi reaksi Entalpi produk<entalpi reaktan. Delta H (-) Entalpi produk>entalpi reaktan. Delta H (+) Reaktan Produk Reaktan

1. Ental pembentukan standar pi • Entalpi pembentukan standar (ΔH°f) adalah energi yang diterima atau dilepas untuk membentuk 1 mol zat dari unsur pembentuknya. • Nilai entalpi pembentukan standar ditentukan menggunakan data entalpi pembentukan standar. • Nilai-nilai entalpi pembentukan standar:

2. Ental penguraian standar pi • Entalpi penguraian standar (ΔH°d) adalah energi yang diterima atau dilepas untuk mengurai 1 mol zat menjadi unsur pembentuknya. • Nilai entalpi penguraian standar berlawanan dengan nilai entalpi pembentukan standar. • Pada reaksi penguraian, reaktan berpindah ke kanan dan produk berpindah ke kiri

3. Ental pembakaran standar pi • Entalpi pembakaran standar (ΔH°c) adalah jumlah energi yang dilepaskan untuk membakar 1 mol zat. • Nilai entalpi pembakaran standar ditentukan menggunakan data entalpi pembakaran standar. • Ciri utama dari reaksi pembakaran adalah: 1) Merupakan reaksi eksoterm. 2) Melibatkan oksigen (O 2) dalam reaksinya. 3) Karbon terbakar menjadi CO 2, hidrogen terbakar menjadi H 2 O, nitrogen terbakar menjadi NO 2, belerang terbakar menjadi SO 2. • Contoh:

4. Perubahan Entalpi Netralisasi Hn 0 Perubahan entalpi netralisasi adalah perubahan entalpi yang terjadi pada saat reaksi antara asam dengan basa baik tiap mol asam atau tiap mol basa. • Contoh: Na. OH(aq) + HCl(aq) Na. Cl(aq) + H 2 O(l) Hn 0 = -57, 1 k. J mol-1
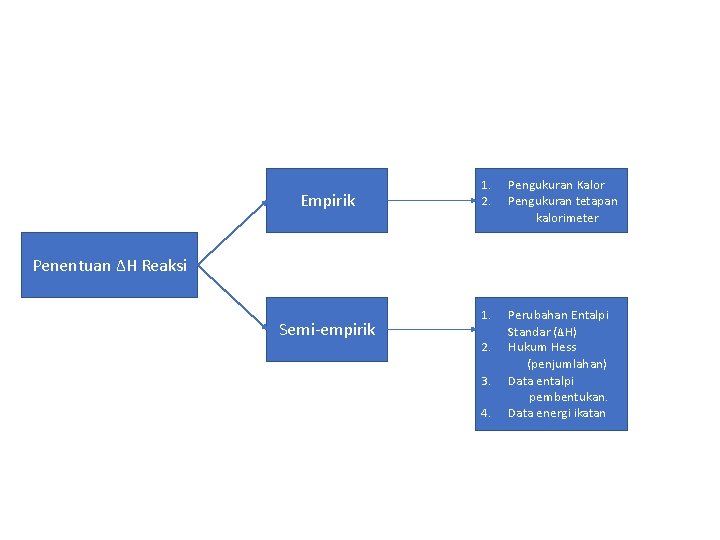
Empirik 1. 2. Pengukuran Kalor Pengukuran tetapan kalorimeter 1. Perubahan Entalpi Standar (ΔH) Hukum Hess (penjumlahan) Data entalpi pembentukan. Data energi ikatan Penentuan ΔH Reaksi Semi-empirik 2. 3. 4.

Penentuan ΔH Reaksi secara Empirik 1. Pengukuran Kalor (q) • Kapasitas kalor adalah banyaknya energi kalor yang dibutuhkan untuk meningkatkan suhu zat 1 o. C. • Kapasitas kalor spesifik (kalor jenis) adalah banyaknya energi kalor yang dibutuhkan untuk meningkatkan suhu 1 gram zat sebesar 1 o. C. • Kalor jenis molar adalah banyaknya energi kalor yang dibutuhkan untuk meningkatkan suhu 1 mol zat sebesar 1 o. C. • Banyaknya kalor = massa zat x kalor jenis x perubhan suhu.

Contoh : Berapakah kalor yang diperlukan untuk meningkatkan suhu 735 gram air dari 21 o. C menjadi 98 o. C (anggaplah bahwa kalor jenis air tetap yaitu 1, 00 kal g-1 o. C-1 dalam seluruh kisaran suhu ini) Jawab : • Banyaknya kalor = massa zat x kalor jenis x perubhan suhu • Q=mc T Δ • Q = 735 gram x 1 kal g-1 o. C-1 x (98 – 21)o. C • Q = 5, 66 x 104 kal

2. Pengukuran Tetapan Kalorimeter • Kalorimetri adalah cara penentuan energi kalor reaksi dengan kalorimeter. • Kalorimeter adalah sistem terisolasi, sehingga semua energi yang dibutuhkan atau dibebaskan tetap berada dalam kalorimeter • Besarnya kalor yang diserap atau dilepaskan oleh kalorimeter dihitung dengan persamaan: Qk = Ck * T Heat gained Temperature difference Heat capacity Total heat evolved = qtotal = qwater + qbomb

Contoh: Ke dalam kalorimeter dituangkan 50 g air dingin (25°C), kemudian ditambahkan 75 g air panas (60°C) sehingga suhu campuran menjadi 35°C. Jika suhu kalorimeter naik sebesar 7°, tentukan kapasitas kalorimeter? Diketahui kalor jenis air = 4, 18 J g– 1 °C– 1. Jawab: • Kalor yang dilepaskan air panas sama dengan kalor yang diserap air dingin dan kalorimeter. • QAir panas = QAir dingin+ QKalorimeter

QAir panas = + m c T Δ QAir dingin = + m c ΔT

Contoh : Dalam kalorimeter yang telah dikalibrasi dan terbuka direaksikan 50 g alkohol dan 3 g logam natrium. Jika suhu awal campuran 30°C dan setelah reaksi suhunya 75°C, tentukan ΔH reaksi. Diketahui kalor jenis larutan 3, 65 J g– 1°C– 1, kapasitas kalorimeter 150 J °C– 1, dan suhu kalorimeter naik sebesar 10°C Jawab : • Kalor yang terlibat dalam reaksi: Qreaksi = ΔHreaksi = – 10, 205 k. J

Kapasitas Kalor

Contoh: • Sepotong besi yang memiliki massa 3 kg, dipanaskan dari suhu 20° C hingga 120° C. Jika kalor yang diserap besi sebesar 135 k. J. Tentukan kapasitas kalor besi dan kalor jenis besi? Diketahui : m = 3 kg ∆T = 120° – 20° = 100° C Q = 135 k. J

Contoh soal Dalam kalorimeter yang telah dikaliberasi dan terbuka, direaksikan 50 g alkohol dan 3 g logam natrium. Jika Suhu awal campuran 30 ⁰C dan setelah reaksi suhunya 75 ⁰C. Tentukan H reaksi. Diketahui kalor jenis larutan 3, 65 J/g ⁰ C. Kapasitas kalorimeter 150 J /⁰ C. Dan suhu kalorimeter sebesar 10 ⁰ C. Tentukan perubahan entalpinya

Q larutan : m. c. t (50+3)gx 3, 65 J/g ⁰ Cx(75 -30) ⁰ C = 8705, 25 J Q kalorimeter: Ck. t 150 J /⁰ C x 10 ⁰ C=1500 J Q reaksi = -(Q larutan+Q kalorimeter ) Q reaksi = -(8705, 25 J+1500 J) =10205, 25 J Jadi reaksi alkohol dengan logan natrium melepaskan kalor sebesar 10205, 25 J (NB: direaksikan pada tekanan tetap) Q reaksi= H=10205, 25 J

Penentuan ΔH secara Semiempirik Perubahan Entalpi Standar (ΔH) a. Pada Reaksi Eksoterm P + Q R + x Kkal P dan Q = zat awal R = zat hasil reaksi x = besarnya panas reaksi Menurut hukum kekekalan energi : Isi panas (P + Q) = Isi panas R + x Kkal H (P + Q) = H ( R) + x Kkal H (R) - H (P + Q) = - x Kkal ΔH = - x Kkal b. Pada Reaksi Endoterm R P+Q Berlaku : H (P + Q) - H (R) ΔH = x Kkal – x Kkal

Contoh : Hitung entalpi perubahan CH 4 (g) menjadi CO 2 (g) dan H 2 O(g) Pada temperatur 298 o. K, bila diketahui pada temperature tersebut : ΔH. CH 4 = -74, 873 KJ mol-1 ; ΔH. O 2 = 0, 00 KJ mol-1; CO 2 = - 393, 522 KJ mol-1 dan ΔH. H 2 O = -241, 827 KJ mol-1 ? Jawab : • CH 4 + O 2 → CO 2 + H 2 O (setimbangkan koefisiennya) • CH 4 + 2 O 2 → CO 2 + 2 H 2 O • ΔH = Δ H {CO 2 + (2 x H 2 O)} – ΔH {CH 4 + (2 x O 2)} • ΔH = {- 393, 522 + (2 x (- 241, 827)} - {- 74, 873 + (2 x 0, 000)} • ΔH = - 802, 303 KJ mol-1 • Tanda negatif menunjukkan bahwa reaksi di atas merupakan reaksi eksoterm.

Hukum Hess • Hukum Hess muncul berdasarkan fakta bahwa banyak pembentukan senyawa dari unsur-unsurnya tidak dapat diukur perubahan entalpinya secara laboratorium. • Berdasarkan hasil pengukuran dan sifat-sifat entalpi, Hess menyatakan bahwa entalpi hanya bergantung pada keadaan awal dan akhir reaksi maka perubahan entalpi tidak bergantung pada jalannya reaksi (proses). • Contoh: Reaksi pembentukan asam sulfat dari unsur-unsurnya. S(s) + H 2(g) + 2 O 2(g)→H 2 SO 4(l) • Pembentukan asam sulfat dari unsur-unsurnya tidak terjadi sehingga tidak dapat diukur langsung perubahan entalpinya
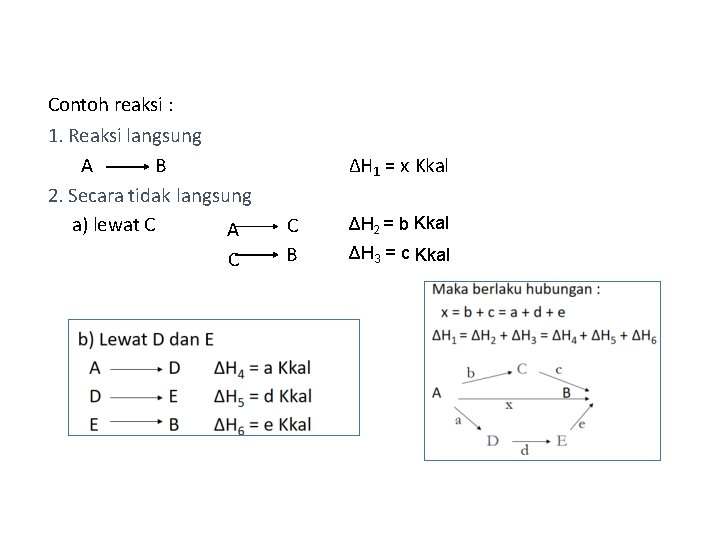
Contoh reaksi : 1. Reaksi langsung A B 2. Secara tidak langsung a) lewat C A C ΔH 1 = x Kkal C B ΔH 2 = b Kkal ΔH 3 = c Kkal

Contoh:
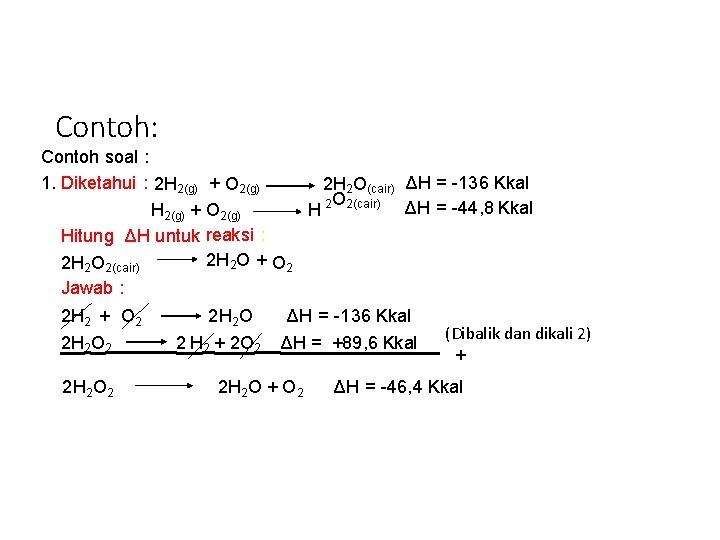
Contoh: Contoh soal : 1. Diketahui : 2 H 2(g) + O 2(g) 2 H 2 O(cair) ΔH = -136 Kkal O H 2 2(cair) ΔH = -44, 8 Kkal H 2(g) + O 2(g) Hitung ΔH untuk reaksi : 2 H 2 O + O 2 2 H 2 O 2(cair) Jawab : 2 H 2 + O 2 2 H 2 O 2 H 2 + 2 O 2 ΔH = -136 Kkal ΔH = +89, 6 Kkal 2 H 2 O + O 2 (Dibalik dan dikali 2) + ΔH = -46, 4 Kkal
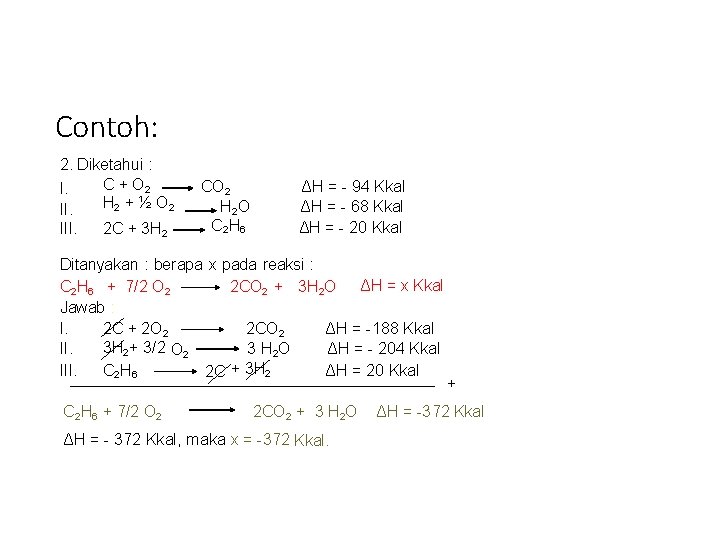
Contoh: 2. Diketahui : C + O 2 I. H 2 + ½ O 2 II. III. 2 C + 3 H 2 CO 2 H 2 O C 2 H 6 ΔH = - 94 Kkal ΔH = - 68 Kkal ΔH = - 20 Kkal Ditanyakan : berapa x pada reaksi : C 2 H 6 + 7/2 O 2 2 CO 2 + 3 H 2 O ΔH = x Kkal Jawab : I. ΔH = -188 Kkal 2 C + 2 O 2 2 CO 2 3 H 2+ 3/2 O 2 II. ΔH = - 204 Kkal 3 H 2 O C 2 H 6 III. ΔH = 20 Kkal 2 C + 3 H 2 C 2 H 6 + 7/2 O 2 2 CO 2 + 3 H 2 O ΔH = - 372 Kkal, maka x = -372 Kkal. + ΔH = -372 Kkal

Contoh:

Soal : 1. Pada pemanasan 400 g air bersuhu 25°C diperlukan kalor 84 k. J. Jika diketahui kalor jenis air = 4, 2 J/g°C, tentukan suhu air setelah pemanasan! 2. Tentukan perubahan entalpi pembakaran gas metana (CH 4), jika diketahui : pembentukan CH 4 = -17, 9 kkal/mol • ΔH • pembentukan CO 2 = -94, 1 kkal/mol ΔH • ΔH pembentukan H 2 O = -68, 3 kkal/mol

Energi Ikatan (EI) / Energi Disosiasi • Adalah energi yang diperlukan untuk memutuskan 1 mol ikatan senyawa dalam wujud gas pada keadaan standar menjadi atom-atom gasnya • Contoh : ΔH = + 435 k. J H 2(g) → 2 H(g) Energi ikatan H—H = + 435 k. J/mol • Pada molekul beratom banyak, energi untuk memutuskan semua ikatan dalam molekul berwujud gas menjadi atom-atom netral berwujud gas dinamakan energi atomisasi. • Contoh : Pemutusan semua ikatan atom C dan H pada metana.
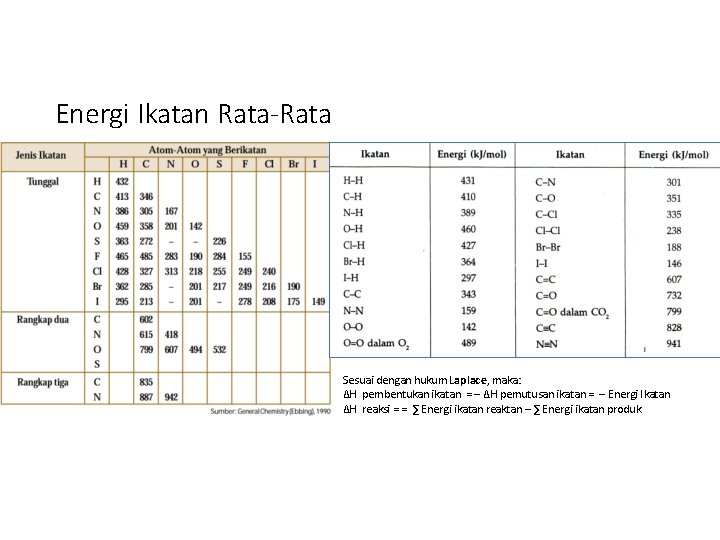
Energi Ikatan Rata-Rata Sesuai dengan hukum Laplace, maka: ΔH pembentukan ikatan = – ΔH pemutusan ikatan = – Energi Ikatan ΔH reaksi = = ∑ Energi ikatan reaktan – ∑ Energi ikatan produk.

Contoh: Dengan menggunakan tabel energi ikatan, tentukan energi yang dibebaskan padapembakaran gas metana. Jawab : Reaksi pembakaran gas metana: • CH 4(g) + 2 O 2(g) → CO 2(g) + 2 H 2 O(g) ∆H = ? • ∆Hr = ∑ energi ikatan pereaksi (ruas kiri) − ∑ energi ikatan produk (ruas kanan) = (4 C−H + 2 O=O) – (2 C=O + 4 O−H) = (4 x 415) + (2 x 494) − (2 x 805) + (4 x 460) = (1660 + 988) − (1610 + 1840) = 2648 – 3450 = - 802 k. J

Contoh: Jika diketahui: • energi ikatan N≡N = 946 k. J/mol, • energi ikatan N—N = 163 k. J/mol, • energi ikatan N—H = 389 k. J/mol, • energi ikatan O—O = 144 k. J/mol, dan • energi ikatan O—H = 464 k. J/mol, maka hitunglah berapa ΔH reaksi berikut: • N 2 H 4 (g) + 2 H 2 O 2 (g) → N 2 (g) + 4 H 2 O (g) Jawab:

Arah Proses Berdasarkan kespontanannya, suatu proses reaksi dapat dibagi menjadi 2, yaitu: a. Proses Spontan • Suatu proses yang berlangsung satu arah, sistem dan lingkungan tidak berada dalam kesetimbangan. • Contoh: - air mengalir dari tempat yang tinggi ke tempat yang rendah - spiritus terbakar b. Proses tidak spontan • Suatu proses yang dapat berangsung karena ada pengaruh dari luar sistem. Sistem dan lingkungan berada pada sistem kesetimbangan. • Contoh: - air membeku - memperoleh aluminium dari oksidanya

Arah Proses • Suatu reaksi kimia berlangsung spontan atau tidak spontan dapat ditentukan dengan melihat fungsi 3 keadaan yaitu:
- Slides: 47