TERMOKIMIA Daftar MateriMateri Pokok A Pengertian Termokimia B
TERMOKIMIA

Daftar Materi-Materi Pokok A. Pengertian Termokimia B. Energi dan Entalpi C. Reaksi Eksoterm dan Endoterm D. Persamaan Termokimia dan Jenisjenis ∆H reaksi E. Penentuan Nilai Perubahan Entalpi F. Entalpi Pembakaran Bahan Bakar

Materi pembelajaran A. Pengertian Termokimia Bagian Dari Ilmu Kimia yang mempelajari perubahan kalor adalah Termokimia. Dengan mempelajari Termokimia, kita dapat mengetahui jumlah Energi yang berubah saat terjadi reaksi. Selain itu, kita juga dapat mengetahui manfaat dan dampak penerapan konsep termokimia dalam industri dan kehidupan sehari-hari.

B. Energi dan Entalpi Secara sederhana Energi didefenisikan sebagai kemampuan untuk melakukan kerja. Energi yang dimiliki benda dapat berupa energi otot, energi angin, energi kiia, energi kalor, dan bentuk-bentuk energi lainnya. Jumlah total energi kalor yang terkandung dalam suatu materi disebut entalpi dan diberi simbol H. Istilah entalpi berasaldari bahasa Jerman yang berarti kandungan. Adapun simbol H berasal dari kata heat content, yang didefinisikan sebagai kandungan kalor suatu zat. Entalpi suatu zat tidak berubah (tetap) selama tidak ada energi yang masuk dan keluar.

Entalpi suatu zat tidak dapat diukur, tetapi perubahan entalpinya dapat diukur. Perubahan entalpi terjadi jika suatu zat mangalami reaksi. Perubahan entalpinya diberi notasi ∆H, simbol ∆ berasal dari bahasa Yunani, delta, yang berarti perubahan. Dalam reaksi kimia, ∆H disebut juga entalpi reaksi. ∆H menyatakan kalor yang diterima atau dilepas oleh suatu reaksi. Dengan kata lain, ∆H merupakan penambahan atau pengurangan energi suatu zat dalam suatu proses perubahan Energi yang berlangsung pada tekanan tetap.

C. Reaksi Eksoterm dan Endoterm 1. Sistem dan Lingkungan Sistem adalah segala sesuatu yang menjadi pusat perhatian yang kita pelajari perubahan energinya. Sedangkan yang disebut lingkungan adalah segala sesuatu di luar sistem. 2. Reaksi eksoterm adalah reaksi kimia yang menghasilkan Kalor. Pada reaksi ini, terjadi perpindahan kalor dari sistem ke lingkungan sehingga lingkungan menjadi lebih panas. Reaksi eksterm akan membebaskan energi sehingga entalpi sistem berkurang dan perubahan entalpi bernilai negatif.

C. Reaksi Eksoterm dan Endoterm 3. Reaksi edoterm adalah reaksi kimia yang menyerap atau menerima kalor. Pada reaksi ini, terjadi perpindahan kalor dari lingkungan ke sistem sehingga suhu lingkungan turun dan menjadi lebih dingin. Reaksi edoterm menyerap sejumlah energi sehingga energi sistem bertambah. Karena entalpi bertambah, perubahan entalpinya bertanda positif.

D. Persamaan Termokimia dan Jenis-jenis ∆H reaksi 1. Persamaan Termokimia Koefisien reaksi pada persamaan termokimia menunjukkan perbandingan jumlah mol, dan juga menyatakan jumlah mol yang bereaksi. Persamaan termokimia juga menyertakan nilai perubahan entalpi.
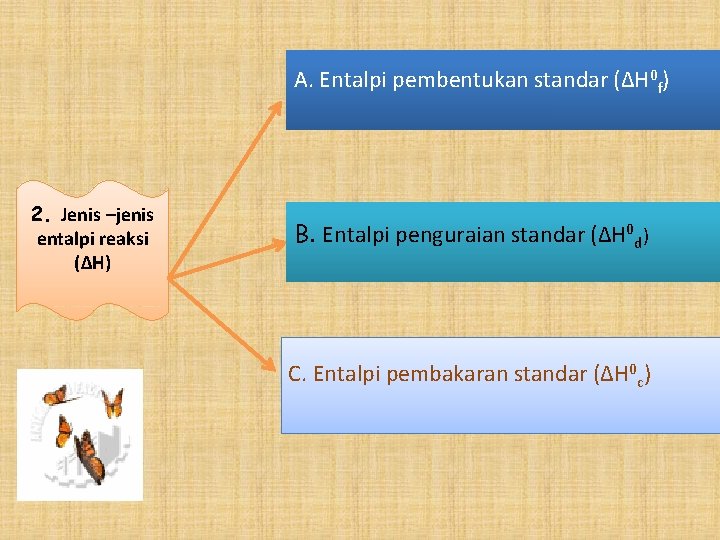
A. Entalpi pembentukan standar (∆H 0 f) 2. Jenis –jenis entalpi reaksi (∆H) B. Entalpi penguraian standar (∆H 0 d) C. Entalpi pembakaran standar (∆H 0 c)

E. Penentuan Nilai Perubahan Entalpi 1. Penentuan nilai ∆H reaksi Melalui Eksperimen sederhana a. Kalor Jenis Air dan Kapasitas Kalor Hubungan antara kapasitas kalor dan Kalor jenis dirumuskan sebagai berikut. C=mxc b. Penentuan ∆H Reaksi Menggunakan Kalorimeter Tekanan Uap Jika kapasitas kalor larutan sebesar 4 k. Jo. C-1 dan kapasitas kalorimeter dianggap nol (sama sekali tidak menyerap kalor), kalor reaksi dapat dihitung sebagai berikut. qsistem = C x ∆T qkalorimeter = 0

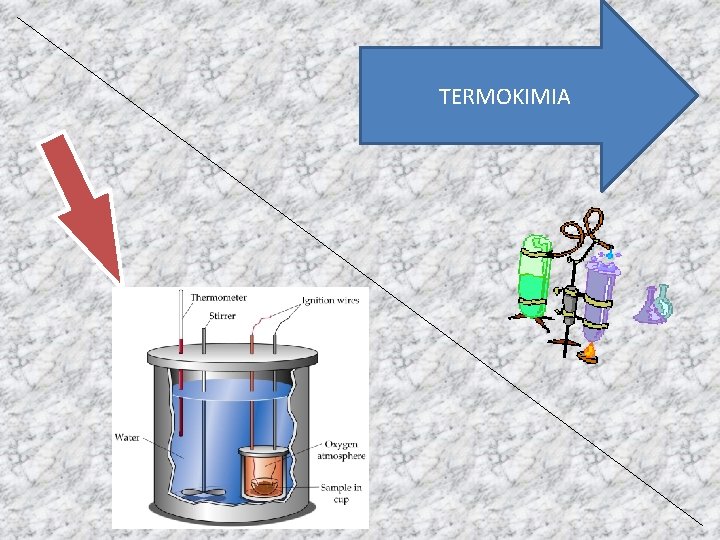
c. Penentuan ∆H Reaksi Menggunakan Kalorimeter Bom Untuk reaksi-reaksi yang melibatkan gas, pengukuran kalor untuk reaksi dapat dilakukan dengan menggunakan kalorimeter bom. Kolorimeter ini dirancang sedemikian rupa sehingga seruruh energi reaksi akan berupa energi kalor. 2. Perhitungan ∆H Reaksi Menggunakan Hukum Hess dikemukakan oleh Germain Henry Hess (18021850), seorang ahli kimia berkebangsaan Swiss. Menurut Hukum Hess “kalor reaksi yang dibebaskan atau diperlukan pada suatu reaksi tidak bergantung pada jalannya reaksi, tetapi hanya bergantung pada keadaan awal dan akhir reaksi”.

3. Perhitungan ∆H Reaksi Berdasarkan Data ∆H Pembentukan Standar Pada cara ini, data entalpi yang diketahui harus berupa data entalpi pembentukan. Zat – zat pereaksi dianggap mengalami reaksi- reaksi pembentukan. Jadi, Entalpi penguraian merupakan kebalikan dari Entalpi pembentukan senyawa yang sama. Dengan demikian, jumlah kalornya sama, tetapi tandanya berlawanan karena reaksi berlawanan arah. 4. Perhitungan ∆H Reaksi Menggunakan Data Energi Ikatan Suatu unsur atau senyawa kimia terbentuk melalui ikatan antaratom penyusunya. Ikatan-ikatan antaratom ini memiliki nilai energi ikatan tertentu. Energi yang terdapat pada ikatan inilah yang selama ini kita kenal sebagai energi kimia.

F. Entalpi Pembakaran Bahan Bakar Reaksi kimia yang umum digunakan untuk menghasilkan energi adalah pembakaran, yaitu suatu reaksi cepat antara bahan bakar denga oksigen yang disertai terjadinya api. Bahan bakar utama dewasa ini adalah bahan bakar fosil, yaitu gas alam, minyak bumi, dan batu bara. Bahan bakar fosil itu berasal dari pelapukan sisa organisme, baik tumbuhan atau hewan. Pembentukan bahan bakar fosil ini memerlukan waktu ribuan sampai jutaan tahun.

SEKIAN DAN TERIMA KASIH
- Slides: 14