SUHU DAN KALOR 1 Pendahuluan Dalam kehidupan seharihari


















- Slides: 24

SUHU DAN KALOR 1

Pendahuluan • Dalam kehidupan sehari-hari sangat banyak didapati penggunaan energi dalam bentuk kalor: – Memasak makanan – Ruang pemanas/pendingin – Dll. 2

TUJUAN INSTRUKSIONAL • Menentukan besaran suhu, kalor jenis, kalor, konduktivitas dalam kaitannya dengan pemuaian, penjalaran kalor, dan perubahan fasa 3

Suhu dan Pemuaian • Pada kehidupan sehari-hari temperatur merupakan ukuran mengenai panas atau dinginnya benda. • Es dikatakan memiliki temperatur rendah • Api dikatakan panas atau bertemperatur tinggi 4

• Temperatur merupakan sifat sistem yang menentukan apakah sistem berada dalam keadaan kesetimbangan dengan sistem lain Kesetimbangan termal ? 5

Tsetimbang • Jika dua sistem dengan temperatur yang berbeda diletakkan dalam kontak termal, maka kedua sistem tersebut pada akhirnya akan mencapai temperatur yang sama. • Jika dua sistem dalam kesetimbangan termal dengan sistem ketiga, maka mereka berada dalam kesetimbangan 6 termal satu sama lain

► Alat yang digunakan untuk mengukur temperatur disebut termometer ► Untuk mengukur temperatur secara kuantitatif, perlu skala numerik seperti o. C, o. F, K, o. R 7

Pemuaian • Suatu zat jika dipanaskan pada umumnya akan memuai dan menyusut jika didinginkan L, A, V = Perubahan L = Lo T panjang, luas dan volume A = Ao T L 0, Ao, Vo = Panjang, luas dan volume awal V = Vo T T = Perubahan suhu (0 C) , , = Koefisien muai panjang, luas dan volume (0 C-1) = 3 dan = 2 8

Contoh soal 1. Sebuah cincin besi berdiameter 1, 5 m pada suhu 200 C. Harus dipanaskan didalam ketel dengan suhu berapakah cincin tersebut agar diameternya menjadi 1, 52 m, jika besi = 12 x 10 -6 / 0 C T? 9

ANOMALI AIR • 4 o. C → 0 o. C : Volumenya membesar • 0 o. C → 4 o. C : Volumenya mengecil dengan massa jenis (ρ) paling tinggi, sehingga perilaku air ini sangat penting untuk bertahannya kehidupan di dalam air laut selama musim dingin 10

Kalor n Kalor merupakan transfer energi dari satu benda ke benda lain karena adanya perbedaan temperatur n Dalam satuan SI, satuan kalor adalah joule dengan 1 kal = 4. 186 J n 1 kalori (kal) = kalor yang dibutuhkan untuk menaikkan temperatur 1 gr air sebesar 1 o. C 11

l Jumlah kalor yang diperlukan untuk mengubah suhu suatu sistem Q = m c T m = massa (gr) c = kalor jenis (kal/g 0 C) T = Perubahan suhu (0 C) 12

Kalor Jenis dan Kapasitas Kalor • Kapasitas kalor adalah kalor yang dibutuhkan oleh benda untuk mengubah suhunya sebesar 1 o C atau 1 K. Q = Kalor ( Joule ) T = Perubahan suhu (o C atau K ) C = kapasitas kalor ( Jolue/ o C atau Jolue/ K)

Kalor Jenis dan Kapasitas Kalor • Kalor Jenis adalah banyaknya kalor yang dibutuhkan untuk menaikkan suhu 1 satuan massa zat sebesar 1 o C atau 1 K. c = kalor jenis ( Jolue/ Kgo C atau Jolue/ Kg. K) m = massa ( Kg ) Hal. : 14 Isi dengan Judul Halaman Terkait

Contoh soal Hitunglah jumlah kalor yang diperlukan untuk menaikkan suhu 20 Kg besi (c = 0, 11 kal/g 0 C) dari 100 C ke 900 C Jawab. Q = m c T = 20 x 103 g x 0, 11 cal/g 0 C x (90 – 10)0 C = 17600000 cal 15

§ Jika bagian yang berbeda dari sistem yang terisolasi berada pada temperatur yang berbeda, kalor akan mengalir dari temperatur tinggi ke rendah § Jika sistem terisolasi seluruhnya, tidak ada energi yang bisa mengalir ke dalam atau keluar, maka berlaku kekekalan energi dengan Qserap = Qlepas 16

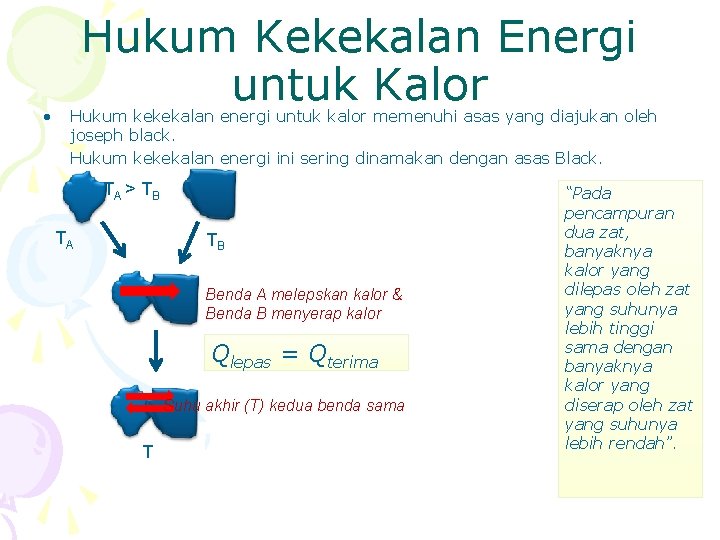
• Hukum Kekekalan Energi untuk Kalor Hukum kekekalan energi untuk kalor memenuhi asas yang diajukan oleh joseph black. Hukum kekekalan energi ini sering dinamakan dengan asas Black. TA > T B TA TB Benda A melepskan kalor & Benda B menyerap kalor Qlepas = Qterima Suhu akhir (T) kedua benda sama T “Pada pencampuran dua zat, banyaknya kalor yang dilepas oleh zat yang suhunya lebih tinggi sama dengan banyaknya kalor yang diserap oleh zat yang suhunya lebih rendah”.

Perubahan Fasa n Zat dapat berbentuk padat, cair atau gas. Ketika terjadi perubahan fasa, sejumlah kalor dilepas atau diserap suatu zat yaitu Q=m. L Q = kalor (kalori atau joule) m = massa (gr atau kg) L = kalor laten (kal/gr atau J/Kg) Kalor penguapan air (1000 C) = 530 kal/gr Kalor peleburan es (00 C) = 80 kal/gr 18

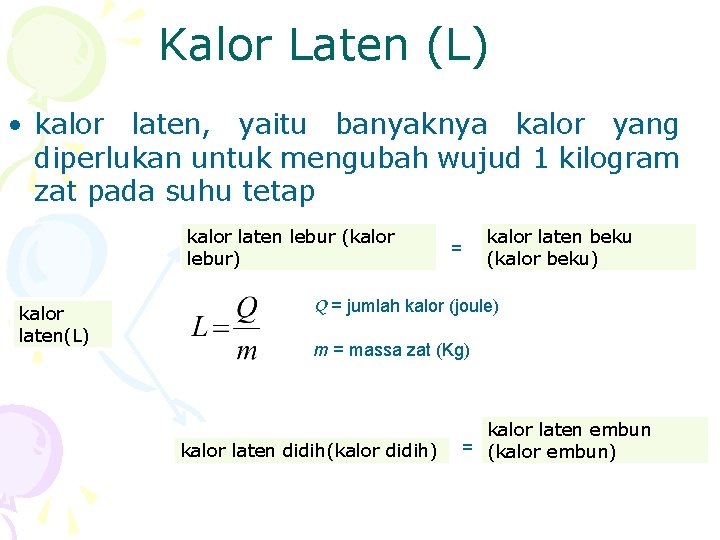
Kalor Laten (L) • kalor laten, yaitu banyaknya kalor yang diperlukan untuk mengubah wujud 1 kilogram zat pada suhu tetap kalor laten lebur (kalor lebur) kalor laten(L) kalor laten beku (kalor beku) = Q = jumlah kalor (joule) m = massa zat (Kg) kalor laten didih(kalor didih) kalor laten embun = (kalor embun)

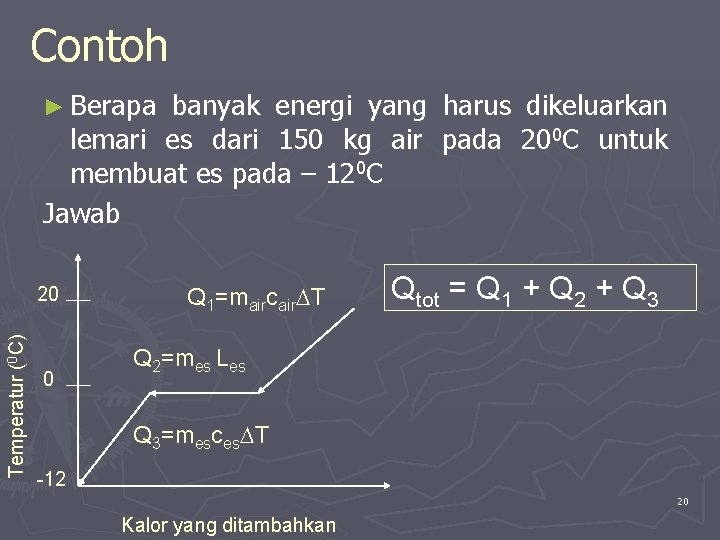
Contoh ► Berapa banyak energi yang harus dikeluarkan lemari es dari 150 kg air pada 200 C untuk membuat es pada – 120 C Jawab Temperatur (0 C) 20 0 Q 1=maircair T Qtot = Q 1 + Q 2 + Q 3 Q 2=mes Les Q 3=mesces T -12 20 Kalor yang ditambahkan

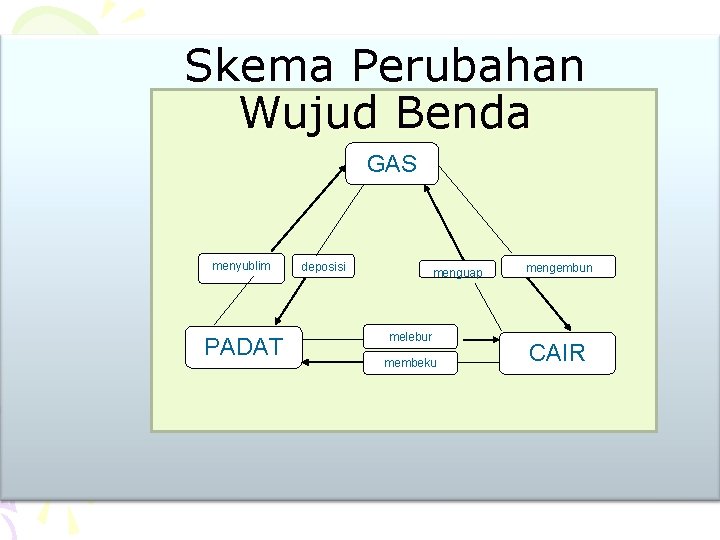
Skema Perubahan Wujud Benda GAS menyublim PADAT deposisi menguap melebur membeku mengembun CAIR

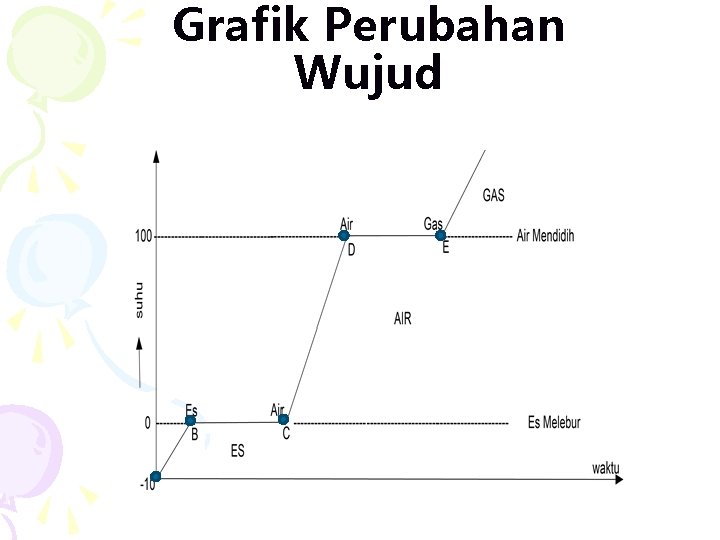
Grafik Perubahan Wujud A

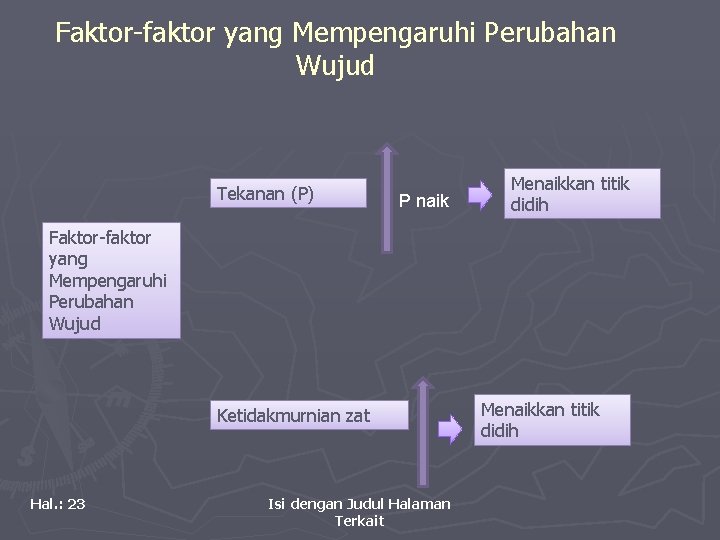
Faktor-faktor yang Mempengaruhi Perubahan Wujud Tekanan (P) P naik Menaikkan titik didih Faktor-faktor yang Mempengaruhi Perubahan Wujud Ketidakmurnian zat Hal. : 23 Isi dengan Judul Halaman Terkait Menaikkan titik didih

n Kalor laten untuk mengubah cairan menjadi gas tidak hanya pada titik didih (1000 C) tetapi juga pada suhu ruang. Hal ini disebut evaporasi 24