kalor Tujuan mempelajari bab ini Siswa diharapkan dapat
kalor

Tujuan mempelajari bab ini Siswa diharapkan dapat: 1. Menyelidiki banyaknya kalor yang diperlukan untuk menaikkan suhu 2. Menyelidiki kalor yang dibutuhkan pada saat mendidih dan melebur 3. Menerapkan hubungan Q = m. c. ΔT; Q = m. U; Q = m. L untuk memecahkan masalah sederhana

Apa itu kalor. . . ? Pengertian kalor berbeda dengan pengertian suhu. Suhu adalah derajat panas atau dinginnya suatu benda, sedangkan kalor adalah energi yang dipindahkandari suatu benda ke benda lainnya kerena perbedaan suhu/temperatur. Kalor memiliki dua macam satuan, yaitu joule dan kalori. Mengenai konversi kedua besaran tersebut, adalah seperti berikut

Faktor-faktor yang mempengaruhi banyaknya kalor yang diperlukan atau mungkin dilepaskan oleh suatu zat adalah sebagai berikut: 1. Massa benda 2. kenaikan suhu 3. Kalor jenis Massa benda semakin banyak massa suatu zat maka kalor yang diperkukan juga semakin banyak. Contoh apabila kita memanaskan air sebesar 1 kg dengan 10 kg, dengan pemanas yang sama, maka waktu yang diperlukan untuk mendidihkan kedua air tersebut berbeda

Kenaikan suhu semakin besar kenaikan suhunya maka semakin besar pula kalor yang diperlukan oleh sebuah zat. Contoh apabila kita memanaskan air selama 5 menit dengan 10 menit dengan pemanas yang sama, maka kenaikan suhunya lebih besar dengan waktu 10 menit Kalor Jenis kalor jenis benda adalah banyaknya kalor yang diperlukan atau dilepaskan oleh suatu benda yang massa 1 kg untuk menaikkan suhu 1 o. C, contoh kalor jenis air sebesar 4200 J/kgo. C ini berarti bahwa kalor yang diperlukan untuk menaikkan suhu 1 kg sebesar 1 o. C sebesar 4200 J

Tabel. kalor jenis zat No Jenis zat Kalor jenis zat (J/kgo. C) 1 Air 4200 11 Kuningan 370 2 Alkohol 2300 12 Marmer 860 3 Alumunium 900 13 Minyak tanah 2200 4 Baja 450 14 Perak 234 5 Besi 460 15 Raksa 140 6 Ema 130 16 Seng 390 7 Es 2100 17 Tembaga 390 8 Gliserin 2400 18 Timah hitam 130 9 Kaca 670 19 Timbal 130 10 Kayu 1700 20 Udara 1000

Secara matematis kalor jenis adalah Contoh soal Berapakah kalor yang diperlukan untuk memanaskan 2 kg air yang suhunya 20 o. C menjadi 70 o. C, jika kalor jenis air 4200 J/kgo. C m = 2 kg T 1 = 20 o. C T 2 = 70 o. C c = 4200 J/kgo. C Jawab Q = m. C. ΔT Q = 2. 4200. (70 – 20) Q = 8400. 50 Q = 420. 000 J = 420 KJ

Soal 1. Berapakah kalor yang dibutuhkan untuk memanaskan sebatang besi yang massanya 5 kg dari suhu 50 o. C menjadi 120 o. C jika kalor jenis 460 J/kgo. C? 2. Kalor yang diperlukan untuk merebus air sehingga suhunya naik 30 o. C adalah 630 KJ. Jika kalor jenis air 4200 J/kgo. C, berapakah massa air? 3. Suhu mula-mula dari 5 kg air adalah 15 o. C dipanaskan dengan membutuhkan kalor 735 KJ. Dan kalor jenis air 4200 J/kgo. C, berapakah suhu akhir air tersebut?

Kapasitas kalor (H) adalah banyaknya kalor yang diperlukan suatu zat untuk menaikkan suhu 1 o. C. Dari definisi tersebut dapat dituliskan dengan persamaan matematis, yaitu: Dimana Q →→→ sehingga H = kapasitas kalor (J/o. C)

Contoh soal Untuk menaikkan suhu air sebesar 50 o. C diperlukan kalor 16. 800 Joule. Berapakah kapasitas kalornya? Penyelesaian Diketahui: ΔT = 50 o. C Q = 16. 800 Joule Ditanya H. . . ? Jawab

Soal 1. Sebatang besi masanya 20 kg, jika kalor jenisnya 460 J/kgo. C, berapakah kapasitas kalornya? 2. Kapasitas kalor suatu zat 2000 J/o. C, jika zat tersebut dipanaskan hingga suhunya naik 40 o. C, berapakah kalor yang dibutuhkan? 3. Massa sebuah tembaga 40 kg, dipanaskan dari suhu 40 o. C sampai 90 o. C, jika kalor jenis tembaga 390 J/kgo. C, berapakah besar kapasitas tembaga?
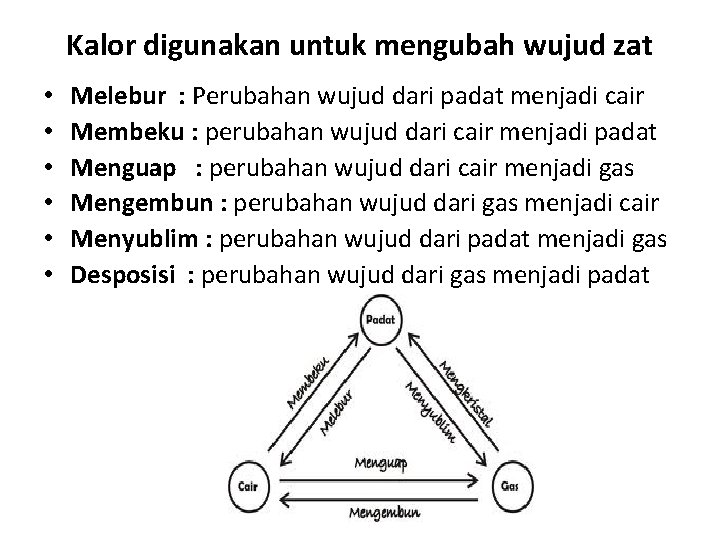
Kalor digunakan untuk mengubah wujud zat • • • Melebur : Perubahan wujud dari padat menjadi cair Membeku : perubahan wujud dari cair menjadi padat Menguap : perubahan wujud dari cair menjadi gas Mengembun : perubahan wujud dari gas menjadi cair Menyublim : perubahan wujud dari padat menjadi gas Desposisi : perubahan wujud dari gas menjadi padat

Pada era modern ini ditemukan lagi zat baru yang bernama plasma

Kalor uap (didih) Kalor uap adalah banyaknya kalor yang digunakan untuk menguapkan 1 kg zat cair pada titik didih Penguapan dapat dipercepat dengan cara: 1. Memanaskan atau memberikan kalor 2. Memperluas permukaan bidang 3. Meniupkan udara disekitar permukaan 4. Mengurangi tekanan pada permukaan Secara matematis kalor uap adalah:

Contoh soal Berapakah kalor yang dibutuhkan untuk menguapkan 5 kg air pada titik didihnya, jika kalor uap air 2. 260. 000 J/kg? penyelesaian Diketahui: Jawab: m = 5 kg U = 2. 2600. 000 J/kg Q = m. U Ditanya Q. . . ? Q = 5. 2. 2600. 000 Q = 1. 130. 000 J Q = 1. 130 KJ

Soal 1. Berapakah kalor yang digunakan untuk menguapkan 0, 5 kg raksa, jika kalor uap raksa 272. 000 J/kg 2. Untuk menguapkan sejumlah alkohol di perlukan kalor 4. 400 KJ. Berapakah massa alkohol jika kalor uap alkohol 1. 100. 000 J/kg?

Kalor Lebur adalah kalor yang digunakan untuk meleburkan 1 kg zat pada titik lebur Secara matematis dapat dirumuskan

Contoh soal Berapa besar kalor yang dilepaskan jika 5 kg air dileburkan, dan kalor lebur air 336. 000 J/kg Penyelesaian Diketahui: m = 5 kg L = 336. 000 J/kg Ditanya: Q. . . ? Jawab: Q=m. L Q = 5. 336. 000 Q = 1. 680. 000 J Q = 1. 160 KJ
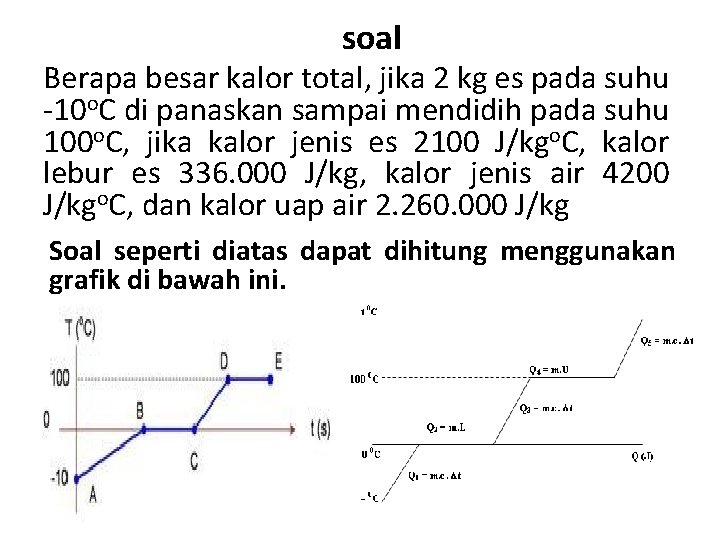
soal Berapa besar kalor total, jika 2 kg es pada suhu -10 o. C di panaskan sampai mendidih pada suhu 100 o. C, jika kalor jenis es 2100 J/kgo. C, kalor lebur es 336. 000 J/kg, kalor jenis air 4200 J/kgo. C, dan kalor uap air 2. 260. 000 J/kg Soal seperti diatas dapat dihitung menggunakan grafik di bawah ini.

Penyelesaian Yang pertama kita hitung Qtotal = Qab + Qbc + Qcd + Qde Perlu diketahui bahwa Qab = m. c. ΔT Qbc = m. L Qcd = m. c. ΔT Qde = m. U

Jawab Qab = m. ces. ΔT = 2 x 2100 x ( 0 – (-10)) Qab = 4200 x 10 = 42. 000 J = 42 KJ Qbc = m. L = 2 x 336. 000 = 672. 000 J Qbc = 672 KJ Qcd = m. ces. ΔT = 2 x 4200 x (100 – 0) Qab = 8400. 100 = 840. 000 J = 840 KJ Qde = m. U = 2 x 2. 260. 000 = 4. 520. 000 Qde = 4. 520 KJ Qtotal = Qab + Qbc + Qcd + Qde Qtotal = 42 + 672 + 840 + 4. 520 = 6. 074 KJ

Soal 1. 4 kg es suhunya -5 o. C di panaskan hingga menjadi air yang mendidih seluruhnya jika kalor jenis es 2100 J/kgo. C, kalor lebur es 336. 000 J/kg, kalor jenis air 4200 J/kgo. C, berapakah kalor yang diperlukan? 2. Perhatikan gambar di bawah Berapa besar kalor yang dibutuhkan?

Asas Black Jika ada dua buah zat cair yang memiliki suhu berbeda (panas dan dingin) bila dicampurkan menjadi satu dalam sebuah wadah maka air akan menjadi hangat. Besaranya kalor yang dilepaskan oleh air yang suhunya tinggi sama dengan kalor yang diterima oleh air yang suhunya rendah. (Teori Josep Black yang kemudia disebut sebagai Asas Balck) Secara matematis Asas Black.

Contoh soal Sebuah logam yang massanya 100 g dipanaskan sampai suhunya 30 o. C kemudian dimasukkan ke dalam air yang massanya 200 g pada suhu 90 o. C. Berapakah suhu akhir campuran apabila kalor dari bejana dan lingkungan sekitar tidak mempengaruhinya (clogam = 0, 2 kal/goc dan cair = 1 kal/goc ) Diketahui: mlogam = 100 g mair = 200 g ΔTlogam = 90 o. C Penyelesaian ΔTair = 30 o. C clogam = 0, 2 kal/goc cair = 1 kal/goc

Jawab

Soal 1. Sepotong besi mempunyai massa 200 g dipanaskan hingga 80 o. C, dimasukkan ke dalam air yang massanya 200 g dengan suhunya 40 o. C apabila tidak ada kalor yang mempengaruhi dari luar, berapa suhu akhir campuran? (cbesi = 460 J/kgo. C dan cair = 4200 J/kgo. C) 2. Sebongkah es yang suhunya -4 o. C massanya 2 kg dicampur dengan air yang massanya 10 g dengan suhu 40 o. C sehingga es melebur keseluruhannya dengan kalor jenis air 1 kal/go. C, kalor jenis es 0, 5 kal/go. C, dan kalor lebur es 80 kal/g. berapa suhu akhir campurannya?

Perpindahan kalor Kalor dapat berpindah dengan tiga cara, yaitu 1. 2. 3. Konduksi (hantaran) perpindahan kalor yang merambat pada medium perantara Konveksi (aliran) perpindahan kalor secara aliran dengan diikuti molekul-molekul yang berpindah tempat Radiasi (pancaran) perpindahan kalor secara pancaran tanpa zat perantara

Materi semester 1 telah selesai Selamat menempuh ujian semester Semoga sukses Sampai ketemu di semester 2
- Slides: 28