MISE AU POINT Solutions dtailles des questions 7







![On remplace dans l’équation, on tire l’expression de [HCO 3 -] : [HCO 3 On remplace dans l’équation, on tire l’expression de [HCO 3 -] : [HCO 3](https://slidetodoc.com/presentation_image/33226c7453549482a2fbbad4c537b2b1/image-9.jpg)


![Corrigé de la question 8 (suite) Le système est : [A-] + [AH] = Corrigé de la question 8 (suite) Le système est : [A-] + [AH] =](https://slidetodoc.com/presentation_image/33226c7453549482a2fbbad4c537b2b1/image-12.jpg)

![Question 10 (suite) Calculer [Na +]. un seul choix autorisé 1. 80 2. 72 Question 10 (suite) Calculer [Na +]. un seul choix autorisé 1. 80 2. 72](https://slidetodoc.com/presentation_image/33226c7453549482a2fbbad4c537b2b1/image-14.jpg)



- Slides: 17

MISE AU POINT Solutions détaillées des questions 7 à 10 du quizz_2_niveau_1

Énoncé question 7 On considère une solution maintenue sous une p. CO 2 fixe et contenant : - 1/ d’une part du bicarbonate de sodium, - 2/ d’autre part un tampon univalent de p. K 6, 8 et de concentration totale 60 mmol. l-1 (tampon ANa/AH). Interprétation de l’énoncé : voire diapos suivantes ↓

p. CO 2 et solubilité A l'équilibre, la pression partielle d'un gaz au-dessus d'un liquide détermine la concentration maximale (de saturation) que présentera ce gaz dans le liquide. Cette propriété est exprimée par la loi de Henry : la solubilité d'un gaz dans un liquide est proportionnelle à sa pression partielle au-dessus du liquide. La solubilité du gaz dissous diminue avec la température La constante d'équilibre (ou constante de Henry) s'écrit : Donc la loi de Henry relie la concentration du gaz dissous à sa pression partielle lorsqu’il est sous forme gazeuse au-dessus de la solution

1/ Le bicarbonate de sodium (l'hydrogénocarbonate de sodium en nomenclature moderne), formule chimique Na. HCO 3 se dissocie en Na+ et HCO 3− : Na. HCO 3 Na+ + HCO 3− L’ion bicarbonate est amphotère, lorsqu’il capte un proton, il forme l’acide carbonique lequel produit du CO 2 dissous et de l’eau : (couple CO 2 dissous /HCO 3− ) HCO 3– + H+ H 2 CO 3 CO 2 + H 2 O La double flèche indique la réaction est une réaction d’équilibre, elle se fait dans les deux sens, ce qui explique la présence du CO 2 gazeux et donc d’une pression partielle de CO 2 au dessus de la solution (acide volatil)

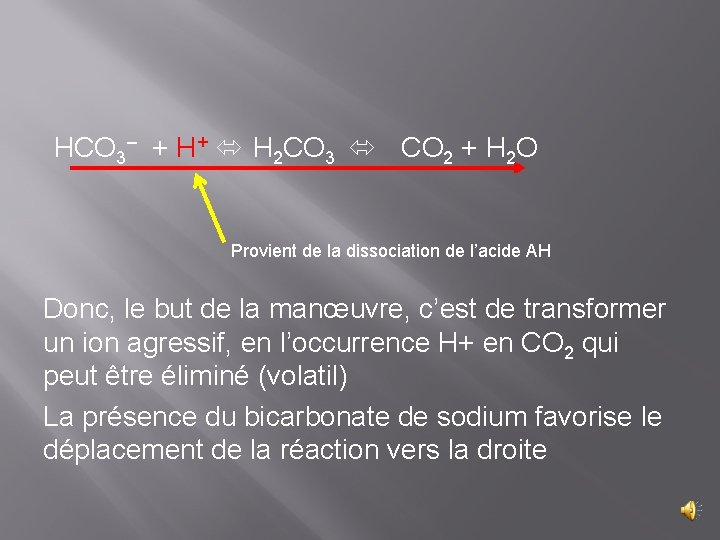
HCO 3– + H+ H 2 CO 3 CO 2 + H 2 O Provient de la dissociation de l’acide AH Donc, le but de la manœuvre, c’est de transformer un ion agressif, en l’occurrence H+ en CO 2 qui peut être éliminé (volatil) La présence du bicarbonate de sodium favorise le déplacement de la réaction vers la droite

2/ Tampon ANa/AH de p. Ka = 6. 8 Ce tampon représente la composante fixe des acides car il ne se volatilise pas contrairement au CO 2. L’acide AH libère un proton : AH A- + H+ L’ion sodium Na+ s’associe à l’ion A- + Na+ ANa Donc on a l’acide fixe AH et sa base conjuguée est A-, La concentration totale de ce tampon est égale à 60 mmol/L, c’est-à-dire : [A-] + [AH] = 60 mmol/L

La question 7 La p. CO 2 est fixée à 40 mm Hg ; le p. H est égal à 7, 4. Calculer [HCO 3 -] un seul choix autorisé 1. 40 2. 38 3. 36 4. 34 5. 30 6. 24

Corrigé question 7 On utilise l’équation de Henderson-Hasselbach : 6, 1 représente le p. Ka du tampon bicarbonate a = 0. 03 coefficient de dissolution du CO 2 à 37°C p. CO 2 la pression partielle du CO 2 Données : p. CO 2 = 40 mm. Hg et p. H = 7, 4 Dans cette équation, si on maintient deux gradeurs constantes (p. H et p. CO 2), alors la troisième est aussi constante ([HCO 3 -])
![On remplace dans léquation on tire lexpression de HCO 3 HCO 3 On remplace dans l’équation, on tire l’expression de [HCO 3 -] : [HCO 3](https://slidetodoc.com/presentation_image/33226c7453549482a2fbbad4c537b2b1/image-9.jpg)
On remplace dans l’équation, on tire l’expression de [HCO 3 -] : [HCO 3 -] = 0. 03 x 40 x 10 (7. 4 – 6. 1) = 0. 03 x 40 x 101. 3 = 0. 03 x 40 x 19. 95 = 23. 94 ≈ 24 Donc : [HCO 3 -] ≈ 24 mmol/L proposition 6

Énoncé question 8 (suite) La p. CO 2 est toujours fixée à 40 mm Hg et le p. H égal à 7, 4. Calculer [A-] un seul choix autorisé 1. 54 2. 48 3. 42 4. 38 5. 32 6. 30

Corrigé de la question 8 Les deux tampons sont au même p. H = 7, 4 Donc si on applique l’équation de Henderson. Hasselbach au tampon fixe on a : (1) Par ailleurs, on sait que : [A-] + [AH] = 60 mmol/L (2) On a donc un système de deux équations à deux inconnues [A-] et [AH]
![Corrigé de la question 8 suite Le système est A AH Corrigé de la question 8 (suite) Le système est : [A-] + [AH] =](https://slidetodoc.com/presentation_image/33226c7453549482a2fbbad4c537b2b1/image-12.jpg)
Corrigé de la question 8 (suite) Le système est : [A-] + [AH] = 60 [A-] = [AH]. 10 (7, 4 – 6, 8) La résolution de ce système par la méthode de substitution donne à la fois : [AH] = [A-]. 10 -(7, 4 - 6, 8) = [A-]. 10 -0, 6 [A-] + [A-]. 10 -0, 6 = 60 [A-]. (1 + 10 -0, 6 ) = 60 [A-]. 0, 251 = 60 D’où [A-] = 48 mmol/L proposition 2

Question 9 (suite) La p. CO 2 est toujours fixée à 40 mm Hg et le p. H égal à 7, 4. Calculer [AH] un seul choix autorisé 1. 40 2. 24 [A-] + [AH] = 60 3. 20 Et on a [A-] = 48 mmol/L 4. 16 5. 12 6. 10
![Question 10 suite Calculer Na un seul choix autorisé 1 80 2 72 Question 10 (suite) Calculer [Na +]. un seul choix autorisé 1. 80 2. 72](https://slidetodoc.com/presentation_image/33226c7453549482a2fbbad4c537b2b1/image-14.jpg)
Question 10 (suite) Calculer [Na +]. un seul choix autorisé 1. 80 2. 72 3. 48 4. 24 5. 12 6. 10

Corrigé de la question 10 On applique le principe de l’électro-neutralité à la solution. Elle contient les ions suivants : HCO 3 -, A-, Na+, mais aussi H+ et OH- dont les concentrations peuvent être négligées lorsque le p. H n’est ni trop faible ni trop élevé ou si les solutions ne sont pas trop diluées. Donc : [HCO 3 -] + [A-] = [Na+] On remplace [HCO 3 -] = 24 mmol/L Et [A-] = 48 mmol/L 24 + 48 = 72 mmol/L = [Na+] proposition 2

POUR CEUX QUI N’ONT PAS PU ASSISTER… L’enregistrement sera déposé (si possible) sur la PF, Sinon, je vous enverrai le document

PROCHAINE ET DERNIÈRE SÉANCE LE 07/07/20 Le diagramme de Davenport et étude des déséquilibres acidobasiques