Ligaes Qumicas 9 ano Ligao Qumica A regra







![Ligação Iônica Exercícios : 3. A fórmula eletrônica de Lewis [ K ]+ [ Ligação Iônica Exercícios : 3. A fórmula eletrônica de Lewis [ K ]+ [](https://slidetodoc.com/presentation_image_h2/ced02a52d0893f4666390ce0c2275ce9/image-10.jpg)




- Slides: 17

Ligações Químicas 9° ano

Ligação Química A regra do octeto: Os átomos tendem a ganhar, perder ou compartilhar elétrons até que eles estejam rodeados por 8 elétrons na camada de valência (ou dois elétrons para o caso do hidrogênio e lítio), adquirindo a configuração de um gás nobre.

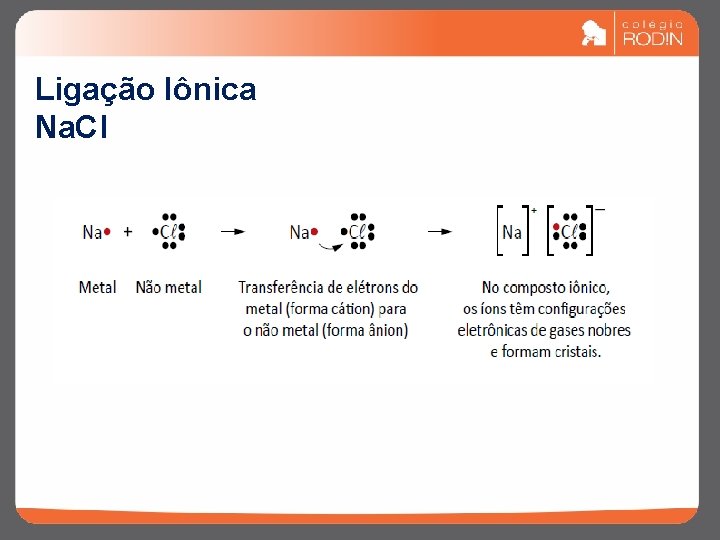
Ligação Iônica v Resulta da transferência de elétrons de um metal para um não- metal. v Os átomos são unidos por forças eletrostáticas v A representação da fórmula molecular do composto iônico se dá por:

Ligação Iônica Na. Cl

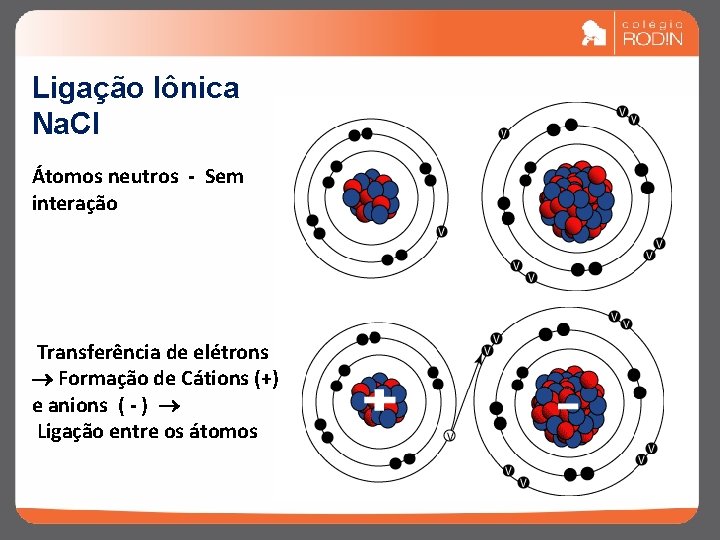
Ligação Iônica Na. Cl Átomos neutros - Sem interação Transferência de elétrons Formação de Cátions (+) e anions ( - ) Ligação entre os átomos

Ligação Iônica Na. Cl Cloro Sódio

Ligação Iônica Outros exemplos:

Ligação Iônica Outros exemplos:

Ligação Iônica Exercícios : 2. Um composto é formado pelo cátion X e pelo ânion Y, com fórmula química representada por X 2 Y 3. A respeito desse composto, assinale a alternativa correta. a. O átomo X possui 2 elétrons na camada de valência. b. O átomo Y possui 6 elétrons na camada de valência. c. O átomo Y possui 2 elétrons na camada de valência. d. O átomo X possui 6 elétrons na camada de valência. e. O composto estabiliza-se por ligação química covalente.
![Ligação Iônica Exercícios 3 A fórmula eletrônica de Lewis K Ligação Iônica Exercícios : 3. A fórmula eletrônica de Lewis [ K ]+ [](https://slidetodoc.com/presentation_image_h2/ced02a52d0893f4666390ce0c2275ce9/image-10.jpg)
Ligação Iônica Exercícios : 3. A fórmula eletrônica de Lewis [ K ]+ [ F ] representa um composto: a. molecular. b. metálico. c. iônico. d. condutor de eletricidade no estado sólido. e. com baixa temperatura de fusão.

Ligação Covalente v. Resulta do compartilhamento de elétrons entre dois átomos. Ocorre entre os elementos não -metálicos (ametais) ou com o hidrogênio. v. Pode ser representada pelas fórmulas; molecular, estrutural e Lewis

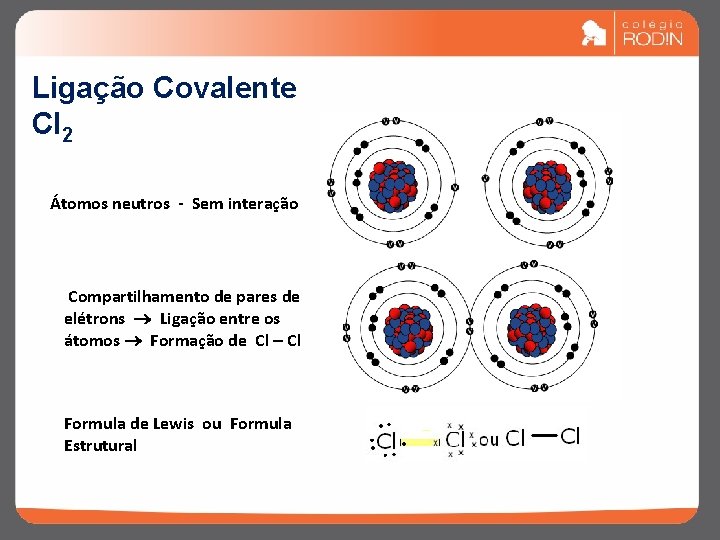
Ligação Covalente Cl 2 Átomos neutros - Sem interação Compartilhamento de pares de elétrons Ligação entre os átomos Formação de Cl Formula de Lewis ou Formula Estrutural

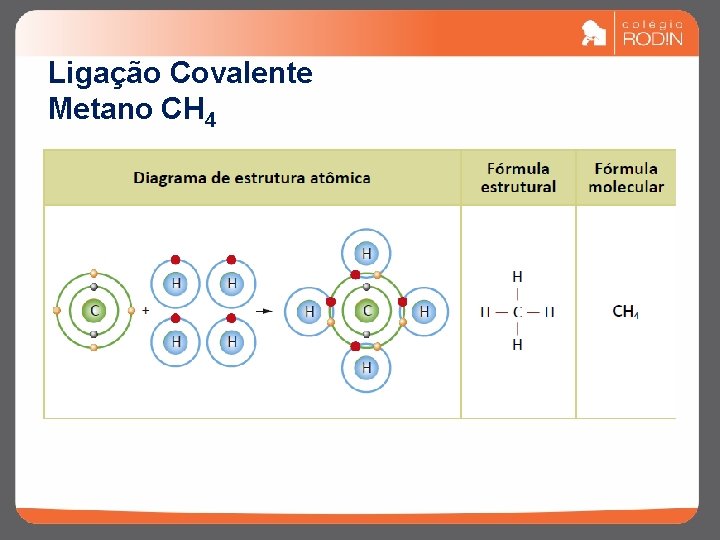
Ligação Covalente Metano CH 4

Ligação Covalente Exercícios 03) A ligação covalente ocorre entre: a. metal e metal. b. metal e ametal. c. ametal e ametal. d. metal e gás nobre. e. ametal e gás nobre.

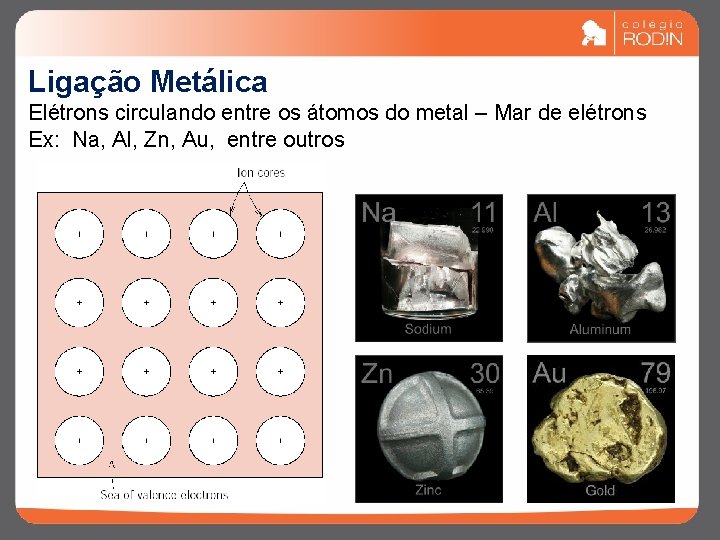
Ligação Metálica Elétrons circulando entre os átomos do metal – Mar de elétrons Ex: Na, Al, Zn, Au, entre outros

Ligação Metálica Exercícios 02) São incontáveis os elementos químicos fundamentais ao funcionamento normal do organismo. Como exemplo, podemos citar o Na (sódio) e o C�(cloro), indispensáveis ao equilíbrio iônico, o F (flúor), componente estrutural de ossos e dentes, e o Mg (magnésio), importante para o metabolismo dos açúcares e para a excitabilidade muscular. Os átomos desses elementos podem ser encontrados de diversas maneiras na natureza, combinados a diferentes átomos do mesmo elemento ou de elementos diferentes. O cloreto de sódio (Na. C�), o flúor (F 2) e o magnésio (Mg) devem apresentar, respectivamente, ligações do tipo: a. metálica, iônica e covalente. b. iônica, iônica e metálica. c. iônica, covalente e metálica. d. covalente, iônica e metálica. e. covalente, metálica e iônica.
