Les cations ce sont des ions chargs positivement



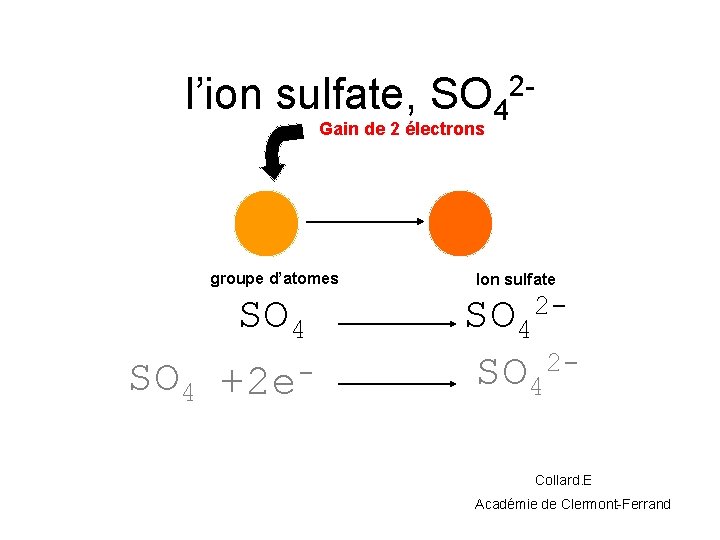






- Slides: 20

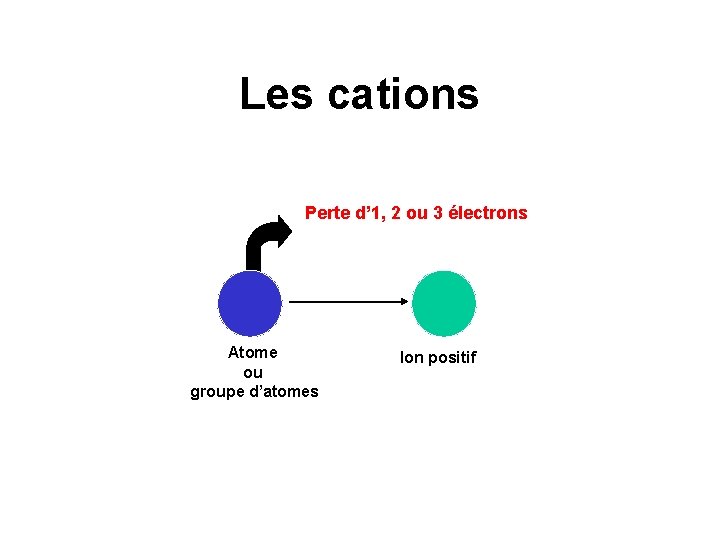
Les cations: ce sont des ions chargés positivement C’est donc un atome ou un groupe d’atomes qui a perdu un ou plusieurs électrons.

Les cations Perte d’ 1, 2 ou 3 électrons Atome ou groupe d’atomes Ion positif

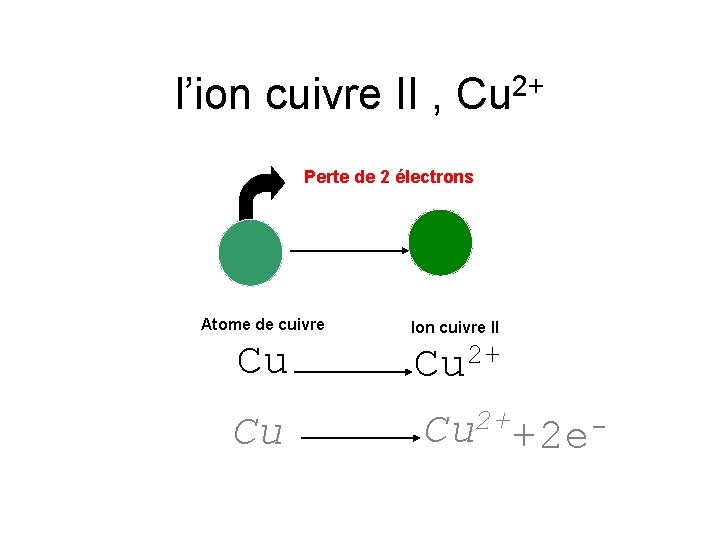
l’ion cuivre II , Cu 2+ Perte de 2 électrons Atome de cuivre Cu Cu Ion cuivre II 2+ Cu Cu 2+ +2 e-

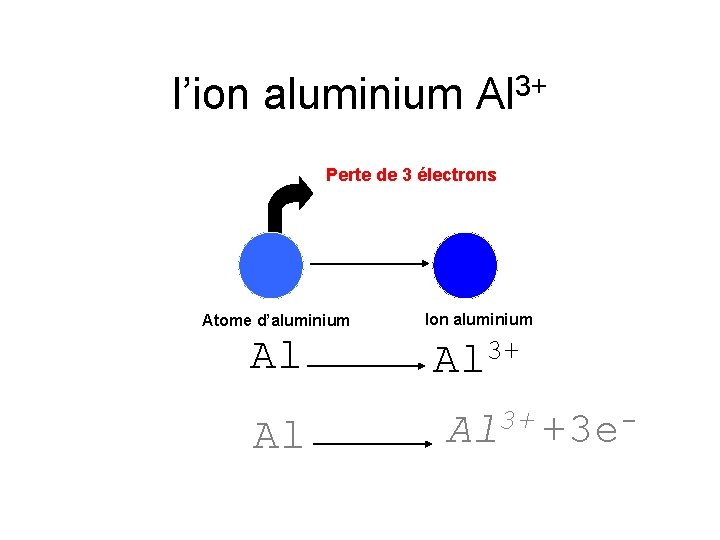
l’ion aluminium Al 3+ Perte de 3 électrons Atome d’aluminium Ion aluminium Al 3+ Al Al Al 3+ +3 e-

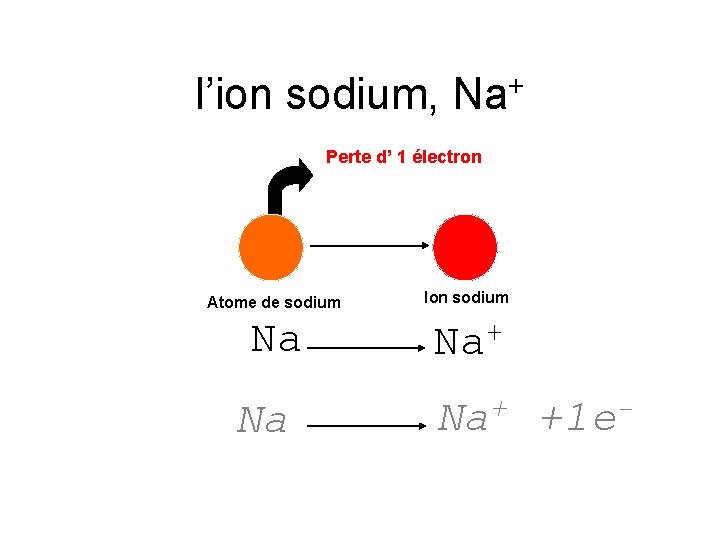
l’ion sodium, Na+ Perte d’ 1 électron Atome de sodium Ion sodium Na Na+ +1 e-

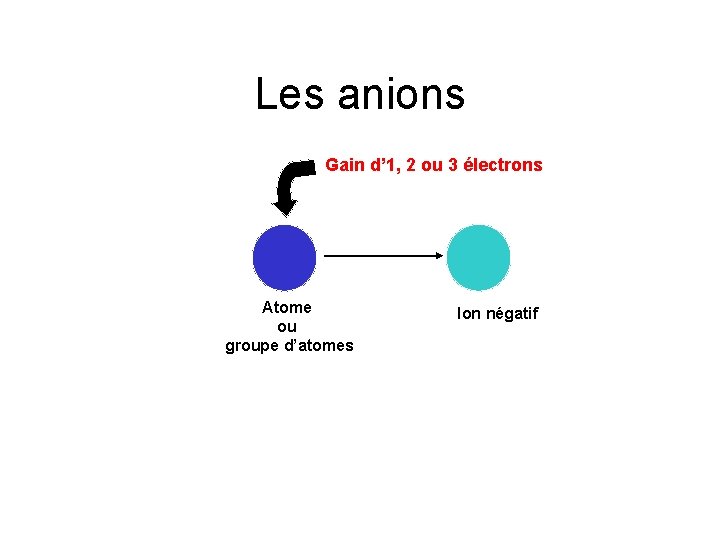
Les anions: ce sont des ions chargés négativement C’est donc un atome ou un groupe d’atomes qui a gagné un ou plusieurs électrons.

Les anions Gain d’ 1, 2 ou 3 électrons Atome ou groupe d’atomes Ion négatif

l’ion chlorure, Cl. Gain d’ 1 électron Atome de chlore Ion chlorure Cl Cl- Cl+1 e- Cl
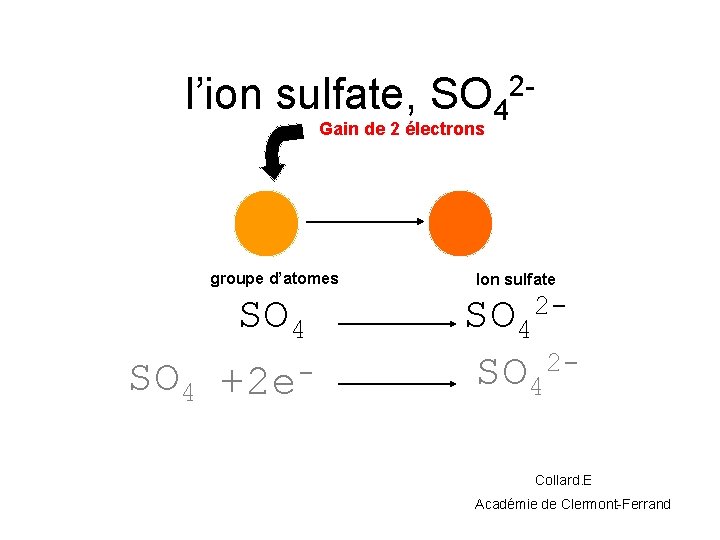
l’ion sulfate, SO 42 Gain de 2 électrons groupe d’atomes SO 4 +2 e- Ion sulfate SO 422 SO 4 Collard. E Académie de Clermont-Ferrand

Les solutions ioniques: corps à structure ionique Apprendre à écrire la formule ionique des solutions suivantes: • Solution de chlorure de sodium • Solution de chlorure de cuivre II • Solution de chlorure de fer III • Solution de sulfate de fer III

Comment obtenir une solution J’ai des cristaux, de chlorure de sodium donc un solide, c’est un corps à structure ionique puisqu’il est constitué d’ions sodium et d’ions chlorure. Na. Cl Au contact de l’eau ces ions vont se disperser et nous allons obtenir une solution de chlorure de sodium Petite animation

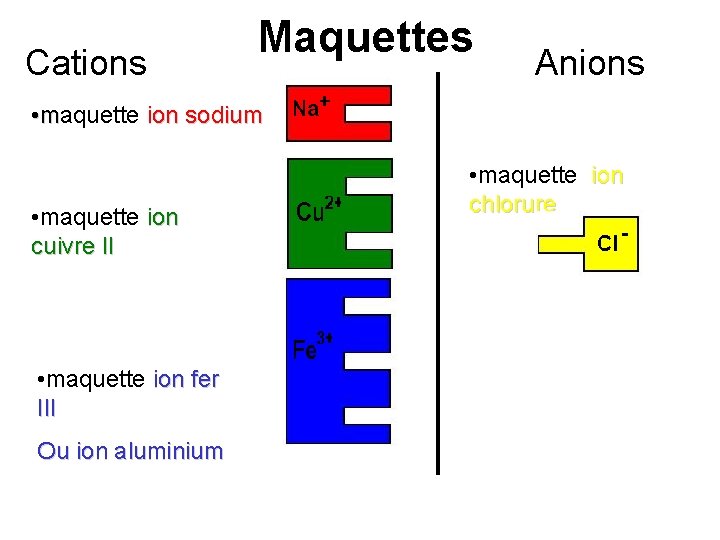
Cations Maquettes Anions • maquette ion sodium • maquette ion cuivre II • maquette ion fer III Ou ion aluminium • maquette ion chlorure

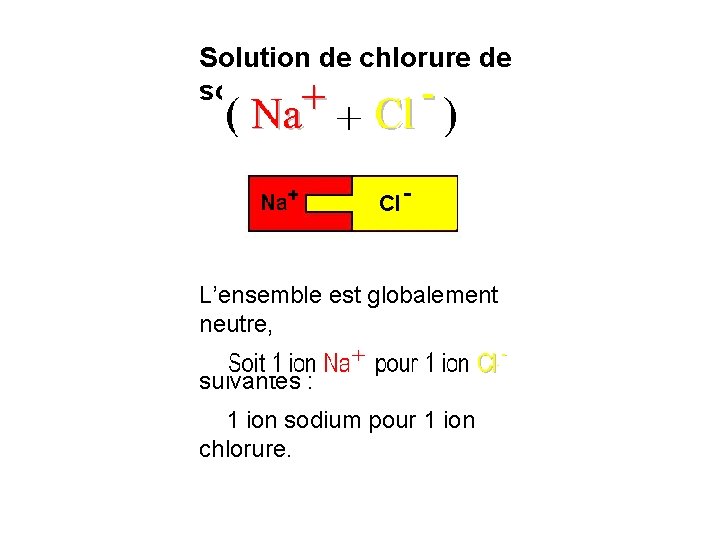
Solution de chlorure de sodium L’ensemble est globalement neutre, Ion sodium Ion chlorure il faut les proportions suivantes : 1 ion sodium pour 1 ion chlorure.

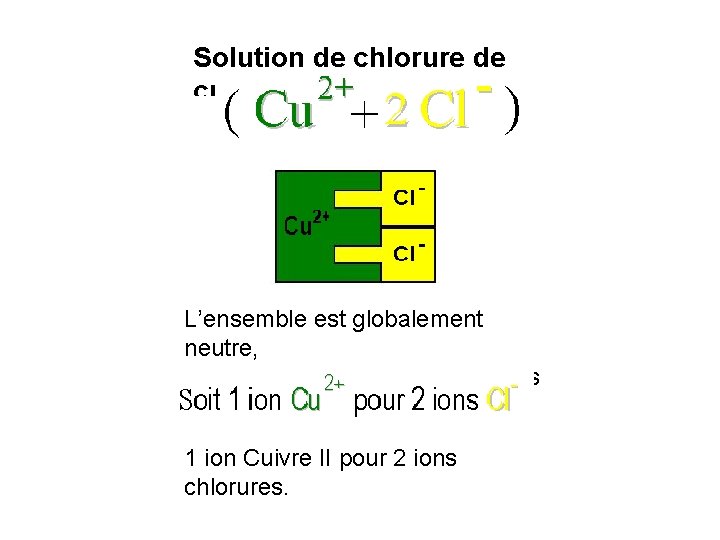
Solution de chlorure de cuivre II L’ensemble est globalement neutre, faut les proportions suivantes Ionil cuivre Ion chlorure : II 1 ion Cuivre II pour 2 ions chlorures.

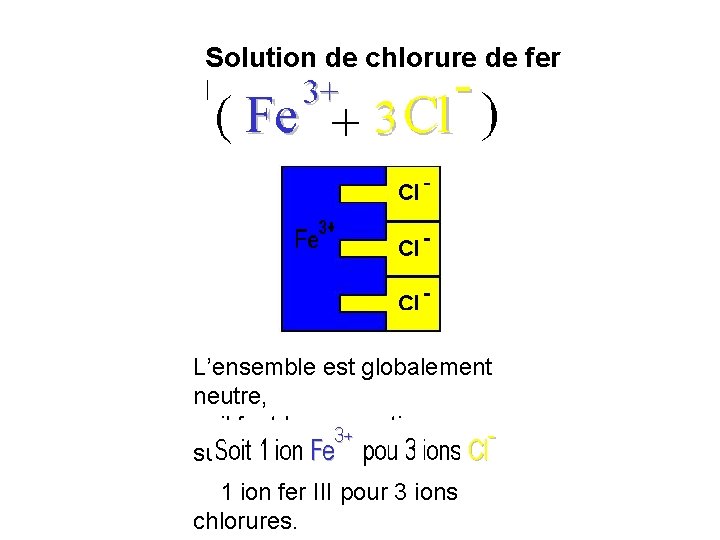
Solution de chlorure de fer III Ion L’ensemble est globalement chlorure neutre, il faut les proportions suivantes : 1 ion fer III pour 3 ions chlorures.

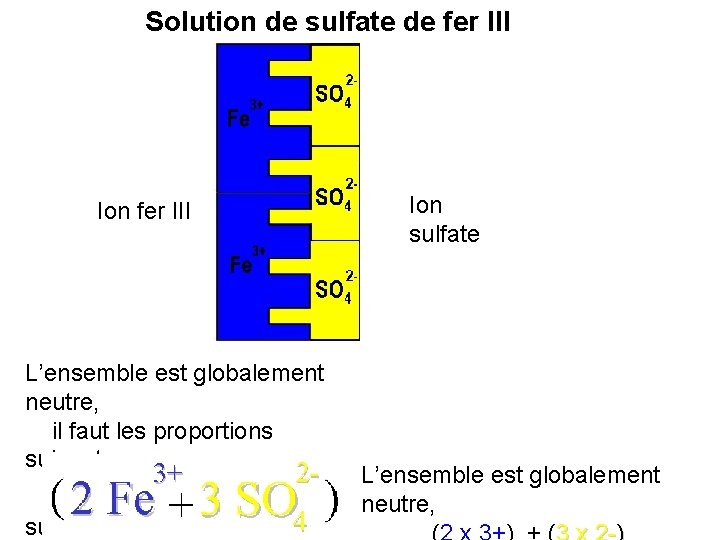
Solution de sulfate de fer III Ion fer III L’ensemble est globalement neutre, il faut les proportions suivantes : 2 ion fer III pour 3 ions sulfate. Ion sulfate L’ensemble est globalement neutre,

Une solution ionique est électriquement neutre: Les charges positives portées par les ions positifs compensent les charges négatives portées par les ions négatifs Collège Camille Guérin Poitiers Souesme. J

Généralisons Je suis une solution de ani… de Je suis une solution de chlorure de cat… fer II J’ai n ions cat…et m ions ani… J’ai 1 ions fer II et 2 ions chlorure ( n. Cm+ + m. An- ) ( 1 Fe 2+ + 2 Cl 1 - ) Ma charge globale est électriquement neutre (n x m + + m x n - ) = (1 x 2 + + 2 x 1 - ) = 0 0 Je peux même écrire sa formule lorsque je suis à l’état solide, mes ions ne se sont pas dissociés : Cn Am soit Fe 1 Cl 2 Fe. Cl 2

Exercice Je suis une solution de sulfate de fer III J’ai des ions fer III et des ions 3+ sulfate ( …Fe J’ai des ions fer III : Fe 3+ et des ions sulfate : SO 42 - + … SO 42 - ) Ma charge globale est électriquement neutre (2 x 3 + + 3 x 2 - ) = 0 ( 2 Fe 3+ soit + 3 SO 42 - ) Je peux même écrire sa formule lorsque je suis à l’état solide, mes ions ne se sont pas dissociés : Fe… SO 4… Fe 2(SO 4)3

http: //www. fsref. com/ref/pdb/