Kmiai reakcik katalzis Egyszer reakcik az elbb ismertetett

Kémiai reakciók katalízis Egyszerű reakciók: az előbb ismertetett módon a katalizátor csökkenti az aktiválási energiát. Pl: Pt 2 H + O 2 H O 2 2 2 Pt felületén megköti a H 2 és O 2 molekulákat, felbontja a H 2 és fellazítja az O 2 kötését, így kisebb energiát kell a reakcióhoz befektetni. Összetett reakciók: az eredeti reakció mellett egy másik, gyorsabban lejátszódó reakcióút nyílik meg. Pl: NH 3 és HCl reakciója víz jelenlétében (katalizátor nélkül a két molekula megfelelő ütközése kellene) NH 3 + H 2 O = NH 4+ + OHNH 4+ + HCl = NH 4 Cl + H+ H+ + OH- = H 2 O A H 2 O átmeneti vegyületet hoz létre NH 3 -al, mely könnyebben reagál a HCl-el. A katalizátor visszaalakul, s újabb reakcióra kész.

Kémiai reakciók katalízis Katalizátorok fajtái: Aszerint, hogy a katalizátor és a reaktánsok azonos vagy különböző fázisban vannak, megkülönböztetünk • homogén katalízis (azonos fázis) – NH 3 és HCl előbbi reakciója (víz = folyadék fázisban) – élő rendszerekben, katalizátorok az enzimek • heterogén katalízis (különböző fázis) – az ipari méretű szintéziseknél, (a reakció után a katalizátor egyszerűen kinyerhető a rendszerből), pl. hidrogénezések = telítetlen szerves vegyületek telítése H 2 -el Pd katalizátor alkalmazásával Katalizátor autókban: Pt (Pd, Rh) környezetre kevésbé ártalmas termékek. kerámia méhsejt szerkezetű mag: • Nitrogén-oxidok redukciója: 2 NOx → x. O 2 + N 2 • CO oxidációja: 2 CO + O 2 → 2 CO 2 • Elégetlen szénhidrogének oxidációja: Cx. H 2 x+2 + 2 x. O 2 → x. CO 2 + 2 x. H 2 O

Kémiai reakciók Szabadentalpia Entrópia (S, k. J/K): egy rendszer rendezetlenségének mértéke. A rendezetlenség kedvezőbb állapot: • kristályos anyag oldódása (oldott anyag oldószerben való eloszlása) • gázok keveredése (kibocsátott CO 2, füst) A természetes folyamatokat az irányítja, hogy: • csökkenjen a rendszer energiája (energia-felszabadulás) • növekedjen a rendezetlenség mértéke G: szabadentalpia, k. J Ezt fejezi ki a szabadentalpia: G = H – TS H: entalpia, k. J Valamely folyamat (kémiai reakció) szabadentalpia változása: DG = DH – TDS T: hőmérséklet, K Spontán folyamat akkor megy végbe, ha szabadentalpia változás negatív (DG<0). Az entrópia tagnak inkább csak magas hőmérséklet esetén (T > 1500 K) van jelentősége, szobahőmérsékleten általában elhanyagolható, azaz DG ≈ DH

Kémiai reakciók egyensúlyi reakciók: A B Minden kémiai reakció elvileg oda-vissza mehet, a fő különbség a befektetendő aktiválási energiában van. Aktivált komplexum DEa Reaktánso k Reakcióút DE’a Termékek DEa Reaktánso k DE’a Termékek Reakcióút (Gyakorlatilag) egyirányú reakciók: • nagyon stabilis a termék • a termék más halmazállapota miatt eltávozik a rendszerből: - gáz: H 2 CO 3 → H 2 O + CO 2 - csapadék: Ag. NO 3 + HCl → Ag. Cl + HNO 3

Kémiai reakciók kémiai egyensúly Kémiai egyensúly kifejeződése a koncentrációkban és a reakciósebességekben: ctermék Idő → egyensúly ckiindulási anyag ctermék Idő → egyensúly Reakcósebesség → ckiindulási anyag Koncentráció → v 1 egyensúly v 2 Idő → • Kiindulási anyagok felé tolódott egyensúlyban végig: ckiindulási anyag > ctermék • Termék felé tolódó egyensúlyban egy idő után: ckiindulási anyag < ctermék • Egyensúlyban az oda-vissza alakulás reakciósebessége megegyezik (v 1 = v 2) ! A koncentrációban nincs változás, de az oda-vissza reakció folyamatosan történik! DINAMIKUS EGYENSÚLYI ÁLLAPOT

Kémiai reakciók egyensúlyi állandó Tömeghatás törvénye: egyensúlyban a termékek megfelelő hatványon vett egyensúlyi koncentrációinak szorzata, osztva a kiindulási anyagok megfelelő hatványon vett egyensúlyi koncentrációinak szorzatával, egy adott hőmérsékleten állandó érték. a. A + b. B c. C + d. D reakcióra: (levezetve: v 1=k 1[A]a[B]b, v 2=k 2[C]c[D]d k 1 [C]c[D]d a b c d = egyensúlyban: v 1=v 2, azaz k 1[A] [B] =k 2[C] [D] → k 2 [A]a[B]b Az egyensúlyi állandó (K) csak a külső körülményektől (nyomás, hőmérséklet) függ, független a koncentráció értékektől. • K>1: egyensúlyban a termékek vannak nagyobb mennyiségben • K<1: egyensúlyban a kiindulási anyagok vannak nagyobb mennyiségben

Kémiai reakciók egyensúlyi állandó Le Chatelier-Braun elv (legkisebb kényszer elve): egy dinamikus egyensúlyban levő rendszer megzavarásakor annak a folyamatnak lesz nagyobb a sebessége, amely a zavaró hatást csökkenteni igyekszik. a) koncentrációváltoztatás (K-t nem változtatja, de a reakciósebességeket igen a. A + b. B c. C + d. D reakcióban megnöveljük B mennyiségét y-al: eredeti egyensúlyban k 1[A]a[B]b=k 2[C]c[D]d, változtatva k 1[A]a[B+y]b→k 2[C]c[D]d új egyensúlyban: k 1 [A-x]a[B+y-x]b=k 2 [C+x]c[D+x]d K= [A-x]a[B+y-x]b b) hőmérsékletváltoztatás: K-t változtatja, s azon keresztül a reakciósebességeket, koncentrációkat. • T növelés: endoterm reakciónál termékképződés (szél) exoterm reakciónál visszaalakulás (ellenszél) • T csökkentés: exoterm reakciónál termékképződés endoterm reakciónál visszaalakulás

Kémiai reakciók egyensúlyi állandó Le Chatelier-Braun elv: c) nyomásváltoztatás: csak molekulaszám változással járó reakciókban K-t változtatja, s azon keresztül a reakciósebességeket, koncentrációkat. • p növelés: molekulák számának csökkenése felé • p csökkentés: molekulák számának növekedése felé pl: H 2 O + CO 2 H 2 CO 3: megfelelő mennyiségű CO 2 -t nyomással oldanak az ásványvízben d) katalizátor nem változtatja meg az egyensúlyi állandót, csak a reakciósebességeket (mindkét irányét) növeli Ok: az egyensúlyi állandó a kiindulási anyagok és végtermékek relatív energiájától függ, ezt pedig a katalizátor nem befolyásolja.

Kémiai reakciók Protolitikus reakciók Hidrogénion (proton) átadással járó reakciók főként vizes oldatban Brönsted szerint: oxónium ion • savak: protont leadó molekulák és ionok (HCl + H 2 O H 3 O+ + Cl-) • bázisok: protont felvevő molekulák és ionok (NH 3 + H 2 O NH 4+ + OH-) Proton sosincs szabad állapotban az oldatban, ezért ezen (mindig) egyensúlyi reakciókban a sav és bázis együttesen van jelen: HCl + H 2 O H 3 O+ + Clsav bázis Amfoter vegyület: partnertől függően savként illetve bázisként reagál: H 2 O A sav-bázis párok erőssége ellentétes: minél erősebb a sav (pl. HCl), annál gyengébb a bázis párja (Cl-). Arrhenius-féle sav-bázis elmélet (korábbi, közelebb áll a mindennapi élethez) Csak vizes oldatokra érvényes! • savak: vízben H+-ionra és anionra disszociálnak: HCl H+ + Cl • bázisok: vízben OH--ionra és kationra disszociálnak: Na. OH Na+ + OH-

Kémiai reakciók Protolitikus reakciók: egyensúlyi állandók Disszociációs egyensúlyi állandók: sav illetve bázis HNO 3 - + H+ NH 4 OH [NO 3 -][H+] Ks= [HNO 3] NH 4+ + OH- [NH 4+][OH-] Kb = [NH 4 OH] A […] koncentrációk mindig az egyensúlyi koncentrációk, nem pedig kiindulási vagy bruttó koncentrációk, ami példákban sokszor szerepel. Víz disszociációja: H 2 O + H 2 O H 3 O+ + OHAutoprotolízis: egy vegyület molekulái egymással lépnek sav-bázis reakcióba [H 3 O+][OH-] A folyamatra felírva a tömeghatástörtet: K= [H 2 O]2 A H 2 O molekulák koncentrációja gyakorlatilag állandó (55, 5 mol/dm 3), ezért összevonható K-val: Kvíz= [H 3 O+][OH-] = 10 -14 (mol/dm 3)2 vízionszorzat 25 ºC-on

Protolitikus reakciók p. H Vízionszorzat jelentése: H 3 O+ (H+) és OH- ionok mindig vannak jelen az oldatban, és meghatározzák egymás koncentrációját. Kémhatás: • savas oldat: H 3 O+ ionok vannak többségben (>10 -7 mol/dm 3) • bázikus (lúgos) oldat: OH- ionok vannak többségben (>10 -7 mol/dm 3) • semleges oldat: [H 3 O+]=[OH-] = 10 -7 mol/dm 3 A kémhatás számszerű jellemzésére a -lg[H 3 O+] értéket használjuk, neve p. H • savas oldat: p. H < 7 • bázikus (lúgos) oldat: p. H > 7 (Analóg módon p. OH is létezik, de a gyakorlatban nem használatos. ) Számítási példa: Mennyi a 0. 1 mol/dm 3 -es HCl illetve Na. OH oldatok p. H-ja? HCl disszociációja után [H 3 O+]=0. 1 mol/dm 3 → p. H=-lg[H 3 O+] =1 Na. OH oldatban [OH-]=0. 1 mol/dm 3 vízionszorzatból [H 3 O+]=10 -13 mol/dm 3 → p. H=13

Protolitikus reakciók Gyenge savak disszociációja Hidrogén-cianid: HCN + H 2 O H 3 O+ + CN- Ks= [H 3 O+][CN-] [HCN] = 10 -9 mol/dm 3 Számítási példa: 1. Mennyi az 1 mol/dm 3 -es HCN oldat p. H-ja? A disszociáció során azonos mennyiségű H 3 O+ és CN- keletkezik: [H 3 O+]=[CN-] A maradó HCN koncentrációja: 1 -[H 3 O+] mol/dm 3 behelyettesítve a tömeghatástörtbe: 10 -9= [H 3 O+]2 1 -[H 3 O+] A másodfokú egyenlet megoldása: [H 3 O+]=3. 2. 10 -5 mol/dm 3 → p. H=4. 5 2. Mennyi lesz a CN--koncentráció, ha a fenti oldat p. H-ját erős savval 2 -re állítjuk? A tömeghatástört: 10 -9= [10 -2][CN-] , melyből [CN -]=10 -7 mol/dm 3 1 -[CN-] Gyenge bázisok p. H számítása analóg, csak ott a végén OH--koncentrációt kapunk, amiből a vízionszorzat segítségével kapjuk meg a H 3 O+-koncentrációt.

Protolitikus reakciók Hidrolízis Erős sav és erős bázis sójának (pl. Na. Cl) vizes oldata semleges kémhatású. Ha vagy a sav, vagy a bázis gyenge, a vizes oldat nem lesz semleges. • gyenge sav+erős bázis (Na. CN): lúgos kémhatás • gyenge bázis + erős sav (NH 4 Cl): savas kémhatás A feloldáskor keletkező ionok reagálnak a víz molekulákkal: lúgos CN- + H 2 O HCN + OHsavas NH 4+ + H 2 O NH 4 OH + H+ (H 3 O+) A fenti hidrolízisek is egyensúlyi folyamatok: [HCN][OH-] K h= [CN-] [NH 4 OH][H 3 O+] és Kh= , [H 2 O] beépítve Kh hidrolízisállandóba + [NH 4 ] A Ks(Kb) disszociációs állandók Kvíz K = és a megfelelő hidrolízisállandók h K s között összefüggés van: Kvíz [H 3 O+][OH-][HCN] =Kh = + [CN ][H 3 O ] Ks
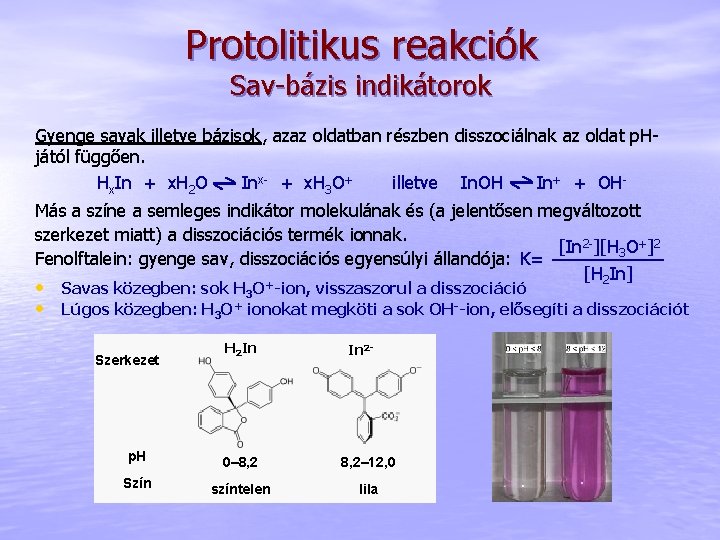
Protolitikus reakciók Sav-bázis indikátorok Gyenge savak illetve bázisok, azaz oldatban részben disszociálnak az oldat p. Hjától függően. Hx. In + x. H 2 O Inx- + x. H 3 O+ illetve In. OH In+ + OHMás a színe a semleges indikátor molekulának és (a jelentősen megváltozott szerkezet miatt) a disszociációs termék ionnak. [In 2 -][H 3 O+]2 Fenolftalein: gyenge sav, disszociációs egyensúlyi állandója: K= [H 2 In] • Savas közegben: sok H 3 O+-ion, visszaszorul a disszociáció • Lúgos közegben: H 3 O+ ionokat megköti a sok OH--ion, elősegíti a disszociációt Szerkezet H 2 In In 2 - p. H 0– 8, 2– 12, 0 Szín színtelen lila

Protolitikus reakciók Univerzális indikátor www. lmpc. edu. au/. . . /indicator. htm encarta. msn. com/. . . /universal_indicator. html Különböző indikátorok (fenolftalein, brómtimolkék, metilvörös, és timolftalein) keveréke, melyek más-más p. H-nál változtatják színüket.

- Slides: 16


















