Jak se tvo nzvy kyselin Definice a rozdlen














- Slides: 15

Jak se tvoří názvy kyselin

Definice a rozdělení kyselin Kyseliny jsou většinou tříprvkové sloučeniny nekovu, kyslíku a vodíku. Jen málo kyselin je dvouprvkových, složených z nekovu a vodíku. Rozdělení kyselin: a/ Kyslíkaté (nekov, O, H) b/ Bezkyslíkaté (nekov, H) Úkol 1: Vyber ze sloučenin kyseliny: Fe(OH)3, HCl, Na. OH, K 2 O, SCl 4, Pb. S, Al. Cl 3, H 2 O, HCl. O 3, Ca(OH)2, HIO 4, H 3 PO 4

Kontrola úkolu 1 HCl, HCl. O 3, HIO 4, H 3 PO 4

Názvosloví bezkyslíkatých kyselin Název kyseliny se skládá z podstatného jména kyselina a přídavného jména odvozeného od názvu nekovu s příponou -ovodíková. Ve vzorci píšeme vodík jako první. Oxidační číslo nekovu je záporné, vodíku +I. Součet oxidačních čísel v molekule je roven 0. Úkol 2: Odvoď název kyseliny HI a vzorec kyseliny fluorovodíkové:

Kontrola úkolu 2 Kyselina jodovodíková, HF

Názvosloví kyslíkatých kyselin Název tvoří podstatné jméno kyselina a přídavné jméno odvozené od nekovu s předponou vyjadřující počet vodíků a příponou odpovídající jeho oxidačnímu číslu. Číslovková předpona pro počet H je: 1 H - mono, 2 H - di, 3 H - tri, 4 H - tetra, 5 H - pentahydrogen, např. H 3 PO 4 je kyselina trihyrogenfosforečná. Oxidační čísla v kyselině jsou O-II, HI, nekov I - VIII. Součet hodnot oxidačních čísel všech atomů v kyselině je 0.

Odvození vzorce kyseliny Postup při odvození vzorce kyseliny dihyrogensírové: Napíšeme značky prvků v pořadí H, nekov, O - HSO. Zapíšeme podle předpony počet vodíků - H 2 SO. U prvků zapíšeme oxidační čísla HI, SVI podle koncovky přídavného jména, O-II - HI 2 SVIO-II Upravíme počet atomů kyslíku tak, aby součet všech oxidačních čísel v molekule byl 0 (2 · 1 + 6) : 2 = 4 - HI 2 SVIO-II 4. Vzorec kyseliny dihydrogensírové je H 2 SO 4.

Úkol 3: Napiš vzorce kyselin: a/ Kyselina monohydrogenchlorečná b/ Kyselina trihydrogenboritá c/ Kyselina dihydrogenuhličitá d/ Kyselina tetrahydrogenkřemičitá e/ Kyselina pentahydrogenjodistá

Kontrola úkolu 3 a/ HCl. O 3 b/ H 3 BO 3 c/ H 2 CO 3 d/ H 4 Si. O 4 e/ H 5 IO 6

Odvození vzorce kyseliny z kyselinotvorného oxidu Postup při odvození vzorce kyseliny sírové: Vzorec každé kyseliny lze odvodit z kyselinotvorného oxidu, který má stejnou koncovku jako kyselina, a vody, v našem případě z oxidu sírového. SO 3 + H 2 O → H 2 SO 4 Vzorec kyseliny sírové je H 2 SO 4.

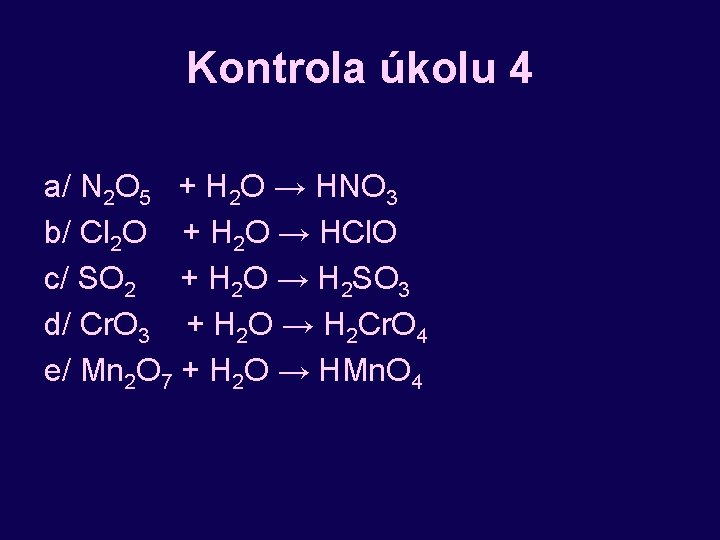
Úkol 4: Odvoď vzorce kyselin z kyselinotvorného oxidu a vody: a/ Kyselina dusičná b/ Kyselina chlorná c/ Kyselina siřičitá d/ Kyselina chromová e/ Kyselina manganistá

Kontrola úkolu 4 a/ N 2 O 5 + H 2 O → HNO 3 b/ Cl 2 O + H 2 O → HCl. O c/ SO 2 + H 2 O → H 2 SO 3 d/ Cr. O 3 + H 2 O → H 2 Cr. O 4 e/ Mn 2 O 7 + H 2 O → HMn. O 4

Odvození názvu kyseliny Postup při odvození názvu H 3 PO 3: Jedná se o kyselinu, neboť obsahuje H, nekov, O. Podle počtu vodíků v kyselině odvodíme předponu v našem případě kyselina trihydrogen. Napíšeme oxidační čísla vodíku a kyslíku HI 3 PO-II 3. Vypočítáme oxidační číslo fosforu 3 · 1 + x + 3 · (-2) = 0 x = 3 oxidační číslo fosforu je 3 - itá Název sloučeniny je kyselina trihydrogenfosforitá.

Úkol 5: Doplň oxidační čísla nekovů a napiš názvy kyselin: a/ HBr. O b/ H 2 Si. O 3 c/ H 3 PO 2 d/ HFO 4 e/ HIO 3 f/ HNO 2

Kontrola úkolu 5 a/ HBr. IO kyselina monohydrogenbromná b/ H 2 Si. IVO 3 kyselina dihydrogenkřemičitá c/ H 3 PIO 2 kyselina trihydrogenfosforná d/ HFVIIO 4 kyselina monohydrogenfluoristá e/ HIVO 3 kyselina monohydrogenjodičná f/ HNIIIO 2 kyselina monohydrogendusitá