Instrumentls metodes Kura mris iepazstint studentus ar dadm










































- Slides: 63

Instrumentālās metodes • Kura mērķis - iepazīstināt studentus ar dažādām instrumentālām metodēm ar pielietojumu molekulārajā un šūnu bioloģijā, bioķīmijā un citās radniecīgās nozarēs • Kurss notiks LU BF un Biomedicīnas pētījumu un studiju centrā (BMC)

Instrumentālo metožu kursa saturs • Proteīnu ekspresija, attīrīšana un elektroforēze (BF, 2 xlekc. , lab. d. ) • Mikroskopija - optiskā (BF), konfokālā (BF), elektronu (BMC), lekc. , lab. d. , demonstr. • Organellu atdalīšana centrifūgas gradientā (BF, lekc. +lab. d) • DNS sekvenēšana (BMC, lekc. +mini-lab. d. ) • Masspektrometrija (BMC, lekc. + mini-lab. d. ) • Reālā laika PCR (BMC, lekc. + mini-lab. d. ) • Plūsmas citometrija (BMC, lekc. + demonstr. ) • Radioaktīvo elementu pielietojums bioloģijā (BF, BMC, lekc. + demonstr. ) • Proteīnu struktūru noteikšanas metodes – rentgenstruktūranalīze un KMR (BMC, BF 2 xlekc. , 1 xmini lab. d. )

Prasības • Sekmīgi nokārtoti visi pārbaudes darbiņi • Apmeklēti visi laboratorijas darbi, par kuriem vēlāk iesniegti protokoli • Sekmīgi nokārtots gala tests • Kavētos pārbaudes darbiņus var uzrakstīt pēc lekcijas 331. telpā vai pēc nodarbībām BMC • Sekmīgi nokārtoto pārbaudes darbiņu pārlikšana nolūkā iegūt augstāku atzīmi netiks atbalstīta • Galīgā atzīme ir aptuveni proporcionāla nodarbību skaitam un tiks izlikta pēc formulas (1 x atzīme pirmajā testā + 2 x atzīme pie Tūra Selgas + 3 x atzīme noslēguma testā)/6. Atzīme pie Tūra Selgas tiek izlikta par mikroskopijas/konfokālās mikroskopijas nodarbībām.

Proteīnu ekspresija un attīrīšana

Kā iegūt proteīnu? • No dabīgā organisma • Mākslīgi producēt citā organismā • Sintezēt (parasti tikai relatīvi īsus peptīdus!)

Proteīna iegūšana no dabīgā organisma • Priekšrocības: • 1. Nav nepieciešamības veikt ģenētiskas manipulācijas • 2. Proteīns vienmēr ir dabīgajā formā • Trūkumi • 1. Var būt grūti iegūt lielus daudzumus • 2. Var būt ētiskas problēmas • 3. Parasti grūti attīrīt • 4. Ierobežotas iespējas pētīt modificētus proteīnus

Piemērs: Liellopu seruma albumīns (BSA) • • Asins serums satur ap 60% albumīna Viegli izolējams ar precipitēšanas metodi Liellopu asins serums ir plaši pieejams BSA plaši pielieto molekulārajā bioloģijā

Proteīnu producēšana (“ekspresija”) citā organismā • Priekšrocības -Var uzproducēt praktiski jebkuru proteīnu -Dabā reti sastopamus proteīnus var uzproducēt lielos daudzumos -Proteīnu var modificēt, lai atvieglotu tā attīrīšanu -Var vikt citas ģenētiskas modifikācijas • Trūkumi -Nepieciešams veikt laikietilpīgas manipulācijas ar rekombinanto DNS -Proteīns var nebūt dabīgajā konformācijā vai izrādīties nešķīstošs

Vektori • Lai gēnu ievietotu citā organismā, lieto t. s. vektorus • Vektori ir divu veidu: • 1. Plazmīdu vektori (vairumā gadījumu) • 2. Vīrusu vektori

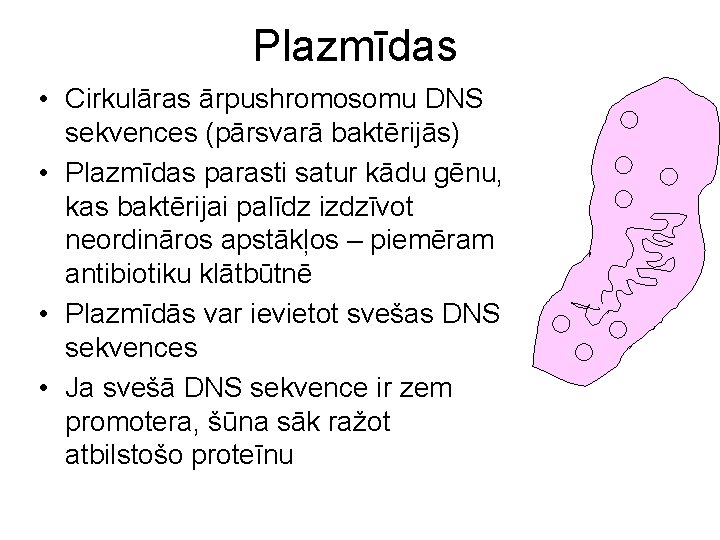
Plazmīdas • Cirkulāras ārpushromosomu DNS sekvences (pārsvarā baktērijās) • Plazmīdas parasti satur kādu gēnu, kas baktērijai palīdz izdzīvot neordināros apstākļos – piemēram antibiotiku klātbūtnē • Plazmīdās var ievietot svešas DNS sekvences • Ja svešā DNS sekvence ir zem promotera, šūna sāk ražot atbilstošo proteīnu

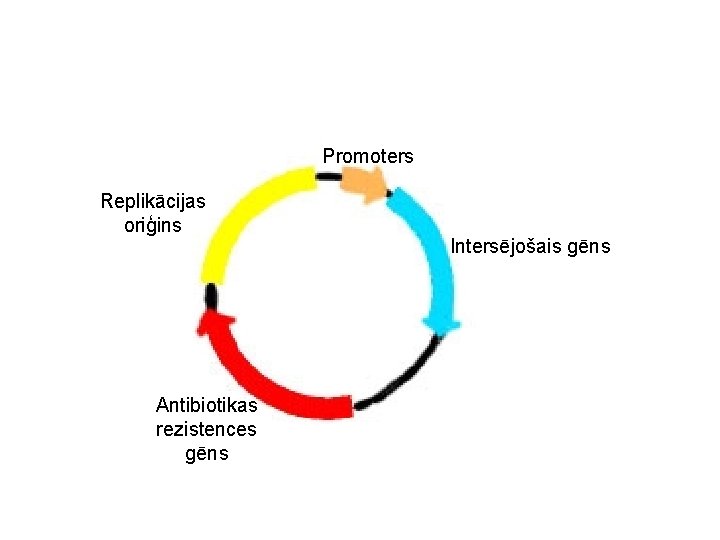
Promoters Replikācijas oriģins Antibiotikas rezistences gēns Intersējošais gēns

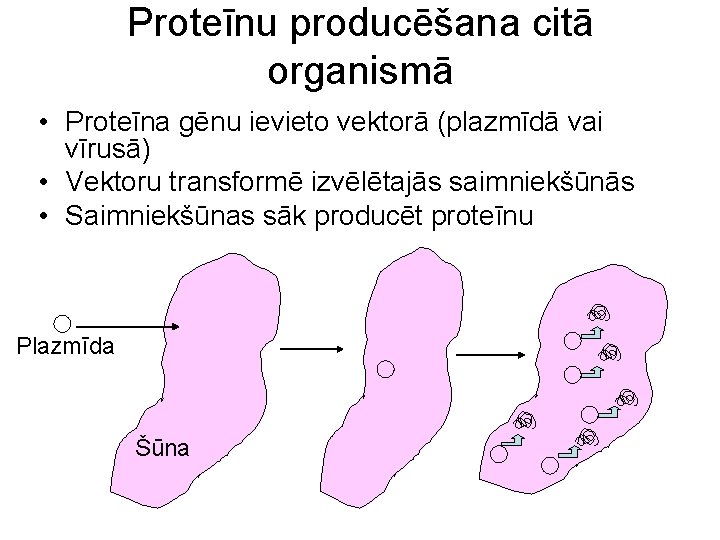
Proteīnu producēšana citā organismā • Proteīna gēnu ievieto vektorā (plazmīdā vai vīrusā) • Vektoru transformē izvēlētajās saimniekšūnās • Saimniekšūnas sāk producēt proteīnu Plazmīda Šūna

Vīrusu vektori • Var būt bakteriāli (bakteriofāgi), insektu, dzīvnieku vai augu • Parasti nebūtisku vīrusa gēnu aizvieto ar interesējošā proteīna gēnu • Šūnas inficē ar rekombinanto vīrusu • Vīrusa proteīni kopā ar interesējošo proteīnu tiek producēti saimniekšūnā

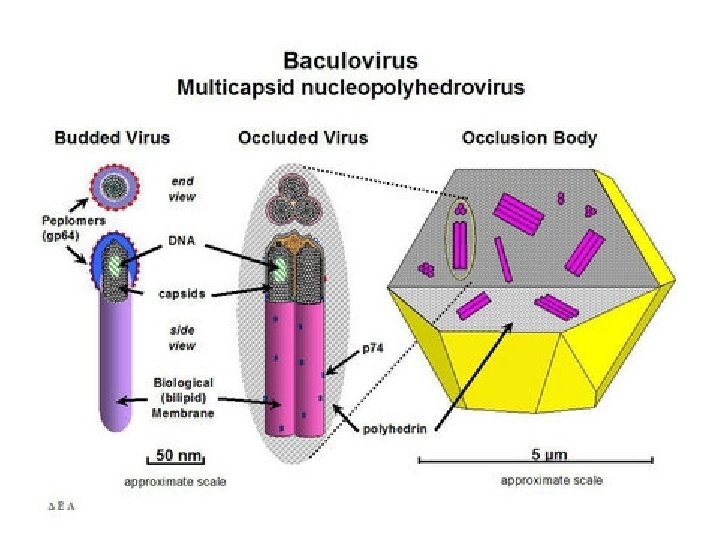
Piemērs: Bakulovīruss • Insektu vīruss • Inficē gan pašus insektus, gan arī kultivētas insektu šūnas • Polihedrīns ir proteīns, kas ietver vairākas vīrusa daļiņas • Polihedrīns palīdz vīrusam izdzīvot apkārtējā vidē • Laboratorijas apstākļos polihedrīns nav būtisks un to var aizvietot


Saimniekšūnu izvēle • Dažādas sistēmas: – Bakteriālā – Raugu – Insektu – Zīdītāju – Augu

• Saimniekšūna var ietekmēt : – Produkcijas daudzumu – Šķīdību – Aminoskābju pēctranslācijas modifikācijas (glikozilēšanu, fosforilēšanu, etc)

• Saimniekšūnas izvēlas atkarībā no: – Pielietošanas mērķa – Nepieciešamā proteīna daudzuma – Proteīna oriģinālā organisma – Cenas – Proteīna potenciālā toksiskuma – Sistēmas vienkāršības

Saimniekšūnas izvēle atkarībā no nepieciešamā proteīna daudzuma • Baktērijas > Raugi >> Insekti > Zīdītāji • Kristalogrāfijai vai NMR ir nepieciešams ļoti daudz proteīna • Šī iemesla pēc ne-bakteriālās sistēmas bieži ir nereālistiskas proteīnu strukturālajiem pētījumiem

Produkcija baktērijās (E. coli) • • • Labās ziņas: Produkcijas apjoms ir augsts Lēti Viekārši strādāt Baktērijas ātri aug Sliktās ziņas: Proteīns bieži ir nešķīstošs Nav pēctranslācijas modifikāciju Ne-baktēriju membrānu proteīnus parasti nav iespējams producēt

Raugi • • Labi: Produkcijas apjoms ir augsts Lēti Samērā vienkārši strādāt (salīdzinot ar zīdītāju šūnām ) Dažas pēctranslācijas modifikācijas ir līdzīgas zīdītāju šūnām Slikti: Ne visas pēctranslācijas modifikācijas ir tādas pašas kā zīdītāju šūnām Proteīni bieži tiek pārglikolizēti

Insektu (Bakulovīrusa) sistēma • Interesējošā proteīna gēnu ievieto bakulovīrusa genomā • Insekta šūnu kultūru vai kāpurus inficē ar rekombinanto bakulovīrusu

Insektu (Bakulovīrusa) sistēma • • Labi: Produkcijas apjoms ir salīdzinoši augsts Lētāk nekā zīdītāju šūnās Lielākā daļa pēctranslācijas modifikāciju ir tādas pašas kā zīdītāju šūnās • Slikti: • Rekombinanta bakulovīrusa konstruēšana ir samērā sarežģīta • Daudz dārgāk nekā baktērijās vai raugos

Zīdītāju šūnas • Parasti izmanto transformētas zīdītāju šūnu kultūras • Visbiežāk COS šūnas (oriģināli no Āfrikas zaļajiem pērtiķiem) vai HEK šūnas (human embryonic kidney) • Šūnas transfecē ar plazmīdām vai inficē ar rekombinantajiem vīrusiem

Zīdītāju šūnas • Labi: • Zīdītāju proteīniem ir autentiskas pēctranslācijas modifikācijas • Proteīni ir šķīstoši • Slikti: • Produkcijas apjoms ir zems • Sarežģīti strādāt • Šūnas aug lēni • Ļoti dārgi

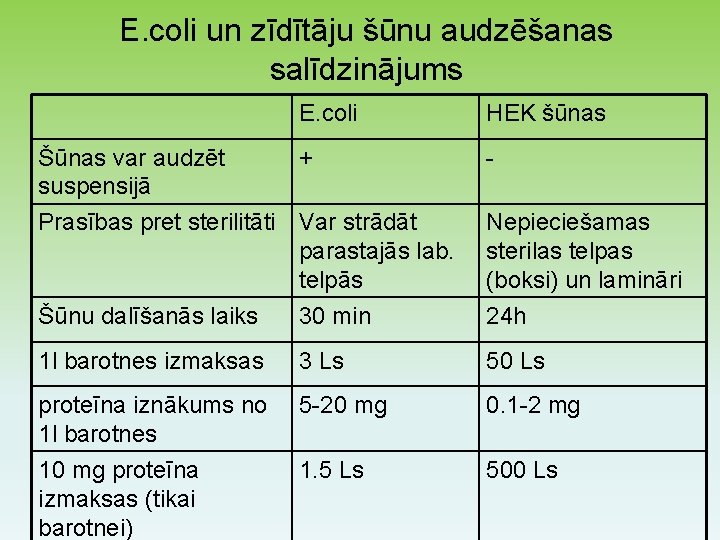
E. coli un zīdītāju šūnu audzēšanas salīdzinājums E. coli HEK šūnas Šūnas var audzēt + suspensijā Prasības pret sterilitāti Var strādāt parastajās lab. telpās - Šūnu dalīšanās laiks 30 min 24 h 1 l barotnes izmaksas 3 Ls 50 Ls proteīna iznākums no 1 l barotnes 10 mg proteīna izmaksas (tikai barotnei) 5 -20 mg 0. 1 -2 mg 1. 5 Ls 500 Ls Nepieciešamas sterilas telpas (boksi) un lamināri

Kā proteīnus dabūt ārā no šūnām ? • Iekššūnas proteīni : šūnu sagraušana • Sekretējamie proteīni – proteīni ir jau sekretēti no šūnām, bet tos nepieciešams koncentrēt • Vairumā gadījumu ir jāstrādā ar iekššūnas proteīniem

Šūnu sagraušana Fizikālās metodes • Ultraskaņa • Frenča prese • Lodīšu dzirnavas Ķīmiskās un fizioķīmiskās metodes • Deterģenti • Enzīmi (lizocīms baktēriju šūnām) • Osmotiskais šoks

Proteīnu iekoncentrēšna • Precipitēšana (ar amonija sulfātu vai polietilēnglikolu) • Ūdens ietvaicēšana vakuumā (jāņem vērā, ka pieaug sāļu koncentrācija) • Ultrafiltrācija

Šķīstošs vai nē? • • Šķīstošs – viss kārtībā! Nešķīstošs (ieslēguma ķermeņi): nav labi : ( – • Var izmēģināt refoldingu Kā mēģināt uzlabot šķīdību: Samazināt ekspresijas apjomu, pazemināt šūnu audzēšanas temperatūru • Nekas nepalīdz? 1. Izmēģināt citu saimniekšūnu veidu 2. Pamest projektu. . .

Bezšūnu proteīnu sintēze • Translāciju ir iespējams veikt in vitro • Daudz sarežģītāks process, nekā, piemēram, in vitro replikācija vai transkripcija • Nepieciešamas ribosomas, aminoskābes, t. RNS, m. RNS, aminoacil-t. RNA sintetāzes, translācijas faktori, . . . • Izmanto šūnu lizātus • Var izmantot gan eikariotisko, gan prokariotisko šūnu lizātus • Parasti izmanto trušu retiklocītu, kviešu dīgļu šūnu vai E. coli lizātus

Bezšūnu proteīnu sintēze • • Pielietojumi: Šūnām toksisku proteīnu sintēze Proteīnu iezīmēšana NMR Membrānu proteīnu sintēze Trūkumi: Ļoti dārga metode Grūti optimizējama metode

Proteīnu attīrīšana • Kāpēc? • Lai proteīnu raksturotu (enzimātiskā aktivitāte, ligandu piesaistīšana, stabilitāte, etc) • Lai noteiktu proteīna 3 D struktūru • Lai identificētu proteīnu, saistītu ar noteiktu aktivitāti • Lai zinātniskiem, industriāliem vai medicīniskiem mērķiem saražotu proteīnu ar zināmu aktivitāti

Proteīnu attīrīšana pamatojas uz: • • Molekulas izmēru Virsmas lādiņu Virsmas hidrofobitāti Afinitāti (spēju piesaistīt citus savienojumus)

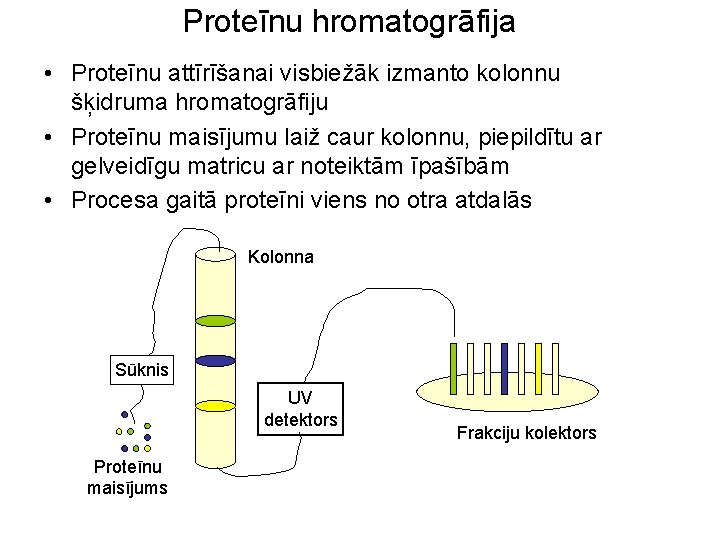
Proteīnu hromatogrāfija • Proteīnu attīrīšanai visbiežāk izmanto kolonnu šķidruma hromatogrāfiju • Proteīnu maisījumu laiž caur kolonnu, piepildītu ar gelveidīgu matricu ar noteiktām īpašībām • Procesa gaitā proteīni viens no otra atdalās Kolonna Sūknis UV detektors Proteīnu maisījums Frakciju kolektors

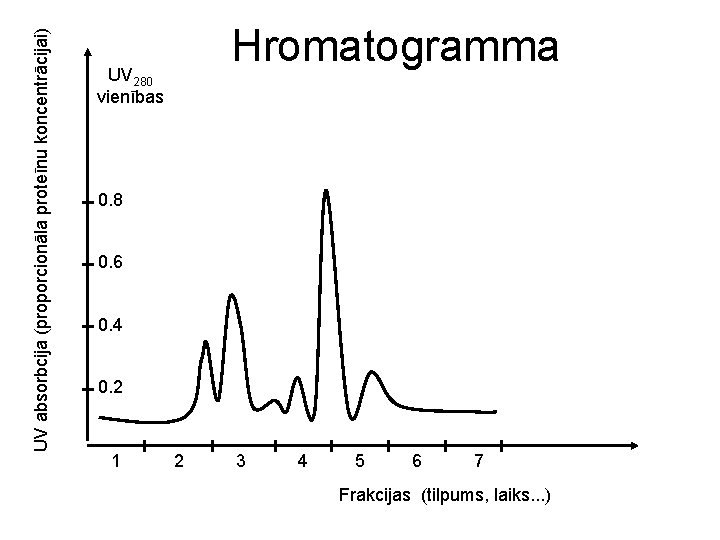
UV absorbcija (proporcionāla proteīnu koncentrācijai) Hromatogramma UV 280 vienības 0. 8 0. 6 0. 4 0. 2 1 2 3 4 5 6 7 Frakcijas (tilpums, laiks. . . )

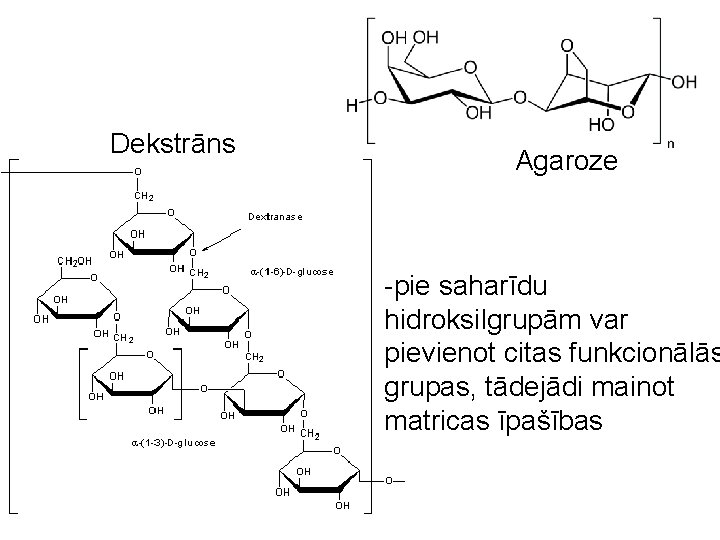
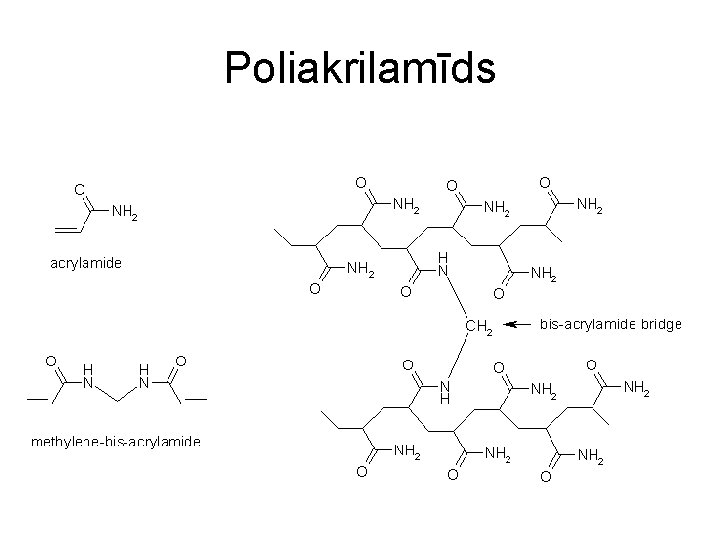
Kolonnas matricu materiāli - dekstrāni (sazaroti glikozes polimēri) - agaroze (galaktozes polimēri) - poliakrilamīds - jaukti agarozes – poliakrilamīda polimēri - pie saharīdu hidroksilgrupām var piešūt citas funkcionālās grupas, tādejādi mainot matricas īpašības

Dekstrāns Agaroze -pie saharīdu hidroksilgrupām var pievienot citas funkcionālās grupas, tādejādi mainot matricas īpašības

Poliakrilamīds

Kolonnas matricu veidi (pēc īpašībām) • • Gēlfiltrācijas (atdala pēc molekulu izmēra) Jonapmaiņas (atdala pēc molekulu lādiņa) Hidrofobās (atdala pēc molekulu šķīdības) Afinitātes (atdala pēc noteiktu proteīnu spējas piesaistīties citām molekulām)

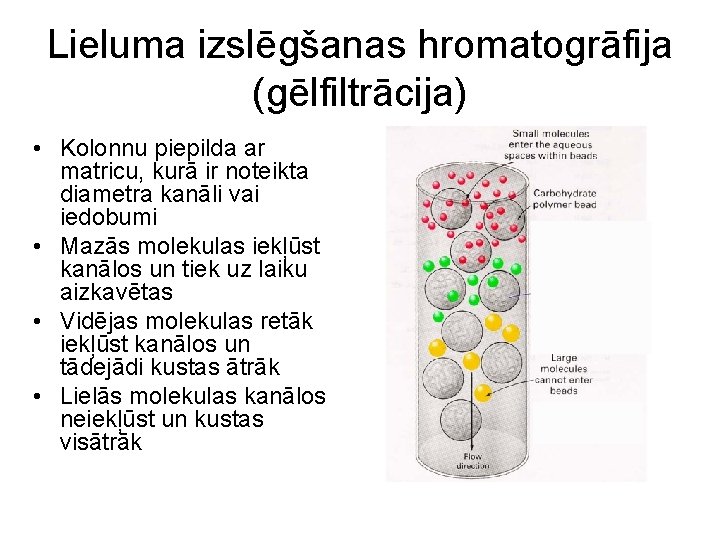
Lieluma izslēgšanas hromatogrāfija (gēlfiltrācija) • Kolonnu piepilda ar matricu, kurā ir noteikta diametra kanāli vai iedobumi • Mazās molekulas iekļūst kanālos un tiek uz laiku aizkavētas • Vidējas molekulas retāk iekļūst kanālos un tādejādi kustas ātrāk • Lielās molekulas kanālos neiekļūst un kustas visātrāk

Lieluma izslēgšanas hromatogrāfija (gēlfiltrācija) • No matricas materiāla veido lodītes ar noteiktu poru diametru • Atšķirīgi poru (kanālu) diametri ir piemēroti dažādu lielumu molekulu attīrīšanai

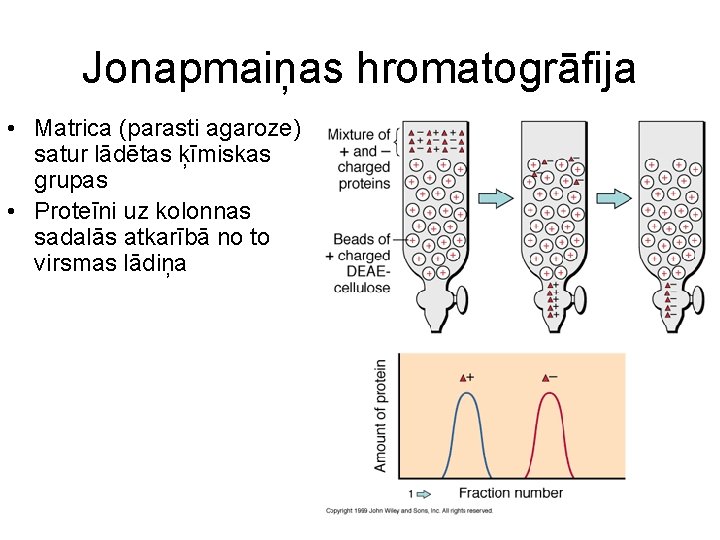
Jonapmaiņas hromatogrāfija • Matrica (parasti agaroze) satur lādētas ķīmiskas grupas • Proteīni uz kolonnas sadalās atkarībā no to virsmas lādiņa

Jonapmaiņas hromatogrāfija • Katjonapmaiņa: Matrica ir negatīvi lādēta piemēram S (Sulfo) un CM (Carboxymethyl) • Anjonapmaiņa Matrica ir pozitīvi lādēta, piem. Q (Quaternary ammonium) un DEAE (Diethylaminoethyl) • Eluēšana: Ar lineāri pieaugošu sāls gradientu, pamatojas uz konkurējošiem joniem • Lielākā daļa proteīnu ir negatīvi lādēti, tāpēc parasti izmanto anjonapmaiņu

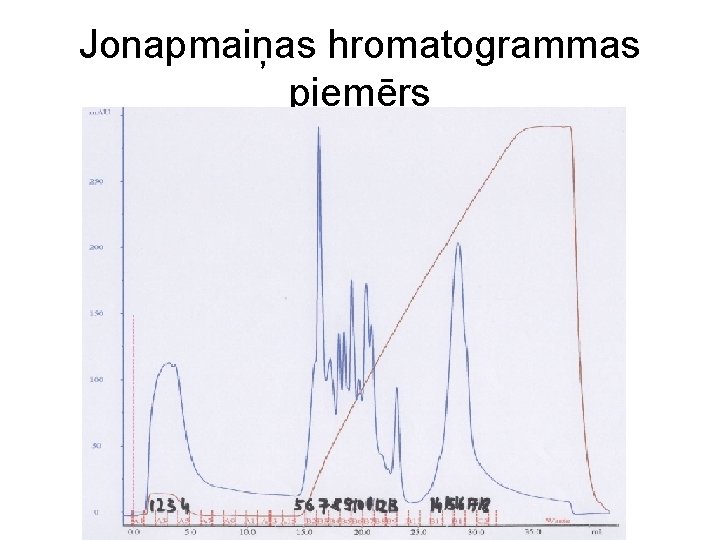
Jonapmaiņas hromatogrammas piemērs

Hidrofobā hromatogrāfija • Pamatojas uz hidrofobajām mijiedarbībām • Kolonnas matrica satur hidrofobas grupas (fenil-, butil-, oktil-, u. c. ) • Proteīnu hidrofobās aminoskābes mijiedarojas ar matriksa hidrofobajām grupām • Hidrofili proteīni kolonnā kustas ātrāk • Proteīnus uz kolonnas var adsorbēt augstā sāls koncentrācijā • Proteīnus pakāpeniski eluē ar samazinošos sāls koncentrācijas gradientu

Afinitātes hromatogrāfija • Pie matricas ir piesaistīts ligands, kurš saistās ar kādu noteiktu proteīnu • Ligands var būt: -metāla joni (Visvairāk izplatītā tehnika!) -antivielas pret noteiktu proteīnu -proteīns, kas saista noteiktu citu proteīnu -mazmolekulārs ligands, kas saista noteiktu proteīnu

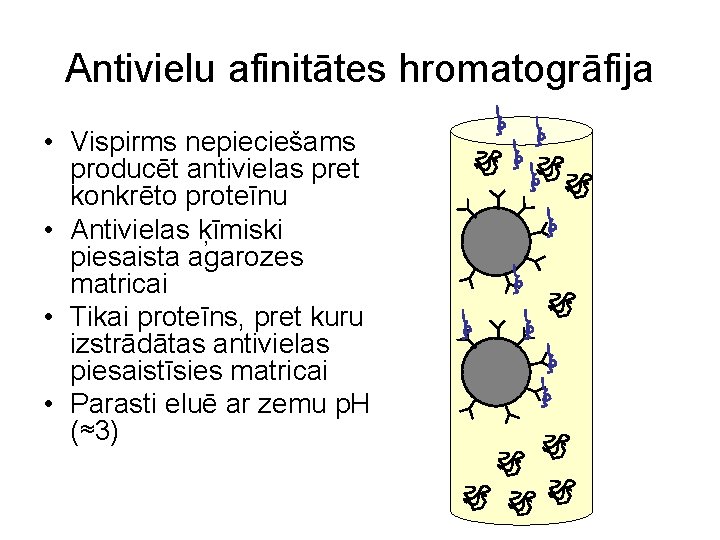
Antivielu afinitātes hromatogrāfija • Vispirms nepieciešams producēt antivielas pret konkrēto proteīnu • Antivielas ķīmiski piesaista agarozes matricai • Tikai proteīns, pret kuru izstrādātas antivielas piesaistīsies matricai • Parasti eluē ar zemu p. H (≈3)

Antivielu afinitātes hromatogrāfija • Priekšrocības: -Ļoti selektīva metode • Trūkumi: -nepieciešams producēt antivielas pret jau attīrītu proteīnu -dārgi -var būt grūtības eluēt proteīnu no kolonnas

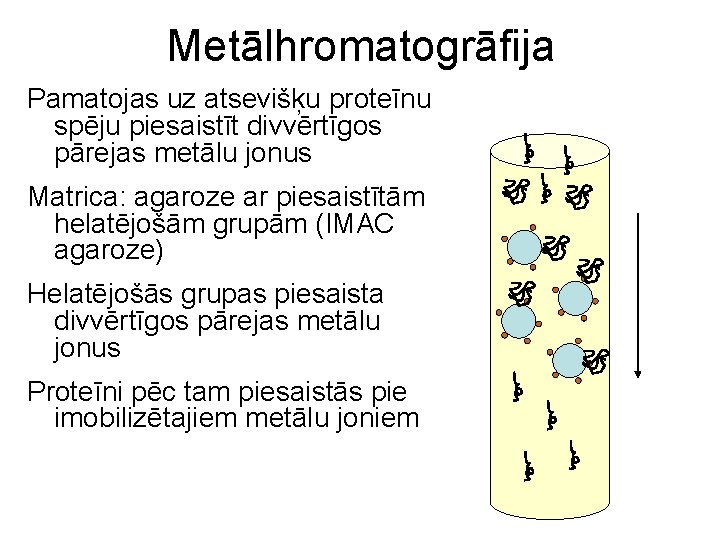
Metālhromatogrāfija Pamatojas uz atsevišķu proteīnu spēju piesaistīt divvērtīgos pārejas metālu jonus Matrica: agaroze ar piesaistītām helatējošām grupām (IMAC agaroze) Helatējošās grupas piesaista divvērtīgos pārejas metālu jonus Proteīni pēc tam piesaistās pie imobilizētajiem metālu joniem

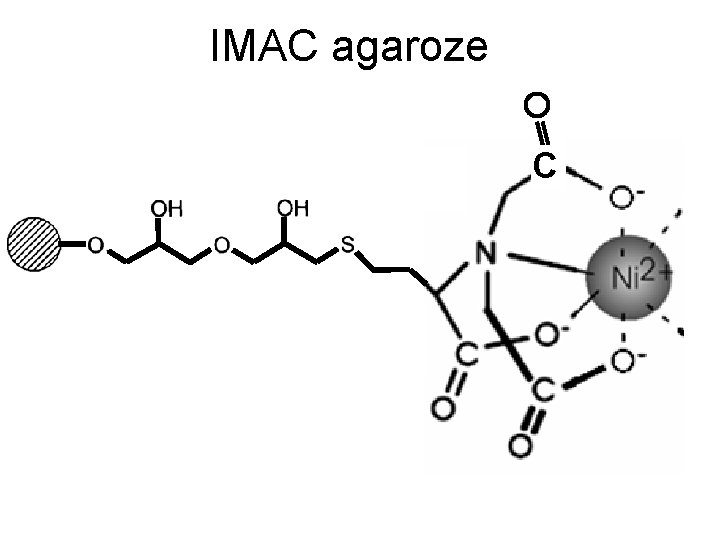
IMAC agaroze C

Kādi proteīni piesaista pārejas metālu jonus? • Tikai daži proteīnu veidi dabīgi spēj piesaistīt metāla jonus • Metāla jonus piesaistošas sekvences var ieviest mākslīgi • Parasti izmanto t. s. His-tag – 6 histidīnus pēc kārtas

His tag ieviešana proteīnos • Histidīnus ievieš mākslīgi ar gēnu inženierijas metodēm • Metodes trūkums: modificētais proteīns var būt neaktīvs • Var ieviest proteāžu saitus, lai pēc attīrīšanas His tag sekvenci varētu viegli atšķelt

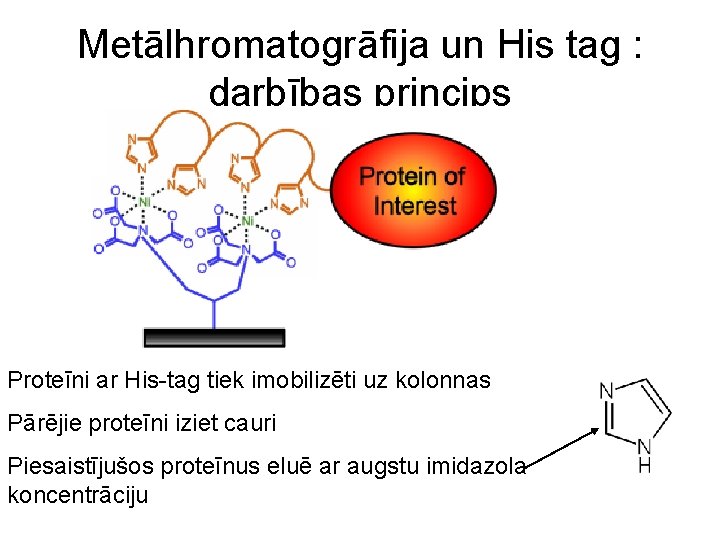
Metālhromatogrāfija un His tag : darbības princips Proteīni ar His-tag tiek imobilizēti uz kolonnas Pārējie proteīni iziet cauri Piesaistījušos proteīnus eluē ar augstu imidazola koncentrāciju

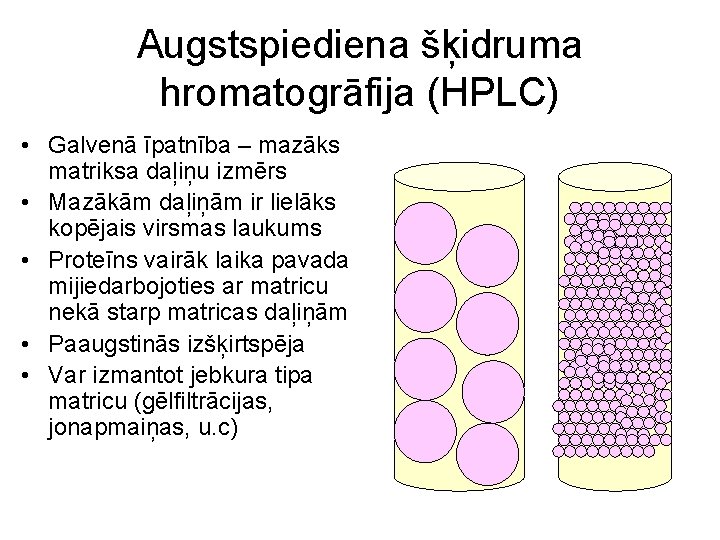
Augstspiediena šķidruma hromatogrāfija (HPLC) • Galvenā īpatnība – mazāks matriksa daļiņu izmērs • Mazākām daļiņām ir lielāks kopējais virsmas laukums • Proteīns vairāk laika pavada mijiedarbojoties ar matricu nekā starp matricas daļiņām • Paaugstinās izšķirtspēja • Var izmantot jebkura tipa matricu (gēlfiltrācijas, jonapmaiņas, u. c)

Kāpēc “augstspiediena” ? • Samazinoties matricas daļiņu izmēram, nepieciešams augstāks spiediens, lai šķīdums tecētu cauri kolonnai • Pieaugot daļiņu lineārajam izmēram, nepieciešamais spiediens pieaug kvadrātiski • 10 x mazākas daļiņas – 100 x lielāks spiediens • Spiediens var sasniegt vairākus simtus atmosfēru • HPLC kolonnas gatavo no tērauda vai bieza stikla

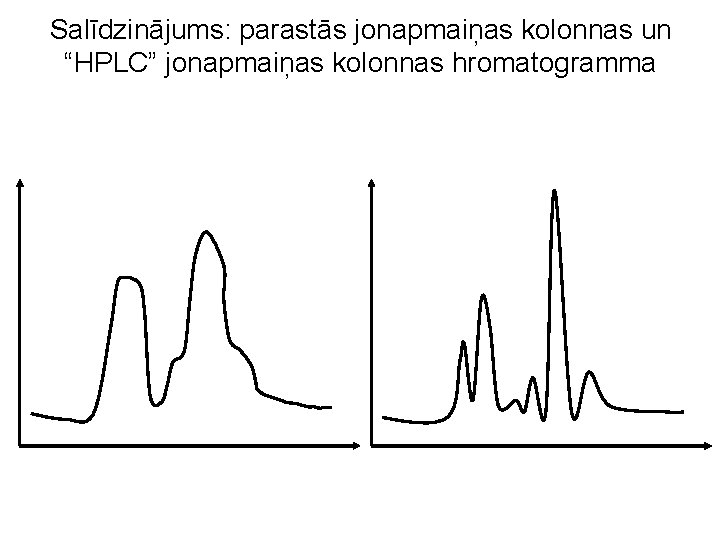
Salīdzinājums: parastās jonapmaiņas kolonnas un “HPLC” jonapmaiņas kolonnas hromatogramma

Proteīnu selektīva precipitēšana • Pamatojas uz dažādu proteīnu atšķirīgu hidrofobitāti – Organiskie precipitanti (piem. polietilēnglikols) – Neorganiskie precipitanti (piem. , amonija sulfāts) – Nav pārāk selektīva metode, var tik izmantota kā pirmais solis attīrīšanā – Efektīvāka, ja proteīns ir ļoti labi vai ļoti slikti šķīstošs

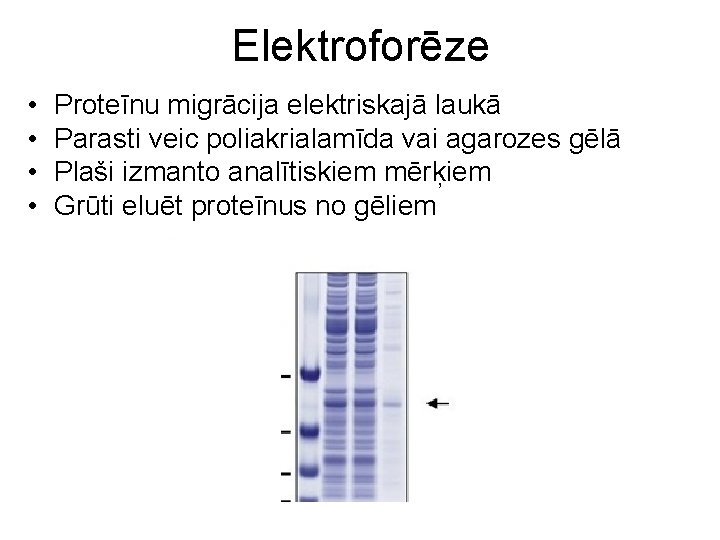
Elektroforēze • • Proteīnu migrācija elektriskajā laukā Parasti veic poliakrialamīda vai agarozes gēlā Plaši izmanto analītiskiem mērķiem Grūti eluēt proteīnus no gēliem

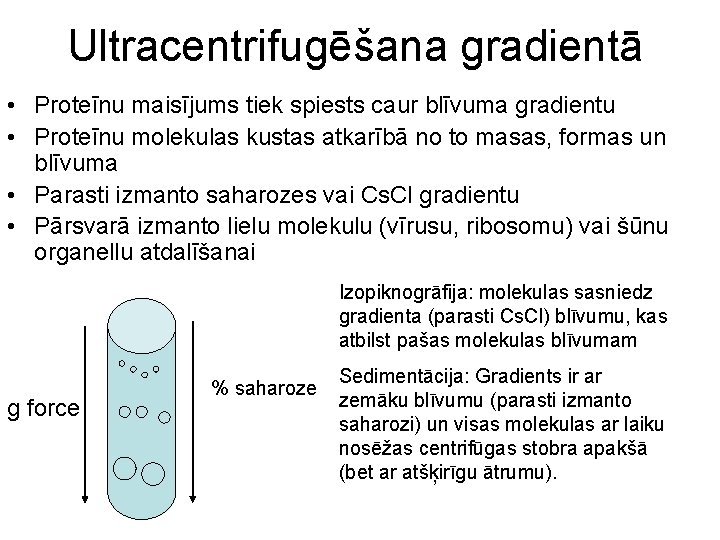
Ultracentrifugēšana gradientā • Proteīnu maisījums tiek spiests caur blīvuma gradientu • Proteīnu molekulas kustas atkarībā no to masas, formas un blīvuma • Parasti izmanto saharozes vai Cs. Cl gradientu • Pārsvarā izmanto lielu molekulu (vīrusu, ribosomu) vai šūnu organellu atdalīšanai Izopiknogrāfija: molekulas sasniedz gradienta (parasti Cs. Cl) blīvumu, kas atbilst pašas molekulas blīvumam g force % saharoze Sedimentācija: Gradients ir ar zemāku blīvumu (parasti izmanto saharozi) un visas molekulas ar laiku nosēžas centrifūgas stobra apakšā (bet ar atšķirīgu ātrumu).

Ultrafiltrēšana • Lieto filtru ar noteiktu poru izmēru, salīdzināmu ar makromolekulu izmēriem • Nav pārāk selektīva metode • Noderīga proteīnu koncentrēšanai un atsāļošanai

Siltuma izturība • Dažādiem proteīniem ir dažāda denaturēšanās temperatūra • Metode ir ļoti noderīga termostabilu proteīnu attīrīšanai • Piemērs: Thermus aquaticus DNS polimerāze, producēta E. coli -Karsē šūnu lizātu pie 80 o. C 15 min -Lielākā daļa E. coli proteīnu (ap 90 %) denaturēsies un izkritīs nogulsnēs

Kā uzzināt, kurā frakcijā ir attīrāmais proteīns? • Pēc pīķiem hromatogrammā • Pēc molmasas analītiskajā elektroforēzē • Detektēšana ar antivielām (proteīnuspecifiskām vai anti-His tag) • Proteīna enzimātiskā aktivitāte • Nav pārliecības? • Var veikt masas spektrometriju vai N–gala sekvenēšanu