Generiki lijekovi KLINIKA FARMAKOLOGIJA diplomski studij SESTRINSTVA Katedra















- Slides: 16

Generički lijekovi KLINIČKA FARMAKOLOGIJA diplomski studij SESTRINSTVA Katedra za farmakologiju Ana Marija Milat, mag. pharm.

Regulacija razvoja lijeka NAJBITNIJE SEP – Središnje etičko povjerenstvo u Hrvatskoj; odobrava sva klinička ispitivanja novih lijekova HALMED – Hrvatska agencija za lijekove i medicinske proizvode; odobrava lijekove za RH http: //www. halmed. hr/ HZZO – Hrvatski zavod za zdravstveno osiguranje; donosi A i B listu lijekova Ministarstvo zdravlja – donosi zakone

Regulacija razvoja lijeka NAJBITNIJE EMA – Europska agencija za lijekove; donosi rješenja o stavljanju lijekova na tržište centraliziranim postupkom http: //www. ema. europa. eu/ema/ FDA – Agencija za lijekove i hranu SAD-a WHO – Svjetska zdravstvena organizacija; donosi smjernice za uporabu lijekova, sabire dokaze iz 4. faze istraživanja, podupire razvoj lijekova za rijetke bolesti …

Regulacija razvoja lijeka NAJBITNIJE Lijek se može registrirati kao: -novi lijek -nova indikacija (off-label je uporaba lijeka u obliku ili svrsi u kojoj nije prethodno registriran) Nova formulacija NIJE novi lijek.

Regulacija razvoja lijeka NAJBITNIJE Novi lijek može biti: -značajno bolji od postojećeg (6 mjeseci do dobivanja odobrenja) -sličan lijekovima na tržištu (10 -12 mjeseci) -za liječenje karcinoma i bolesti koje ugrožavaju život (ubrzani postupak)

Regulacija razvoja lijeka NAJBITNIJE Generički lijek NIJE novi lijek – to je bioekvivalent postojećem originalnom lijeku kojemu je isteklo razdoblje ekskluzivnosti Razdoblje ekskluzivnosti je vrijeme u kojemu proizvođač originalnog lijeka jedini ima pravo na plasman (6 -14 godina, ovisno o državi) Patent je zaštita originalne formule ili proizvodnog postupka (uglavnom 20 godina)

The team of Croatian scientists in Pliva, Zagreb, Croatia, which discovered Sumamed in 1980: Gabrijela Kobrehel, Slobodan Đokić, Gorjana Radobolja-Lazarevski and dr. Zrinka Tamburašev.

Azitromicin (Sumamed) -jedan od najbolje prodavanih antibiotika u svijetu -najviše se koristi za infekcije srednjeg uha, streptokokne angine, upale pluća, bronhitise i sinuitise -otkriven 1980. godine, u Plivi, voditelj istraživačkog tima S. Đokić -istraživači dobili nagradu Američkog kemijskog društva “Heroes of Chemistry” 2000. godine -procjenjuje se da je Sumamed Plivi donosio 1, 5 miljardu $ godišnje, do isteka patenta 1999. godine -na hrvatskom tržištu danas postoji 11 generičkih kopija u 6 različitih formulacija -Hrvatska je tako postala jedna od 9 država sa svojim originalnim antibiotikom http: //www. croatia. org/crown/articles/10440/1/Azithromycin-or-Sumamed-one-of-worlds-best-selling-antibioticsproduct-of-Croatian-company-PLIVA-Zagreb. html

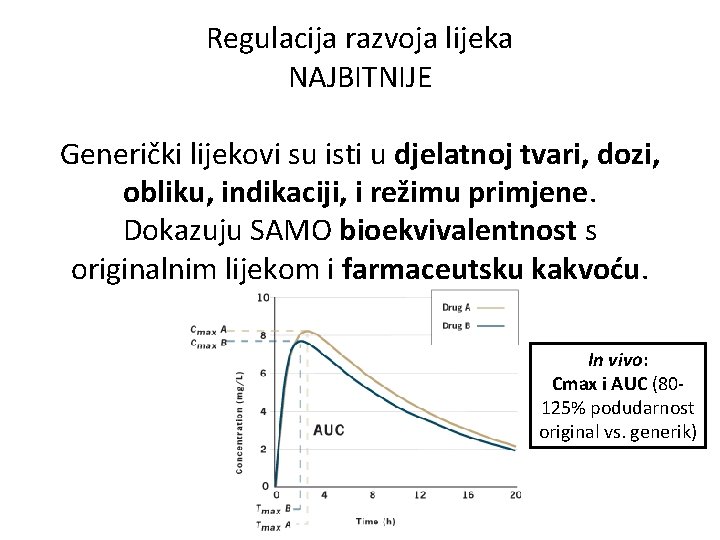
Regulacija razvoja lijeka NAJBITNIJE Generički lijekovi su isti u djelatnoj tvari, dozi, obliku, indikaciji, i režimu primjene. Dokazuju SAMO bioekvivalentnost s originalnim lijekom i farmaceutsku kakvoću. In vivo: Cmax i AUC (80125% podudarnost original vs. generik)

In vitro: Dissolution test “surogat” za ljudske studije

Regulacija razvoja lijeka NAJBITNIJE Generički lijekovi razlikovat će se u: -pomoćnim tvarima -cijeni -pacijentovoj suradljivosti (s obzirom na popularnost originalnog lijeka, povjerenje, naviku, oblik ili boju ambalaže i farmaceutskog spremnika…) Generička supstitucija je zamjena propisanog lijeka njegovim generikom zbog stanja zaliha ili cijene.

Regulacija razvoja lijeka NAJBITNIJE Bioslični lijekovi (engl. Biosimilars) su biološki “generički lijekovi”, skoro identični biološkom originalnom lijeku proizvedeni od drugog proizvođača. Razlike zbog kompleksnosti molekule tj. proizvodnog postupka i nemogućnosti razvoja lijeka iz identičnog biološkog soja (stanične banke, molekularnog klona). Ispituju se (iznova, skraćeno) sigurnost, čistoća i potentnost. Delta dozvoljena. Rijetka odobrenja. Manja cijena. “Generička” supstitucija nedozvoljena.

“On March 6, 2015, Sandoz’s filgrastim (trade name Zarxio), obtained the FDA's approval as a biosimilar to Amgen’s filgrastim (trade name Neupogen). Zarxio was approved as a first biosimilar, not as an interchangeable product, the FDA notes. ”

Regulacija razvoja lijeka NAJBITNIJE Kemijski naziv lijeka je naziv njegove glavne aktivne tvari (po IUPAC nomenklaturi) (2 R, 3 S, 4 R, 5 R, 8 R, 10 R, 11 R, 12 S, 13 S, 14 R)-2 -ethyl-3, 4, 10 -trihydroxy-3, 5, 6, 8, 10, 12, 14 -heptamethyl-15 -oxo- 11 -{[3, 4, 6 trideoxy-3 -(dimethylamino)-β-D-xylo-hexopyranosyl]oxy}-1 -oxa-6 -azacyclopentadec-13 -yl 2, 6 -dideoxy-3 -C-methyl-3 O-methyl-α-L-ribo-hexopyranoside INN (International Non-Property Name) međunarodni nezaštićeni naziv je generički naziv lijeka (pr. azitromicin) Trade Name – tvornički naziv je zaštićeni naziv lijeka (pr. Sumamed®) API (active product ingridient) – glavna aktivna tvar

Orphan drugs ili “lijekovi siročići” Rijetka bolest EU: 1 ili manje na 2 000 stanovnika; kronična, i s teškim posljedicama SAD: 1 ili manje na 1 500 stanovnika Problemi: mala populacija za istraživanje, nepoznati mehanizmi patofiziologije, cijena (ciljno tržište) POPIS EU http: //ec. europa. eu/health/documents/communityregister/html/alforphreg. htm http: //www. fda. gov/For. Industry/Developing. Productsfor. Rare. Diseases. Cond itions/ucm 2005525. htm

na tržištu postoje… Lijekovi na recept Bezreceptni lijekovi (BR, OTC) Bezreceptni lijekovi s dozvoljenom prodajom u specijaliziranim prodavaonicama (BRX) Biljni tradicionalni lijekovi Homeopatski pripravci Dodaci prehrani … i pripadajući regulatorni zakoni.
 Diplomski studij sestrinstva zadar
Diplomski studij sestrinstva zadar Sveučilište u zadru sestrinstvo
Sveučilište u zadru sestrinstvo Diplomski studij sestrinstva zadar
Diplomski studij sestrinstva zadar Porezni studij
Porezni studij Studij sestrinstva zagreb
Studij sestrinstva zagreb Generiki
Generiki Enterocela
Enterocela Uputa o pravnom lijeku
Uputa o pravnom lijeku Girvan
Girvan Kako napisati master rad
Kako napisati master rad Teme za diplomski rad informacione tehnologije
Teme za diplomski rad informacione tehnologije Brunkow metoda
Brunkow metoda Magisterij sestrinstva
Magisterij sestrinstva Povijest sestrinstva u svijetu
Povijest sestrinstva u svijetu Dipl ms
Dipl ms Poslijediplomski studij menadžment u zdravstvu
Poslijediplomski studij menadžment u zdravstvu Stručni i sveučilišni studij
Stručni i sveučilišni studij





























