FISIKA PENYELAMAN Hukum Boyle Hukum ini menyatakan bahwa

FISIKA PENYELAMAN

Hukum Boyle Hukum ini menyatakan bahwa dalam suhu yang tetap, besar suatu volume gas akan berbanding terbalik dengan tekanannya
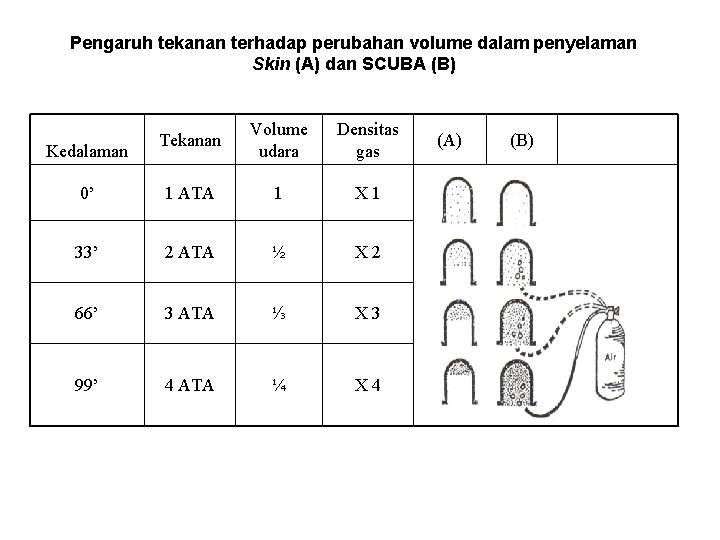
Pengaruh tekanan terhadap perubahan volume dalam penyelaman Skin (A) dan SCUBA (B) Tekanan Volume udara Densitas gas 0’ 1 ATA 1 X 1 33’ 2 ATA ½ X 2 66’ 3 ATA ⅓ X 3 99’ 4 ATA ¼ X 4 Kedalaman (A) (B)

misalkan volume paru adalah 6 liter. X menyelam SCUBA hingga kedalaman 30 m. . Apa yang terjadi bila dia menahan napas pada saat naik?

Dengan SCUBA, volume parunya tidak berubah. Bila ia menahan nafas kemudian naik ke permukaan maka seiring dengan berkurangnya tekanan terjadilah ke naikan volume sebesar 4 x, dan paru X mau tidak mau harus menjadi 6 x 4 = 24 liter. Bila rongga dadanya masih sanggup menahan ia akan selamat. Tetapi bila tidak maka akan terjadi pecahnya paru (over expansion lung). Hal ini tidak akan terjadi dalam penyelaman skin, karena pada penyelaman ini volume rongga udara dalam tubuh berubah sesuai dengan berubahnya tekanan

Hukum Dalton Hukum ini menyatakan bahwa; tekanan total gas dari suatu campuran gas sama dengan jumlah tekanan par sial gas penyusunnya. Hukum ini berhubungan dengan campuran gas dalam tabung selam yang digunakan dalam penyelaman SCUBA. Komposisi udara yang kita hirup secara umum terdiri dari 80% N 2 dan 20% O 2. Demikian pula halnya dengan komposisi udara dalam tabung SCUBA yang digunakan oleh penyelam
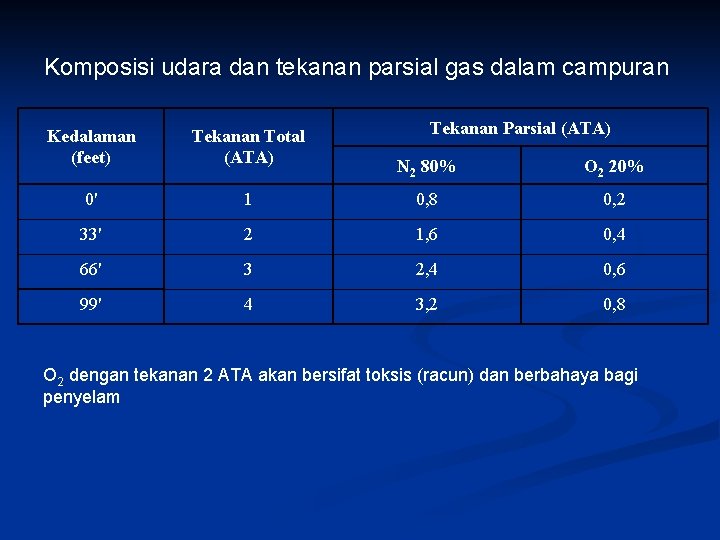
Komposisi udara dan tekanan parsial gas dalam campuran Kedalaman (feet) Tekanan Total (ATA) 0' Tekanan Parsial (ATA) N 2 80% O 2 20% 1 0, 8 0, 2 33' 2 1, 6 0, 4 66' 3 2, 4 0, 6 99' 4 3, 2 0, 8 O 2 dengan tekanan 2 ATA akan bersifat toksis (racun) dan berbahaya bagi penyelam

Pada kedalaman berapakah gas oksigen manjadi racun? ? Dengan komposisi gas seperti di atas maka tekanan 2 ATM bagi O 2 akan dicapai pada tekanan total 10 ATM atau pada kedalaman 90 m

Hukum Henry Hukum ini menyatakan bahwa jumlah gas yang dapat diserap oleh suatu cairan pada suhu tertentu berbanding lurus dengan tekanan parsial gas tersebut. Bila suatu cairan berada dalam kondisi tekanan tertentu maka jumlah gas yang diserap oleh cairan tersebut berbanding lurus dengan besarnya tekanan yang bekerja pada cairan tadi.


Hukum Charles Hukum ini menyatakan bahwa tekanan akan berubah seiring dengan perubahan temperatur. Semakin tinggi temperatur akan semakin besar pula tekanan, demikian pula sebaliknya.

- Slides: 12






















