Efni og efnatengi Heiti einfaldra efna 6 kafli








































- Slides: 54

Efni og efnatengi Heiti einfaldra efna 6. kafli

Upprifjun n Öll atóm leita eftir stöðugleika með því að. . ¨ Gefa ¨ Þiggja ¨ Deila n Rafeindum Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 2

Efni og efnatengi n Atóm efna haldast saman með tengjum í frumefnum og efnasamböndum og á milli sameinda ¨ rafkraftar á milli plús- og mínushleðslu Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 3

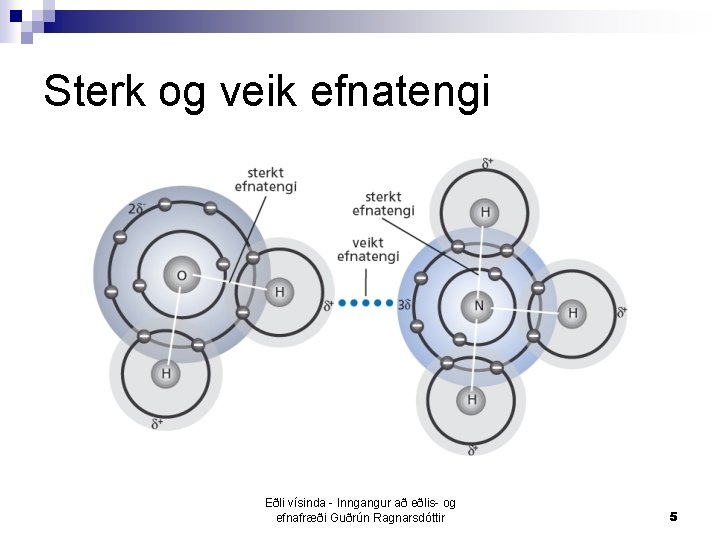
Efnatengi n Rafkraftarnir eru missterkir og flokkast efnatengi eftir þeim styrkleika ¨ Sterk efnatengi sem byggja á heilum hleðslum á milli atóma í frumefni eða efnasambandi n málmtengi, samgild tengi og jónatengi ¨ Veik efnatengi sem byggja á hlutahleðslum á milli sameinda n Van der Waals kraftar og vetnistengi Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 4

Sterk og veik efnatengi Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 5

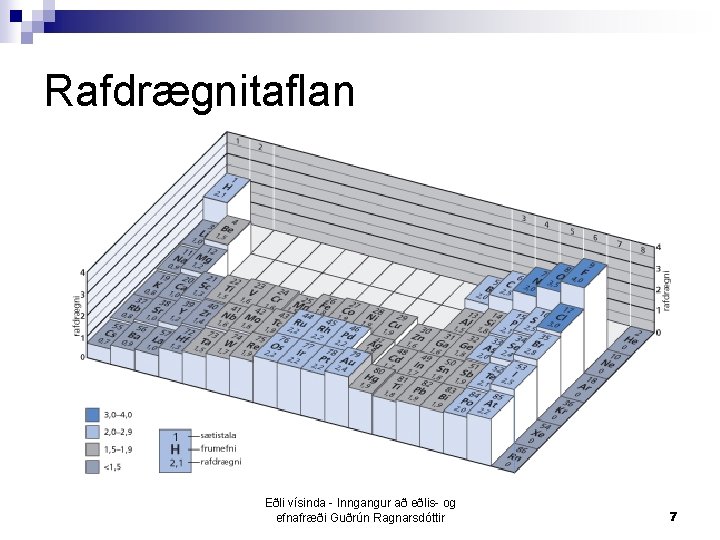
Rafdrægnitaflan Segir til um það hversu mikla tilhneigingu atóm hafa til þess að draga til sín rafeindir n Rafdrægni eykst frá vinstri til hægri og upp lotukerfið n Rafdrægnimismunur segir til um hvernig efnatengi er líklegast að atóm myndi þegar þau tengjast n ¨ Rafdrægnigildin eru dregin hvert frá öðru Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 6

Rafdrægnitaflan Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 7

Rafdrægnitaflan, rafdrægnimismunur og efnatengi Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 8

Efnatengi Mundu Dæmi Rafdrægnimismunur Jónatengi >1, 7 Skautað samgilt tengi 0, 1 -1, 7 Samgilt tengi <0, 1 Efnasamband Rafdrægnimismunur Efnatengi Na. Cl 3 -0, 9=2, 1 Jónatengi H 2 O 3, 5 -2, 1=1, 4 Skautað samgilt tengi O 2 2, 1 -2, 1=0, 0 Samgilt tengi Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 9

Efnatengi Mundu Fylltu inn í Efnasamband Rafdrægnimismunur Jónatengi >1, 7 Skautað samgilt tengi 0, 1 -1, 7 Samgilt tengi <0, 1 Efnatengi Na. Br H 2 S N 2 Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 10

Jónir myndast þegar atóm gefur frá sér eða tekur til sín rafeindir n n n Atómjónir n ¨ plús eða mínushlaðið atóm Plúsjón ¨ fleiri róteindir en rafeindir n ¨ Málmar ¨ Mg 2+ Mínusjón ¨ fleiri rafeindir en róteindir n ¨ Málmleysingjar ¨ O 2 - Sameindajónir ¨ plús eða mínushlaðin sameind Samanstanda af fleiri en einu atómi málmleysingja sem tengjast með samgildum tengjum Dæmi ¨ SO 42¨ NH 4+. Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 11

Rafeindaskipan Atóm, jónir og eðalgastegundir Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 12

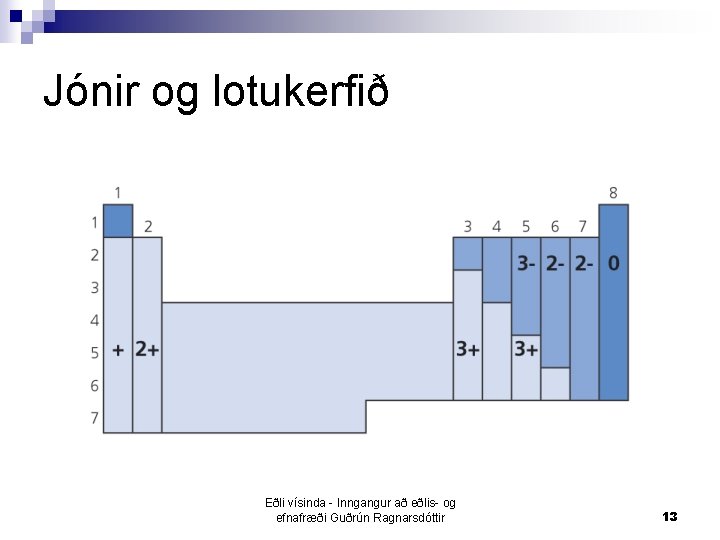
Jónir og lotukerfið Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 13

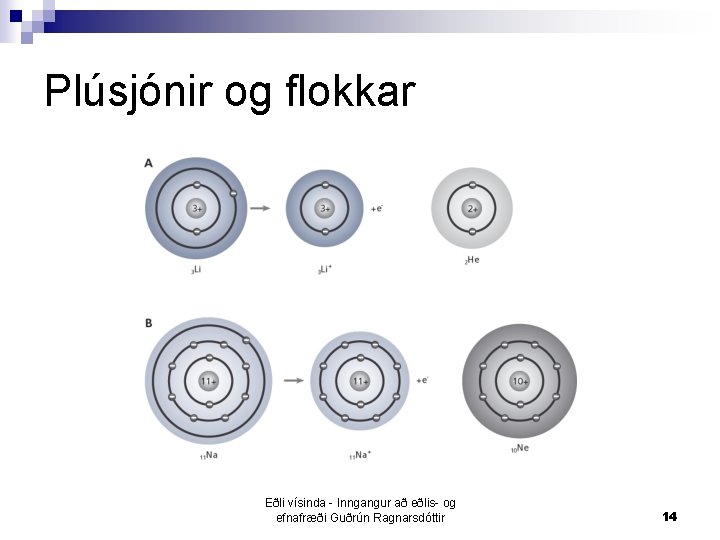
Plúsjónir og flokkar Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 14

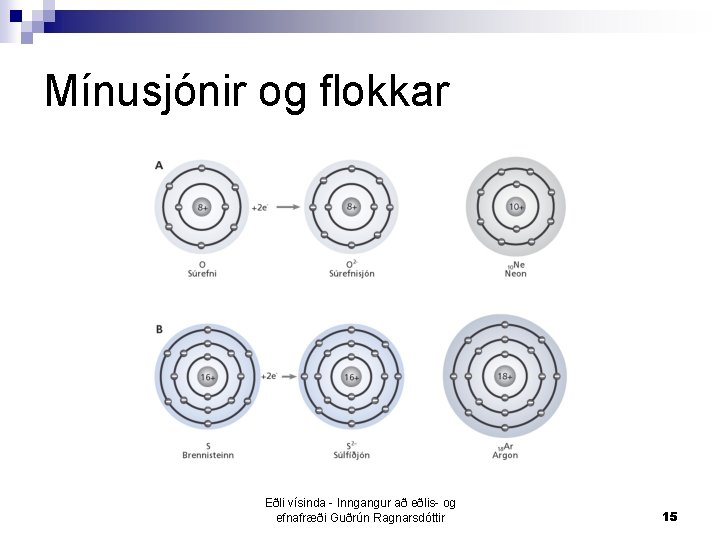
Mínusjónir og flokkar Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 15

Jónefni n Úr jónum málma og málmleysingja Plús- og mínushlaðini jón ¨ Rafeindaflutningur ¨ n n n Atóm málma með fáar gildisrafeindir gefa rafeindir til atóma málmleysingja með margar gildisrafeindir og uppfylla þá bæði atómin átturegluna Málmatómið fær þá plúshleðslu og atóm málmleysingjans fær mínushleðslu Plúsinn og mínusinn dragast hver að öðrum og jónefni myndast Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 16

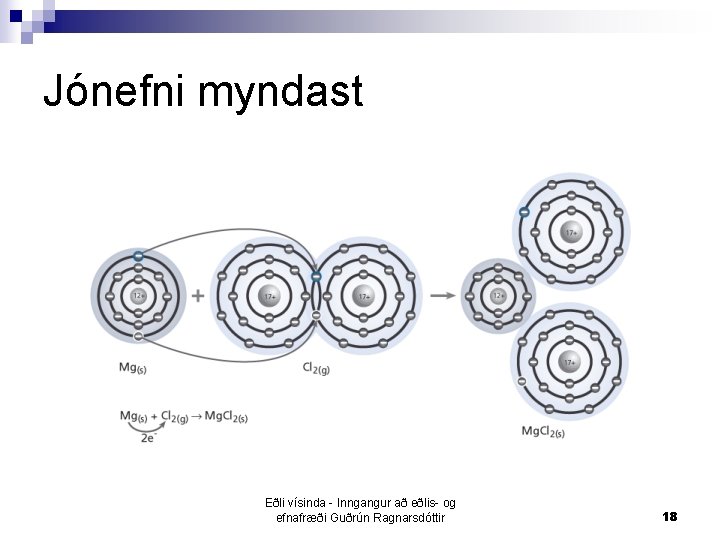
Jónatengi n Rafkraftar á milli plús- og mínusjóna + Málmleysingi Jónefni ¨ 2 Na(s) + Cl 2(g) 2 Na+ + 2 Cl- 2 Na. Cl(s) ¨ Málmur Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 17

Jónefni myndast Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 18

Jónakristall n n Úr jónefni sem gert er úr plús- og mínusjónum Jónirnar raða sér upp skipulega Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 19

Ritaðu stöðugasta form atómanna og segðu til um fjölda raf- og róteinda. Atóm Stöðugasta Fjöldi form róteinda Fjöldi rafeinda Na N Ca S Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 20

Sameind og samgild tengi Frumefni eða efnasambönd úr málmleysingjum n Samgild tengi halda atómunum saman n ¨ atómin deila með sér rafeindum, tengirafeindir ¨ tengirafeindirnar ferðast umhverfis atómin og rafkraftar verka á milli plúshleðslu kjarnans og mínushleðslu tengirafeindanna ¨ Samgild tengi eru ýmist skautuð eða óskautuð Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 21

Sameindaformúla Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 22

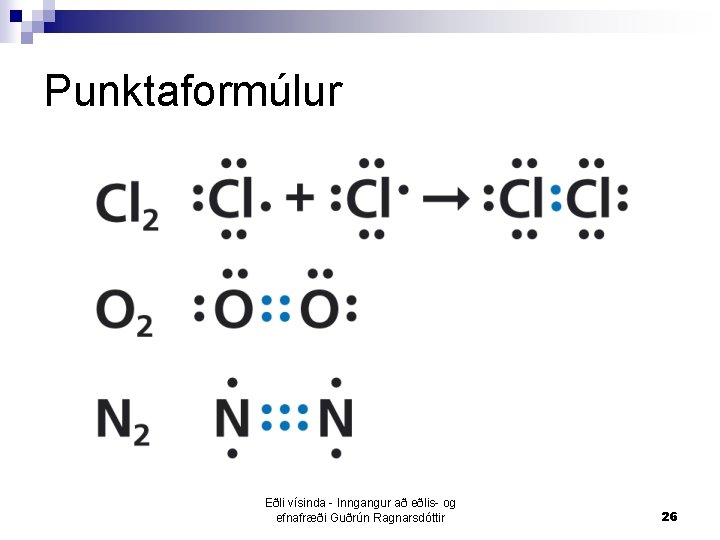
Punktaformúlur n n n Notaðir eru punktar til þess að lýsa samgildum tengjum Gildisrafeindir atóms eru ritaðir sem punktar umhverfis tiltekið atóm Þær tengirafeindir sem atóm deila eru ritaðar á milli atómanna = samgilda tengið Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 23

Punktaformúla kolefnisatóms Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 24

Punktaformúla flúrorsameindar, F 2 Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 25

Punktaformúlur Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 26

Byggingarformúlur Einfalda punktaformúlurnar n Rafeindapörin sem eru á milli atómanna táknaðar með striki. n ¨ Eintengi, eitt strik, eitt rafeindapar. ¨ Tvítengi, tvö strik, tvö rafeindapör. ¨ Þrítengi, þrjú strik, þrjú rafeindapör. Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 27

Byggingarformúlur Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 28

Punkta- og byggingarformúlur sameinda Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 29

Punkta og byggingarformúlur sameinda Lífræn efni Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 30

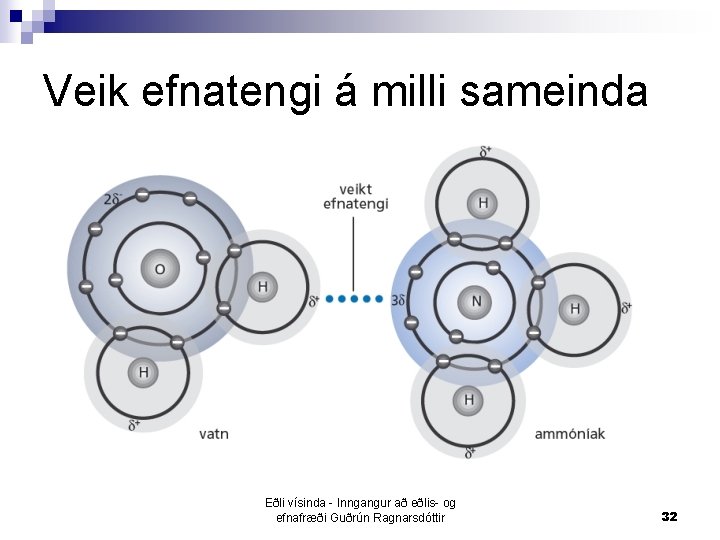
Veik efnatengi alltaf á milli sameinda n vara einungis í föstu og fljótandi formi n stafa af hlutahleðslum sem eru táknaðar með + eða n Vetnistengi eða Van der Waalskraftar n Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 31

Veik efnatengi á milli sameinda Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 32

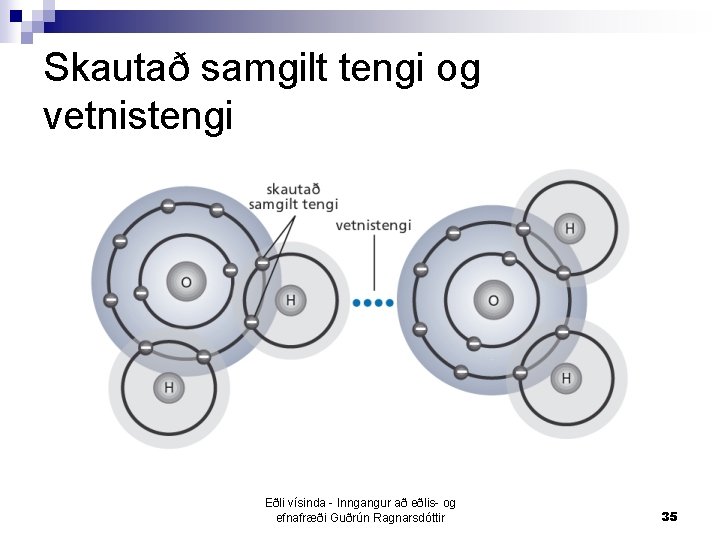
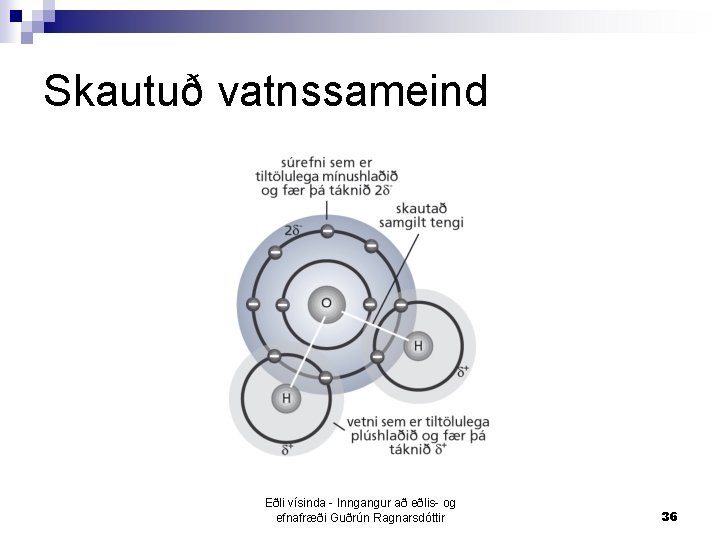
Skautað samgilt tengi n Tengirafeindir samgilda tengisins eru nær því atómi sem hefur hærra rafdrægnigildi ¨ það n atóm er frekara á tengirafeindirnar Við þetta dreifast rafeindirnar ekki jafnt um sameindina ¨ Skautuð n sameind Það atóm sem er með lægra rafdrægnigildi fær plús hlutahleðslu (frá kjarnanum) og rafdrægna atómið með hærra rafdrægnigildi fær mínus hlutahleðslu => hleðsluröskun verður innan sameindarinnar ¨ Sýnt með hlutahleðslunum + eða Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 33

Vetnistengi n Vetni verður að vera í sameind ásamt mjög rafneikvæðu atómi (O, N, F og Cl) ¨ Skautað samgilt tengi með rafdrægnimismuninn, 0, 1 -1, 7 ¨ Ójöfn hleðsludreifing innan sameindarinnar sem leiðir til þess að sameindin verður skautuð Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 34

Skautað samgilt tengi og vetnistengi Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 35

Skautuð vatnssameind Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 36

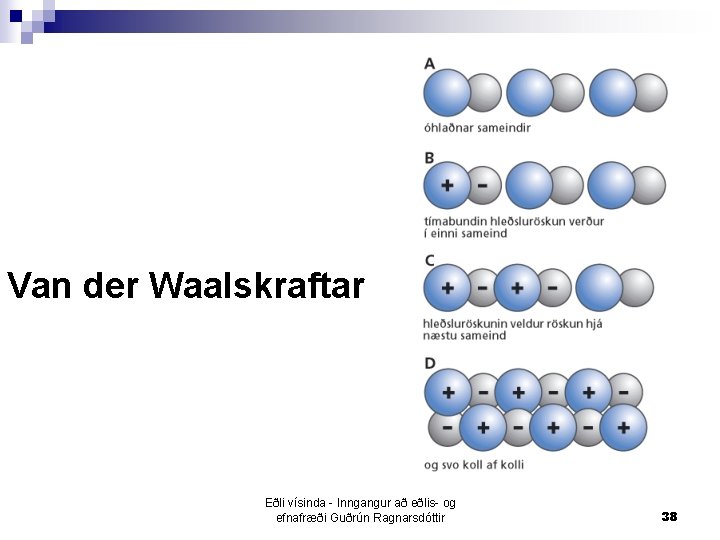
Van der Waalskraftar n Stafa af tímabundinni hleðslu á milli sameinda í sameindaefni í föstu og fljótandi formi ef sameindin inniheldur ekki vetni ¨ hleðsluröskun n innan sameindarinnar hluti hennar fær plúshleðslu og hinn hlutinn mínushleðslu. ¨ Skautaða sameindin skapar rafsvið í kringum sig og veldur skautun í nálægri sameind og þannig koll af kolli. ¨ Plúshleðslan í annarri sameindinni dregst svo að mínushleðslunni í hinni sameindinni og rafkraftarnir vara í skamman tíma Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 37

Van der Waalskraftar Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 38

Efni og efnatengi Rafdrægni- Veikt efnatengi á milli mismunur sameinda Jónefni og jónatengi Sameind og skautað samgilt tengi Sameind og samgilt tengi >1, 7 Ekkert 0, 1 -1, 7 Vetnistengi (ef H er í sameind) annars Van der Waals kraftar <0, 1 Van der Waals kraftar Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 39

Málmar Úr málmatómum sem mynda málmkristal n Í málmkristal raða málmatómin sér upp í skipulega byggingu. n Málmatómin haldast saman með málmtengjum. n ¨ Tengið byggir á rafkröftum á milli mínushleðslu, laustbundinna gildisrafeinda sem eru á fleygiferð umhverfis plúshleðslu málmjónanna í málmkristalnum. Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 40

Málmtengi Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 41

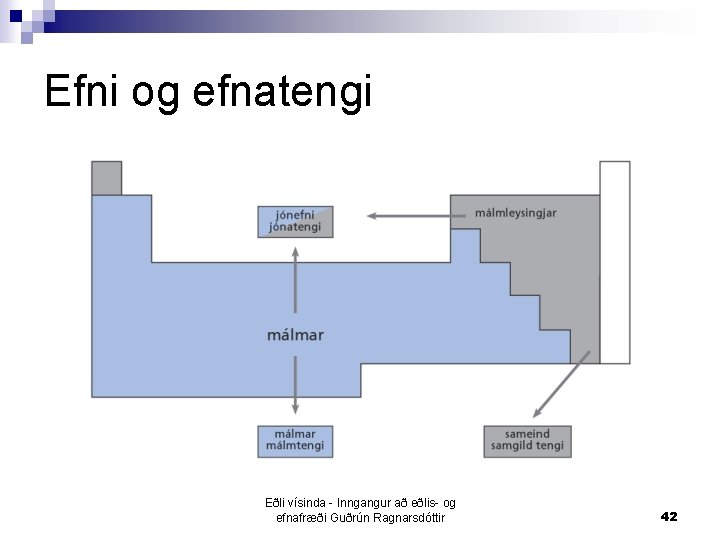
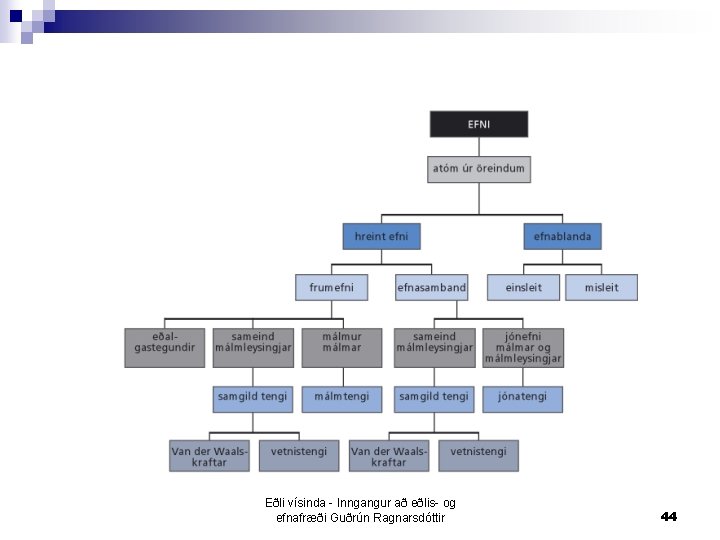
Efni og efnatengi Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 42

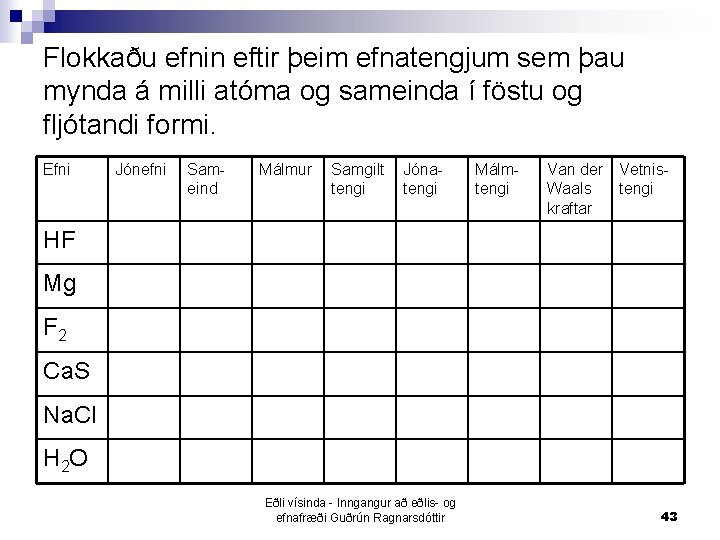
Flokkaðu efnin eftir þeim efnatengjum sem þau mynda á milli atóma og sameinda í föstu og fljótandi formi. Efni Jónefni Sameind Málmur Samgilt tengi Jónatengi Málmtengi Van der Waals kraftar Vetnistengi HF Mg F 2 Ca. S Na. Cl H 2 O Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 43

Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 44

HEITI TVÍEFNA OG FORMÚLUR ÞEIRRA Tvíefni er efnasamband samsett úr tveimur ólíkum atómum eða jónum (atóm- og/eða sameindajónum). n Nafngiftir fara eftir því hvort um er að ræða sameind eða jónefni. n Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 45

Jónefni og formúlur n Eftirfarandi reglur ber að hafa í huga þegar formúlur jónefna eru ritaðar: ¨ Plúsjónin er alltaf rituð á undan. ¨ Jafna verður upp hleðsluójafnvægi ¨ Ef um sameindajón er að ræða ber að rita sviga utan um alla sameindajónina ef hún er margfölduð upp ¨ Ekki skal rita sviga nema þegar sameindajónir eru margfaldaðar upp. Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 46

Jónefni og heiti n n Nafn plúsjónarinnar er alltaf ritað á undan. Nota heiti jónanna og styðjast þar við jónatöfluna. Ef jón hefur fleiri en eina hleðslu ber að sýna með rómverskum tölustöfum hleðslu jónanna Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 47

Jónataflan Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 48

Formúlur jónefna Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 49

Fylltu inn í töfluna fyrir jónefni Heiti Natríumklóríð Kalsíumklóríð Járn(III)oxíð Kalsíumnítrat Formúla Fe. O Cu 2 O Blý(IV)súlfat Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 50

Sameindir og nafnakerfið n Notuð grísk forskeyti (notuð framan við heiti) sem vísa til fjölda atóma tiltekins frumefnis í sameindinni. ¨ Nota skal forskeytin mónó-(1), dí-(2), trí-(3), tetra-(4), penta-(5) og hexa-(6) fyrir framan heitin. ¨ Forskeytið mónó- er aldrei notað í byrjun heitis. Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 51

Forskeyti og viðskeyti málmleysingja Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 52

Dæmi um formúlu og heiti sameinda Sameind Heiti NO Niturmónoxíð N 2 O Díniturmónoxíð N 3 O 2 Tríniturdíoxíð NO 2 niturdíoxíð Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 53

Fylltu inn í töfluna fyrir sameindir Formúla Heiti PO P 2 O Trífosfórdíoxíð Eðli vísinda - Inngangur að eðlis- og efnafræði Guðrún Ragnarsdóttir 54