ZDRAVOTNICK PROSTEDKY OSOBN OCHRANN PROSTEDKY A NOTIFIKOVAN OSOBA

ZDRAVOTNICKÉ PROSTŘEDKY, OSOBNÍ OCHRANNÉ PROSTŘEDKY A NOTIFIKOVANÁ OSOBA ITC 08. 09. 2020

INSTITUT PRO TESTOVÁNÍ A CERTIFIKACI, a. s. Institut pro testování a certifikaci, a. s. je česká nezávislá společnost poskytující služby v oblasti testování, certifikace kvality a bezpečnosti výrobků, metrologie, certifikace systémů managementu, v oblasti technické normalizace a vzdělávání.
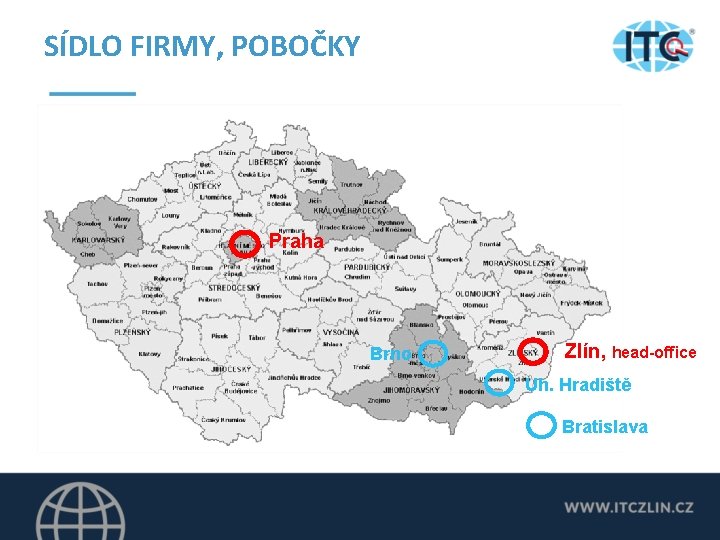
SÍDLO FIRMY, POBOČKY Praha Brno Zlín, head-office Uh. Hradiště Bratislava
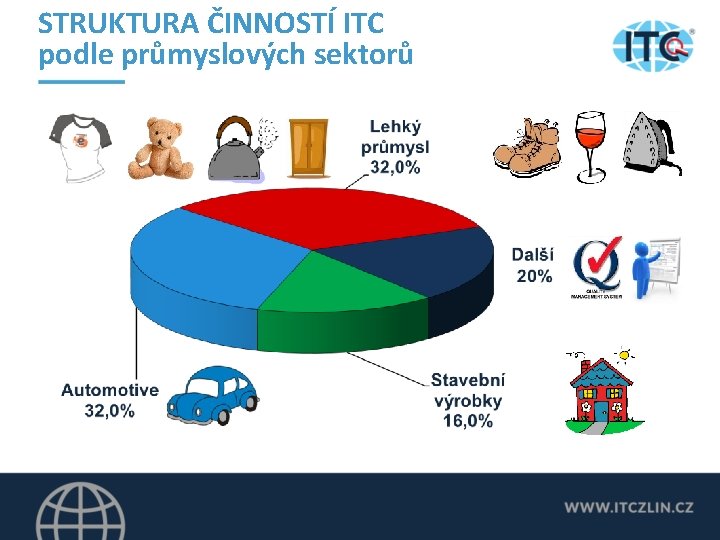
STRUKTURA ČINNOSTÍ ITC podle průmyslových sektorů

POSUZOVÁNÍ SHODY - ZNAČENÍ CE Notifikovaná osoba/Oznámený subjekt hračky osobní ochranné prostředky stavební výrobky zdravotnické prostředky diagnostické zdrav. prostředky in vitro elektromagnetická kompatibilita tlakové nádoby (pouze tlakové hrnce) Směrnice 2009/48/EC Nařízení 2016/425 Nařízení 305/2011 Směrnice 93/42/EEC Směrnice 98/79/EC Směrnice 2014/14/EU Směrnice 2014/68/EU

AKTUÁLNÍ STAV – ITC A MDD Ø ITC jako notifikovaná osoba bere své postavení a odpovědnost v systému posuzování shody (a to nejen v oblasti zdravotnických prostředků) velmi vážně. ITC velmi citlivě a intenzivně vnímá potřebu zvyšování nároků na posuzování shody, včetně zvyšování nároků na odbornou a technickou způsobilost. Naším zájmem je a nadále bude, zejména bezpečnost výrobků uváděných a uvedených na trh (v případě zdravotnických prostředků vždy s důrazem na bezpečnost evropských pacientů).

AKTUÁLNÍ STAV – ITC A MDD Ø ITC jako notifikovaná osoba v oblasti zdravotnických prostředků dosáhla ve společném zájmu - bezpečnosti zdravotnických prostředků a evropských pacientů - velkého progresu v kvalitě posuzování shody zdravotnických prostředků a současně ve zvyšování úrovně odpovědnosti výrobců zdravotnických prostředků. Je také zřejmé, že ITC jako notifikovaná osoba byla a je schopna odpovídajícím způsobem reagovat na požadavky bezpečnosti zdravotnických prostředků neboť přes přísné podmínky dozoru a kontrol provádění posuzování nebyl doposud identifikován případ, kdy by ITC vydal certifikát nebezpečný pro zdravotnický prostředek resp. nebezpečný pro zdraví pacientů.

AKTUÁLNÍ STAV – ITC A MDD Ø Počet platných certifikátů: ü Celkem 130 (z toho je 35 certifikátů ES přezkoumání návrhu, které jsou komplementární k certifikátům systému kvality jeden výrobek třídy III musí mít 2 certifikáty tedy 95 certifikačních řízení). ü Celkem 86 výrobců Øz toho je 48 výrobců EU+EFTA (56 %) a z toho je 40 výrobců z ČR + SR (47 %) Øz toho 38 třetí země (44%)

Scope ITC v MDD – souhrn neaktivních ZP Neaktivní neimplantabilní ZP Ø Ø ZP pro intenzivní péči, anestezii, transfuze, dialýzu Oftalmologické prostředky Nástroje, ZP s měřicí funkcí Sterilizační, čisticí a desinfekční prostředky pro ZP Neaktivní implantabilní Ø Ortopedické a funkční implantáty Ø Implantáty měkkých tkání ý NE – prsní implantáty, kardiovaskulární implantáty Prostředky na ošetření ran Ø Obvazy, prostředky na krytí ran, s léčivy i bez nich, oplachy na rány Ø Chirurgické šicí materiály a svorky Stomatologické prostředky Ø Stomatologické materiály, dentální implantáty, nástroje

Scope ITC v MDD – souhrn aktivních ZP Všeobecné aktivní ZP Ø Ø ý ZP pro mimotělní oběh, infúzi a hemaferezi, anestézii, kyslíkovou terapii Rozvody medicinálních plynů a jejich díly Sterilizátory Software NE – ZP pro asistovanou reprodukci ART a in-vitro oplodňování IVF Zobrazovací a monitorovací prostředky Ø Zobrazovací prostředky využívající neionizující záření Ø Zobrazovací prostředky využívající ionizující záření Ø Prostředky monitorující životně důležité funkce Terapeutické prostředky Ø Terapeutické ZP využívající neionizující záření Ø ZP pro hypotermii/hypertermii ý NE – terapeutické prostředky využívající ionizující záření, litotrypse

AKTUÁLNÍ STAV – ITC A MDD – OPĚTOVNÝ PŘEZKUM CERTIFIKÁTŮ NA ŽÁDOST EK V období 2018 – 2019 ITC plně vyhověl požadavku EK na provedení urgentního přezkoumání kompletní technické dokumentace k certifikátům zařazeným mezi nejrizikovějších skupin (tzn. s důrazem na požadavek EK aplikovat při sestavení plánu přezkumů „a risk based approach“ Celkem bylo v tomto období přezkoumáno: ü všech 33 certifikátů CN/NB, ZP tř. III ü 30 certifikátů QS/NB, ZP tř. IIb ve skupině „IIb implantabilní“, která zahrnuje nejrizikovější zdravotnické prostředky z tř. IIb. ü všech 7 certifikátů QS/NB ZP borderline

AKTUÁLNÍ STAV – ITC A MDD - OPĚTOVNÝ PŘEZKUM CERTIFIKÁTŮ NA ŽÁDOST EK ü Přezkumy všech plánovaných certifikátů byly provedeny v plánovaném časovém intervalu. ü Výrobci na zjištění identifikovaná ITC reagují a pracovníci ITC tato nápravná opatření kontrolují a vyhodnocují. ü Tento proces běží standardním způsobem. ü Na veškeré obdržené připomínky ÚNMZ pracovníci ITC reagovali, vypracovali analýzu příčiny apod. a přijali adekvátní nápravná a preventivní opatření. ü Nálezy v oblasti CAPA jsou s výrobci komunikovány a celý proces běží stejným způsobem jako přezkumy certifikátů.

AKTUÁLNÍ STAV MDD/MDR – ÚVOD DO PROBLÉMU/PŘECHODNÉ OBDOBÍ Platnost směrnice MDD měla skončit dnem 26. května 2020 – měla být zrušena Nařízením (EU) č. 2017/745 (dále jen „MDR“). V souvislosti s pandemií COVID-19 bylo přijato Nařízení (EU) č. 2020/561, jehož účelem bylo o jeden rok odložit použitelnost těch ustanovení nařízení MDR, která by se jinak začala používat ode dne 26. května 2020, včetně ustanovení, kterým by byla směrnice MDD zrušena. V souvislosti s pandemií COVID-19 přijatým Nařízením (EU) č. 2020/561 bylo přijato Nařízení (EU) č. 2020/666, kterým se mění prováděcí nařízení (EU) č. 920/2013, pokud jde o prodloužení platnosti jmenování oznámených subjektů, dohled nad nimi a jejich monitorování.

ITC A MDR Datum podání žádosti ITC o MDR: 12. 2019 Doba trvání řízení o žádosti (joint assessment +„notifikace“ dle MDR): min. 18 měsíců Předpokládaný scope ITC dle MDR je stanoven na základě vlastního posouzení odborné, personální a technické způsobilosti, založené na oboru VŠ vzdělání, praxi v oboru, zkušenostech s podobnými typy výrobků a kapacitě ITC.

Navrhovaný MDR scope – souhrn aktivních ZP Aktivní ZP pro zobrazování, monitorování a diagnostiku Zobrazovací prostředky využívající ionizující i neionizující záření Monitorovací a diagnostické ZP ý NE – aktivní implantabilní ZP Aktivní neimplantabilní terapeutické prostředky Terapeutické prostředky využívající neionizující záření Prostředky pro mimotělní oběh, podávání látek, hemaferézu Prostředky pro ORL, oftalmologické, chirurgické a dentální, ZP pro péči o rány a kůži Software Systémy pro dodávky medicinálních plynů Prostředky pro sterilizaci, desinfekci, čištění ý NE – terapeutické prostředky využívající ionizující záření

Navrhovaný MDR scope – souhrn neaktivních ZP Neaktivní implantabilní Osteo- a ortopedické a dentální implantáty Kardiovaskulární implantáty Implantáty měkkých tkání ý NE – prsní implantáty Neaktivní neimplantabilní ZP ZP pro intenzivní péči, anestezii, transfuze, dialýzu Oftalmologické prostředky Prostředky pro péči o rány a o kůži Sterilizační, čisticí a desinfekční prostředky pro ZP Dentální materiály Nástroje včetně chirurgických nástrojů pro opakované použití Neaktivní neimplantabilní antikoncepční prostředky Neaktivní diagnostické prostředky

AKTUÁLNÍ STAV MDD/MDR – ÚVOD DO PROBLÉMU/PŘECHODNÉ OBDOBÍ Ø MDR klade na výrobce a jejich zdravotnické prostředky podstatně přísnější požadavky, zejména v oblasti klinických zkoušek a klinického hodnocení, jejichž splnění si vyžádá značný čas, nehledě na personální náročnost. Aby byl zajištěn hladký přechod na novou legislativu a omezilo se riziko nedostupnosti některých zdravotnických prostředků, stanoví článek 120 MDR přechodné období trvající od vstupu MDR v účinnost do 26. 5. 2024.

AKTUÁLNÍ STAV MDD/MDR – ÚVOD DO PROBLÉMU/PŘECHODNÉ OBDOBÍ Ø Během přechodného období jsou výrobci oprávněni uvádět na trh zdravotnické prostředky pokryté platným certifikátem vydaným podle předchozí legislativy MDD za předpokladu, že budou splněny podmínky: • výrobci uvedou do souladu s MDR své postupy týkající se sledování po uvedení na trh, vigilance a registrace výrobců a prostředků, • nedojde k podstatným změnám v konstrukci a určeném účelu certifikovaného zdravotnického prostředku, • výrobci budou předmětem dozoru, který bude provádět vydavatel certifikátu.

AKTUÁLNÍ STAV MDD/MDR – ÚVOD DO PROBLÉMU/PŘECHODNÉ OBDOBÍ Ø Notifikovaná osoba (Oznámený subjekt), která vydala certifikát podle MDD, bude provádět odpovídající dozor po celou dobu přechodného období, bez ohledu na skutečnost, že dnem 26. května 2021 pozbývá platnosti jakékoliv oznámení (notifikace) podle směrnice MDD. • Na základě pokynů z evropské koordinace notifikovaných osob vyvstane nejpozději v průběhu 1 Q 2021 nutnost uzavření smluv mezi notifikovanou osobou, která vydala dozorovaný certifikát, a výrobcem ZP. • Účelem smluv na provádění dozorů je zajistit po celou dobu platnosti vydaných certifikátů (nejdéle však do konce přechodného období) řádné plnění podmínek dle předchozího snímku a umožnit v případě zjištění neshod také pozastavení nebo zrušení vydaného certifikátu.

AKTUÁLNÍ STAV MDD/MDR – ÚVOD DO PROBLÉMU/PŘECHODNÉ OBDOBÍ Ø Jediným subjektem oprávněným k dozoru je podle MDR notifikovaná osoba, která daný certifikát v souladu s MDD vydala, a ta nemůže být nahrazena jakoukoliv jinou osobou ani institucí. Ø Dozor nad „notifikovanými osobami“ dle MDD, provádí po dobu přechodného období dle MDR příslušná národní autorita. Ø Výrobci většinou na ustanovení o přechodném období spoléhají (a to i s ohledem na stav přípravy prováděcích předpisů a počet a stav posuzování notifikovaných osob Komisí dle nařízení MDR – zatím dle MDR pouze 16!) a předpokládají, že do května roku 2024 budou schopni naplnit nové požadavky úpravou postupů a technické dokumentace.
AKTUÁLNÍ STAV - MDR (RIZIKA) Počet notifikovaných osob dle MDR ke dni 04. 09. 2020: 16

AKTUÁLNÍ STAV - MDR (RIZIKA) Počet notifikovaných osob dle MDD ke dni 04. 09. 2020: 54

AKTUÁLNÍ STAV - MDR (RIZIKA) J Máme sice Nařízení, ale chybí prováděcí předpisy (implementační nařízení a delegované akty v přenesené pravomoci). MDR ukládá Komisi, pověřuje ji či zmocňuje k vydání prováděcích aktů celkem v 70 případech (někdy se překrývajících), z toho ve 30 případech jde o mandatorní požadavky, ve 40 případech záleží na Komisi, zda svou pravomoc uplatní. K dnešnímu dni vydáno pouze 5 předpisů (NANDO kódy pro MD a IVD, pravidla činnosti odborných skupin podle čl. 106 a jmenování vydávajících subjektů pro přidělování kódů UDI, Pokyn 2020/C 259/02 Komise pro odborné skupiny v oblasti ZP o jednotném výkladu kritérií pro rozhodování v konzultačním postupu v oblasti klinického hodnocení, Prováděcí Nařízení Komise (EU) 2020/1207 ze dne 19. srpna 2020, kterým se stanoví pravidla pro uplatňování nařízení Evropského parlamentu a Rady (EU) 2017/745, pokud jde o společné specifikace pro obnovu prostředků pro jedno použití - tento předpis však není pro ČR relevantní, neboť u nás je reprocesing jednorázových ZP zakázán) a 2 corrigenda.

AKTUÁLNÍ STAV - MDR (RIZIKA) J Další 3 úkoly Komise splnila bez nutnosti vydávat zvláštní předpis (aktualizace informací v NANDO databázi, zajištění koordinace notifikovaných osob, podpora spolupráce mezi kompetentními autoritami členských států). J Byly vydány další předpisy, které se však týkají specificky situace s nákazou Covid-19 L Stále chybí splnění cca 80% úkolů mandatorní povahy a v dalších 40 případech může Komise dle svého rozhodnutí změnit či upřesnit pravidla a postupy.

AKTUÁLNÍ STAV - MDR (RIZIKA) Ø Chybí společné specifikace (common specification – CS) – to vnáší značnou nejistotu do každé oblasti, která jimi může být dotčena, a to jak na straně výrobců, tak notifikovaných osob. Ø Příloha XVI se zdravotnickými prostředky bez léčebného účinku je vázána na vydání společných specifikací, které nejsou dosud vydány. Regulační status těchto výrobků se může změnit ze dne na den. Dnes nejsou stanovenými výrobky, po vydání společných specifikací se stanou ZP. Ø Chybí jakékoliv normy harmonizované k MDR. Použití norem harmonizovaných k MDD je možné, avšak neposkytuje podstatnou věc, kterou je předpoklad shody s požadavky na bezpečnost a funkční způsobilost (účinnost) ZP.

AKTUÁLNÍ STAV - MDR (RIZIKA) Ø Typický příklad problému, kterým je absence dokumentu, který měl k datu účinnosti existovat: – MDR, příloha VII, bod 4. 6. , čtvrtá odrážka: • Oznámený subjekt ke každému konkrétnímu projektu poskytne podrobnou zprávu, která vychází ze standardního formátu obsahujícího minimální soubor prvků určený Koordinační skupinou pro zdravotnické prostředky. • ITC má nastavený systém vypracování zpráv, včetně vzájemně provázaných formulářů. Avšak až/jakmile MDCG zveřejní standardní formát zprávy, bude nutno řadu dokumentů a formulářů přepracovat.

ÚVOD DO PROBLEMATIKY – POSUZOVÁNÍ SHODY, UVÁDĚNÍ VÝROBKŮ NA TRH EU Ø Jedním ze základních cílů EU je vytvoření jednotného trhu zajišťujícího volný pohyb zboží ve všech členských státech Unie. K tomu slouží především odstranění administrativních a fiskálních překážek obchodu, mezi něž patří dovozní a vývozní kvóty a celních poplatky při pohybu zboží mezi jednotlivými členskými státy. Překážkou obchodu jsou i jiná opatření jako dovozní licence, pravidla původu zboží, dotace nebo investice podporující obchod se zbožím členského státu.

ÚVOD DO PROBLEMATIKY – POSUZOVÁNÍ SHODY, UVÁDĚNÍ VÝROBKŮ NA TRH EU Ø Ochrana života a zdraví občanů a dalších aspektů veřejného zájmu je v EU prioritou nejvyšší kategorie, a proto nelze technické překážky obchodu odstranit jednoduchým zákazem stanovení jakýchkoliv požadavků na výrobky a procesy. Existuje však cesta, která slučuje požadavky na ochranu veřejného zájmu s požadavkem na zajištění volného pohybu zboží. Touto cestou je stanovení bezpečnostních a kvalitativních požadavků, které jsou pro daný typ výrobku společné a platné pro všechny členské státy (tzv. harmonizované požadavky). To znamená, že výrobek splňující příslušné požadavky ve kterémkoliv státě splňuje současně požadavky všech ostatních členských států Unie. Harmonizované požadavky jsou geograficky a politicky neutrální, neupřednostňují tedy výrobky žádného členského státu a nebrání tedy volnému pohybu zboží v rámci EU.

ÚVOD DO PROBLEMATIKY – POSUZOVÁNÍ SHODY, UVÁDĚNÍ VÝROBKŮ NA TRH EU Ø Proces stanovení společných technických požadavků na výrobky dodávané na trh EU se nazývá technická harmonizace, která se realizuje prostřednictvím harmonizačních legislativních předpisů, zpravidla směrnic nebo nařízení. Vzhledem k tomu, že unijní předpisy mají přednost před národními předpisy řešícími stejnou problematiku, je právně zajištěno uplatňování totožných harmonizovaných požadavků ve všech státech EU a Evropského společenství volného obchodu (ESVO, EFTA).

ÚVOD DO PROBLEMATIKY – POSUZOVÁNÍ SHODY, UVÁDĚNÍ VÝROBKŮ NA TRH EU Ø Přestože Nový přístup k technické harmonizaci podstatně omezil počet nezbytných harmonizačních předpisů, je nemyslitelné, aby tyto předpisy pokryly úplně všechny výrobky. Ve skutečnosti jsou technické požadavky stanoveny formou legislativních předpisů pouze na výrobky, jejichž použití představuje vysokou úroveň ohrožení veřejného zájmu. Tyto výrobky se označují jako stanovené výrobky a existují pro ně národní nebo evropské regulační předpisy. Protože se na výrobky vztahují právní předpisy (regulace), nazývá se oblast takových výrobků regulovanou sférou. Jestliže se na stanovený výrobek vztahuje evropský regulační (harmonizační) předpis, spadá tento výrobek do regulované harmonizované sféry.

ÚVOD DO PROBLEMATIKY – POSUZOVÁNÍ SHODY, UVÁDĚNÍ VÝROBKŮ NA TRH EU Ø Výrobky mimo regulovanou sféru („nestanovené výrobky“) smí výrobci uvádět na trh, aniž by se řídili specifickými předpisy, musí však zajistit, aby byl výrobek při rozumně předvídatelném způsobu použití bezpečný. Pro tyto výrobky se uplatní Směrnice Evropského parlamentu a Rady 2001/95/ES ze dne 3. prosince 2001 o obecné bezpečnosti výrobků a český zákon 102/2001 Sb. o obecné bezpečnosti výrobků.

ÚVOD DO PROBLEMATIKY – ROZLIŠENÍ VÝROBKŮ Ø Kvalifikací výrobku se rozumí jeho zařazení pod regulační předpis, který definuje požadavky na tento výrobek. Kvalifikace výrobku tedy říká, zda je výrobek hračkou, tlakovým zařízením, kosmetickým přípravkem, osobním ochranným prostředkem, zdravotnickým prostředkem, stavebním výrobkem nebo léčivem. Ø Kvalifikace výrobku se řídí účelem jeho použití, které mu určil jeho výrobce, a kterému podřídil jeho návrh a vlastnosti. Pro kvalifikaci není důležitý jeho vnější vzhled ani výrobní technologie.

ÚVOD DO PROBLEMATIKY – ROZLIŠENÍ VÝROBKŮ Ø Jestliže např. výrobce označí nerezovou trubku jako kůl ke stromkům, je výrobek kvalifikován jako nestanovený, výrobek spadající pod zákon o obecné bezpečnosti výrobků a není nutno aplikovat postupy posouzení shody. Ovšem v případě, že výrobce označí tutéž nerezovou trubku jako součást systému pro rozvod pitné vody, je tento výrobek kvalifikován jako stavební výrobek podléhající posouzení shody podle nařízení vlády č. 163/2002 Sb. , kterým se stanoví technické požadavky na vybrané stavební výrobky. Je samozřejmé, že jednotlivec ani stavební firma nesmí trubku určenou k podpírání stromků zabudovat do rozvodu pitné vody, ačkoliv jsou materiály i technologie identické.

ÚVOD DO PROBLEMATIKY – ROZLIŠENÍ OOP A ZP Ø Některé harmonizační předpisy dále rozčleňují výrobky v daném sektoru podle jejich nebezpečnosti ve vztahu k uživateli a jeho okolí. Sektor zdravotnických prostředků (ZP) dělí (klasifikuje) prostředky do rizikových tříd I, IIa, IIb a III podle vzrůstající úrovně rizika, které je s aplikací výrobku u pacienta spojeno, přičemž riziková třída I má ještě doplňkové třídy Is pro ZP dodávané na trh ve sterilním stavu a Im pro ZP s měřicí funkcí. Naproti tomu osobní ochranné prostředky (OOP) se rozdělují do kategorií I, II a III podle vzrůstající úrovně rizika, vůči kterému svého nositele chrání.

ÚVOD DO PROBLEMATIKY – ROZLIŠENÍ OOP A ZP Ø Předchozí odstavec je vysvětlením, proč např. zdánlivě stejná rouška je klasifikována jako ZP nejnižší třídy I, avšak je-li výrobcem kvalifikována jako OOP, spadá do nejvyšší třídy III s nejpřísnějšími požadavky na posouzení shody. V případě kvalifikace jako ZP je riziko, které způsobuje rouška svému nositeli relativně malé (výjimečně může dojít při nesprávném používání k sensibilizaci kůže nebo alergickým reakcím) a odpovídá třídě I. Na druhé straně riziko infekce biologickým agens, proti kterému rouška kvalifikovaná jako OOP nositele chrání, je velmi vysoké a srovnatelné s rizikem působení radiace nebo chemických látek, proto musí být tento OOP zařazen do nejvyšší kategorie III. Analogická situace nastává v případě plášťů a overalů kvalifikovaných jako ZP nebo OOP.

ÚVOD DO PROBLEMATIKY – POSUZOVÁNÍ SHODY OOP A ZP Ø V prvé řadě je důležité si uvědomit, že požadavky a podmínky pro uvádění stanovených výrobků, jako jsou rovněž OOP či ZP jsou stanoveny příslušnými harmonizačními předpisy Evropské unie (Nařízení EU a Směrnice) a konkretizovány harmonizovanými normami a jsou pro danou kategorii výrobků stejné a závazné pro každého, kdo chce uvést takový výrobek na trh EU. Ø Posuzování shody je velmi složitý a zdlouhavý proces, který vyžaduje řadu kroků, které musí být dodržovány. Notifikovaná osoba, pokud se posuzování shody účastní dle příslušné legislativy, si nemůže dovolit vynechat žádnou část procesu. Vše v tomto procesu posuzování shody musí být notifikovanou osobou řádně provedeno a zdokumentováno a dodržování je kontrolováno notifikujícím orgánem a Evropskou komisí.

ÚVOD DO PROBLEMATIKY – POSUZOVÁNÍ SHODY OOP A ZP Ø Zejména musí být zajištěno, že tyto výrobky nebudou mít škodlivý účinek na zdraví a bezpečnost. Je tedy nezbytně nutné, být seznámen s příslušnou legislativou a dodržovat stanovené podmínky a pravidla, tedy např. splnit náležitosti, jakými je především řádné provedení posouzení/potvrzení shody s požadavky stanovenými příslušnou legislativou (např. provedení zkoušek je jen jednou, nikoliv jedinou náležitostí!), řádné označení výrobku CE, vystavení prohlášení o shodě či získání příslušného certifikátu.

AKTUÁLNÍ STAV/COVID-19/UVÁDĚNÍ OOP A ZP NA TRH EU Ø Světová zdravotnická organizace WHO jako koordinační autorita v oblasti veřejného zdraví označila dne 12. března 2020 šíření koronaviru SARS-Cov-2 způsobujícího onemocnění Covid-19 (dále jen COVID-19) za celosvětovou pandemii. Na takovou situaci nebyla materiálně vybavena prakticky žádná země, ČR nevyjímaje. Prostředky omezující šíření pandemie nebo snižující dopady onemocnění na zasažené osoby nebyly k dispozici v dostatečném množství. Evropská komise se nastalou situací zabývala a vydala Doporučení Komise (EU) 2020/403, ve kterém vyzývá výrobce a všechny hospodářské subjekty v celém dodavatelském řetězci, jakož i oznámené subjekty (v češtině běžně označované vžitým názvem „notifikované osoby“) a orgány dozoru nad trhem, aby využily všech opatření, která mají k dispozici k zajištění dodávky OOP a ZP na celém trhu Evropské unie (EU) pro potřeby rostoucí poptávky. Nezbytným předpokladem při realizaci opatření je zachování odpovídající úrovně ochrany zdraví a bezpečnosti uživatelů (viz i reakce ITC – doplnění scope v oblasti OOP).

AKTUÁLNÍ STAV/COVID-19/UVÁDĚNÍ OOP A ZP NA TRH EU Ø Doporučení se týká zdravotnických prostředků a osobních ochranných prostředků, zahrnujících obličejové masky, ochranné, chirurgické a vyšetřovací rukavice, ochranné kombinézy a oděvy nebo prostředky na ochranu očí. Následně Komise vydala širší seznam zdravotnických prostředků významných z hlediska boje s infekcí způsobující onemocnění Covid-19 a omezení jeho dopadů na pacienty. Seznam obsahuje kromě výše uvedených výrobků řadu dalších zdravotnických prostředků a in-vitro diagnostik (celkem 65 položek).

AKTUÁLNÍ STAV/COVID-19/UVÁDĚNÍ OOP A ZP NA TRH EU Ø Řada podnikatelských subjektů vyslyšela doporučení Komise a upravila své výrobní programy tak, aby se mohla podílet na pokrytí rostoucí poptávky po uvedených komoditách, mezi nimiž převažují nedostatkové obličejové masky, ochranné obličejové štíty a respirátory. Vzhledem k tomu, že mnozí z těchto výrobců se dosud nezabývali výrobou ZP ani OOP, nejsou dostatečně seznámeni s požadavky předpisů, které musí být splněny při uvádění daných výrobků na jednotný trh EU.

PŘÍKLAD – ROUŠKA „ÚSTENKA“ JAKO OOP A/NEBO ZP Ø Buď se jedná o OOP tzn. prostředek chránící jejich nositele proti virům, anebo se jedná o ZP (pokud má chránit okolí – typicky pacienta), dále s rozlišením a rozdílnými podmínkami provedení posouzení shody v případě výrobku nesterilního nebo sterilního. Kategorizaci/zařazení provádí výrobce, který musí vědět „co vyrábí“ a jaký konkrétní účel má jeho výrobek plnit. Pokud má chránit jak nositele, tak okolí, tak by výrobek musel splňovat požadavky jak na OOP, tak na ZP. ü ROUŠKA JAKO OOP - Prostr edky chra ni ci jejich nositele proti viru m jsou podle Nar i zeni (EU) 2016/425 osobni m ochranny m prostr edkem kategorie III, vyz aduji ci m posouzeni shody za u c asti ozna mene ho subjektu (Notified body). Jednou z důležitých podmínek pozitivního výsledku posouzení shody (tzn. certifikace) i pozitivní výsledek sady zkoušek dle EN 149.

PŘÍKLAD - ROUŠKA „ÚSTENKA“ JAKO OOP A/NEBO ZP ü ROUŠKA JAKO ZP „nesterilní“ - V případě nesterilní roušky chránící pacienta (zejména chirurgické roušky – surgical mask) by se jednalo o neinvazivní zdravotnický prostředek třídy I. Posouzení shody provádí výrobce bez účasti třetí osoby (ITC ani žádná jiná notifikovaná osoba nesmí v takovém případě posouzení shody provádět). Za účelem posouzení shody výrobce podle Směrnice 93/42/EEC (MDD), příloha VII, zpracuje technickou dokumentaci, provede nebo nechá provést zkoušky dle ČSN EN 14683+AC: 2020 Zdravotnické obličejové masky – Požadavky a metody zkoušení, vypracuje zprávu o klinickém hodnocení (zpravidla založeném na literární rešerši nebo na srovnání s ekvivalentním výrobkem konkurence, který již je legálně na trhu), zavede systém řízení kvality zahrnující postup vyhodnocování zkušeností získaných se zdravotnickými prostředky uvedenými na trh, včetně klinického hodnocení a jeho aktualizace, postupy pro případ vigilance, nápravná opatření atd. Pak vydá prohlášení o shodě, označí výrobek CE bez čísla notifikované osoby, zaregistruje prostředek u SÚKL a uvádí jej na trh.

PŘÍKLAD - ROUŠKA „ÚSTENKA“ JAKO OOP A/NEBO ZP ü ROUŠKA JAKO ZP „sterilní“ – jsou-li roušky dodávány na trh ve sterilním stavu, jsou klasifikovány jako sterilní zdravotnické prostředky třídy Is a jejich posouzení shody provádí výrobce s účastí notifikované osoby. Podle MDD přílohy VII, odstavce 5, se pro sterilní výrobky tř. Is použije některý z postupů uvedených v přílohách II, IV, V nebo VI (pro jednoduchost je nejvhodnější postup podle přílohy V), vždy omezený na aspekty sterility. Na aspekty sterility je omezen i dozor notifikované osoby. K povinnostem a prvkům systému kvality uvedeným v předchozím odstavci 1 je nutno přidat prvky systému kvality zabývající se prostředím ve výrobě (čisté prostory) a sterilizaci. Implementovaný systém kvality musí prověřit výrobcem zvolená notifikovaná osoba z hlediska aspektů sterilizace. Tato hlediska zahrnují zejména: - kvalifikaci použitého sterilizátoru, - validaci sterilizačního procesu, - validaci obalu a procesu balení z hlediska dlouhodobého udržení sterility balených výrobků sterilizovaných v konečném obalu,

PŘÍKLAD - ROUŠKA JAKO OOP A/NEBO ZP ü ROUŠKA JAKO ZP „sterilní“ - stanovení exspirační doby (shelf life, životnost) výrobku limitované ve Vašem případě zejména schopností obalu udržet sterilní stav (lze použít urychlené metody testování životnosti, ale současně nasadit dlouhodobé testy životnosti, - v případě sterilizace ethylenoxidem stanovení reziduí, - v případě sterilizace ionizujícím zářením i radiační bezpečností, - značení výrobku a dokumentaci poskytovanou uživatelům (např. návod k použití). Má-li výrobce procesy zavedeny, validovány a dokumentovány, požádá notifikovanou osobu o počáteční audit a v kladném případě o vydání certifikátu. Po obdržení certifikátu vydá výrobce prohlášení o shodě a označuje každý výrobek CE, tentokrát i s číslem notifikované osoby, která provedla audit a vydala certifikát. Následuje registrace u SÚKLu, který bude požadovat mj. certifikát a zprávu z klinického hodnocení.

PŘÍKLAD - RESPIRÁTORY Ø Obličejové masky (označované jako filtrační polomasky nebo respirátory) jsou osobním ochranným prostředkem poskytujícím ochranu dýchacích orgánů, které se podle Přílohy I Nařízení (EU) 2016/425 řadí do kategorie III, jestliže chrání proti působení škodlivých biologických činitelů, mezi které virus SARS-Cov-2 bezesporu patří. Je nutno zdůraznit, že jejich účelem je chránit svého nositele, nikoliv jeho okolí, a je-li maska vybavena výdechovým ventilem, mohou infikované kapalné aerosoly vydechované COVID-19 pozitivním nositelem masky volně proudit do okolí. Norma ČSN EN 149+A 1: 2009 (Ochranné prostředky dýchacích orgánů – Filtrační polomasky k ochraně proti částicím – Požadavky, zkoušení a značení) rozeznává podle celkového průniku zkušebního aerosolu maskou a průniku filtračním materiálem tři třídy ochrany, označené FFP 1, FFP 2 a FFP 3. Je-li maska určena pouze pro jednorázové použití (jednu směnu), použije se doplňkové označení NR, je-li určena pro více směn, je doplňkové označení R.

PŘÍKLAD - RESPIRÁTORY Ø Nelze zaměňovat typy zdravotnické obličejové masky s třídami ochranných filtračních polomasek. To znamená, že rouška kvalifikovaná jako zdravotnický prostředek nesmí nést označení FFP 1, FFP 2 nebo FFP 3 a naopak rouška kvalifikovaná jako osobní ochranný prostředek nesmí být označena jako Typ I, Typ, II nebo Typ III. Např. označení FFP 3 znamená automaticky, že se jedná o osobní ochranný prostředek, nikoliv o zdravotnický prostředek.

KONTAKT Mgr. Jiří Heš, generální ředitel Institut pro testování a certifikaci, a. s. sídlo: divize certifikace: tel: e-mail: internet: třída Tomáše Bati 299, Louky, 763 02 Zlín třída Tomáše Bati 5264 (budova 113 Svit), 763 02 Zlín +420 572 779 922 itc@itczlin. cz www. itczlin. cz
- Slides: 47