WYKAD III A Najwysze stopnie utlenienia pierwiastkw chemicznych












- Slides: 21

WYKŁAD III A. Najwyższe stopnie utlenienia pierwiastków chemicznych. Najlepsze dostępne utleniacze i reduktory. Metalizacja niemetali. B. Projektowanie nowych funkcjonalnych materiałów – reguły gry. Wybór kluczowego parametru opisującego złożoną własciwość lub proces, i sterowanie nim. C. Sterowanie parametrami mikroskopowymi molekuł. Pomost między parametrami atomów i prostych molekuł, a parametrami ciał stałych. Sterowanie parametrami makroskopowymi ciał stałych. D. Przykłady korelacji parametrów atomów i ciał stałych, oraz parametrów molekuł i ciał stałych. Licz ligandy! Licz elektrony!

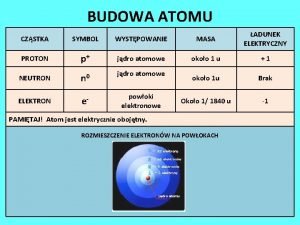
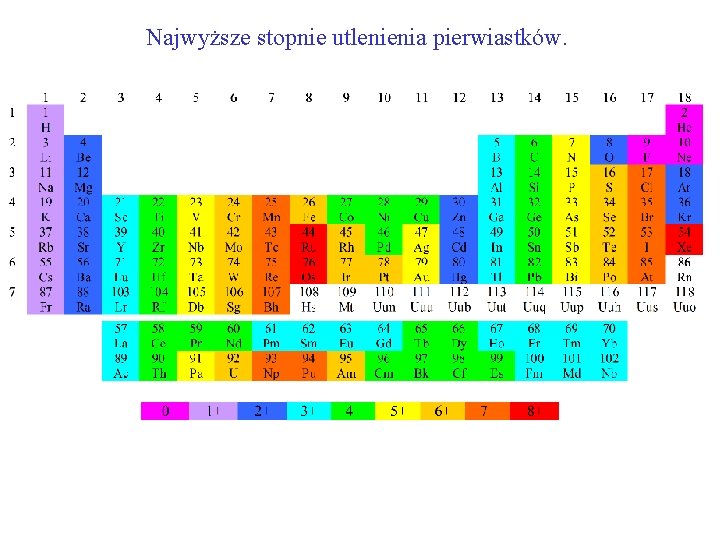
Najwyższe stopnie utlenienia pierwiastków.

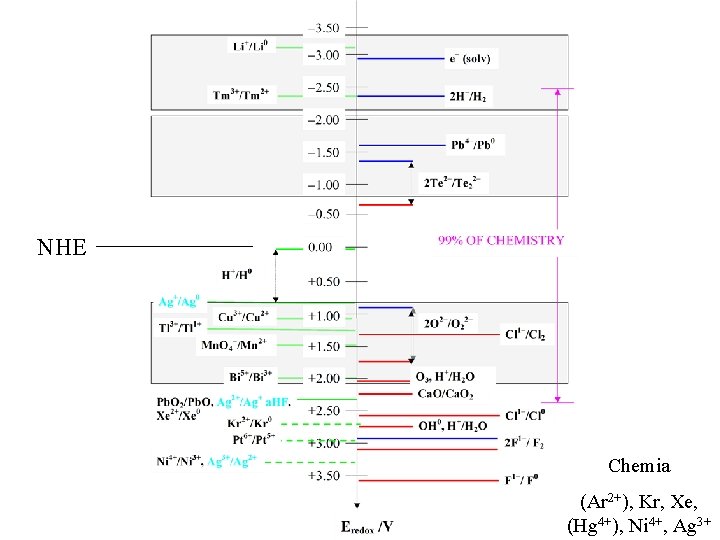
NHE Chemia (Ar 2+), Kr, Xe, (Hg 4+), Ni 4+, Ag 3+

Frontier orbitals Highest Occupied Molecular Orbital & Lowest Unoccupied Molecular Orbital W 2+ d 4, W W (2002) *

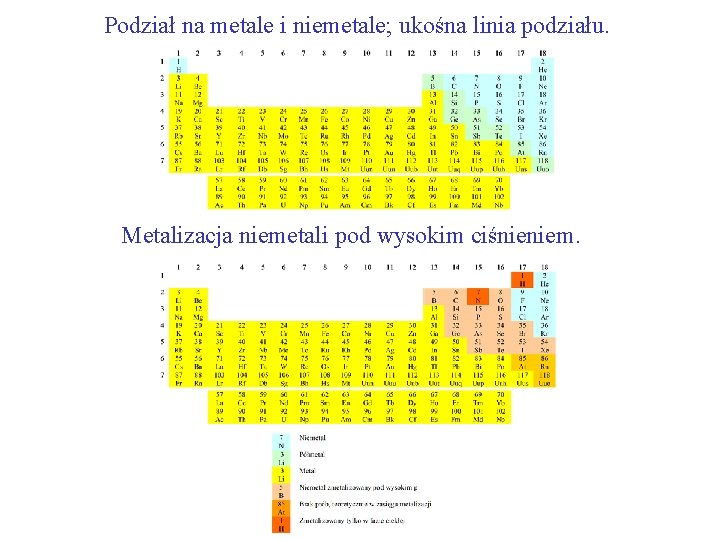
Podział na metale i niemetale; ukośna linia podziału. Metalizacja niemetali pod wysokim ciśnieniem.

Projektowanie nowych funkcjonalnych materiałów – ALGORYTM SUKCESU. 1. Ustal jaką makroskopową cechą materiału, C, chcesz sterować w danym materiale. 2. Zbuduj możliwie najprostszy model atomowy lub molekularny rozsądnie symulujący zadany materiał. 3. Wybierz kluczowy mikroskopowy parametr atomowy lub molekularny, p, symulujący własność C. 4. Ustal zakres zmienności p w istniejących układach, włączając dotychczasowe rekordowe wartości. 5. Zastanów sie jak wykorzystując dostępne pierwiastki chemiczne sterować monotonicznie parametrem p. 6. Wykorzystaj pierwiastek/-tki E 1, E 2… (gwarantujący/-e nową rekordową wartość p w modelowym układzie) do konstrukcji układu makroskopowego. 7. Sprawdź wartość cechy C. 1. Być może otrzymałeś nowy rekord świata…!

Jak chemicznie sterować parametrami mikroskopowymi molekuł? - podstawienie izoelektronowe/izolobalne - wędrówka wdłuż danego okresu i grupy układu okresowego - zaburzenie elektroujemności - kowalencyjność / jonowość - podstawniki i elektrodonorowe i elektroakceptorowe, - podstawniki miękkie i twarde, polaryzujące i utwardzające, neutralne i naładowane - podstawniki (“bulky”) = osłaniające (efekty steryczne) - podstawniki wymuszające organizację 1 D, 2 D, 3 D - wiązania wodorowe i inne … - skomplikowane struktury makromolekularne wyższego rzędu

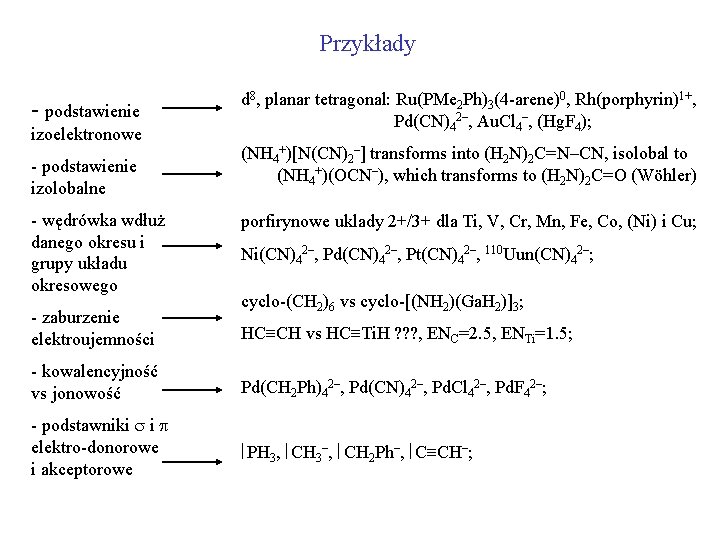
Przykłady - podstawienie izoelektronowe - podstawienie izolobalne - wędrówka wdłuż danego okresu i grupy układu okresowego - zaburzenie elektroujemności d 8, planar tetragonal: Ru(PMe 2 Ph)3(4 -arene)0, Rh(porphyrin)1+, Pd(CN)42–, Au. Cl 4–, (Hg. F 4); (NH 4+)[N(CN)2–] transforms into (H 2 N)2 C=N–CN, isolobal to (NH 4+)(OCN–), which transforms to (H 2 N)2 C=O (Wöhler) porfirynowe uklady 2+/3+ dla Ti, V, Cr, Mn, Fe, Co, (Ni) i Cu; Ni(CN)42–, Pd(CN)42–, Pt(CN)42–, 110 Uun(CN)42–; cyclo-(CH 2)6 vs cyclo-[(NH 2)(Ga. H 2)]3; HC CH vs HC Ti. H ? ? ? , ENC=2. 5, ENTi=1. 5; - kowalencyjność vs jonowość Pd(CH 2 Ph)42–, Pd(CN)42–, Pd. Cl 42–, Pd. F 42–; - podstawniki i elektro-donorowe i akceptorowe PH 3, CH 3–, CH 2 Ph–, C CH–;

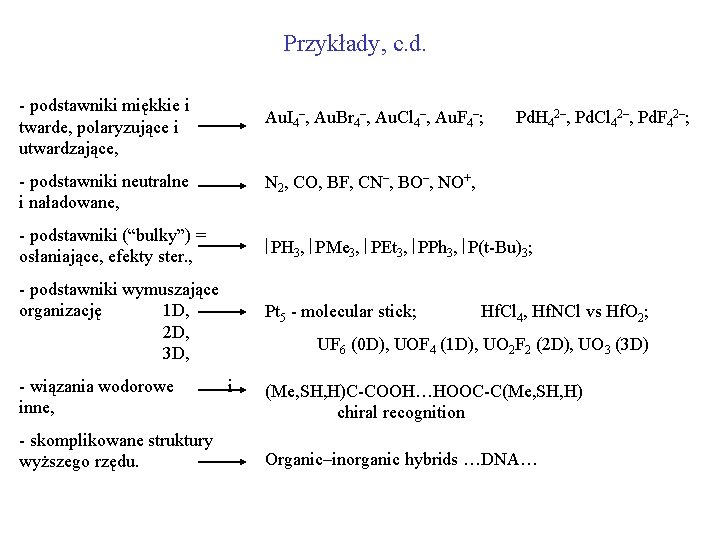
Przykłady, c. d. - podstawniki miękkie i twarde, polaryzujące i utwardzające, Au. I 4–, Au. Br 4–, Au. Cl 4–, Au. F 4–; Pd. H 42–, Pd. Cl 42–, Pd. F 42–; - podstawniki neutralne i naładowane, N 2, CO, BF, CN–, BO–, NO+, - podstawniki (“bulky”) = osłaniające, efekty ster. , PH 3, PMe 3, PEt 3, PPh 3, P(t-Bu)3; - podstawniki wymuszające organizację 1 D, Pt 5 - molecular stick; Hf. Cl 4, Hf. NCl vs Hf. O 2; 2 D, UF 6 (0 D), UOF 4 (1 D), UO 2 F 2 (2 D), UO 3 (3 D) 3 D, - wiązania wodorowe i inne, (Me, SH, H)C-COOH…HOOC-C(Me, SH, H) chiral recognition - skomplikowane struktury wyższego rzędu. Organic–inorganic hybrids …DNA…

Parametry mikroskopowe atomów i molekuł a własności makroskopowe ciał stałych. - Si&Ge - semiconducting Si&Ge in the diamond structure - C - insulating diamond, fullerene and high-temperature [–C C] , conducting graphite; amorphous & glassy C - Sn - metallic Sn and semiconducting gray tin - Na. Cl - ionic Na. Cl crystal (octahedral coordination of each atom) - C 6 H 6 - 3 D structure of crystalline benzene, …H interactions - C 2 H 2 - polymeric acetylene (poly-C 2 H 2), sp 2 … … - ? - Na 1. 000 Cl 0. 999 (colour centres vel color centers) - ? - La 2–x. Bax. Cu. O 4 (superconductor) - ? - various surfaces of In. N single crystal - ? - La 2 Mn. O 4 (giant magnetoresistance) - ? - Li. Tl = (Li+)(Tl– 1) (diamond net, Zintl phases)

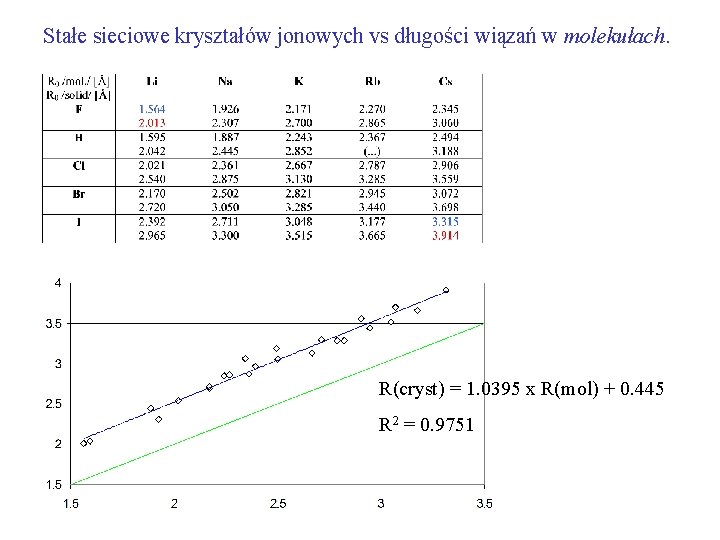
Stałe sieciowe kryształów jonowych vs długości wiązań w molekułach. R(cryst) = 1. 0395 x R(mol) + 0. 445 R 2 = 0. 9751

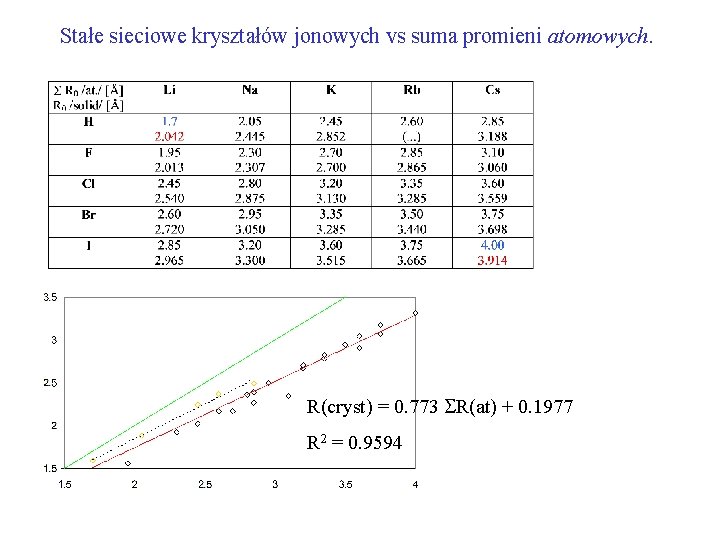
Stałe sieciowe kryształów jonowych vs suma promieni atomowych. R(cryst) = 0. 773 R(at) + 0. 1977 R 2 = 0. 9594

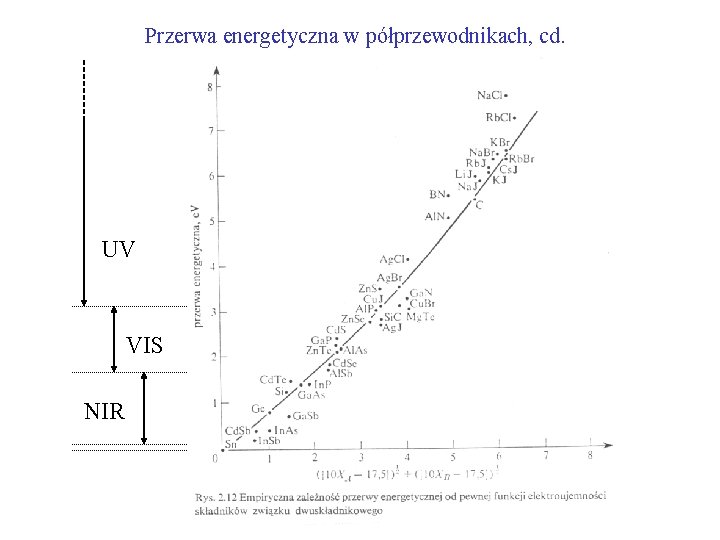
Przerwa energetyczna w półprzewodnikach, cd. UV VIS NIR

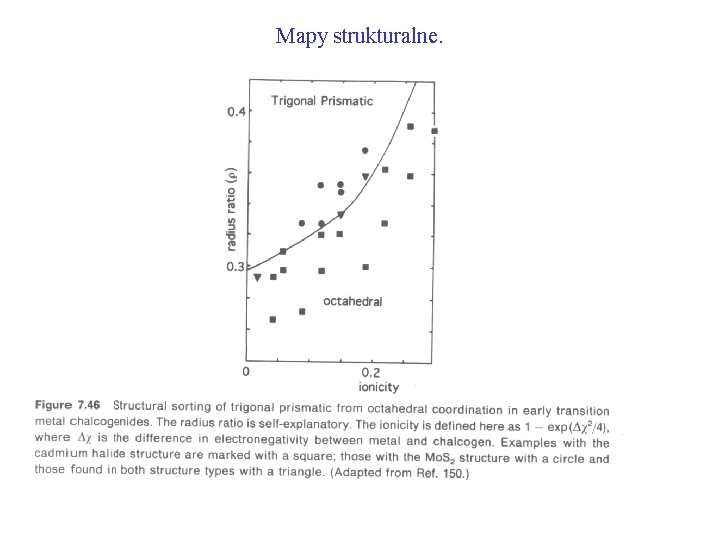
Mapy strukturalne.

Przewidywanie struktury /odmiany polimorficzne/.

Przewidywanie wymiarowości i parowanie rodników w ciele stałym. (a) UF 6 (0 D), UOF 4 (1 D), UO 2 F 2 (2 D), UO 3 (3 D); (b) Re. F 6 (0 D), Re. F 5 (1 D), Re. F 4 (2 D), Re. F 3 (3 D); Liczyć ligandy! 3 D (c) Li 4 Sr 2 Cr 2 N 6 Li. I 4 Sr. II 2[Cr. V 2 N–III 6] Cr. V = 3 d 1 (d) Zintl-Klemm phases: Na. Sb, Li 2 Sb and Li. Ba. Sb Sb–I s 2 p 4 = Te, Sb–II s 2 p 5 = I, Sb–III s 2 p 6 = Xe Liczyć elektrony!


Jak chemicznie sterować parametrami makroskopowymi ciał stałych? - przerwa energetyczna - podstawienie izoelektronowe z zachowaniem stosunku stechiometrycznego (elektroujemność), cienkie powłoki, ciśnienie zewn. - DOSF - zmiana ilości elektronów (podstawienie w tym samym okresie, domieszkowanie), ciśnienie zewn. - stała sieciowa - umiarkowane podstawienie izolobalne bez “krytycznego zaburzenia struktury; jednokładność” (Li 2 C 2=Rb 2 O 2), ciśnienie zewn. - jonowość - podstawienie izolobalne, ciśnienie zewn. - liczba koord. - podstawienie izolobalne, ciśnienie zewn. - wymiarowość - (a) Hf. Cl 4, Hf. NCl vs Hf. O 2; (b) UF 6 (0 D), UOF 4 (1 D), UO 2 F 2 (2 D), UO 3 (3 D); (c) zmiana stopnia utlenienia: Re. F 6 (0 D), Re. F 5 (1 D), Re. F 4 (2 D), Re. F 3 (3 D); (d) dodatki wymuszające wymiarowość (organic–inorganic hybrids np. UFO) (e) zmiana kwasowości Lewisa: inverse perovskite Li. Ba. F 3 = [Li. F 2–][Ba. F+] - przewodnictwo elektr. - (a) domieszkowanie n i p (Si: B, Si: P), (b) zmiana ilości elektronów, (c) fotoprzewodnictwo, (d) ciśnienie zewn.

Jak chemicznie sterować …? (cd. ) - gęstość energii - materiały wybuchowe: (a) quasi–stable redox pairs, (b) Mmol - pojemność elektr. - charge capacitors; - pojemność cieplna - thermal energy stores; Mmol - rozszerz. cieplna - thermocouple - moduł Younga - stress–resistant materials (kevlar, diamond); - wytrzym. mechan. , twardość, ściśliw. - ultrahard (Cdiam, BN), ultrasoft and ultrabrittle materials - adhezyjność /powłoki/ - teflon/Ti. F 3 and Fe. F 3; ochrona przed korozją! - tmelt - Ta. C & Hf. C (ca. 3900 o. C) [Hf 2233 o. C, Ta 3017 o. C, and Cgraph 3650 o. C], compare to W (3422 o. C); - tboil - Re (5596 o. C); Zr. C (5100 o. C) & Hf. C ? , WC 6000 o. C - tsubl - Cgraph ca. 3300 o. C; Mmol: UF 6 (projekt Manhattan) - tthermal decomp - energy barrier; decompos. pathway, quasi–stable redox pairs

Jak chemicznie sterować …? (cd. ) - t. Curie (ferroelektr) - Li. Nb. O 3 (1483 o. C) - t. Curie, t. Neel - Curie point (FM): Co (1331 o. C), Neél point (AFM): La. Fe. O 3 (738 o. C), Ni. O (647 o. C); twardość, miekkość i straty - tcrit - 1223: Hg. Ba 2 Cu 3 O 8+x (– 140 o. C, – 125 o. C = 158 K pod wysokim ciśn. ); Mg. B 2 (39 K), Cs 3 C 60 (33 K) - gęstość nadprądu - 3 D >> 2 D >> 1 D - Hc (supercond. ) - V 3 Ga (32 MA/m) at 0 K - wsp. załam. i dysp. - diament vs. Sr. Ti. O 3 (żółć); Ba. F 2 (dysp. red/yell/blue) - zakres przepuszcz. - filters for X-Ray, IR, UV-VIS, Raman & microwave spectroscopy; notch and interference filters - dwójłom. , polaryz. - filtry polaryzacyjne, ćwierć- i półfalówki - hiperpolaryzow. - SHG, optic materials, lasers, nonlinear crystals - skrecalność właśc. , magnetochiralność - (so far) properties without practical significance - …

Parametry C (a) Rozmiar (b) Jonowość (c) Wymiarowość (d) Temperatura specyficzna (e) Przerwa energetyczna (f) Gęstość stanów elektron. (g) Parametry mechaniczne (h) Parametry elektryczne (i) Parametry magnetyczne (j) Paramtery optyczne (k) Gęstość energii … Projekt Manhattan Parametry p (a) Liczba elektronów (b) Liczba ligandów (c) Elektroujemność (d) Twardość (e) Jonowość (f) Ładunek elektryczny (g) Rozmiar (h) Masa molowa (i) Częstość drgań (j) Parametry termodynamiczne (k) Potencjał redox … + Ciśnienie zewnętrzne/objętość Temperatura
 Właściwości fizyczne manganu
Właściwości fizyczne manganu Synproporcjonowania
Synproporcjonowania Stopien utlenienia siarki w s8
Stopien utlenienia siarki w s8 Hybrydyzacja dsp3
Hybrydyzacja dsp3 Tablice przesunięć chemicznych nmr
Tablice przesunięć chemicznych nmr Adunek
Adunek Hamlet act iii scene ii
Hamlet act iii scene ii 3 rodzaje ewakuacji
3 rodzaje ewakuacji Prz
Prz Stopnie w marynarce wojennej
Stopnie w marynarce wojennej Stopnie alarmowe crp
Stopnie alarmowe crp Stopnie oparzenia
Stopnie oparzenia Korpusy w policji
Korpusy w policji Stopnie w policji
Stopnie w policji Halban i grzegorz porownanie
Halban i grzegorz porownanie Stopnie oparzenia
Stopnie oparzenia Stopnie w policji
Stopnie w policji Skala fahrenheita
Skala fahrenheita Astma stopnie
Astma stopnie Leo iii outlawed crucifixes as idolatry
Leo iii outlawed crucifixes as idolatry Sample filled up erf form
Sample filled up erf form Microaggressions
Microaggressions