Wykad 10 Entalpia w ujciu masy kontrolnej przykady








- Slides: 16

Wykład 10 Entalpia w ujęciu masy kontrolnej; przykłady: adiabatyczne dławienie gazu dla przepływu ustalonego odwracalne izobaryczne rozprężanie gazu nieodwracalne napełnianie gazem pustego zbiornika I zasada termodynamiki; masa kontrolna i entalpia I zasada termodynamiki dla układów otwartych Układ otwarty w ujęciu masy kontrolnej Układ otwarty w ujęciu objętości kontrolnej: prawo zachowania masy prawo zachowania energii 1

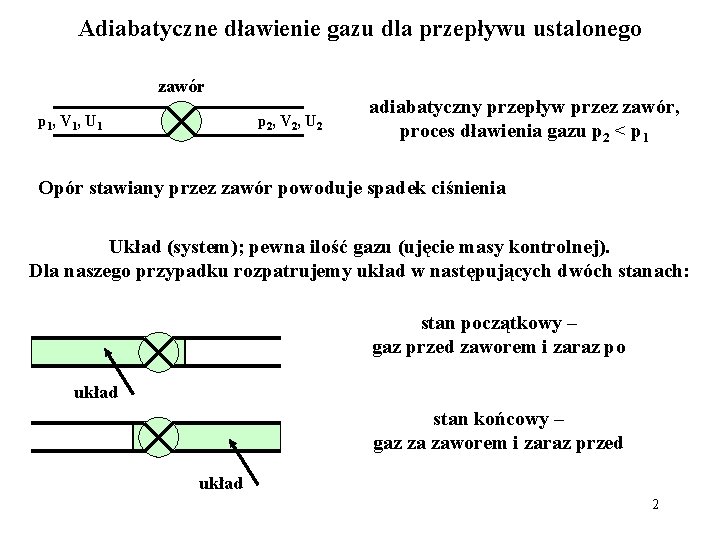
Adiabatyczne dławienie gazu dla przepływu ustalonego zawór p 1, V 1, U 1 p 2, V 2, U 2 adiabatyczny przepływ przez zawór, proces dławienia gazu p 2 < p 1 Opór stawiany przez zawór powoduje spadek ciśnienia Układ (system); pewna ilość gazu (ujęcie masy kontrolnej). Dla naszego przypadku rozpatrujemy układ w następujących dwóch stanach: stan początkowy – gaz przed zaworem i zaraz po układ stan końcowy – gaz za zaworem i zaraz przed układ 2

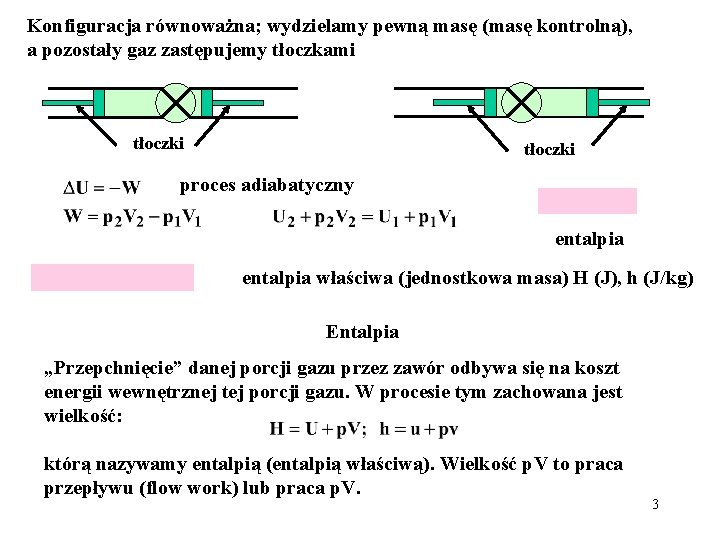
Konfiguracja równoważna; wydzielamy pewną masę (masę kontrolną), a pozostały gaz zastępujemy tłoczkami tłoczki proces adiabatyczny entalpia właściwa (jednostkowa masa) H (J), h (J/kg) Entalpia „Przepchnięcie” danej porcji gazu przez zawór odbywa się na koszt energii wewnętrznej tej porcji gazu. W procesie tym zachowana jest wielkość: którą nazywamy entalpią (entalpią właściwą). Wielkość p. V to praca przepływu (flow work) lub praca p. V. 3

Interpretacja entalpii: Licząc całkowitą energię obiektu o objętości V należy uwzględnić, że jego „wytworzenie” wymagało dostarczenia energii na „odepchnięcie” otoczenia. Jeśli ciśnienie p wywierane przez otoczenie na obiekt wynosi p, to praca wykonana na wytworzenie miejsca dla obiektu wyniosła p. V. Tak więc całkowita energia obiektu to jego energia wewnętrzna plus ekstra energia p. V, którą „odzyskalibyśmy” gdyby obiekt zniknął (skurczył się do zera). Tę całkowitą energię obiektu nazywamy entalpią. Wniosek W procesie adiabatycznego dławienia entalpia gazu przed i za zaworem dławiącym jest zachowana. Wykonanie pracy przepływu odbywa się na koszt energii wewnętrznej gazu. 4

Odwracalne izobaryczne rozprężanie gazu pomimo „rozprężania” ciśnienie spada, bo gaz równocześnie podgrzewamy! W przemianie izobarycznej dostarczane ciepło powoduje wzrost entalpii gazu; choć ciśnienie jest stałe ale rośnie objętość; zatem rośnie zarówno energia wewnętrzna gazu (rośnie temperatura) jak i człon p. V. 5

Jeśli w przemianie izobarycznej rozprężamy gaz, ciśnienie będzie stałe, gdyż dostarczamy ciepła Q. Ciepło Q powoduje wzrost temperatury (ΔU) zatem: gdyż podgrzewanie i rozprężanie gazu zachodzi przy stałym ciśnieniu. n to liczba moli gazu Mamy zatem: podobnie jak dla przemiany izochorycznej: Warto zauważyć, że ponieważ U i H są funkcjami stanu więc zależności te są prawdziwe dla każdej przemiany, pomimo, iż wyprowadzone zostały dla konkretnych przemian; izobarycznej i izochorycznej. 6

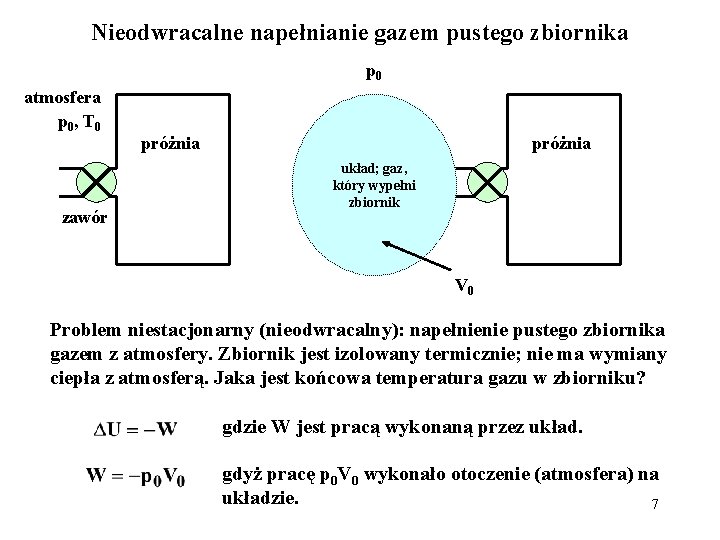
Nieodwracalne napełnianie gazem pustego zbiornika p 0 atmosfera p 0 , T 0 zawór próżnia układ; gaz, który wypełni zbiornik V 0 Problem niestacjonarny (nieodwracalny): napełnienie pustego zbiornika gazem z atmosfery. Zbiornik jest izolowany termicznie; nie ma wymiany ciepła z atmosferą. Jaka jest końcowa temperatura gazu w zbiorniku? gdzie W jest pracą wykonaną przez układ. gdyż pracę p 0 V 0 wykonało otoczenie (atmosfera) na układzie. 7

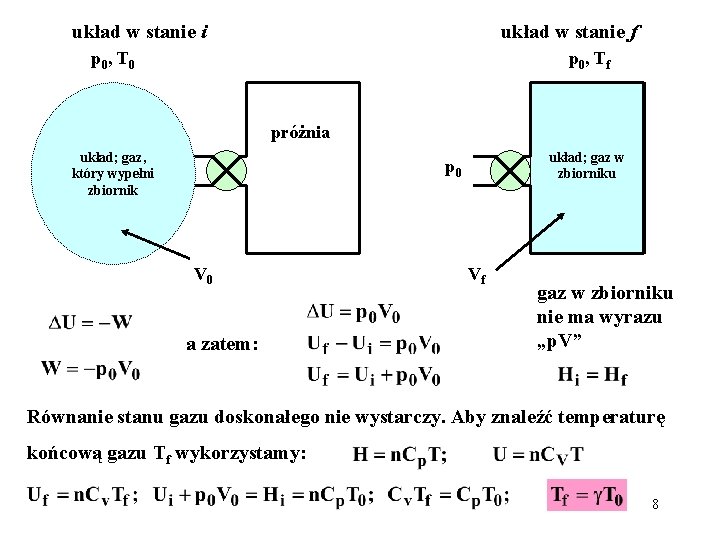
układ w stanie i układ w stanie f p 0 , T 0 p 0 , T f próżnia układ; gaz, który wypełni zbiornik układ; gaz w zbiorniku p 0 V 0 a zatem: Vf gaz w zbiorniku nie ma wyrazu „p. V” Równanie stanu gazu doskonałego nie wystarczy. Aby znaleźć temperaturę końcową gazu Tf wykorzystamy: 8

I zasada termodynamiki; masa kontrolna i entalpia Dla pewnej masy (kontrolnej) czynnika: Korzystając z definicji entalpii, po zróżniczkowaniu: i podstawieniu : Ponieważ dla przemiany odwracalnej: Ostatecznie mamy: , brak pracy nieobjętościowej skąd, dla procesów dla których ciśnienia początkowe i końcowe są równe oraz uwzględniając, że entalpia jest funkcją stanu mamy: entalpia, jako zawartość ciepła czyli ilość ciepła dostarczonego do układu jest równa zmianie entalpii. 9

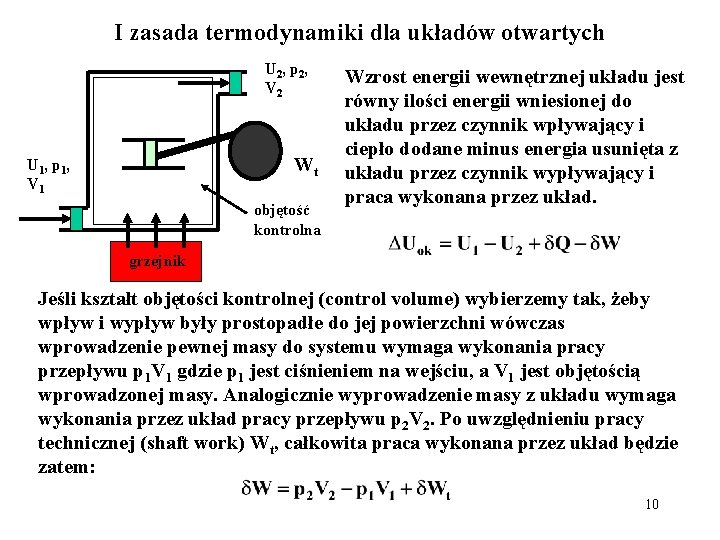
I zasada termodynamiki dla układów otwartych U 2, p 2, V 2 Wt U 1, p 1, V 1 objętość kontrolna Wzrost energii wewnętrznej układu jest równy ilości energii wniesionej do układu przez czynnik wpływający i ciepło dodane minus energia usunięta z układu przez czynnik wypływający i praca wykonana przez układ. grzejnik Jeśli kształt objętości kontrolnej (control volume) wybierzemy tak, żeby wpływ i wypływ były prostopadłe do jej powierzchni wówczas wprowadzenie pewnej masy do systemu wymaga wykonania pracy przepływu p 1 V 1 gdzie p 1 jest ciśnieniem na wejściu, a V 1 jest objętością wprowadzonej masy. Analogicznie wyprowadzenie masy z układu wymaga wykonania przez układ pracy przepływu p 2 V 2. Po uwzględnieniu pracy technicznej (shaft work) Wt, całkowita praca wykonana przez układ będzie zatem: 10

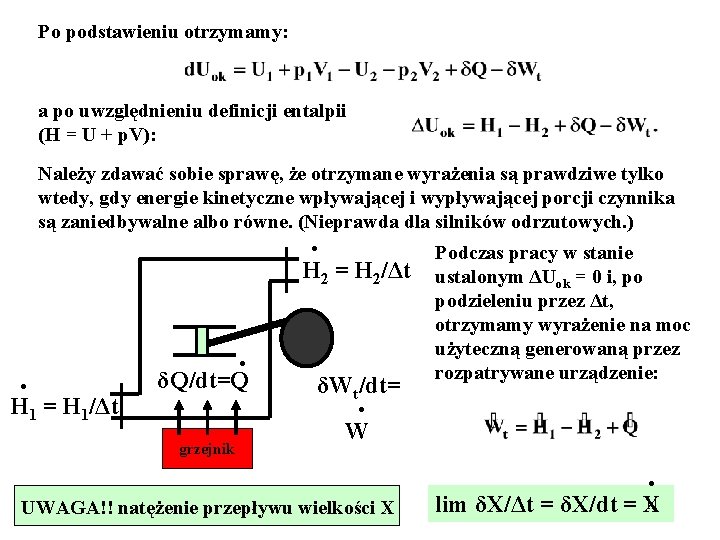
Po podstawieniu otrzymamy: a po uwzględnieniu definicji entalpii (H = U + p. V): Należy zdawać sobie sprawę, że otrzymane wyrażenia są prawdziwe tylko wtedy, gdy energie kinetyczne wpływającej i wypływającej porcji czynnika są zaniedbywalne albo równe. (Nieprawda dla silników odrzutowych. ) ·H · H 1 = H 1/Δt · δQ/dt=Q grzejnik 2 = H 2/Δt δWt/dt= Podczas pracy w stanie ustalonym ΔUok = 0 i, po podzieleniu przez Δt, otrzymamy wyrażenie na moc użyteczną generowaną przez rozpatrywane urządzenie: · W UWAGA!! natężenie przepływu wielkości X · lim δX/Δt = δX/dt = X 11

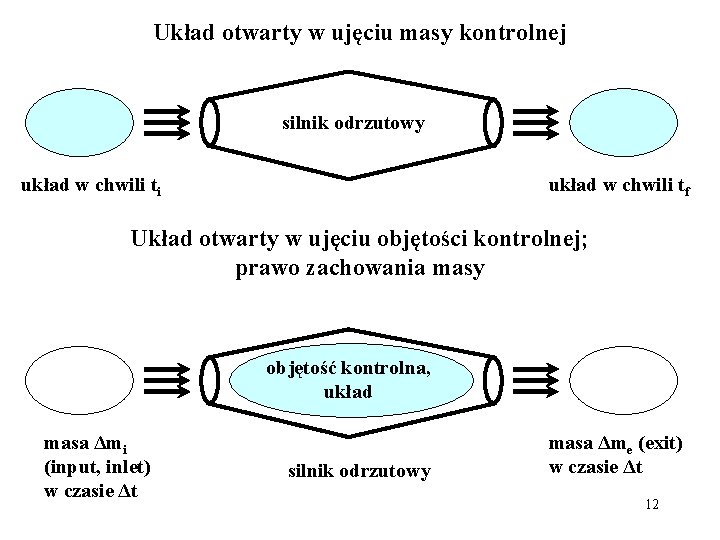
Układ otwarty w ujęciu masy kontrolnej silnik odrzutowy układ w chwili ti układ w chwili tf Układ otwarty w ujęciu objętości kontrolnej; prawo zachowania masy objętość kontrolna, układ masa Δmi (input, inlet) w czasie Δt silnik odrzutowy masa Δme (exit) w czasie Δt 12

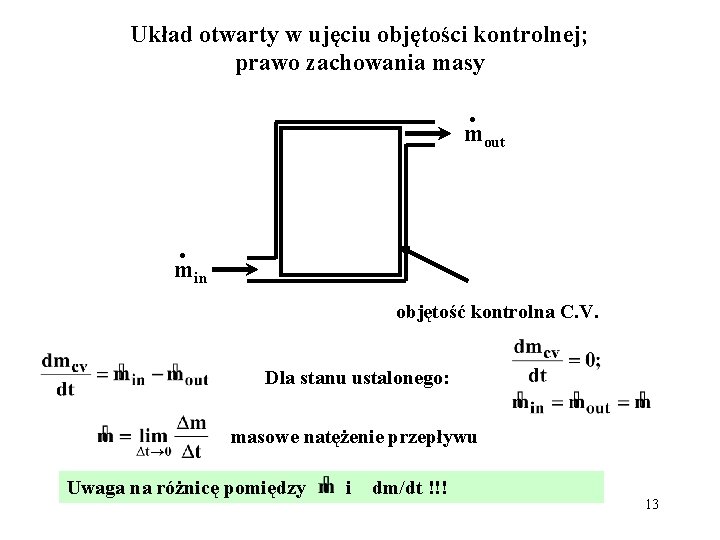
Układ otwarty w ujęciu objętości kontrolnej; prawo zachowania masy . mout . min objętość kontrolna C. V. Dla stanu ustalonego: masowe natężenie przepływu Uwaga na różnicę pomiędzy i dm/dt !!! 13

Układy otwarte w ujęciu objętości kontrolnej; prawo zachowania energii Pierwsza zasada termodynamiki jako równanie kinetyczne: gdzie: By otrzymać I zasadę termodynamiki w ujęciu objętości kontrolnej musimy śledzić zmiany energii w czasie w objętości kontrolnej C. V. : (ciepło dodane do C. V. – praca wykonana + wpływ energii do C. V. – wypływ energii z C. V. ) na sekundę Pracę W wykonywaną przez układ dzielimy na pracę przepływu Wflow (flow work) i pracę techniczną Wts, Wtp (shaft work). 14

Praca przepływu będzie różnicą prac wykonanych przez gaz w punkcie wyjścia i wejścia: Energia wpływająca do C. V. i wypływająca z C. V. związana jest z przepływem masy przez C. V. Gaz o masie dm, wchodzący lub wychodzący z układu, ma energię: Podsumowując, I zasada termodynamiki dla układów otwartych przyjmie postać: gdzie suma zawiera odpowiedni znak dla wpływu do i wypływu z C. V. 15

Wprowadzając entalpię do wyrażenia na pracę przepływu i energię całkowitą otrzymamy: I zasada termodynamiki w sformułowaniu objętości kontrolnej przyjmie wówczas postać: Dla stanu ustalonego (d/dt = 0, oraz zaniedbując wyraz gz otrzymamy: ) i dzieląc przez 16