TEGANGAN PERMUKAAN ANTARMUKA SBW MATERI KE 15 TEGANGAN

TEGANGAN PERMUKAAN - ANTARMUKA SBW MATERI KE 15

TEGANGAN PERMUKAAN • ISTILAH INI UNTUK MENJELASKAN: • FENOMENA PERMUKAAN ZAT CAIR KONTAK DENGAN GAS/UDARA DIATASNYA, NAMPAK SEPERTI LAPISAN PERMUKAAN TIPIS YANG ELASTIK

TEGANGAN ANTAR MUKA • Antarmuka adalah batas antara dua fase atau LEBIH • Tegangan antarmuka: gaya/satuan panjangyang terdapat pada antarmuka dua fase cair yang tidak bercampur. Satuan dyne/cm • Penggolongan Antarmuka
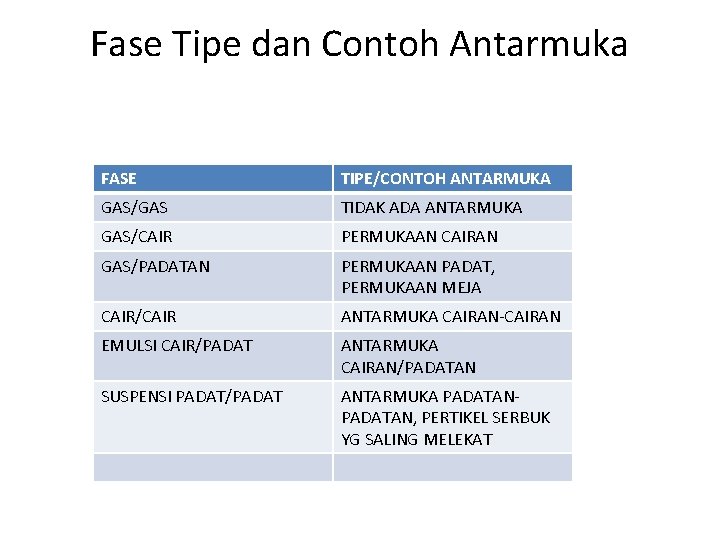
Fase Tipe dan Contoh Antarmuka FASE TIPE/CONTOH ANTARMUKA GAS/GAS TIDAK ADA ANTARMUKA GAS/CAIR PERMUKAAN CAIRAN GAS/PADATAN PERMUKAAN PADAT, PERMUKAAN MEJA CAIR/CAIR ANTARMUKA CAIRAN-CAIRAN EMULSI CAIR/PADAT ANTARMUKA CAIRAN/PADATAN SUSPENSI PADAT/PADAT ANTARMUKA PADATAN, PERTIKEL SERBUK YG SALING MELEKAT

TEG. PERMUKAAN-INTERMOLECULAR FORCE Gaya antar molekul (intermolecular) merupakan gaya yang terjadi antar 2 molekul yang mempengaruhi sifat-sifat fisika dari suatu zat. INTERMOLECULAR FORCE : gaya Van der Waals. Tegangan permukaan juga berhubungan dengan gaya antar molekul dalam cairan. Molekulmolekul dalam cairan menarik satu sama lain. Sebuah molekul dalam sebagian besar zat cair tertarik sama pada semua sisi sehingga tarik menarik antarmolekul data dihilangkan antaranya atau dikatakan nol. Namun, gaya tarik menarik molekul di permukaan hanya ke bawah, oleh karena itu molekul permukaan mengalami gaya tarik resultan ke bawah dari dalam cairan, yang cenderung membuat area permukaan cairan sekecil mungkin. Hal ini menyebabkan molekul di permukaan yang tertarik ke dalam sebagai gaya seb-akibat dari gaya resultan kebawah, sehingga selalu ada beberapa kekuatan ketidakseimbangan yang bekerja pada permukaan cairan, hal tersebut disebut sebagai tegangan permukaan.

DEFINISI ANTAR MUKA • Tegangan antar muka adalah tegangan antara dua fase yang berbeda . Pada fenomena ini diketahui bahwa gaya kohesi lebih besar dibandingkan dengan gaya adhesi. Dikarenakan lebih besarnya gaya kohesi maka menyebabkan sangat sulitnya atau bahkan tidak dapat bersatu antara dua fase yang berbeda.

SATUAN UNIT SURFACE TENSION • Gaya per satuan panjang yang harus diberikan sejajar PADA PERMUKAAN untuk mengimbangi tarikan ke dalam. SATUAN UNIT NYA: N/m; walaupun yang umum satuan nya : dyne/cm • γ= gamma= gaya permuk. = dyne/cm • γ = fb / 2 L

• Tegangan permukaan suatu zat cair didefinisikan sebagai gaya tiap satuan panjang. Jika pada suatu permukaan sepanjang l bekerja gaya sebesar F yang arahnya tegak lurus pada l, dan menyatakan tegangan permukaan, maka persamaannya adalah sebagai berikut. • • • γ = f/l Keterangan: F : gaya (N) l : panjang permukaan (m) γ : tegangan permukaan (N/m) • Persamaan di atas menunjukkan bahwa ketika kita mengatakantegangan permukaan suatu cairan sabun 40 dyne/cm, ini artinya yang bekerja pada tiap cm panjang lapisan sabun adalah 40 dyne.

• Contoh 1: • Panjang bidang permukaan cairan = 5 cm • Massa yang diperlukan untuk memecah film dari larutan sabun sepanjang 5 cm = 0. 5 g. • Berapa γ larutan sabun tsb. • Jawab: • γ= 0. 5 g X 981 cm/detik 2 / 2 L = (0. 5 X 981)/10 • = 49 dyne/cm
Pengertian ADHESI VS KOHESI

• GAYA ANTARMUKA SELALU LEBIH KECIL DARI PADA GAYA PERMUKAAN, KARENA GAYA ADHESI. • CONTOH: • CAIRAN WATER-ALKOHOL, BERCAMPUR SEMPURNA, MAKA HARGA TEGANGAN ANTARMUKA WATER DAN ALKOHOL TIDAK ADA, ATAU NOL
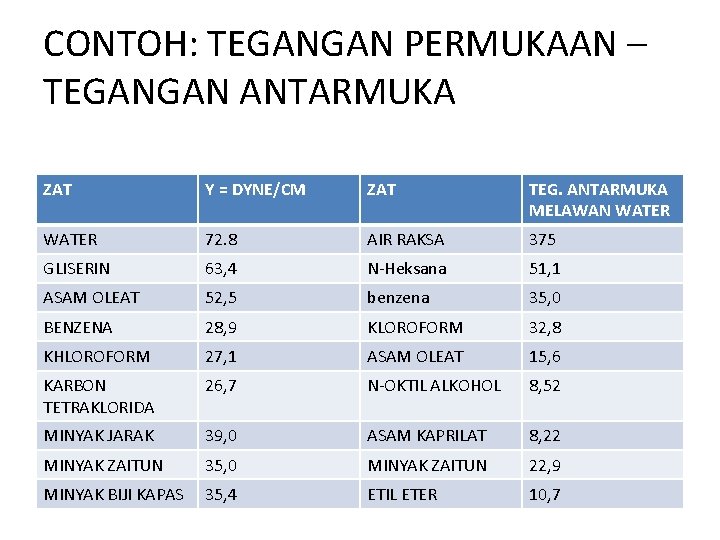
CONTOH: TEGANGAN PERMUKAAN – TEGANGAN ANTARMUKA ZAT Y = DYNE/CM ZAT TEG. ANTARMUKA MELAWAN WATER 72. 8 AIR RAKSA 375 GLISERIN 63, 4 N-Heksana 51, 1 ASAM OLEAT 52, 5 benzena 35, 0 BENZENA 28, 9 KLOROFORM 32, 8 KHLOROFORM 27, 1 ASAM OLEAT 15, 6 KARBON TETRAKLORIDA 26, 7 N-OKTIL ALKOHOL 8, 52 MINYAK JARAK 39, 0 ASAM KAPRILAT 8, 22 MINYAK ZAITUN 35, 0 MINYAK ZAITUN 22, 9 MINYAK BIJI KAPAS 35, 4 ETIL ETER 10, 7

FAKTOR-FAKTOR YG MEMPENGARUHI TEGANGAN PERMUKAAN/ANTAR MUKA • A. JENIS CAIRAN: WATER KARENA GAYA INTERMOLECULER NYA BESAR, GAYA PERMUKAAN JUGA besar. SEBALIKNYA BENSIN γ= KECIL • B. SUHU NAIK, MAKA γ KECIL, KARENA ANTAR MOLEKUL SALING BERGERAK CEPAT DAN MENJAUH SATU DENGAN YG LAIN, SHG γ KECIL

• C. ADANYA ZAT TERLARUT • Adanya zat terlarut pada cairan dapat menaikkan ataumenurunkan tegangan permukaan. Untuk air adanya elektrolit anorganik dan non elektrolit tertentu seperti sukrosa dan gliserin menaikkan tegangan permukaan. Sedangkan adanya zat-zat seperti sabun, detergen, dan alkohol adalah efektif dalammenurunkan tegangan permukaan ( Yazid, 2005)

• D. Surfaktan (surface active agents), zat yang dapat mengaktifkan permukaan, karena cenderung untuk terkonsentrasi pada permukaan atau antar muka. Surfaktan mempunyai orientasi yang jelas sehingga cenderung pada rantai lurus. Sabun merupakan salah satu contoh dari surfaktan.

• E. KONSENTRASI ZAT TERLARUT • Konsentrasi zat terlarut (solut) suatu larutan biner mempunyai pengaruh terhadap sifat-sifat larutan termasuk tegangan muka dan adsorbsi pada permukaan larutan. Telah diamati bahwa solut yang ditambahkan kedalam larutan akan menurunkan tegangan muka, karena mempunyai konsentrasi dipermukaan yang lebih besar daripada didalam larutan. Sebaliknya solut yang penambahannya kedalam larutan menaikkan tegangan muka mempunyai konsentrasi dipermukaan yang lebih kecil daripada didalam larutan.
ENERGI BEBAS PERMUKAAN • PENGERTIAN: ENERGI BEBAS YANG BEKERJA DI SUATU PERMUKAAN ZAT

• PERSAMAAN: γ = fb / 2 L • BILA LUAS PERMUKAAN, ABCD DIPERLUAS menjadi JARAK ds karena ditarik oleh gaya f KE BAWAH, MAKA KERJA d. W (gaya dikalikan jarak) • d. W = f X ds = γ X 2 L X ds; karena 2 L X ds = d. A • Maka d. W = γ X d. A; SEHINGGA • W = Energi Bebas Permukaan = γ Δ A

Contoh 2 • BERAPA W yang DIPERLUKAN UNTUK MEMPERLUAS PERMUKAAN 10 CM 2, MAKA • W = 49 dyne/cm X 10 cm 2 =490 erg • Erg adalah satuan energi bebas permukaan.

Teknik mengukur tegangan permukaan • METODE KENAIKAN KAPILER: • γ= ½ rhρg • CONTOH 3: • CAIRAN KLOROFORM naik h 3, 67 cm @ 20 o. C dalam jari 2 tabung kapiler 0, 01 cm, ρ=1, 476 g/cm 3. Berapa γ? γ= ½ x 0, 01 x 3, 67 x 1, 476 x 981 cm/detik 2 = 26, 6 g. cm/detik 2 cm = 26, 6 dyne/cm

• Teknik mengukur tegangan permukaan yang lain: 1. Cincin Du Nuouy 2. Tetes (Weight – Drop)

• Ring (Du Nouy) Tensiometer the principle of the instrument depends on the fact that: the force necessary to detach a platinum-iridium ring immersed at the surface or interface is proportional to the surface or interfacial tension. • The force of detachment is recorded in dynes on a calibrated dial The surface tension is given by: Where: F = the detachment force R 1 and R 2= the inner and outer radii of the ring. γ = F / 2 π (R 1 + R 2) For measuring surface and interfacial tensions.
- Slides: 22