Szilrd fzis peptidszintzis polisztiroldivinilbenzol gyantn x funkcionalizls x
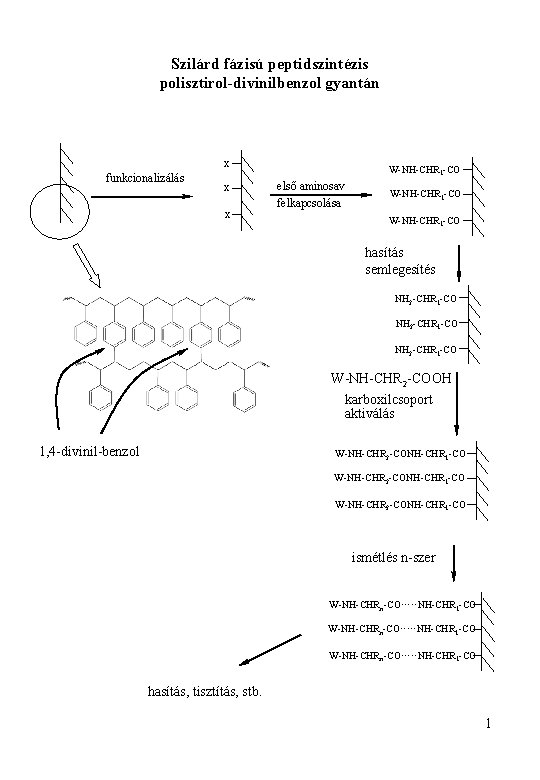
Szilárd fázisú peptidszintézis polisztirol-divinilbenzol gyantán x funkcionalizálás x x W-NH-CHR 1 -CO első aminosav felkapcsolása W-NH-CHR 1 -CO hasítás semlegesítés NH 2 -CHR 1 -CO W-NH-CHR 2 -COOH karboxilcsoport aktiválás 1, 4 -divinil-benzol W-NH-CHR 2 -CONH-CHR 1 -CO ismétlés n-szer W-NH-CHRn-CO·····NH-CHR 1 -CO hasítás, tisztítás, stb. 1

Szükséges feltételek a sikeres szilárd fázisú peptidszintézishez A) Hordozó polimer 1. Tartalmazzon funkcionalizálható reaktív rész 2. A kialakított peptid-polimer kötés hatékonyan hasítható legyen 3. Stabil legyen fizikai behatásokra és a kémiai szintézis körülményei között 4. A növekvő peptidlánc jó hozzáférhetősége az oldószerek és a reagensek számára B) Védőcsoport kombináció 1. A peptid-polimer kötés stabil legyen végig a szintézis alatt 2. Átmeneti a-aminocsoport védelem 3. A szintézis során stabil oldallánc védőcsoportok 4. A peptid-polimerkötés és az oldallánc védőcsoportok egylépéses hatékony hasíthatósága C) Reagensek 1. Aktiválószerk 2. Hasítóelegyek 2
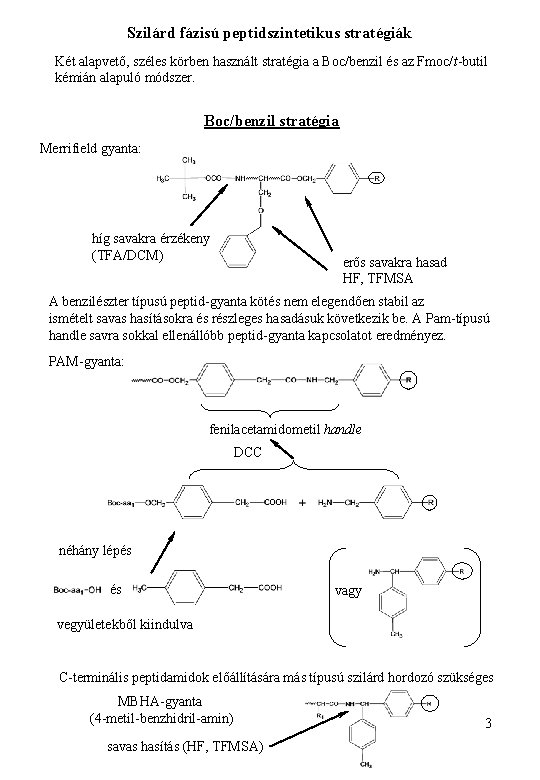
Szilárd fázisú peptidszintetikus stratégiák Két alapvető, széles körben használt stratégia a Boc/benzil és az Fmoc/t-butil kémián alapuló módszer. Boc/benzil stratégia Merrifield gyanta: híg savakra érzékeny (TFA/DCM) erős savakra hasad HF, TFMSA A benzilészter típusú peptid-gyanta kötés nem elegendően stabil az ismételt savas hasításokra és részleges hasadásuk következik be. A Pam-típusú handle savra sokkal ellenállóbb peptid-gyanta kapcsolatot eredményez. PAM-gyanta: fenilacetamidometil handle DCC néhány lépés és vagy vegyületekből kiindulva C-terminális peptidamidok előállítására más típusú szilárd hordozó szükséges MBHA-gyanta (4 -metil-benzhidril-amin) savas hasítás (HF, TFMSA) 3
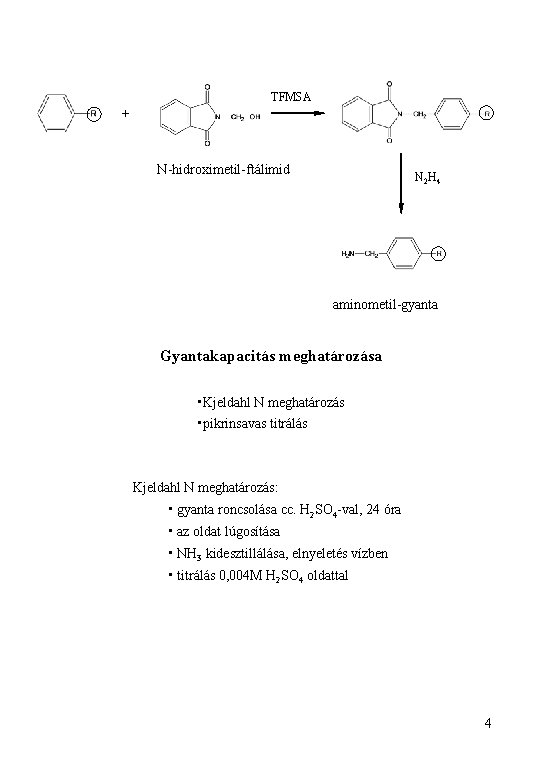
TFMSA + N-hidroximetil-ftálimid N 2 H 4 aminometil-gyanta Gyantakapacitás meghatározása • Kjeldahl N meghatározás • pikrinsavas titrálás Kjeldahl N meghatározás: • gyanta roncsolása cc. H 2 SO 4 -val, 24 óra • az oldat lúgosítása • NH 3 kidesztillálása, elnyeletés vízben • titrálás 0, 004 M H 2 SO 4 oldattal 4
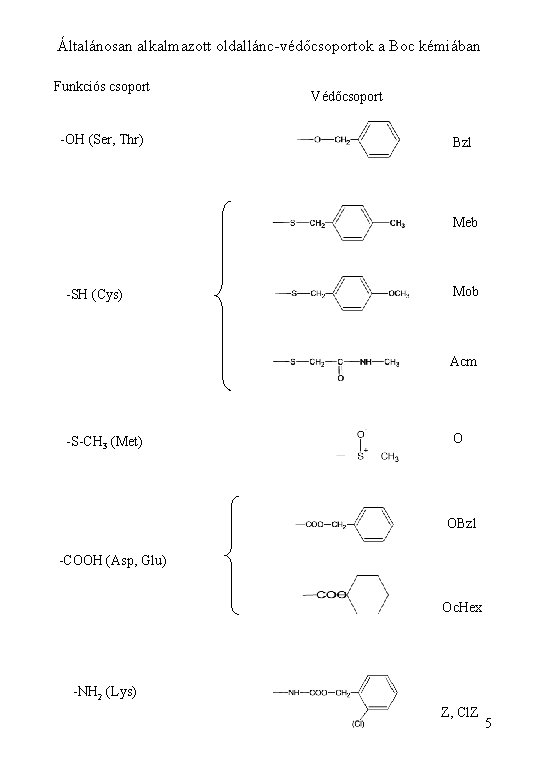
Általánosan alkalmazott oldallánc-védőcsoportok a Boc kémiában Funkciós csoport -OH (Ser, Thr) Védőcsoport Bzl Meb -SH (Cys) Mob Acm -S-CH 3 (Met) O OBzl -COOH (Asp, Glu) Oc. Hex -NH 2 (Lys) Z, Cl. Z 5
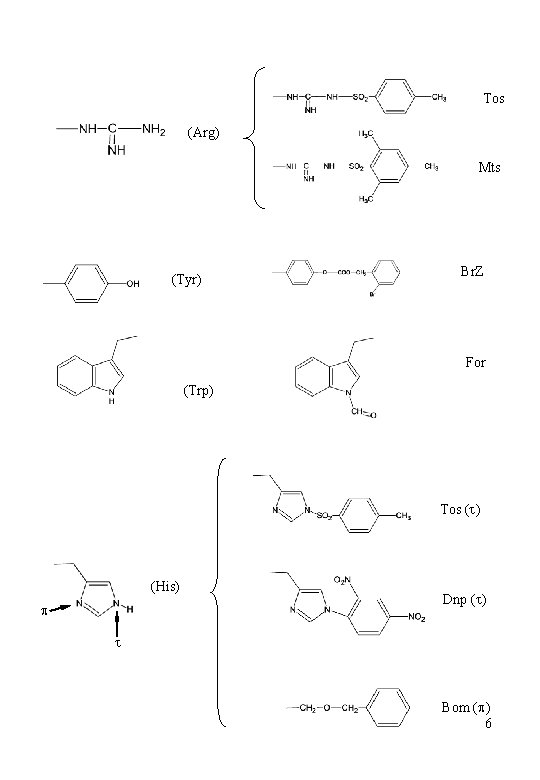
Tos (Arg) Mts (Tyr) Br. Z For (Trp) Tos (t) (His) p Dnp (t) t Bom (p) 6

Boc-szintézis protokollja I. Peptid szekvencia: MW (védett peptid): (szabad peptid): II. Kiindulási polimer szubsztitúció (mmol/g): gyanta mennyiség (g): össz. mmol: Boc (PAM-gyanta) III. Lánchosszabbítás DCC/HOBt eljárással Aminosav dátum: Boc-származék idő (perc) A. hasítás 35% TFA/DCM 2 20 B. mosás DCM 1 10% DIEA/DCM 1 C. semlegesítés D. mosás E kapcsolás ismétlés Boc-aminosav (3 ekv, g) minimális térfogat DCM DCC/HOBt (3 ekv, g) minimális térfogat DMF 30 F. mosás DMF 1 G. mosás DCM 1 ninhidrin negatív pozitív H. ellenőrzés / MW: reagens/oldószer lépés / Negatív teszt: folytatás az A lépéstől a következő aminosav-származékkal Pozitív teszt: újrakapcsolás (ismétlés a C lépéstől) 7
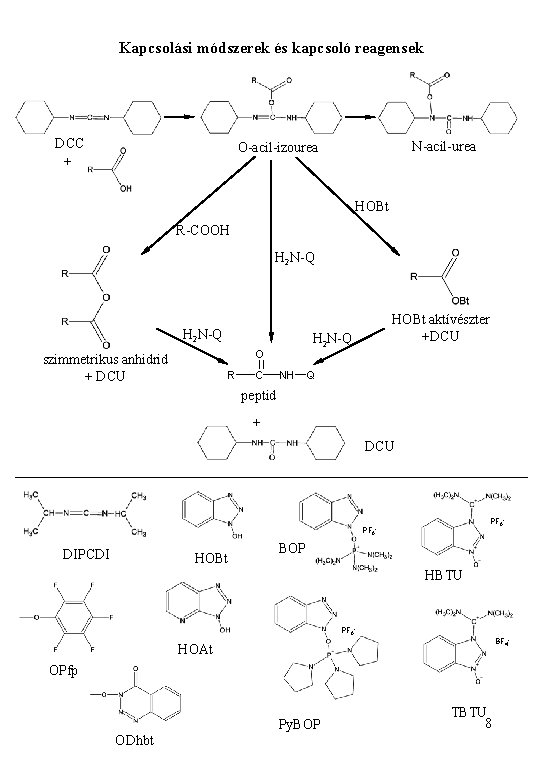
Kapcsolási módszerek és kapcsoló reagensek DCC + N-acil-urea O-acil-izourea HOBt R-COOH H 2 N-Q O szimmetrikus anhidrid + DCU R C HOBt aktívészter +DCU NH Q peptid + DCU PF 6 - DIPCDI HOBt BOP HBTU PF 6 BF 4 - HOAt OPfp Py. BOP ODhbt TBTU 8
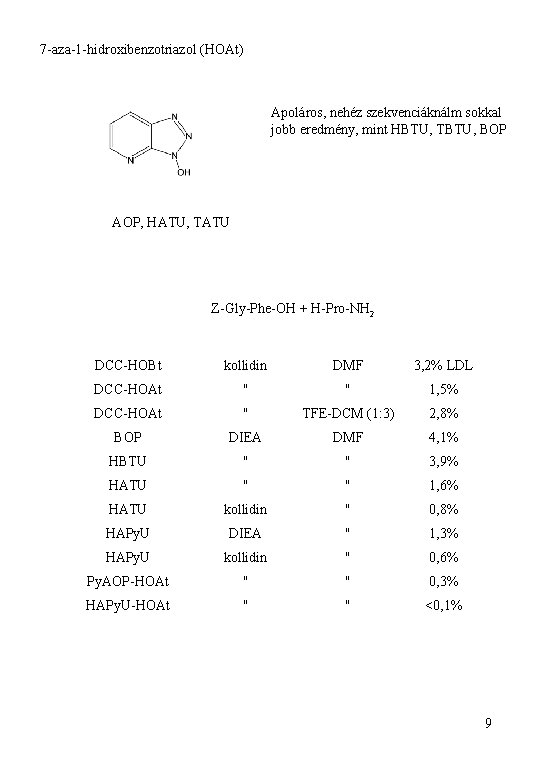
7 -aza-1 -hidroxibenzotriazol (HOAt) Apoláros, nehéz szekvenciáknálm sokkal jobb eredmény, mint HBTU, TBTU, BOP AOP, HATU, TATU Z-Gly-Phe-OH + H-Pro-NH 2 DCC-HOBt kollidin DMF 3, 2% LDL DCC-HOAt " " 1, 5% DCC-HOAt " TFE-DCM (1: 3) 2, 8% BOP DIEA DMF 4, 1% HBTU " " 3, 9% HATU " " 1, 6% HATU kollidin " 0, 8% HAPy. U DIEA " 1, 3% HAPy. U kollidin " 0, 6% Py. AOP-HOAt " " 0, 3% HAPy. U-HOAt " " <0, 1% 9

In situ semlegesítés Schnölzer M. et al. : Int J Pept Protein Res. 40, 180 (1992) Problémák a semlegesítés és a kapcsolás alatt: • C-terminális 1 v. 2 pozícióban Pro diketopiperazin képződés, dipeptidvesztés a gyantáról • piroglutaminsav képződés • láncletörés HBTU v. TBTU kapcsolódás útján • acetileződés (Boc-AA-k Et. OAc-ból kristályosítva bomlástermékként HOAc-t tartalmaz 100% TFA hasítás 2 x 1 perc DMF mosás folyamatos v. többször kapcsolás, aktivált Boc-AA, DIEA 10 perc DMF mosás DIC/HOBt esetén 1, 5 ekv DIEA a gyantakapacitásra számolva HBTU esetén pl. 0, 2 mmol gyanta, 0, 8 mmol Boc-AA-OH 0, 76 mmol HBTU, 1, 2 mmol DIEA A problémákat kiküszöbölték és racemizációt sem tapasztaltak! 10
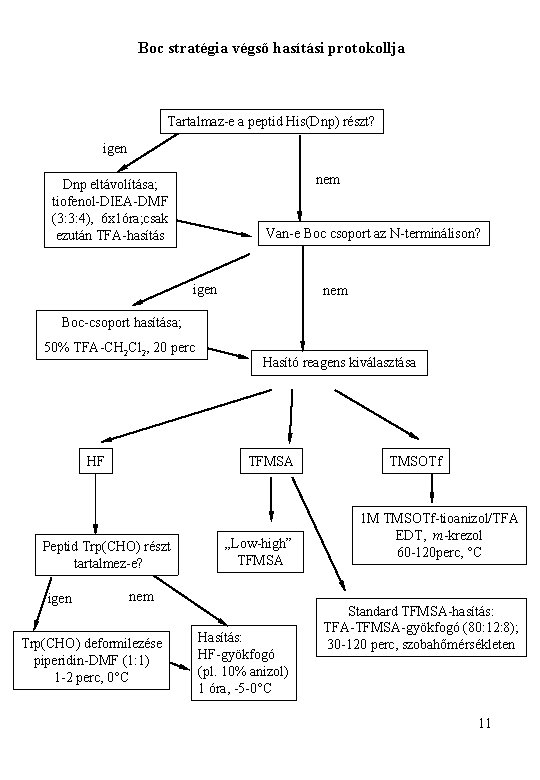
Boc stratégia végső hasítási protokollja Tartalmaz-e a peptid His(Dnp) részt? igen nem Dnp eltávolítása; tiofenol-DIEA-DMF (3: 3: 4), 6 x 1óra; csak ezután TFA-hasítás Van-e Boc csoport az N-terminálison? igen nem Boc-csoport hasítása; 50% TFA-CH 2 Cl 2, 20 perc HF TFMSA Peptid Trp(CHO) részt tartalmez-e? igen Hasító reagens kiválasztása „Low-high” TFMSA nem Trp(CHO) deformilezése piperidin-DMF (1: 1) 1 -2 perc, 0°C Hasítás: HF-gyökfogó (pl. 10% anizol) 1 óra, -5 -0°C TMSOTf 1 M TMSOTf-tioanizol/TFA EDT, m-krezol 60 -120 perc, °C Standard TFMSA-hasítás: TFA-TFMSA-gyökfogó (80: 12: 8); 30 -120 perc, szobahőmérsékleten 11
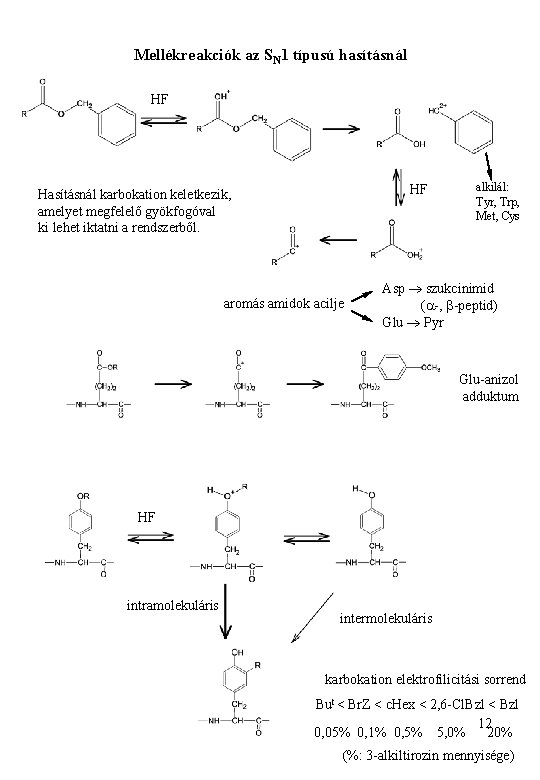
Mellékreakciók az SN 1 típusú hasításnál HF HF Hasításnál karbokation keletkezik, amelyet megfelelő gyökfogóval ki lehet iktatni a rendszerből. aromás amidok acilje alkilál: Tyr, Trp, Met, Cys Asp szukcinimid (a-, b-peptid) Glu Pyr Glu-anizol adduktum HF intramolekuláris intermolekuláris karbokation elektrofilicitási sorrend But < Br. Z < c. Hex < 2, 6 -Cl. Bzl < Bzl 12 0, 05% 0, 1% 0, 5% 5, 0% 20% (%: 3 -alkiltirozin mennyisége)
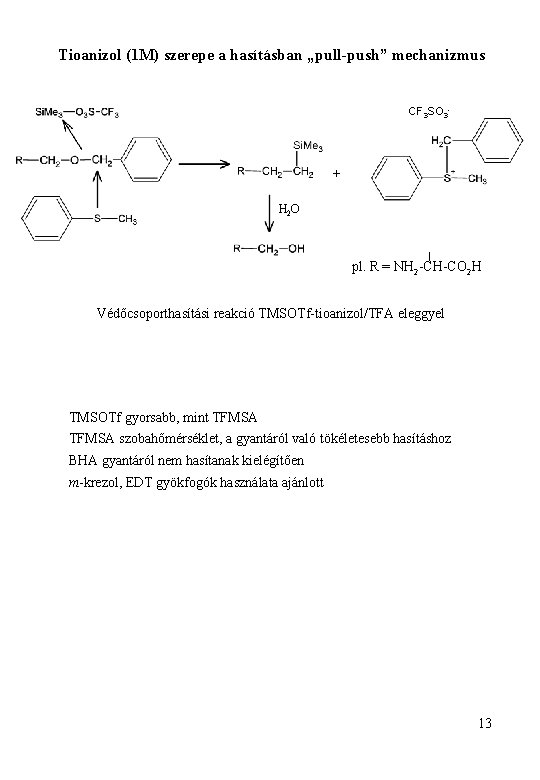
Tioanizol (1 M) szerepe a hasításban „pull-push” mechanizmus CF 3 SO 3 - + H 2 O pl. R = NH 2 -CH-CO 2 H Védőcsoporthasítási reakció TMSOTf-tioanizol/TFA eleggyel TMSOTf gyorsabb, mint TFMSA szobahőmérséklet, a gyantáról való tökéletesebb hasításhoz BHA gyantáról nem hasítanak kielégítően m-krezol, EDT gyökfogók használata ajánlott 13
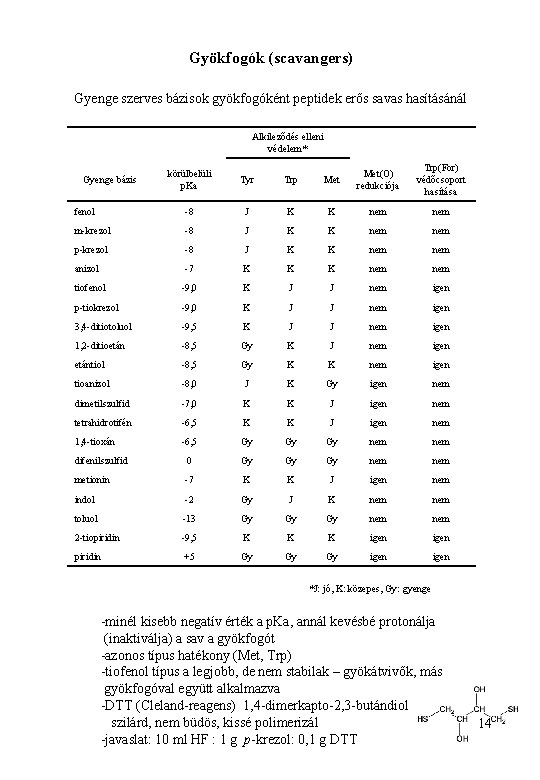
Gyökfogók (scavangers) Gyenge szerves bázisok gyökfogóként peptidek erős savas hasításánál Alkileződés elleni védelem* körülbelüli p. Ka Tyr Trp Met(O) redukciója Trp(For) védőcsoport hasítása fenol -8 J K K nem m-krezol -8 J K K nem p-krezol -8 J K K nem anizol -7 K K K nem tiofenol -9, 0 K J J nem igen p-tiokrezol -9, 0 K J J nem igen 3, 4 -ditiotoluol -9, 5 K J J nem igen 1, 2 -ditioetán -8, 5 Gy K J nem igen etántiol -8, 5 Gy K K nem igen tioanizol -8, 0 J K Gy igen nem dimetilszulfid -7, 0 K K J igen nem tetrahidrotifén -6, 5 K K J igen nem 1, 4 -tioxán -6, 5 Gy Gy Gy nem difenilszulfid 0 Gy Gy Gy nem metionin -7 K K J igen nem indol -2 Gy J K nem toluol -13 Gy Gy Gy nem 2 -tiopiridin -9, 5 K K K igen piridin +5 Gy Gy Gy igen Gyenge bázis *J: jó, K: közepes, Gy: gyenge -minél kisebb negatív érték a p. Ka, annál kevésbé protonálja (inaktiválja) a sav a gyökfogót -azonos típus hatékony (Met, Trp) -tiofenol típus a legjobb, de nem stabilak – gyökátvivők, más gyökfogóval együtt alkalmazva -DTT (Cleland-reagens) 1, 4 -dimerkapto-2, 3 -butándiol szilárd, nem büdös, kissé polimerizál -javaslat: 10 ml HF : 1 g p-krezol: 0, 1 g DTT 14
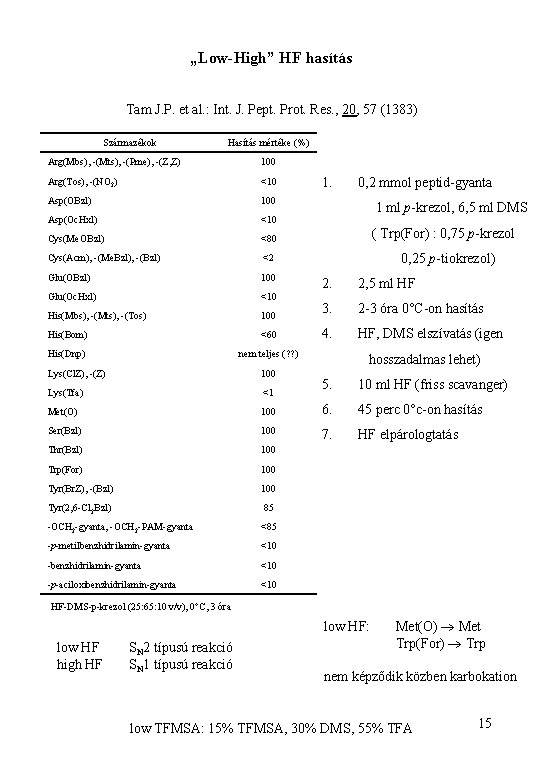
„Low-High” HF hasítás Tam J. P. et al. : Int. J. Pept. Prot. Res. , 20, 57 (1383) Származékok Hasítás mértéke (%) Arg(Mbs), -(Mts), -(Pme), -(Z, Z) 100 Arg(Tos), -(NO 2) <10 Asp(OBzl) 100 Asp(Oc. Hxl) <10 Cys(Me. OBzl) <80 Cys(Acm), -(Me. Bzl), -(Bzl) <2 Glu(OBzl) 100 Glu(Oc. Hxl) <10 His(Mbs), -(Mts), -(Tos) 1. 0, 2 mmol peptid-gyanta 1 ml p-krezol, 6, 5 ml DMS ( Trp(For) : 0, 75 p-krezol 0, 25 p-tiokrezol) 2. 2, 5 ml HF 100 3. 2 -3 óra 0°C-on hasítás His(Bom) <60 4. HF, DMS elszívatás (igen His(Dnp) nem teljes (? ? ) Lys(Cl. Z), -(Z) 100 Lys(Tfa) <1 Met(O) hosszadalmas lehet) 5. 10 ml HF (friss scavanger) 100 6. 45 perc 0°c-on hasítás Ser(Bzl) 100 7. HF elpárologtatás Thr(Bzl) 100 Trp(For) 100 Tyr(Br. Z), -(Bzl) 100 Tyr(2, 6 -Cl 2 Bzl) 85 -OCH 2 -gyanta, -OCH 2 -PAM-gyanta <85 -p-metilbenzhidrilamin-gyanta <10 -p-aciloxibenzhidrilamin-gyanta <10 HF-DMS-p-krezol (25: 65: 10 v/v), 0°C, 3 óra low HF: low HF high HF SN 2 típusú reakció SN 1 típusú reakció Met(O) Met Trp(For) Trp nem képződik közben karbokation low TFMSA: 15% TFMSA, 30% DMS, 55% TFA 15
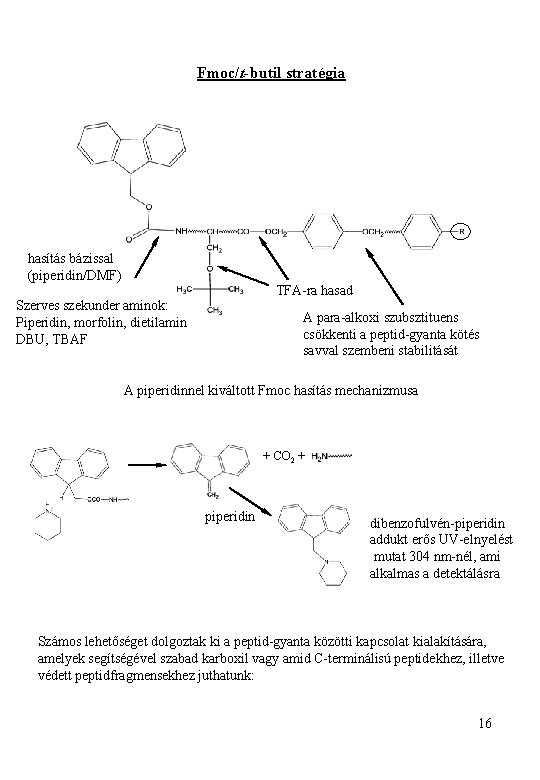
Fmoc/t-butil stratégia hasítás bázissal (piperidin/DMF) TFA-ra hasad Szerves szekunder aminok: Piperidin, morfolin, dietilamin DBU, TBAF A para-alkoxi szubsztituens csökkenti a peptid-gyanta kötés savval szembeni stabilitását A piperidinnel kiváltott Fmoc hasítás mechanizmusa + CO 2 + piperidin dibenzofulvén-piperidin addukt erős UV-elnyelést mutat 304 nm-nél, ami alkalmas a detektálásra Számos lehetőséget dolgoztak ki a peptid-gyanta közötti kapcsolat kialakítására, amelyek segítségével szabad karboxil vagy amid C-terminálisú peptidekhez, illetve védett peptidfragmensekhez juthatunk: 16
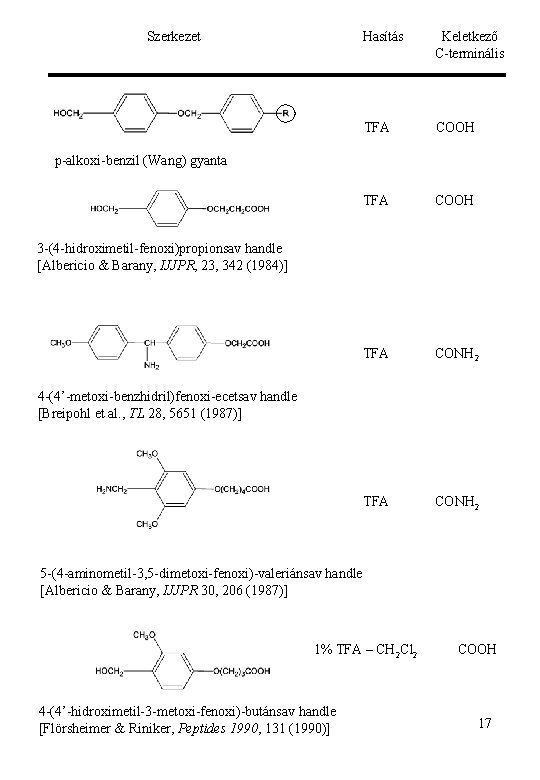
Szerkezet Hasítás Keletkező C-terminális TFA COOH TFA CONH 2 p-alkoxi-benzil (Wang) gyanta 3 -(4 -hidroximetil-fenoxi)propionsav handle [Albericio & Barany, IJJPR, 23, 342 (1984)] 4 -(4’-metoxi-benzhidril)fenoxi-ecetsav handle [Breipohl et al. , TL 28, 5651 (1987)] 5 -(4 -aminometil-3, 5 -dimetoxi-fenoxi)-valeriánsav handle [Albericio & Barany, IJJPR 30, 206 (1987)] 1% TFA – CH 2 Cl 2 4 -(4’-hidroximetil-3 -metoxi-fenoxi)-butánsav handle [Flörsheimer & Riniker, Peptides 1990, 131 (1990)] COOH 17
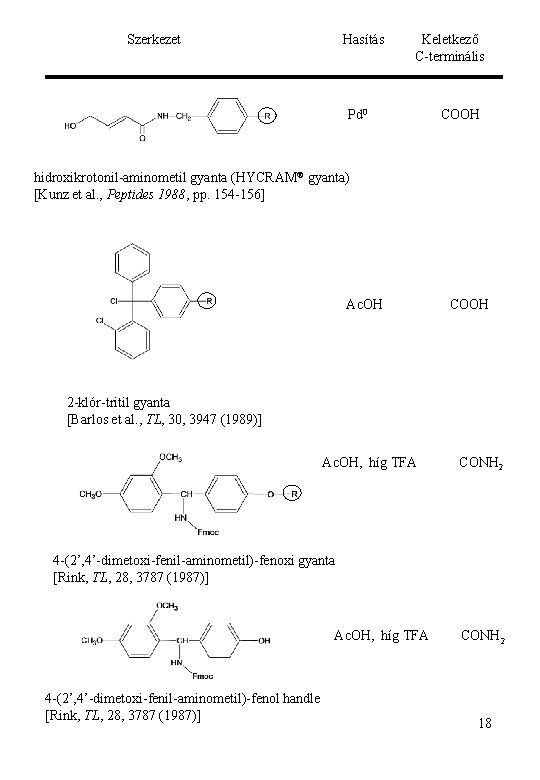
Szerkezet Hasítás Keletkező C-terminális Pd 0 COOH hidroxikrotonil-aminometil gyanta (HYCRAM® gyanta) [Kunz et al. , Peptides 1988, pp. 154 -156] Ac. OH COOH 2 -klór-tritil gyanta [Barlos et al. , TL, 30, 3947 (1989)] Ac. OH, híg TFA CONH 2 4 -(2’, 4’-dimetoxi-fenil-aminometil)-fenoxi gyanta [Rink, TL, 28, 3787 (1987)] Ac. OH, híg TFA 4 -(2’, 4’-dimetoxi-fenil-aminometil)-fenol handle [Rink, TL, 28, 3787 (1987)] CONH 2 18
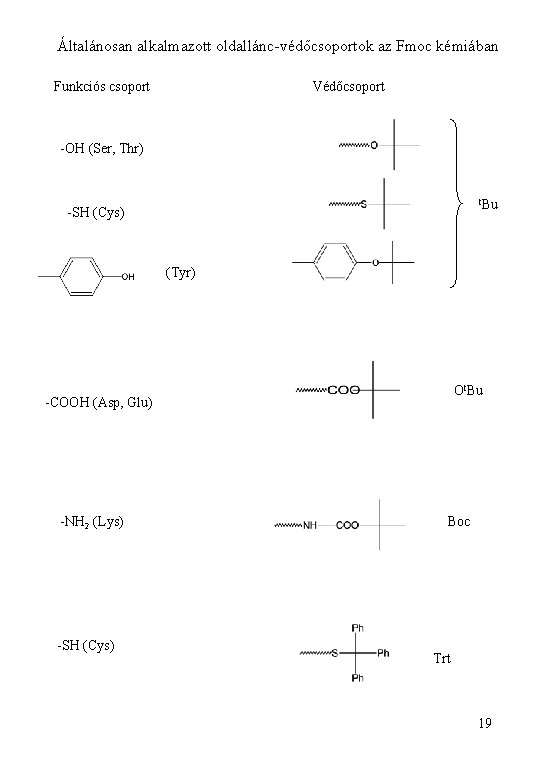
Általánosan alkalmazott oldallánc-védőcsoportok az Fmoc kémiában Funkciós csoport Védőcsoport -OH (Ser, Thr) t. Bu -SH (Cys) (Tyr) Ot. Bu -COOH (Asp, Glu) -NH 2 (Lys) -SH (Cys) Boc Trt 19
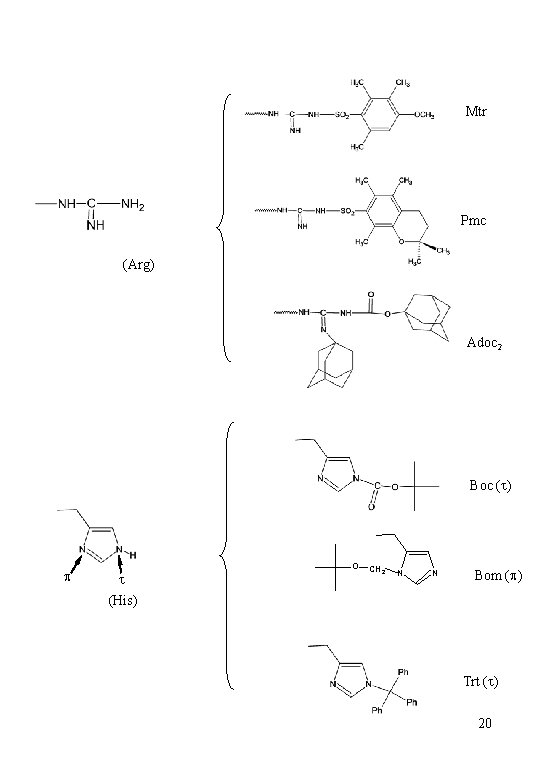
Mtr Pmc (Arg) Adoc 2 Boc (t) t O p CH 2 N N Bom (p) (His) Trt (t) 20

Fmoc-szintézis protokollja I. Peptid szekvencia: MW (védett peptid): (szabad peptid): II. Kiindulási polimer Fmoc -OCH 2 -F-R (Wang-gyanta) szubsztitúció (mmol/g): gyanta mennyiség (g): össz. mmol: III. Lánchosszabbítás DIC/HOBt eljárással Aminosav dátum: Fmoc-származék idő (perc) A. hasítás 20% piperidin/DMF 1 20 B. mosás DMF 1 C. kapcsolás D. mosás E. ellenőrzés / MW: reagens/oldószer lépés / ismétlés Fmoc-aminosav (3 ekv, g) minimális térfogat DMF DIC/HOBt (3 ekv, g) minimális térfogat DMF 30 DMF 1 ninhidrin negatív pozitív Negatív teszt: folytatás az A lépéstől a következő aminosav-származékkal Pozitív teszt: újrakapcsolás (ismétlés a C lépéstől) 21
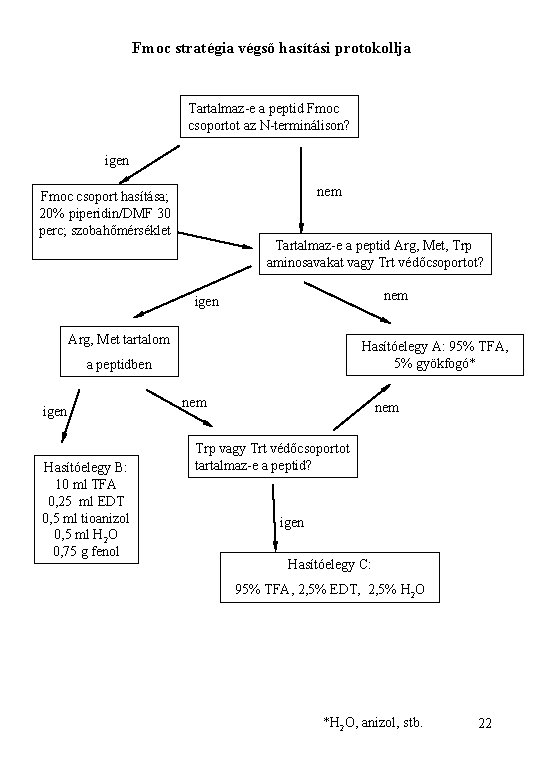
Fmoc stratégia végső hasítási protokollja Tartalmaz-e a peptid Fmoc csoportot az N-terminálison? igen nem Fmoc csoport hasítása; 20% piperidin/DMF 30 perc; szobahőmérséklet Tartalmaz-e a peptid Arg, Met, Trp aminosavakat vagy Trt védőcsoportot? nem igen Arg, Met tartalom Hasítóelegy A: 95% TFA, 5% gyökfogó* a peptidben igen Hasítóelegy B: 10 ml TFA 0, 25 ml EDT 0, 5 ml tioanizol 0, 5 ml H 2 O 0, 75 g fenol nem Trp vagy Trt védőcsoportot tartalmaz-e a peptid? igen Hasítóelegy C: 95% TFA, 2, 5% EDT, 2, 5% H 2 O *H 2 O, anizol, stb. 22
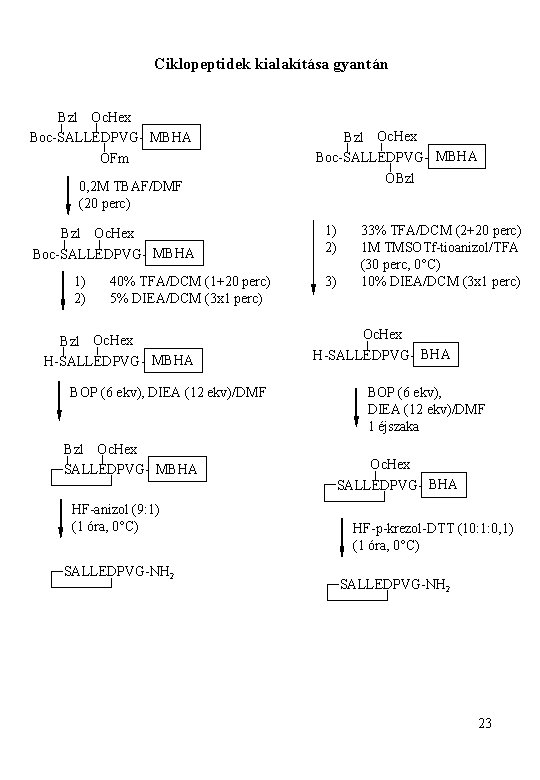
Ciklopeptidek kialakítása gyantán Bzl Oc. Hex Boc-SALLEDPVG- MBHA OFm 0, 2 M TBAF/DMF (20 perc) Bzl Oc. Hex Boc-SALLEDPVG- MBHA 1) 2) 40% TFA/DCM (1+20 perc) 5% DIEA/DCM (3 x 1 perc) Bzl Oc. Hex H-SALLEDPVG- MBHA BOP (6 ekv), DIEA (12 ekv)/DMF Bzl Oc. Hex SALLEDPVG- MBHA HF-anizol (9: 1) (1 óra, 0°C) SALLEDPVG-NH 2 Bzl Oc. Hex Boc-SALLEDPVG- MBHA OBzl 1) 2) 3) 33% TFA/DCM (2+20 perc) 1 M TMSOTf-tioanizol/TFA (30 perc, 0°C) 10% DIEA/DCM (3 x 1 perc) Oc. Hex H-SALLEDPVG- BHA BOP (6 ekv), DIEA (12 ekv)/DMF 1 éjszaka Oc. Hex SALLEDPVG- BHA HF-p-krezol-DTT (10: 1: 0, 1) (1 óra, 0°C) SALLEDPVG-NH 2 23
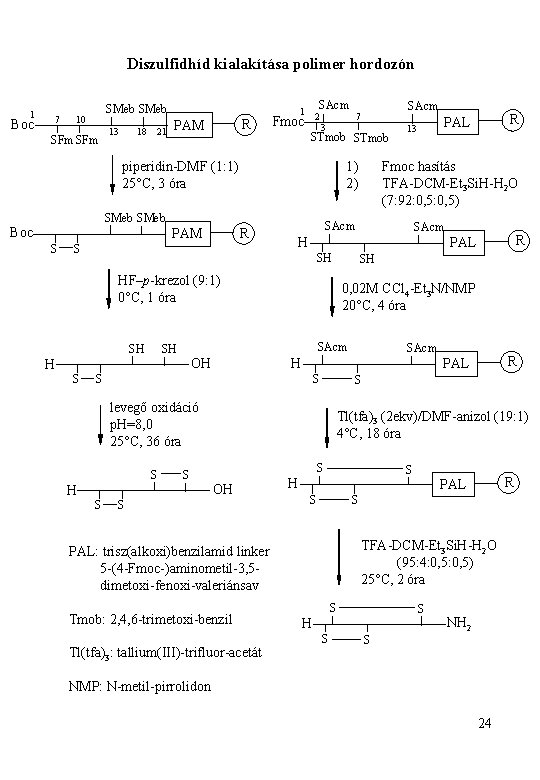
Diszulfidhíd kialakítása polimer hordozón 1 Boc 7 SMeb 10 SFm 13 18 21 R PAM SAcm 1 2 Fmoc 3 STmob 1) 2) piperidin-DMF (1: 1) 25°C, 3 óra SMeb Boc S HF–p-krezol (9: 1) 0°C, 1 óra S levegő oxidáció p. H=8, 0 25°C, 36 óra Tl(tfa)3 (2 ekv)/DMF-anizol (19: 1) 4°C, 18 óra S S OH S R PAL S H SAcm H S S SH SAcm OH R 0, 02 M CCl 4 -Et 3 N/NMP 20°C, 4 óra SH H S SAcm PAL SH SH Fmoc hasítás TFA-DCM-Et 3 Si. H-H 2 O (7: 92: 0, 5) H S R PAL 13 SAcm R PAM SAcm 7 S S H S S TFA-DCM-Et 3 Si. H-H 2 O (95: 4: 0, 5) 25°C, 2 óra PAL: trisz(alkoxi)benzilamid linker 5 -(4 -Fmoc-)aminometil-3, 5 dimetoxi-fenoxi-valeriánsav Tmob: 2, 4, 6 -trimetoxi-benzil Tl(tfa)3: tallium(III)-trifluor-acetát R PAL S S H S NH 2 S NMP: N-metil-pirrolidon 24
- Slides: 24