Periodiska systemet egenskaper reaktioner Samma grupp liknande egenskaper









- Slides: 10

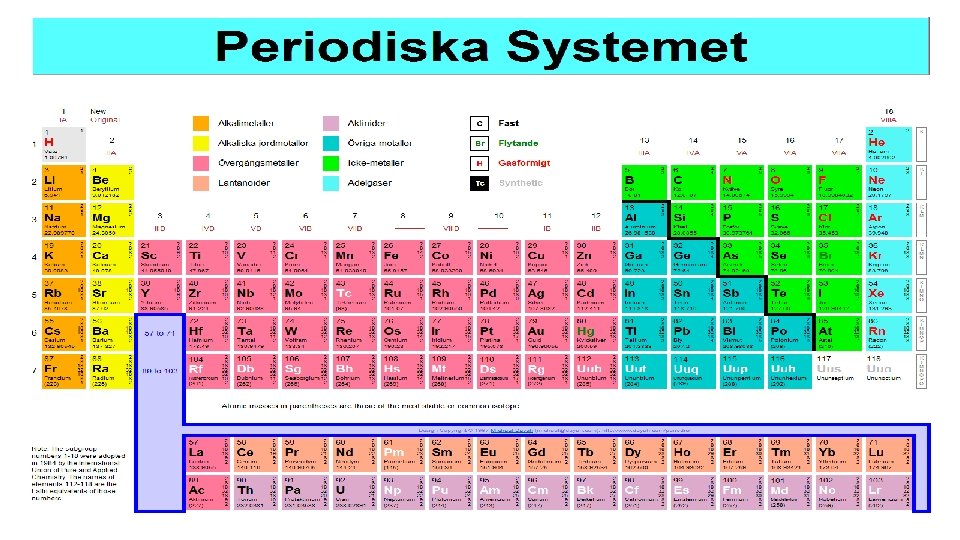
Periodiska systemet – egenskaper, reaktioner

Samma grupp - liknande egenskaper • De grundämnen som står i samma kolumn tillhör samma GRUPP. • Deras atomer har samma antal valenselektroner. • De har därför ofta liknande egenskaper. • Det är vi människor som har grupperat ämnena och därför passar inte alla ämnen in i grupperna.


Grupp 1 Alkalimetallerna • Metallerna i grupp 1 kallas för alkalimetaller. • Det är mjuka metaller som går bra att skära i med kniv. • Varje alkalimetall har en typisk lågfärg • Salter med dessa joner ingår ofta i fyrverkerier.

Reaktiva! • Dom har alla en valenselektron. • Det gör att dom är mycket reaktiva´, reagerar häftigt med andra ämnen. • De bildar då stabilare joner med ädelgasstruktur och laddningen 1+ • Förekommer bara som joner i naturen • Vid reaktion med vatten bildas vätgas och hydroxidjoner. Måste förvaras i fotogen. • Ju länge ner i periodiska systemet ju reaktivare • Alkali, alkalisklösning = basisk lösning

Grupper 3 -12 • Övergångsmetaller • Oftast i fast form ( kvicksilver flytande Hg) • Glänser • Leder ström och värme • Brytts ner i oxidationen (rost)

Halvmetaller • Visa egenskaper som metaller och visa egenskaper som icke metaller fast svagare • Det finns inte någon klar regel för vad som särskiljer en halvmetall från de båda andra grupperna, och ibland klassas några av dem alternativt som rena metaller resp. icke-metaller

Icke metaller • Saknar metalliska egenskaper (leder ej ström, ej glänsande osv) • Kan vara gaser, flytande- eller fastämne (i rumstemperatur) • I bindningar drar de elektronpar (eller hela elektroner till sig)

Grupp 17 Halogenerna • Dessa har 7 valenselektroner och bildar 1 - joner. • Dom är reaktiva och tar gärna en elektron. • I fri form är de giftiga och angriper slemhinnor mm. • Förekommer bara i jonform i naturen, fluorid, klorid, bromid, jodid. • Betyder saltbildare • Jod sublimerar • Brom – flytande, kan orsaka erektionsproblem

Oktettregel • Alla ämnen vill ha fullt uppfylld sina yttersta elektronskal (som har alltid plats bara för 8 valenselektroner) • Väte (H) och Helium (He) är undantagna från denna regel eftersom deras atomer har bara K skalen (som rymmer högst 2 elektroner) • Ämnen strävar för att uppfylla oktettregel på olika sett – kemiska bindningar