KEMISKA FRENINGAR MOLEKYLFRENINGAR eller JONFRENINGAR PERIODISKA SYSTEMET Grupp








- Slides: 15

KEMISKA FÖRENINGAR MOLEKYLFÖRENINGAR eller JONFÖRENINGAR

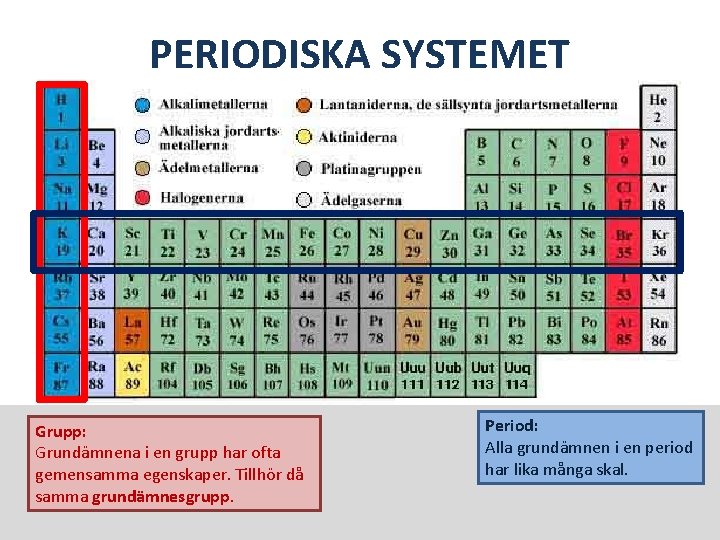
PERIODISKA SYSTEMET Grupp: Grundämnena i en grupp har ofta gemensamma egenskaper. Tillhör då samma grundämnesgrupp. Period: Alla grundämnen i en period har lika många skal.

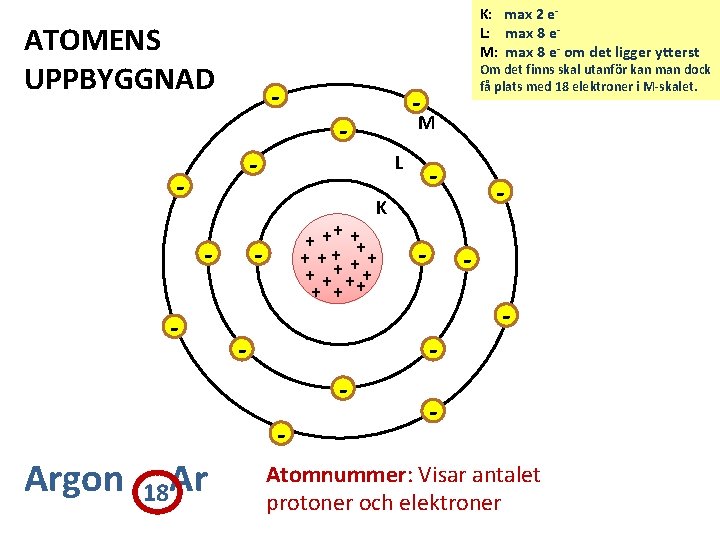
K: max 2 e. L: max 8 e. M: max 8 e- om det ligger ytterst ATOMENS UPPBYGGNAD - - - M L - - K - + ++ + + + +++ + + - 18 Ar - - - Argon Om det finns skal utanför kan man dock få plats med 18 elektroner i M-skalet. - - Atomnummer: Visar antalet protoner och elektroner

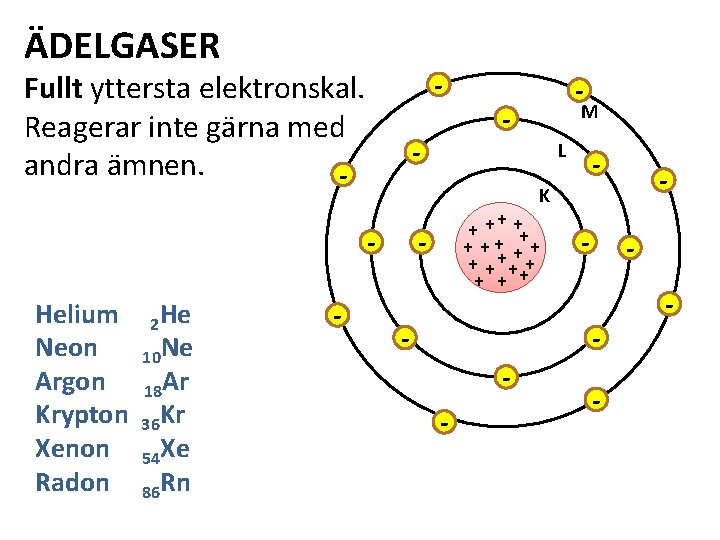
ÄDELGASER - Fullt yttersta elektronskal. Reagerar inte gärna med andra ämnen. - - 2 He 10 Ne 18 Ar 36 Kr 54 Xe 86 Rn - M L - - K Helium Neon Argon Krypton Xenon Radon - + ++ + + + +++ + + - - -

VALENSELEKTRONER • De elektroner som finns i atomens yttersta skal kallas valenselektroner. Obs! Ämnen med fullt yttersta skal (ädelgaser) har inga valenselektroner • Ämnen med få valenselektroner bildar ädelgasstruktur genom att avge sina valenselektroner • Ämnen med många valenselektroner bildar ädelgasstruktur genom att ta upp så många elektroner att de får ädelgasstruktur

HUR KEMISKA FÖRENINGAR BILDAS • Vid kemiska reaktioner strävar ämnena efter att uppnå ädelgasstruktur (fullt yttersta elektronskal) • Detta kan ske på flera sätt: – Molekylförening Atomerna binds samman genom att dela på valenselektroner. – Jonförening Atomerna lämnar ifrån sig eller tar upp elektroner och blir joner. Jonerna hålls sedan ihop av elektriska krafter.

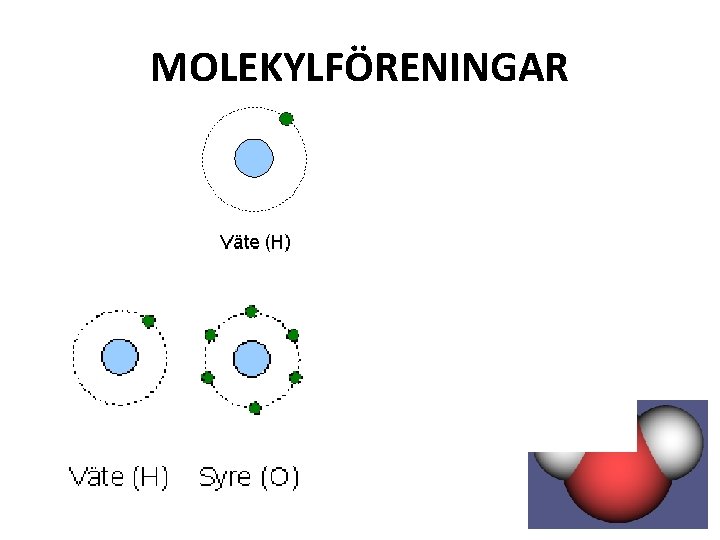
MOLEKYLFÖRENINGAR I molekylföreningar binds atomerna samman genom att dela på elektroner. Det kallas elektronparbindning eller kovalent bindning.

MOLEKYLFÖRENINGAR

JONFÖRENINGAR • Många kemiska föreningar bildas genom att atomerna omvandlas till joner • Jonerna har olika laddningar (+ eller ). • Jonföreningar byggs upp av positiva och negativa joner som hålls samman av elektriska krafter

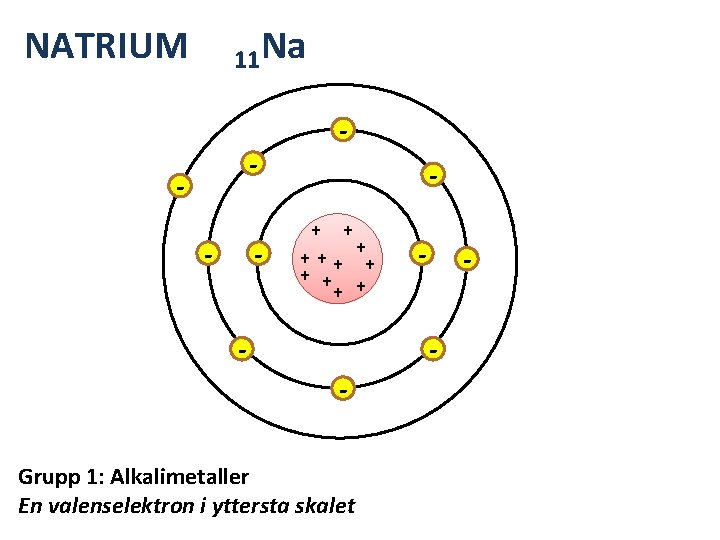
PERIODISKA SYSTEMET Grupp 1: ALKALIMETALLERNA Har en enda elektron i det yttersta skalet. Reagerar lätt med andra ämnen (lämnar ifrån sig elektronen i yttersta skalet). Alla grundämnen i gruppen är metaller utom väte.

NATRIUM 11 Na - - - + +++ + + - - - Grupp 1: Alkalimetaller En valenselektron i yttersta skalet

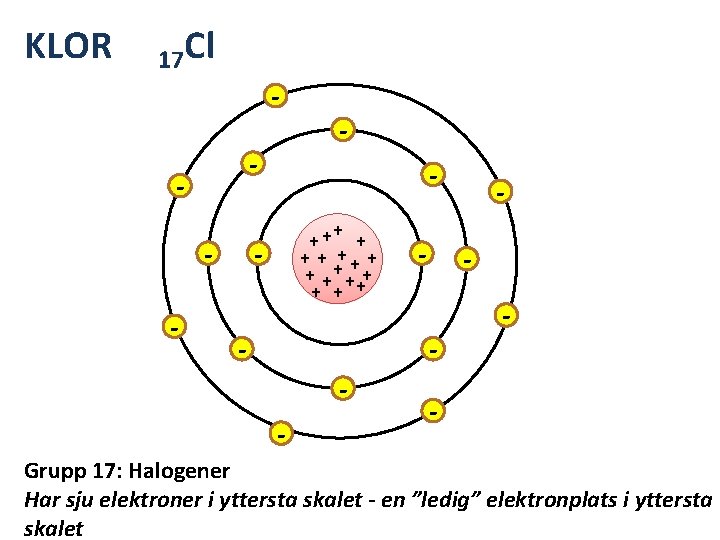
PERIODISKA SYSTEMET Grupp 17: HALOGENERNA Har en ledig elektronplats i yttersta skalet. Bildar gärna kemiska föreningar med andra ämnen (tar då till sig en elektron).

KLOR 17 Cl - - + ++ + + +++ + + - - - - Grupp 17: Halogener Har sju elektroner i yttersta skalet - en ”ledig” elektronplats i yttersta skalet

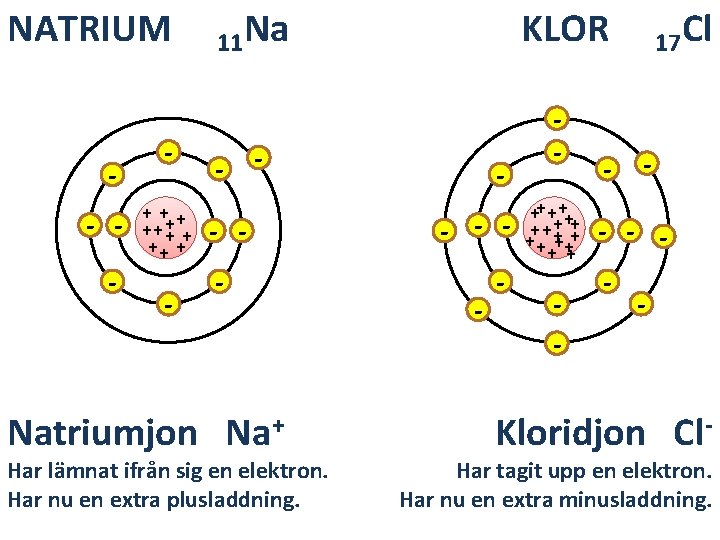
NATRIUM - - +++ + + ++ + - 11 Na - KLOR - - - Natriumjon Na+ Har lämnat ifrån sig en elektron. Har nu en extra plusladdning. - - ++ + + ++ ++ + + - - 17 Cl - - - Kloridjon Cl- Har tagit upp en elektron. Har nu en extra minusladdning.

Natriumkloridkristall • Jonerna har olika elektriska laddningar Natriumjonen: positivt laddad (lämnat ifrån sig en elektron) Kloridjonen: negativt laddad (tagit upp en elektron) • Olika laddningar dras till varandra → de ordnar sig i ett kristallmönster Natriumjon, Na+ Kloridjon, Cl