Parallelen Geschichte der Chemie in den Schularten Antike








- Slides: 14

Parallelen Geschichte der Chemie in den Schularten Antike Empedokles, 450 v. Chr. : die Welt besteht aus vier Elementen. Luft Wasser Lehrplan GS Fach: Heimat- und Sachkunde Grobziel: Kind und Natur Erfahrungen mit Luft (Jgst. 2) Erfahrungen mit Wasser (Jgst. 2) Natürl. Wasserkreislauf (Jgst. 4) Umgang mit Feuer (Jgst. 1) Verbrennung (Jgst. 3) Erde Feuer Lehrplan HS Fach Biologie/Chemie/Physik Erde Wie GS (Jgst. 5– 9) Zu Wasser, Luft, Verbrennung noch: Boden Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

Parallelen Geschichte der Chemie in den Schularten Mittelalter Stoffwissen als „geheime“ Steckbriefe. Stoffe trennen, unterscheiden, kennen (Jgst. 5) und Säuren, Laugen, Salze (Jgst. 8) Neuzeit Lehrpläne für RS und Gymnasium Chemie als Naturwissenschaft PSE (111 Elemente), Verbindungen Reaktionsmechanismen Fachsystematische Orientierung PSE (111 Elemente), Verbindungen Reaktionsmechanismen Ähnlich: Lehrplan HS (Jgst. 10) Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

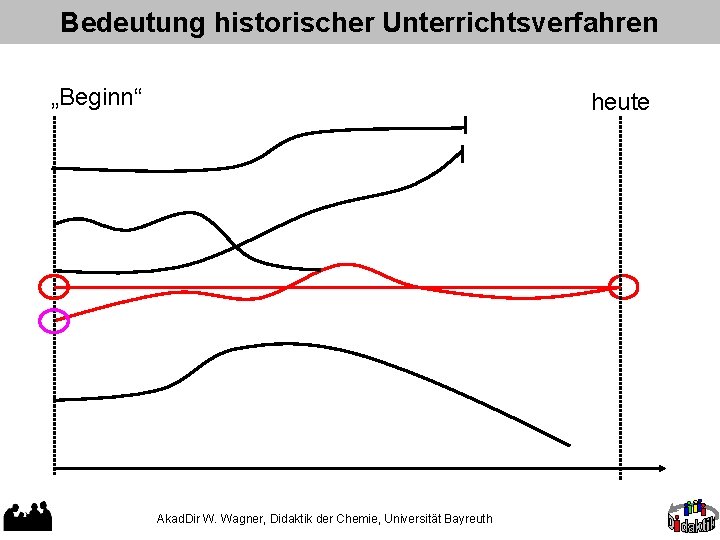
Bedeutung historischer Unterrichtsverfahren „Beginn“ heute Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

Artikulation nach dem historisch-problemorientierten Unterrichtsverfahren Bsp. Realschule: Die Struktur von Benzen (Benzol) Voraussetzungen: Elementarformel Lehrziel: Aufklärung submikroskopische Strukturen, ohne diese direkt zu sehen. Feinziele: • Mehrere Theorien stehen jeweils in Konkurrenz zueinander; Erkennen der begrenzten Gültigkeit. • Erkennen, dass Erkenntnisschwierigkeiten der Forscher früher die gleichen Schwierigkeiten sind, die Schüler heute haben. • Kennen lernen des Menschen im Forscher: Kekulé bzw. van´t Hoff; Menschlich. Allzumenschliches aus der Auseinandersetzung um Theorien (das Aufeinanderprallen von „allgemein anerkannter Lehrmeinung“ und neuer Theorie). Methodische Planung: Sozialform: Gruppenarbeit Modelleinsatz Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

Artikulation nach einem historischen Unterrichtsverfahren Artikulationsstufe 1: Problemstellung Entscheidung erforderlich für eine räumliche Struktur aus einer Reihe denkbarer Artikulationsstufe 2: Information • Das Wissen zur Zeit Kekulés, Ladenburgs, Dewars - Verhältnisformel aus CH-Analyse - Vermutung über den ungesättigten Charakter - Reaktion mit Brom - Substitutionsprodukte. • Aussage moderner theoretischer Modelle heute: - Das Computerprogramm MOLGEN errechnet 217 denkbare Isomere für die Molekülformel C 6 H 6. Artikulationsstufe 3: Lösung des Problems (schülerzentriert) • Arbeitsauftrag: Tragen Sie Argumente für die drei o. a. Strukturvorschläge zusammen! • Arbeitsphase: §Interpretation vorliegender Analysedaten (das Wissen der Zeit). §Errechnen aller denkbaren Strukturen für C 6 H 6 mit Mol. Gen. §Ausschließen von Strukturen auf Grund der Analysedaten. Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

Artikulation nach dem historisch-problemorientierten Unterrichtsverfahren • Diskussion: § Vorstellen der übriggebliebenen Strukturvorschläge. § Vergleich der Argumente. § Entscheidung für die wahrscheinlichste Struktur. Artikulationsstufe 4: Erweiterung, z. B. • Der heutige Stand des Wissens. • Fortbestehende Probleme der modernen Bindungstheorie. • Probleme mit der Schreibweise. • Schicksal von anderen Strukturvorschlägen (Dewar-Benzol 1963 synthetisiert, Ladenburg-Benzol 1973). • Andere Aromaten (Phenol, Naphthalin, Benzoesäure, . . . ) Artikulationsstufe 5: Sicherung • Fixierung theoretischer Grundzüge (Arbeiten mit Modellen, Wandlung von Modellen über die Zeit, Vereinbarungen über Schreibweisen…) Erfolgskontrollen • nach den verschiedenen Anforderungsbereichen I-III Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

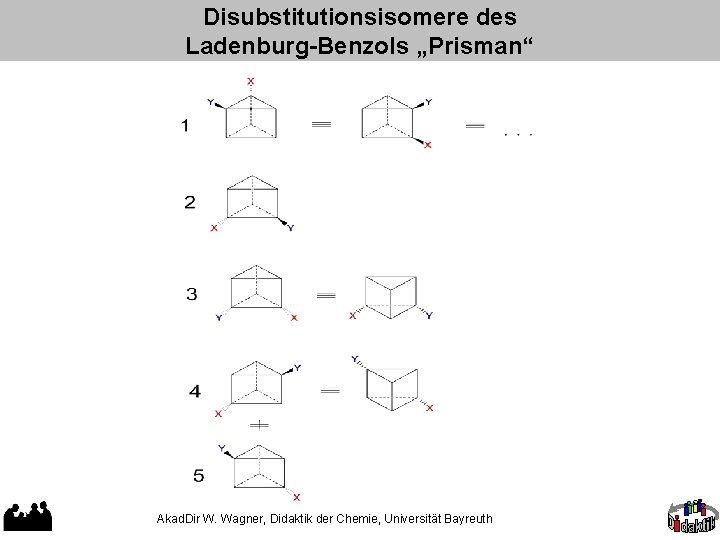
Disubstitutionsisomere des Ladenburg-Benzols „Prisman“ Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

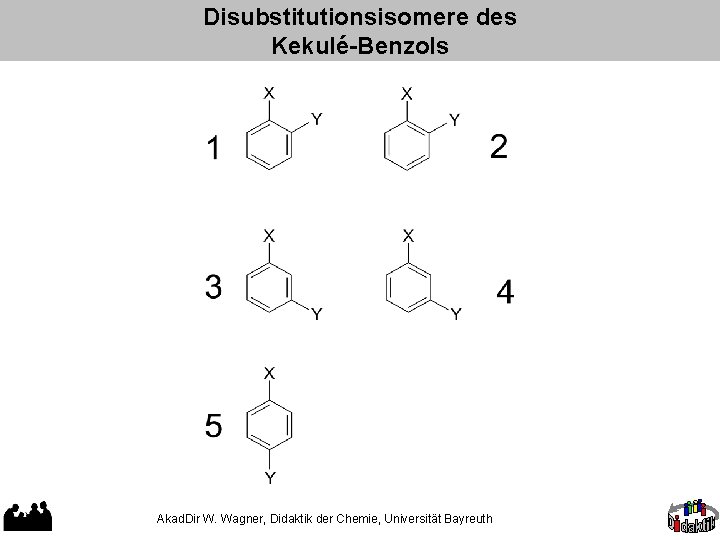
Disubstitutionsisomere des Kekulé-Benzols Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

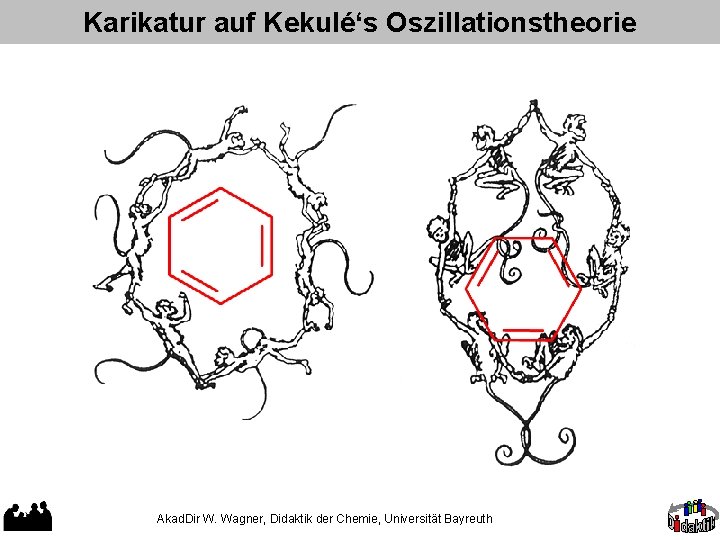
Karikatur auf Kekulé‘s Oszillationstheorie Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

Artikulation nach dem historisch-problemorientierten Unterrichtsverfahren Bsp. Gymnasium: Die Struktur von Methan Voraussetzungen: Elementarformel, Gaschromatographie, Isomerie-Begriff (Stellungsisomerie), Chlorierung Lehrziel: Korrekte Raumstruktur heraus finden, ohne dass man einzelne Moleküle sehen kann. Feinziele: • Mehrere Theorien stehen jeweils in Konkurrenz zueinander; Erkennen der begrenzten Gültigkeit. • Erkennen, dass Erkenntnisschwierigkeiten der Forscher früher die gleichen Schwierigkeiten sind, die Schüler heute haben. • Kennen lernen des Menschen im Forscher: Kekulé bzw. van´t Hoff; Menschlichallzumenschliches aus der Auseinandersetzung um Theorien (das Aufeinanderprallen von „allgemein anerkannter Lehrmeinung“ und neuer Theorie). Methodische Planung: Sozialform: Gruppenarbeit Modelleinsatz Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

Artikulation nach einem historischen Unterrichtsverfahren Artikulationsstufe 1: Problemstellung (lehrerzentriert) Zwei verschiedene räumliche Strukturen von Methan werden diskutiert: die planare und die tetraedrische. Welche ist richtig? Artikulationsstufe 2: Informationsphase Das Wissen von van´t Hoff (Molekülformel aus CH-Analyse, Reaktion mit Chlor, Substitutionsprodukte). Vorstellen von Substitutionsprodukten. Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

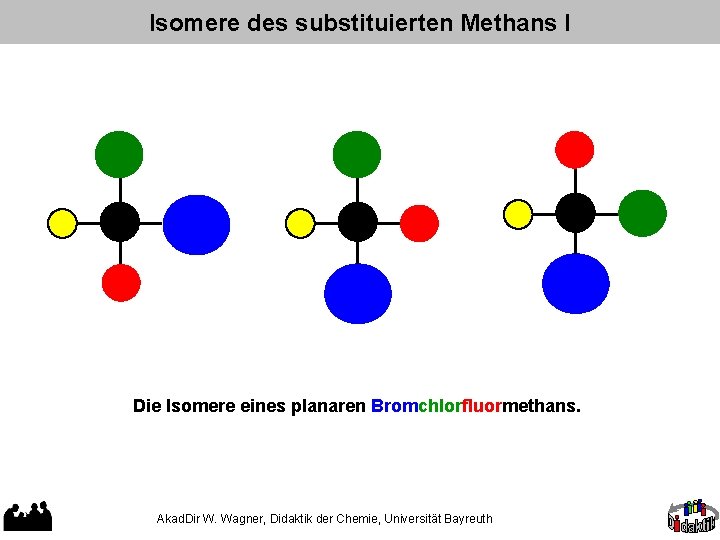
Isomere des substituierten Methans I Die Isomere eines planaren Bromchlorfluormethans. Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

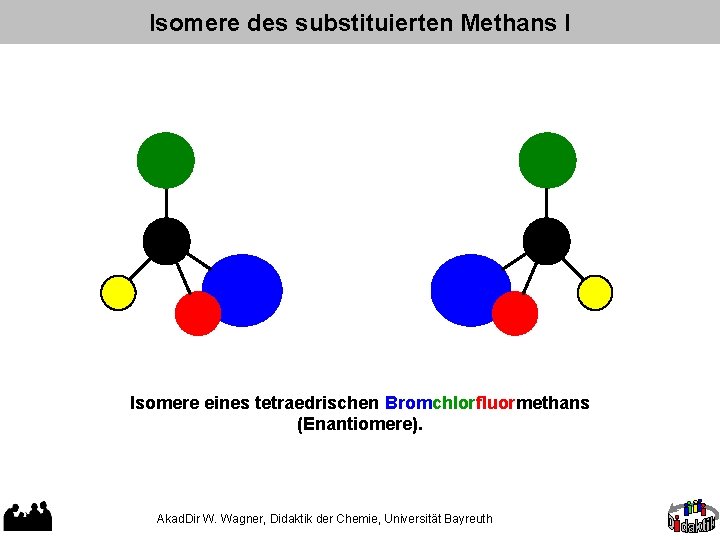
Isomere des substituierten Methans I Isomere eines tetraedrischen Bromchlorfluormethans (Enantiomere). Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth

Artikulation nach einem historischen Unterrichtsverfahren Artikulationsstufe 3: Durchführung (schülerzentriert) • Überprüfen anhand von Modellen, welche Anordnung von 4 Liganden um ein Zentralatom machbar sind. Arbeiten in mehreren Gruppen. Verfolgen der planaren und der tetraedrischen Hypothese. Artikulationsstufe 4: Abstraktion • Erkenntnis verallgemeinert: Moleküle sind nicht planar, sie sind räumlich. • Übertragung auf alle Moleküle. Artikulationsstufe 5: Sicherung Heft- und Tafelskizzen der Methanstruktur Erfolgskontrolle • Wiederholung der Methanstruktur (Anf. Bereich I) • Übertragung auf Tetrachlormethan (Anf. Bereich II) • Übertragung auf Ethan (Anf. Bereich III) Akad. Dir W. Wagner, Didaktik der Chemie, Universität Bayreuth