Mikrofilamenti Mikrofilamenti Mikrofilamentus veido vissmalkkie olbaltumvielu pavedieni To

Mikrofilamenti

Mikrofilamenti Mikrofilamentus veido vissmalkākie olbaltumvielu pavedieni. To diametrs ir apmēram 8 nm. Vislabāk izpētīti ir aktīna mikrofilamenti. Aktīns ir plaši izplatīta olbaltumviela un sastopams visās eikariotiskajās šūnās. Īpaši lielos daudzumos (20% no kopējā šūnas olbaltumvielu daudzuma) aktīns ir atrodams muskuļu šūnās, kur tas rada muskuļu kontrakcijas.

Mikrofilamenti Aktīns šūnās ir atrodams divos veidos: kā atsevišķas globulāras aktīna molekulas (G-aktīns) un fibrillu veidā kā polimerizētas aktīna molekulas (F-aktīns). Noteiktā zonā, pēc atslēgas slēdzenes principa, G-aktīna moleklai ir pievienota ATF molekula.
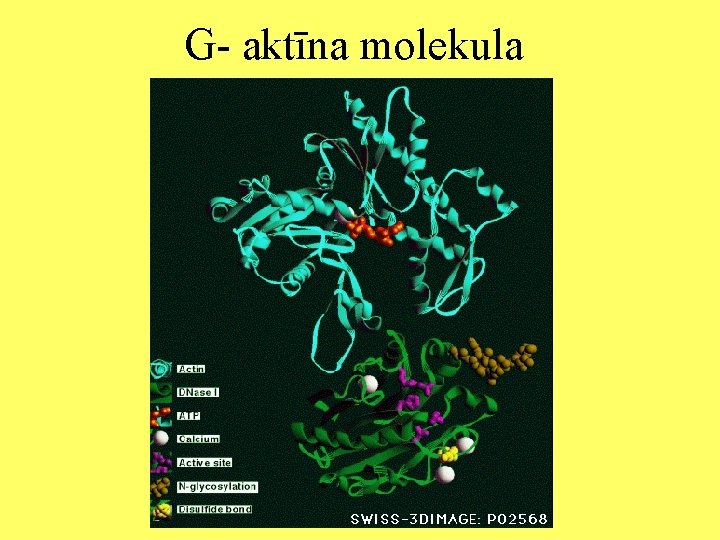
G- aktīna molekula
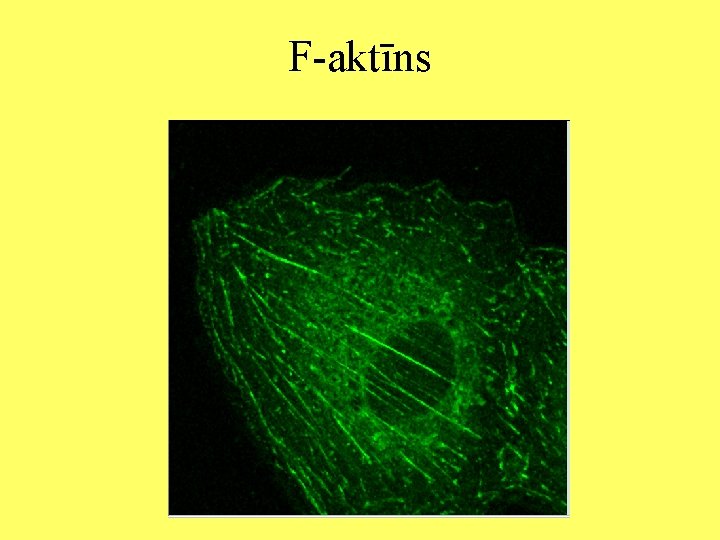
F-aktīns

Aktīna polimerizācija • Jaunu aktīna fibrillu (F-aktīna) veidošanās procesu sauc par nukleāciju. • Esoša aktīna filamenta pagarināšanos sauc par elongāciju. • F-aktīna molekulu kopējais garums daudzkārt pārsniedz šūnas garumu.

Aktīna polimerizācija 2 In vitro apstākļos aktīna polimerizācija ir atkarīga no globulārā aktīna koncentrācijas. Ja tā ir lielāka par kritisko - 0, 1μ 0, 1 M, tad var notikt polimerizācija. Šajos apstākļos molekulu polimerizācijai nav nepieciešama ATF hidrolīze. ATF vietā var izmantot sintētiskus analogus, kuri nevar atdalīt fosfāta grupas.

Aktīna polimerizācija Filma • Axis 292 c 30/The cell

Aktīna polimerizācija 3 Ja globulārā aktīna – ATP kompleksa koncentrācija ir lielāka par kritisko (0, 1 μM “+” galā un 0, 8 μM “-” galā), tad veidojas mikrofilaments. Pārsniedzot kritisko koncentrāciju, monomēru koncentrācija saglabājas nemainīga, bet mikrofilamentu masa proporcionāli pieaug.
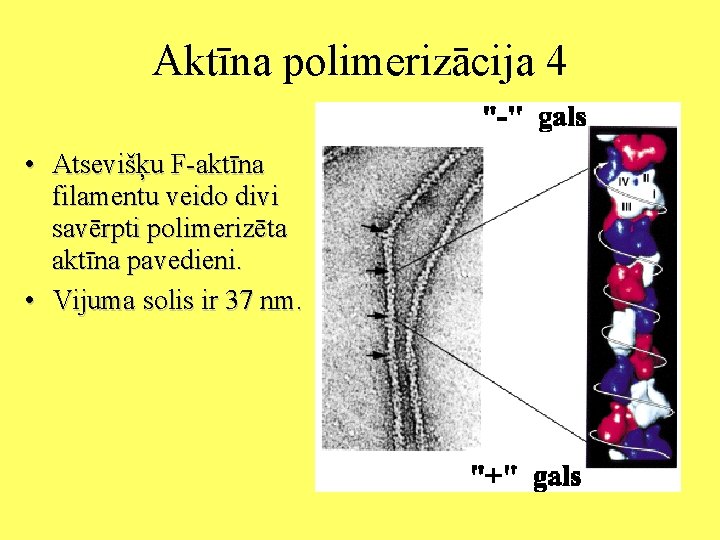
Aktīna polimerizācija 4 • Atsevišķu F-aktīna filamentu veido divi savērpti polimerizēta aktīna pavedieni. • Vijuma solis ir 37 nm.

Aktīna polimerizācija 5 • F-aktīna filamentam izšķir plus galu un mīnus galu. Pie plus gala aktīvāk pievienojas jaunas G-aktīna molekulas, bet no mīnus gala tās aktīvāk atdalās. Pie plus gala pievienojas aktīna molekulas, kuras satur ATF. Mīnus galā ATF hidrolizējas un izveido ADF. Tas vājina saites starp galējo aktīna molekulu un filamentu un tā rezultātā molekula atdalās.
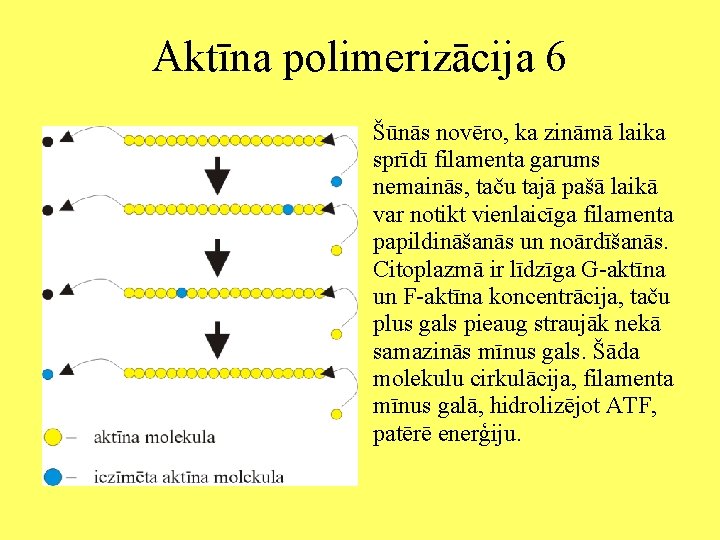
Aktīna polimerizācija 6 Šūnās novēro, ka zināmā laika sprīdī filamenta garums nemainās, taču tajā pašā laikā var notikt vienlaicīga filamenta papildināšanās un noārdīšanās. Citoplazmā ir līdzīga G-aktīna un F-aktīna koncentrācija, taču plus gals pieaug straujāk nekā samazinās mīnus gals. Šāda molekulu cirkulācija, filamenta mīnus galā, hidrolizējot ATF, patērē enerģiju.

Eksperimentos izmantojamās vielas • CITOHALAZĪNS D (sēņu alkaloids) -neļauj mikrofilamenta “+” galā pievienot monomērus • LATRUNKULĪNS - pievienojas G-aktīnam un neļauj šiem monomēriem pievienoties pie filamenta • FALAOIDĪNS - pievienojas G-aktīna monomēriem to savienojuma vietā un stabilizē mikrofilamentus. Izmanto arī kā aktīna specifisku krāsvielu.

Polimerizāciju regulējošie mehānismi • Šūnu no pastiprinātas aktīna polimerizēšanās un depolimerizēšanās pasargā vairāki mehānismi. Tās ir dažādas regulator-olbaltumvielas, kas pievienojās pie aktīna molekulām. Šīs vielas saistās ar globulārajām aktīna molekulām vai ar aktīna mikrofilamentiem. • Salīdzinot kritisko aktīna koncentrāciju un pastāvīgo aktīna koncentrāciju šūnās, var likties, ka praktiski viss aktīns šūnās ir polimerizētā formā. Tomēr dzīvās šūnās tikai 60% aktīna ir fibrillārā formā. To nosaka dažādu citu olbaltumvielu klātbūtne. No pastiprinātas aktīna polimerizācijas šūnas pasargā divas olbaltumvielas timozīns 4 un profilīns.

Polimerizāciju regulējošie mehānismi 2 Timozīns b 4 ir neliela olbaltumviela, kuras molekulmasa ir 5 k. D. Tā var piesaistīties atsevišķām G-aktīna molekulām. Šādi molekulu kompleksi nespēj veidot F-aktīnu. Šūnās eksistē līdzsvars starp šiem četriem veidiem: brīvo Gaktīnu, G-aktīna un timozīna b 4 kompleksu, brīvo timozīnu 4, un F-aktīnu. Izmainot viena komponenta daudzumu, mainīsies arī pārējie. Piemēram, izmantojot mikroinjekcijas metodi, šūnās palielināja timozīna 4 koncentrāciju un tas noveda pie fibrillārā aktīna izzušanas.
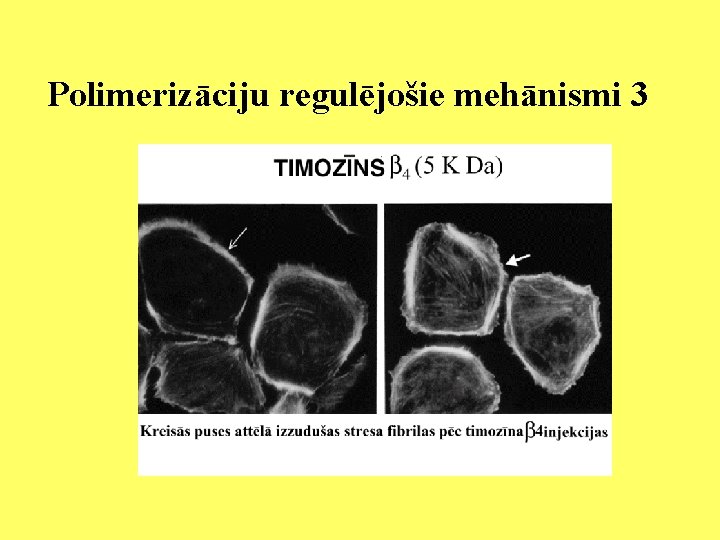
Polimerizāciju regulējošie mehānismi 3

Polimerizāciju regulējošie mehānismi 4

Polimerizāciju regulējošie mehānismi 5 Nedaudz savādākā veidā F-aktīna koncentrāciju regulē profilīns. Tā ir 15 k. D liela olbaltumviela. Tā piesaistās G-aktīna molekulai zonā, kas atrodas tālu no ATFADF pievienošanas saita. Tā kā brīvajām aktīna molekulām, kas satur ADF ir tendence to aizvietot ar ATF, tad var teikt, ka profilīns palīdz saglabāt globulārā formā ATF saturošas aktīna molekulas. Tās aktīna molekulas, kas ir saistītas ar profilīnu ir pasargātas no saistīšanās ar timozīnu. Šādā formā atrodas apmēram 20% no šūnas brīvajām aktīna molekulām.

Polimerizāciju regulējošie mehānismi 6 • Profilīna molekulas var pievienoties arī plazmatiskās membrānas lipīdiem. Tajā gadījumā tās nevar pievienot aktīnu. Ja vides apstākļi liek paātrināt polimerizāciju, tad no membrānām atdalās profilīns. Šūnas signālsistēma nodrošina to atbrīvošanos no membrānas. Tas palīdz G-aktīna molekulām pievienot ATF. Pēc tam aktīna molekulas atbrīvojas no profilīna un plazmatiskās membrānas tuvumā veido F-aktīna pavedienus. • Savukārt, In vitro apstākļos aktīna polimerizāciju stimulē arī K+, Mg 2+ un Ca 2+ jonu koncentrācijas palielināšanās.

Polimerizāciju regulējošie mehānismi 7 • Ar aktīna mikrofilamentiem saistās aktīnu pārraujošās un aktīnu pārklājošās olbaltumvielas (tabula seko). To darbību var pamanīt, vērojot citoplazmas konsistenci dažādās šūnas zonās. Šūnas centrā citoplazma ir šķidrāka (t. i. sola stāvoklī), bet šūnas perifērijā tā ir viskozāka (t. i. gēla stāvoklī). Turklāt šie stāvokļi dažādās šūnas zonās var strauji mainīties. Lielā mērā to nodrošina mikrofilamentu polimerizācija un depolimerizācija. Mikrofilamentu noārdīšanos nodrošina aktīnu pārraujošās olbaltumvielas.

Kofilīns • Pievienojas F-aktīnam • Palīdz atdalīt aktīna -ADF kompleksus • Inhibē ATF/ADF maiņu • Kavē F-aktīna veidošanos • Zināmos apstākļos pārrauj Faktīna ķēdes. • Pēc fosforilācijas atdalās no aktīna-ADF kompleksa

Aktīnu pārraujošās un aktīnu pārklājošās olbaltumvielas 2 • Ar aktīna mikrofilamentiem saistās aktīnu pārraujošās un aktīnu pārklājošās olbaltumvielas. To darbību var pamanīt, vērojot citoplazmas konsistenci dažādās šūnas zonās. Šūnas centrā citoplazma ir šķidrāka (t. i. sola stāvoklī), bet šūnas perifērijā tā ir viskozāka (t. i. gēla stāvoklī). Turklāt šie stāvokļi dažādās šūnas zonās var strauji mainīties. Lielā mērā to nodrošina mikrofilamentu polimerizācija un depolimerizācija. Mikrofilamentu noārdīšanos nodrošina aktīnu pārraujošās olbaltumvielas.

Aktīnu pārraujošās olbaltumvielas • Pie aktīnu pārraujošajām olbaltumvielām pieder gelozīns, severīns un villīns. Šo olbaltumvielu molekulmasa ir lielāka nekā tām olbaltumvielām, kas saistās ar globulāro aktīnu. • Visas šīs olbaltumvielas piestiprinās kādā aktīna mikrofilamenta zonā un pārrauj saiti starp divām blakus stāvošām aktīna molekulām.

Aktīnu pārraujošās olbaltumvielas 2 • Pēc pavediena pārraušanas tās paliek pievienotas pie pavediena „+”gala. Tas neļauj „+” galā šiem mikrofilamentiem pagarināties. Savukārt tas neietekmē pavediena „-” galā notiekošo aktīna polimerizāciju un depolimerizāciju. Gelozīns saistītā stāvoklī saglabājas vairākas nedēļas. Tas samazina brīvā gelozīna koncentrāciju šūnā. Tādējādi šūnas ir pasargātas no pastiprinātas aktīna mikrofilamentu noārdīšanas. Pārrāvējolbaltumvielu aktivitāti regulē Ca 2+ un citu vielu koncentrācija. Tās kļūst aktīvas tikai tad, ja tām pievienojas Ca 2+ joni vai citas regulatorvielas.
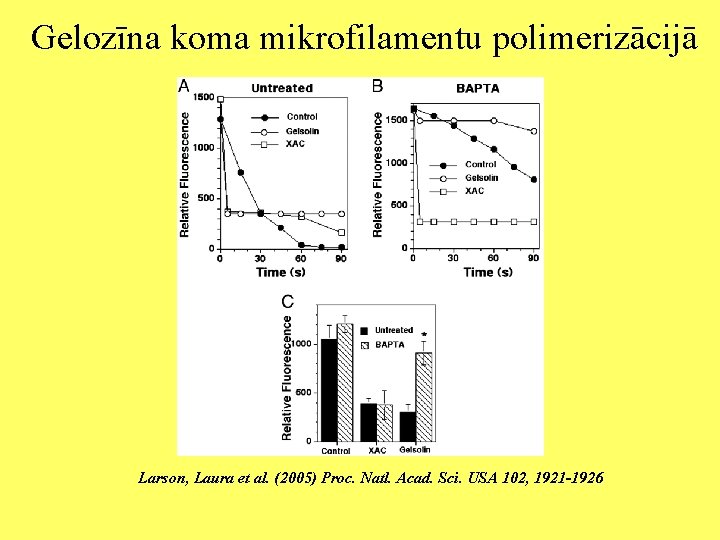
Gelozīna koma mikrofilamentu polimerizācijā Larson, Laura et al. (2005) Proc. Natl. Acad. Sci. USA 102, 1921 -1926

Aktīnu pārklājošās olbaltumvielas • Savukārt no pastiprinātas noārdīšanas mikrofilamentus pasargā aktīnu pārklājošās olbaltumvielas. Tās biežāk ir sastopamas šūnās, kuru skeleta struktūra ir samērā stabila. Šķērssvītroto muskuļu šūnās pie aktīna mikrofilamentu + gala var pievienoties Cap. Z olbaltumvielas. Tās pārtrauc aktīna molekulu atdalīšanos. Tās arī ir ārkārtīgi stabilas un atdalās no mikrofilamenta apmēram pēc trīsdesmit dienām. Pie Aktīna mikrofilamentu stabilitāte palielinās, ja tiem ir pievienotas tropomiozīna molekulas. Tad to “-” galā var vēl piestiprināties tropomodulīna molekulas.
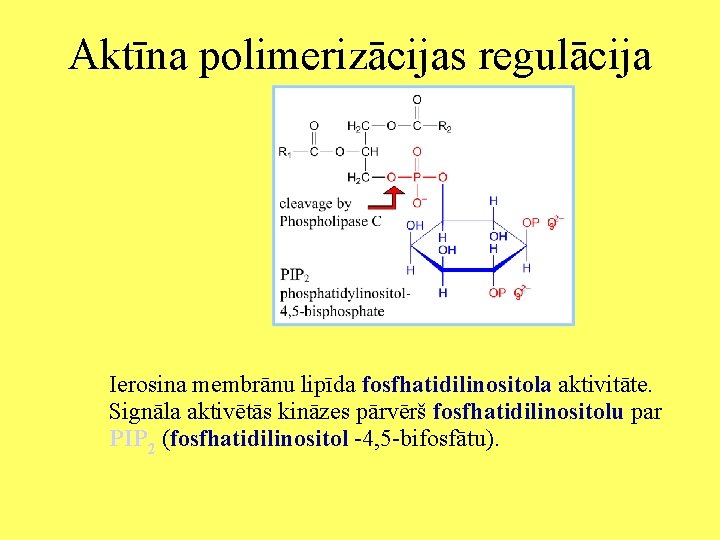
Aktīna polimerizācijas regulācija Ierosina membrānu lipīda fosfhatidilinositola aktivitāte. Signāla aktivētās kināzes pārvērš fosfhatidilinositolu par PIP 2 (fosfhatidilinositol -4, 5 -bifosfātu).
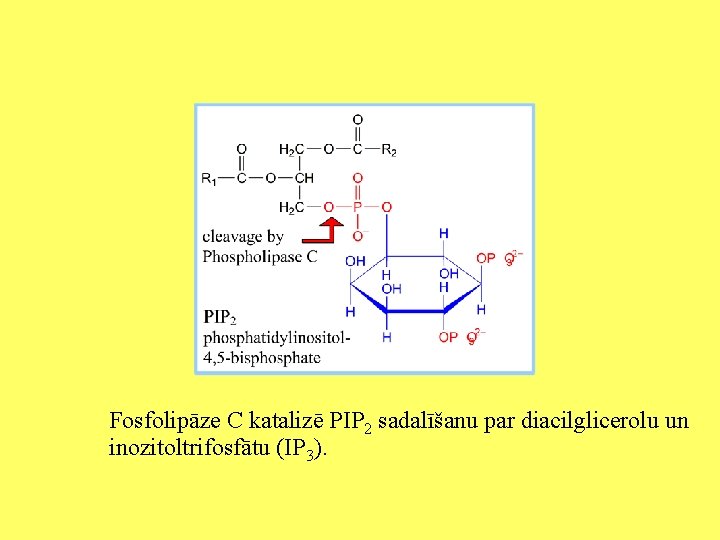
Fosfolipāze C katalizē PIP 2 sadalīšanu par diacilglicerolu un inozitoltrifosfātu (IP 3).
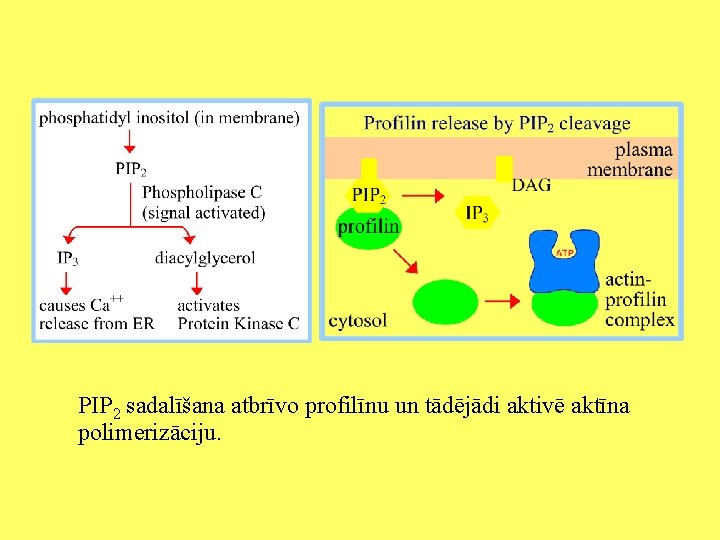
PIP 2 sadalīšana atbrīvo profilīnu un tādējādi aktivē aktīna polimerizāciju.

Nukleācijas veicināšanas faktori • Nukleācijas veicināšanas faktoru kompleksā ietilpst Arp 2/3, WASP un Scar. • WASP un Scar ir domēni (VCA), kas var pievienoties pie Arp 2/3 kompleksa un citi domēni, kas pievieno signālmolekulas. • Tādējādi, tie nosaka šūnas reģionu, kurā var sākties aktīna polimerizācija. • WASP var pievienoties pie PIP 2 vai Rho proteīniem. • Listeria ģints baktērijas satur olbaltumvielas, kas ir homologas WASP. Rezultātā notiek F-aktīna pagarināšanās.
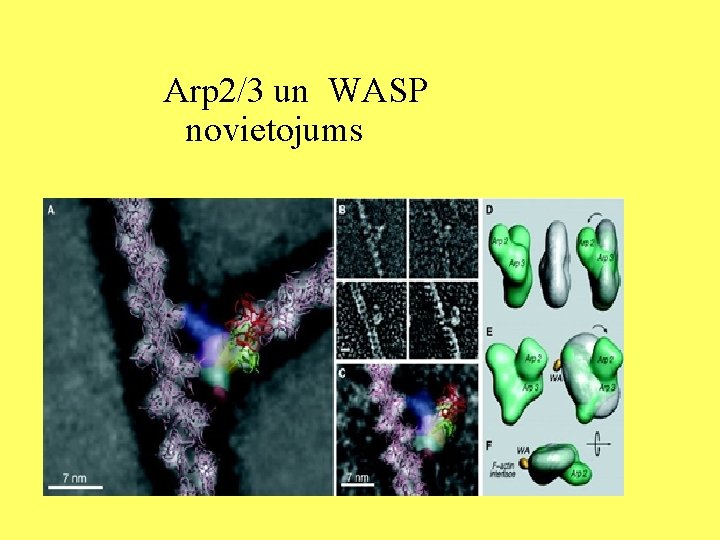
Arp 2/3 un WASP novietojums
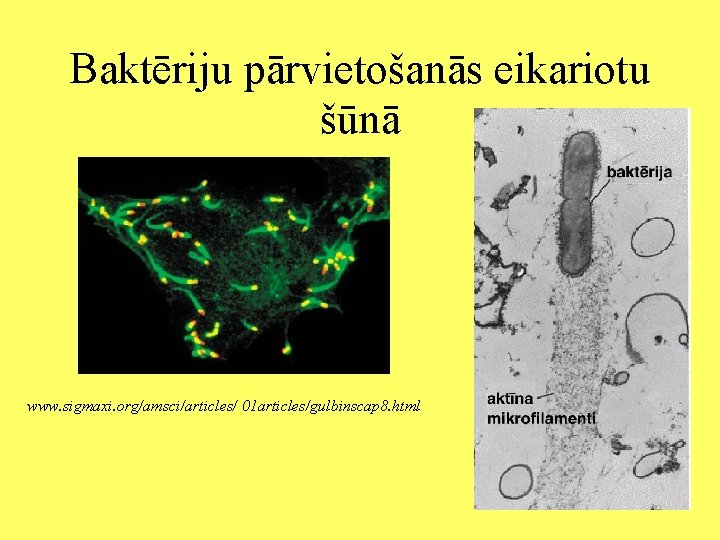
Baktēriju pārvietošanās eikariotu šūnā www. sigmaxi. org/amsci/articles/ 01 articles/gulbinscap 8. html

Baktēriju pārvietošanās eikariotu šūnā Priede/grozs/2 kurss-shuuna/filmas/listeria-filma 2 http: //ww 2. mcgill. ca/biology/undergra/c 201 b/listeria. mov
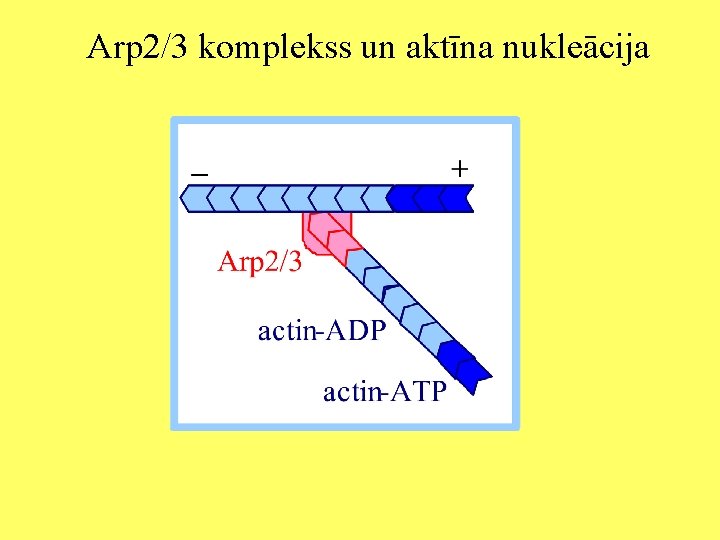
Arp 2/3 komplekss un aktīna nukleācija
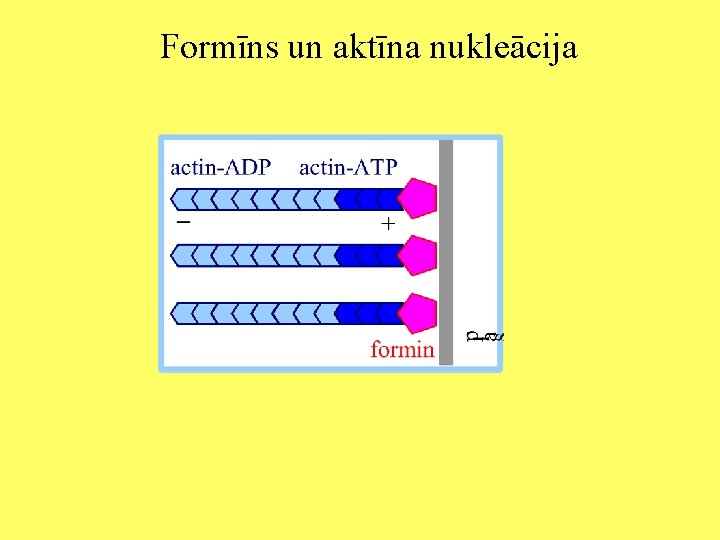
Formīns un aktīna nukleācija
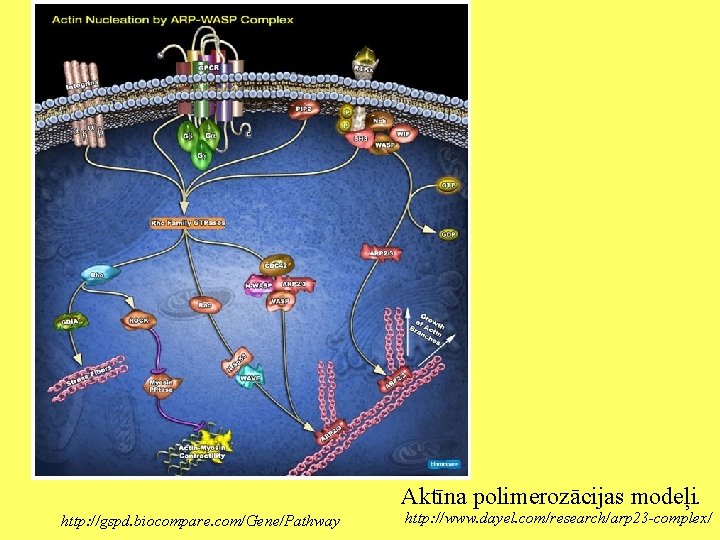
Aktīna polimerozācijas modeļi. http: //gspd. biocompare. com/Gene/Pathway http: //www. dayel. com/research/arp 23 -complex/

Kināzes • Regulē fokālās adhēzijas veidošanos un sadalīšanos. • Ar integrīnu saistītā kināze (ILK) pievienojas pie plazmatiskās membrānas integrīniem un vairākām aktīnam pievienojamajām olbaltumvielām un izraisa aktīna pievienošanu plazmatiskajai membrānai. • ILK fosforilē un aktivē proteīnkināzi B, nosakot daudzveidīgu regulatoro iedarbību. • Fokālās adhēzijas kināze (FAK) nosaka pievienošanos pie ārpusšūnas matriksa.

ERM ģimenes olbaltumvielas • Ezrīns, radiksīns un moezīns regulē aktīna pievienošanu plazmatiskajai membrānai. • ERM olbaltumvielas pievienojas membrānas integrālajām olbaltumvielām un aktīnam. • Tos regulē ar signāla inducētu fosforilāciju vai PIP 2.

Kalpaini • Tās ir Ca 2+ aktivējamas cisteīna proteāzes, kas regulē šūnu adhēziju. Tās atdala stresa fibrilu sastāvdaļas un fokālās adhēzijas zonas un veicina šūnu kustīgumu. • Kalpaini pārrauj sekojošas olbaltumvielas: • aktīnam pievienotās olbaltumvielas-aktinīns, talīns, spektrīns. • Plazmatiskās membrānas integrībnu subvienības; • erzīnu • Kalpainus regulē fosforilācija un tos inhibē kalpastatīns.

Rho • Rho ir nelieli GTF-pievienotie proteīni, kas regulē aktīna citoskeletu. • Aktīvā forma satur GF • Tie aktivē: • lamelopodiju veidošanos; • kopā ar Cdc 42 aktivē filopodiju veidošanos • kopā ar Rac lamellopodiju un fokālo kontaktu veidošanos • Veido stresa fibrilas un fokālās adhēzijas kontaktzonas. http: //cellix. imolbio. oeaw. ac. at/Videotour/video_tour_9. html


Mikrofilamentu novietojums šūnā Eikariotu šūnās var novērot vairāku veidu aktīna mikrofilamentu kompleksus. Mikrofilamenti var būt sakārtoti kūlīšos vai veidot tīklu. Kūlīšos mikrofilamentiem ir paralēls vai antiparalēls novietojums. Savukārt tīklā mikrofilamenti ir daudz retāki un viens pret otru cenšas novietoties apmēram 900 leņķī. Izdala paralēlos kūlīšus, kontraktilos kūlīšus un gēlam līdzīgo tīklojumu.
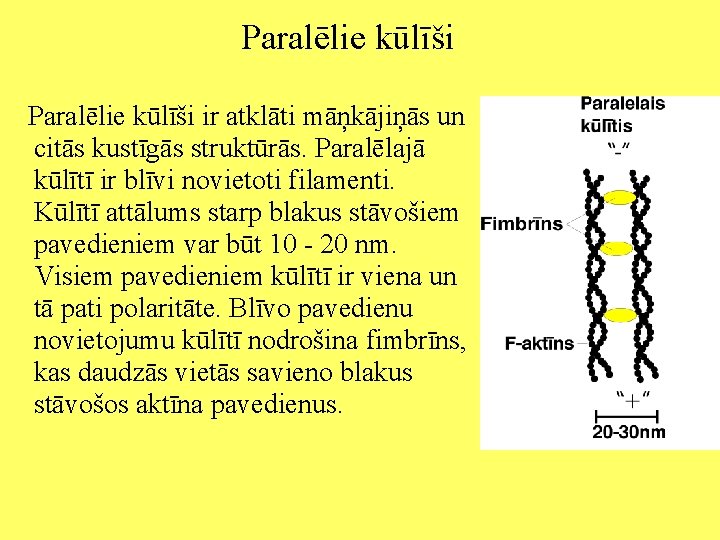
Paralēlie kūlīši ir atklāti māņkājiņās un citās kustīgās struktūrās. Paralēlajā kūlītī ir blīvi novietoti filamenti. Kūlītī attālums starp blakus stāvošiem pavedieniem var būt 10 - 20 nm. Visiem pavedieniem kūlītī ir viena un tā pati polaritāte. Blīvo pavedienu novietojumu kūlītī nodrošina fimbrīns, kas daudzās vietās savieno blakus stāvošos aktīna pavedienus.

Kontraktilie kūlīši ir konstatēti stresa fibrillās un kontraktilajā gredzenā, kas citokinēzes laikā pārdala dzīvnieku šūnas. Kūlītī novietotajiem pavedieniem ir pretēja polaritāte. Turklāt pavedieni nav arī tik blīvi novietoti. Attālums starp blakus stāvošiem pavedieniem ir 30 - 60 nm. Kūlīšus palīdz veidot aktinīns. Arī tas savieno blakus stāvošos pavedienus, bet aktinīna garums ir lielāks kā fimbrīnam. Līdz ar to lielāks ir attālums starp pavedieniem. Kūlīšos atrodas arī miozīns II. Miozīns II piestiprinās pie pavediena un palīdz pārvietot pavedienus.
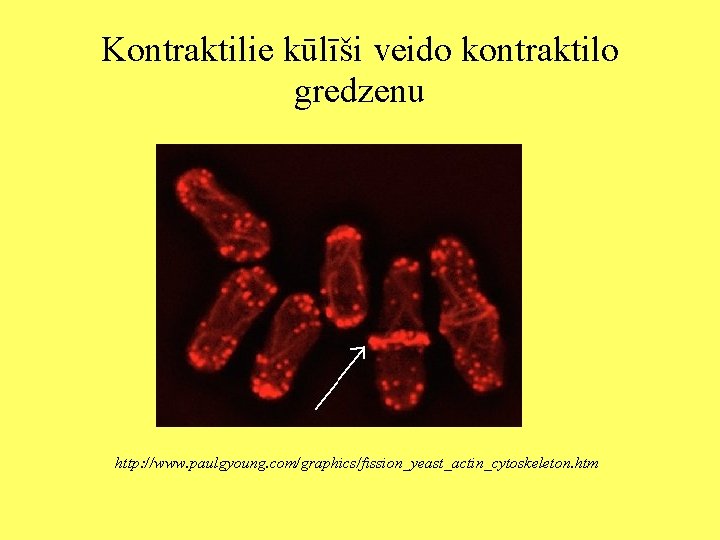
Kontraktilie kūlīši veido kontraktilo gredzenu http: //www. paulgyoung. com/graphics/fission_yeast_actin_cytoskeleton. htm
Kontraktilie kūlīši veido kontraktilo gredzenu Filma • Axis 292 c 30/The cell
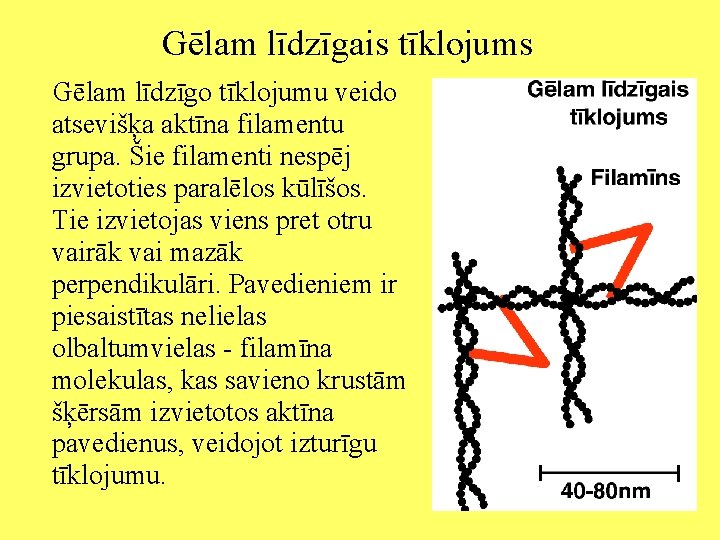
Gēlam līdzīgais tīklojums Gēlam līdzīgo tīklojumu veido atsevišķa aktīna filamentu grupa. Šie filamenti nespēj izvietoties paralēlos kūlīšos. Tie izvietojas viens pret otru vairāk vai mazāk perpendikulāri. Pavedieniem ir piesaistītas nelielas olbaltumvielas - filamīna molekulas, kas savieno krustām šķērsām izvietotos aktīna pavedienus, veidojot izturīgu tīklojumu.
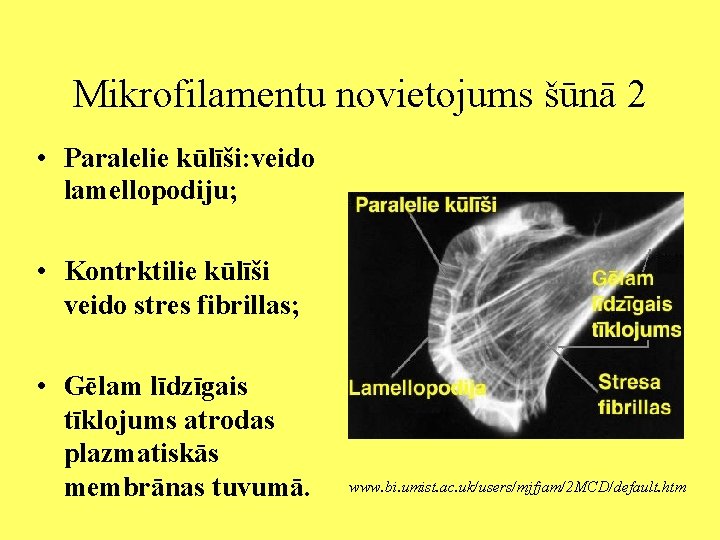
Mikrofilamentu novietojums šūnā 2 • Paralelie kūlīši: veido lamellopodiju; • Kontrktilie kūlīši veido stres fibrillas; • Gēlam līdzīgais tīklojums atrodas plazmatiskās membrānas tuvumā. www. bi. umist. ac. uk/users/mjfjam/2 MCD/default. htm

Mikrofilamentu novietojums šūnā 3 • Veidu, kādā tiek sakārtoti mikrofilamenti, nosaka aktīnam piesaistītās olbaltumvielas. Mikrofilamenti var sakārtoties kontraktilajos kūlīšos un piesaistīt miozīna II molekulas, ja augošiem aktīna pavedieniem pievienojas pavedienus stabilizējošais tropomiozīns. Ja augošam aktīna mikrofilamentam piesaistīsies filamīns, tad izveidojas gēlveidīgais tīklojums. Tomēr šūnās eksistē vairāk nekā tikai šie pieminētie mikrofilamentu sakārtojuma veidi. Šūnas signālu sistēma ļauj ātri palielināt vai samazināt aktīna mikrofilamentu daudzumu un mainīt sakārtojuma veidu, atbilstoši noteiktajiem apkārtējās vides apstākļiem.

Mikrofilamenti pie plazmatiskās membrānas Dzīvnieku šūnās pie plazmatiskās membrānas ir piesaistīti citoskeleta elementi. To piesaistīšanu nodrošina dažādas olbaltumvielas. Dzīvnieku eritrocītos aktīna piestiprināšanu pie membrānas nodrošina tās olbaltumvielu komplekss, ko veido α aktinīns, spektrīns, ankirīns un dažas nepilnīgi izpētītas olbaltumvielas.

Mikrofilamenti pie plazmatiskās membrānas • Spektrīns ir heterodimērs un to veido divas nedaudz savītas polipeptīdu ķēdes. Vienas ķēdes aminoterminālais gals ir saistīts ar otras ķēdes karboksilterminālo galu. Heterodimēra viena puse ir fosforilēta, lai varētu piesaistīt otru heterodimēru. • Spektrīna pavedienus pie plazmatiskās membrānas piestiprina divi membrānas olbaltumvielu kompleksi. Visa plazmatiskās membrānas iekšpuse ir tīkla veidā izklāta ar spektrīna pavedieniem. Aktīns piestiprinās spektrīnam īpašos mezglu punktos. Šajā zonā savienojas plazmatiskās membrānas olbaltumvielas, spektrīna pavedieni un īsi, apmēram 13 monomērus gari, aktīna mikrofilamenti. Aktīna mikrofilamentu garumu nodrošina mikrofilamentiem piestiprinātās tropomiozīna molekulas. www. embl-heidelberg. de/Cell. Biophys/Local. Probes/spectrin. htm

Mikrobārkstiņas Zarnu epitēlija šūnai var būt vairāki tūkstoši mikrobārkstiņu. Mikrobārkstiņas diametrs ir 0, 08 m, bet garums līdz 1 mm. Mikrobārkstiņas palīdz šajā šūnas zonā palielielināt plazmatiskās membrānas absorbējošās virsmas lielumu. Mikrobārkstiņas centrālo daļu veido paralēlu aktīna mikrofilamentu kūlītis, kas sastāv no 20 - 30 mikrofilamentiem.
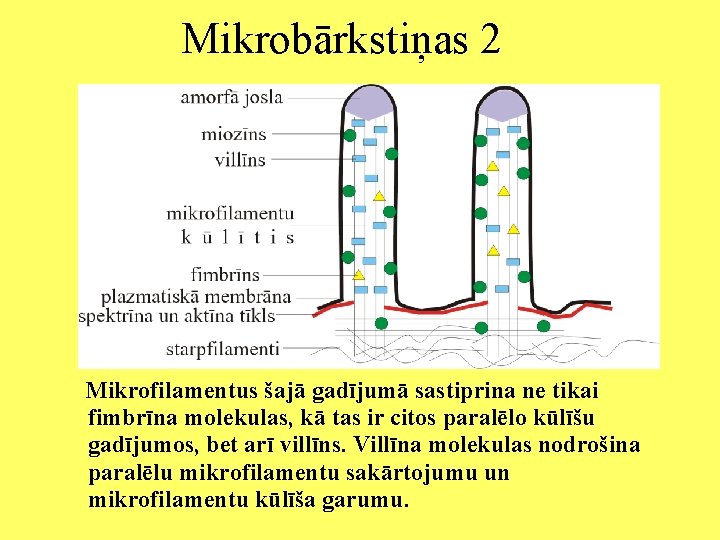
Mikrobārkstiņas 2 Mikrofilamentus šajā gadījumā sastiprina ne tikai fimbrīna molekulas, kā tas ir citos paralēlo kūlīšu gadījumos, bet arī villīns. Villīna molekulas nodrošina paralēlu mikrofilamentu sakārtojumu un mikrofilamentu kūlīša garumu.
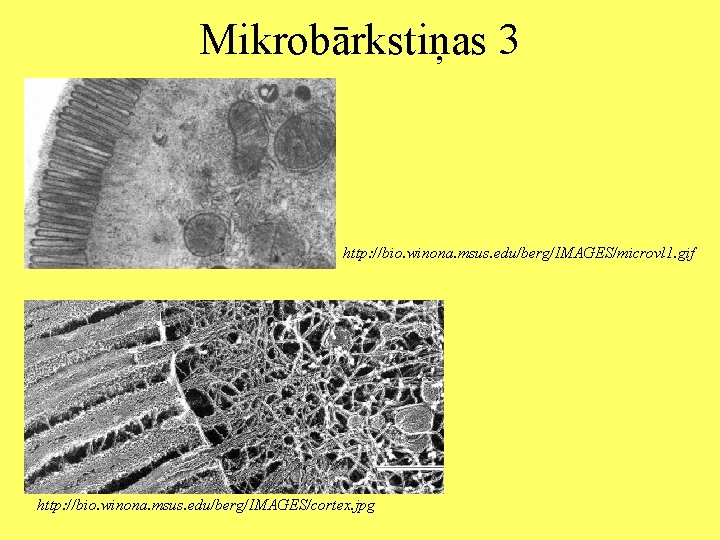
Mikrobārkstiņas 3 http: //bio. winona. msus. edu/berg/IMAGES/microvl 1. gif http: //bio. winona. msus. edu/berg/IMAGES/cortex. jpg

Aktīns un šūnu pārvietošanās Video: Ameba Amēbas, makrofāgi un citas šūnas pārvietojas izstiepjot pseidopodijas.

Aktīns un šūnu pārvietošanās • Pseidopodiju veidošanās ir pētīta, analizējot amēbu hemotaksijas. • Amēbām uz plazmatiskās membrānas ir receptori, kas reaģē uz apkārtējā vidē esošajām molekulām. • Receptori iedarbina šūnas signālu sistēmu. Tā rezultātā šūnā tiek aktivētas brīvās G-aktīna molekulas un atbilstošajā šūnas zonā sākas strauja mikrofilamentu elongācija.
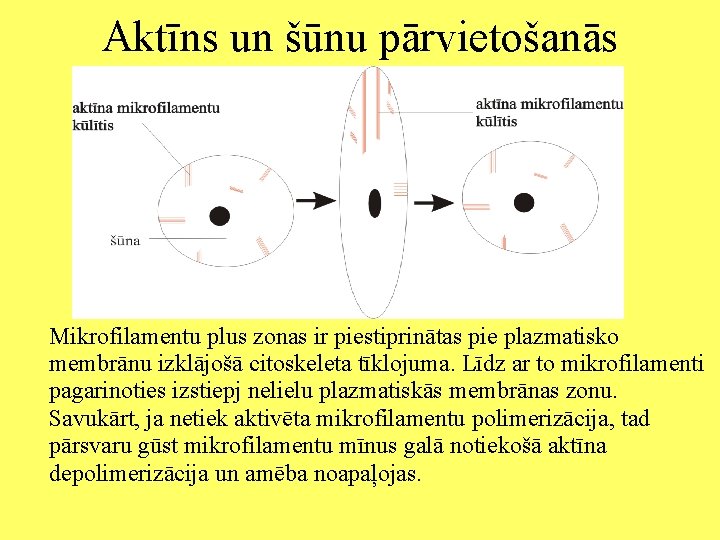
Aktīns un šūnu pārvietošanās Mikrofilamentu plus zonas ir piestiprinātas pie plazmatisko membrānu izklājošā citoskeleta tīklojuma. Līdz ar to mikrofilamenti pagarinoties izstiepj nelielu plazmatiskās membrānas zonu. Savukārt, ja netiek aktivēta mikrofilamentu polimerizācija, tad pārsvaru gūst mikrofilamentu mīnus galā notiekošā aktīna depolimerizācija un amēba noapaļojas.
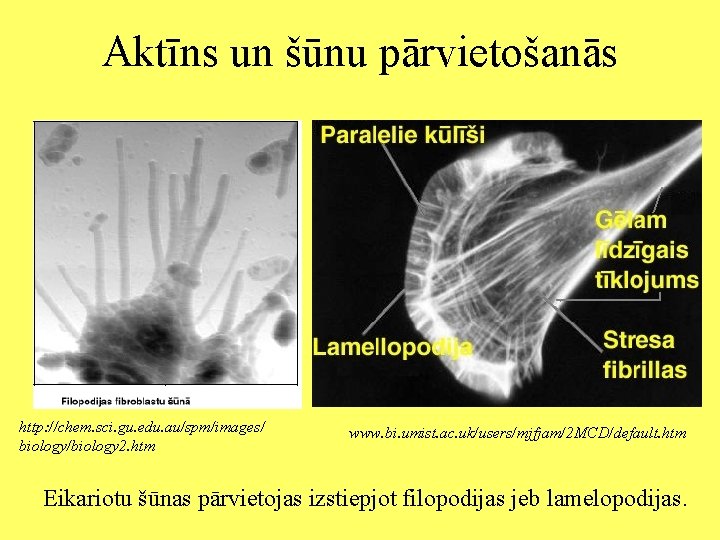
Aktīns un šūnu pārvietošanās http: //chem. sci. gu. edu. au/spm/images/ biology/biology 2. htm www. bi. umist. ac. uk/users/mjfjam/2 MCD/default. htm Eikariotu šūnas pārvietojas izstiepjot filopodijas jeb lamelopodijas.
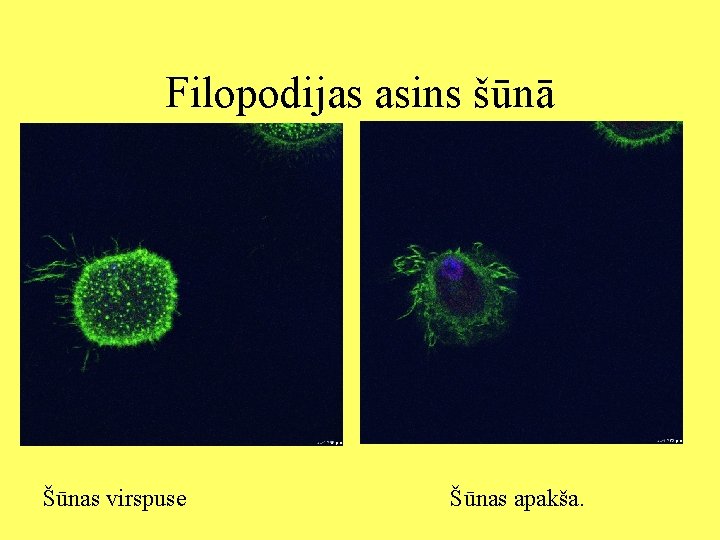
Filopodijas asins šūnā Šūnas virspuse Šūnas apakša.
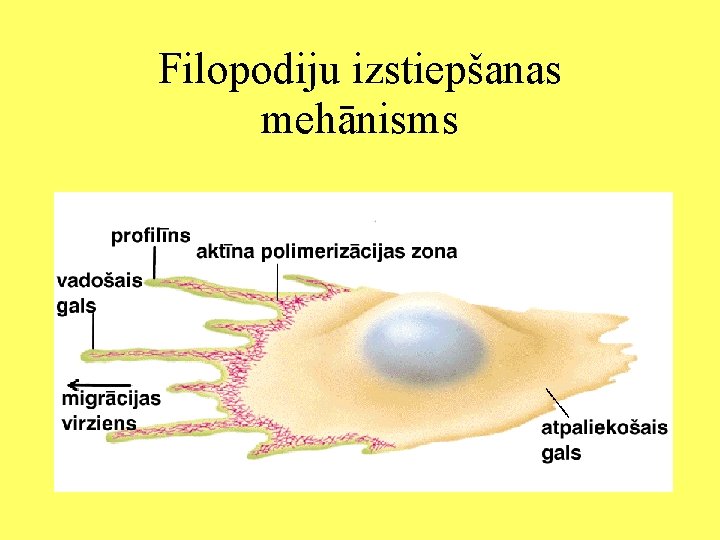
Filopodiju izstiepšanas mehānisms
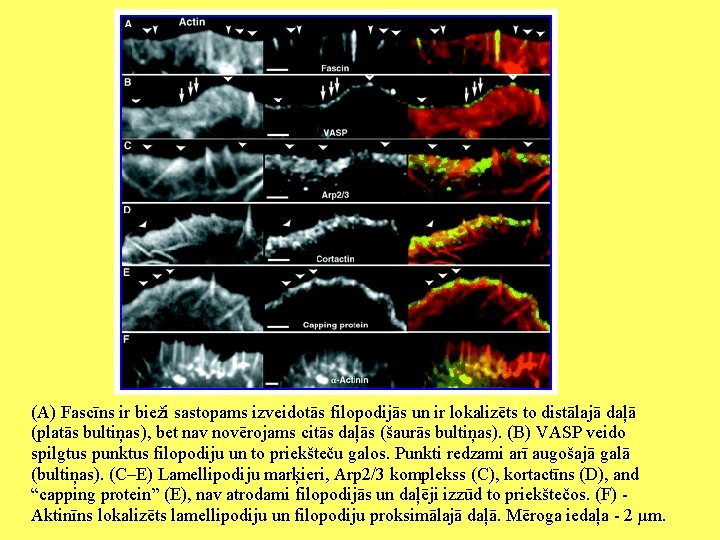
(A) Fascīns ir bieži sastopams izveidotās filopodijās un ir lokalizēts to distālajā daļā (platās bultiņas), bet nav novērojams citās daļās (šaurās bultiņas). (B) VASP veido spilgtus punktus filopodiju un to priekšteču galos. Punkti redzami arī augošajā galā (bultiņas). (C–E) Lamellipodiju marķieri, Arp 2/3 komplekss (C), kortactīns (D), and “capping protein” (E), nav atrodami filopodijās un daļēji izzūd to priekštečos. (F) Aktinīns lokalizēts lamellipodiju un filopodiju proksimālajā daļā. Mēroga iedaļa - 2 µm.
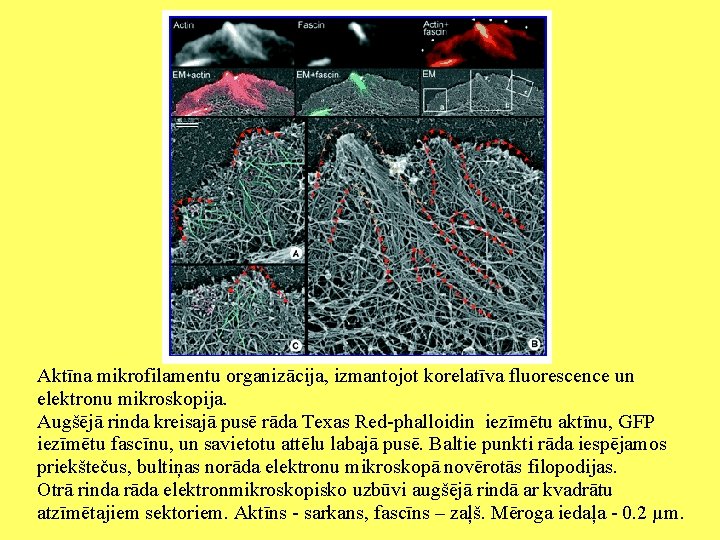
Aktīna mikrofilamentu organizācija, izmantojot korelatīva fluorescence un elektronu mikroskopija. Augšējā rinda kreisajā pusē rāda Texas Red-phalloidin iezīmētu aktīnu, GFP iezīmētu fascīnu, un savietotu attēlu labajā pusē. Baltie punkti rāda iespējamos priekštečus, bultiņas norāda elektronu mikroskopā novērotās filopodijas. Otrā rinda rāda elektronmikroskopisko uzbūvi augšējā rindā ar kvadrātu atzīmētajiem sektoriem. Aktīns - sarkans, fascīns – zaļš. Mēroga iedaļa - 0. 2 µm.

Miozīns un aktīna mikrofilamentu loma vielu un organellu transportā Mikrofilamenti un to motorās olbaltumvielas nodrošina aktīvus iekššūnas transporta procesus. Motorajām olbaltumvielām aminoterminālā daļa var piesaistīties pie aktīna mikrofilamentiem, bet blakus domēni piesaista un hidrolizē ATF. Molekulu karboksilterminālā daļa, atkarībā no tās uzbūves, pievienojas pie noteiktiem lipīdiem vai olbaltumvielām. Pie mikrofilamentu motorajām olbaltumvielām pieder miozīna molekulas.

Miozīns • Visbiežāk eikariotu šūnās ir sastopamas miozīna I, II, V un VI molekulas. Visām miozīna molekulām ir līdzīga molekulas galvas daļa, bet ļoti var atšķirties to karboksilterminālā daļa. Līdz ar to šūnās tām ir atšķirīgas funkcijas.
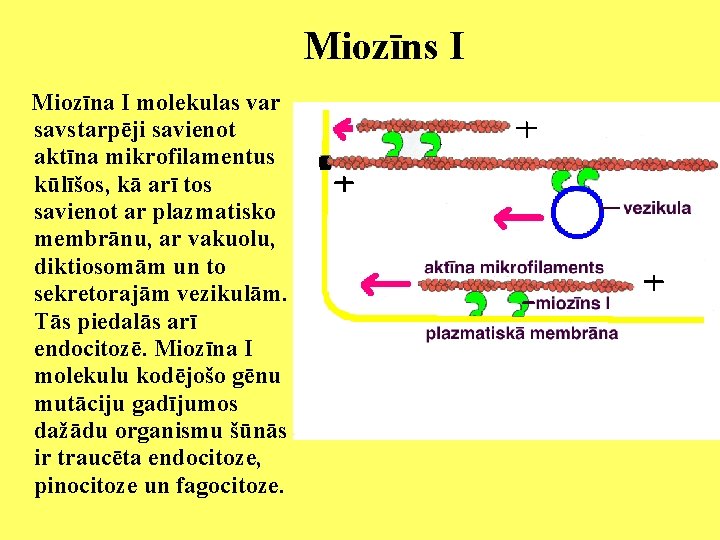
Miozīns I Miozīna I molekulas var savstarpēji savienot aktīna mikrofilamentus kūlīšos, kā arī tos savienot ar plazmatisko membrānu, ar vakuolu, diktiosomām un to sekretorajām vezikulām. Tās piedalās arī endocitozē. Miozīna I molekulu kodējošo gēnu mutāciju gadījumos dažādu organismu šūnās ir traucēta endocitoze, pinocitoze un fagocitoze.

Miozīns II nodrošina mugurkaulnieku muskuļu šūnu kontrakcijas, bet citos šūnu tipos - kontraktilā gredzena veidošanos un šūnu atdalīšanu citokinēzē.

Miozīns V un VI Miozīna V un VI molekulas ir konstatētas gandrīz visos mugurkaulnieku šūnu tipos. Tās nodrošina membrānu, vezikulu un organellu transportu. Atšķirībā no mikrocaurulītēm, dzīvnieku šūnas mikrofilamenti nodrošina vielu pārvietošanos nelielā dažu mikrometru lielā attālumā. Uzskata arī, ka tie nodrošina tikai vienvirziena vielu transportu mikrofilamenta "+" gala virzienā.
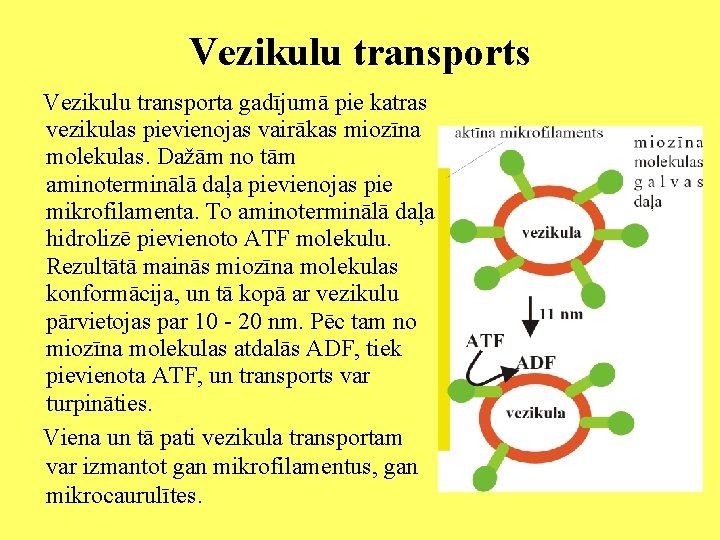
Vezikulu transports Vezikulu transporta gadījumā pie katras vezikulas pievienojas vairākas miozīna molekulas. Dažām no tām aminoterminālā daļa pievienojas pie mikrofilamenta. To aminoterminālā daļa hidrolizē pievienoto ATF molekulu. Rezultātā mainās miozīna molekulas konformācija, un tā kopā ar vezikulu pārvietojas par 10 - 20 nm. Pēc tam no miozīna molekulas atdalās ADF, tiek pievienota ATF, un transports var turpināties. Viena un tā pati vezikula transportam var izmantot gan mikrofilamentus, gan mikrocaurulītes.
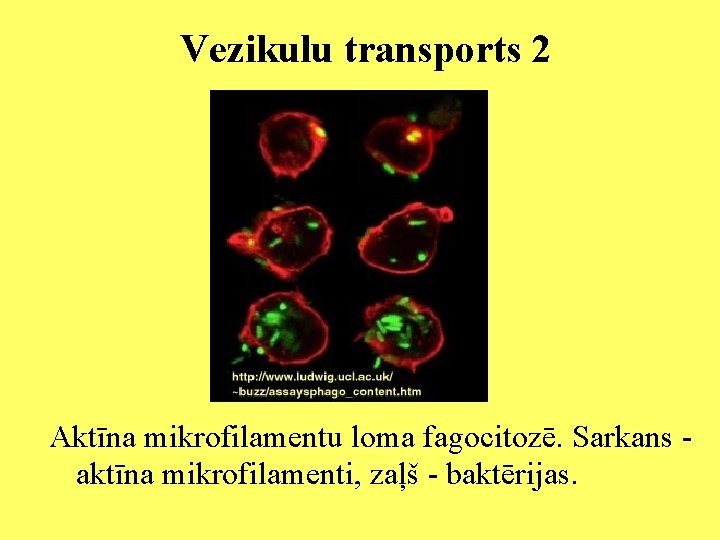
Vezikulu transports 2 Aktīna mikrofilamentu loma fagocitozē. Sarkans aktīna mikrofilamenti, zaļš - baktērijas.

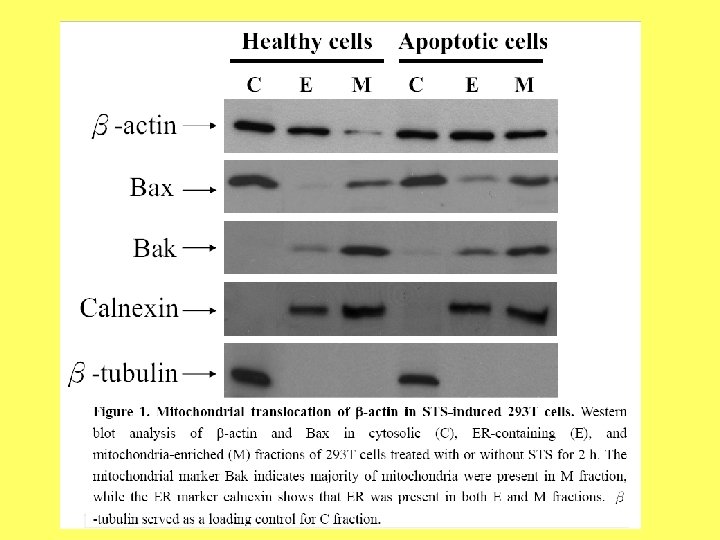
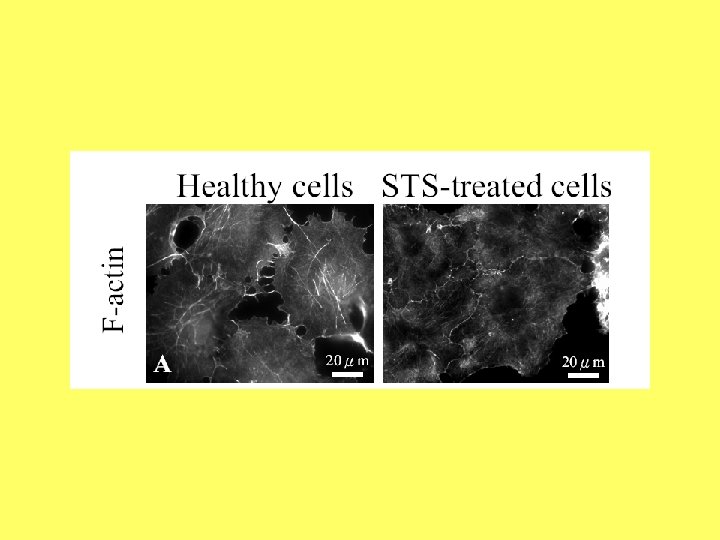
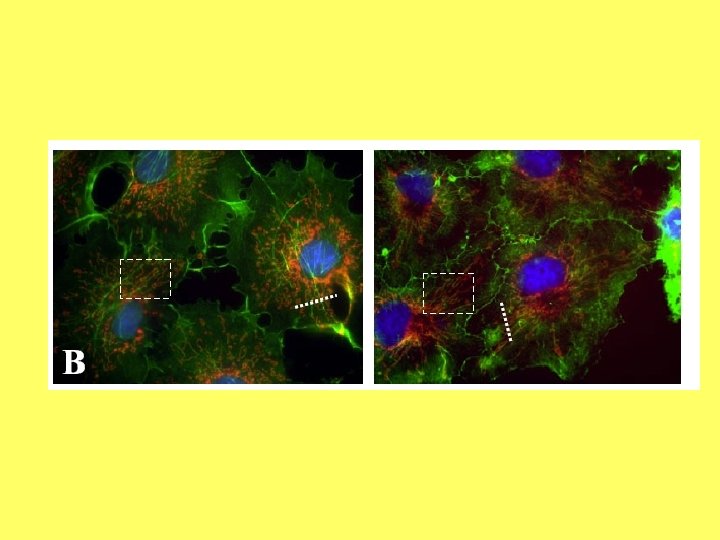
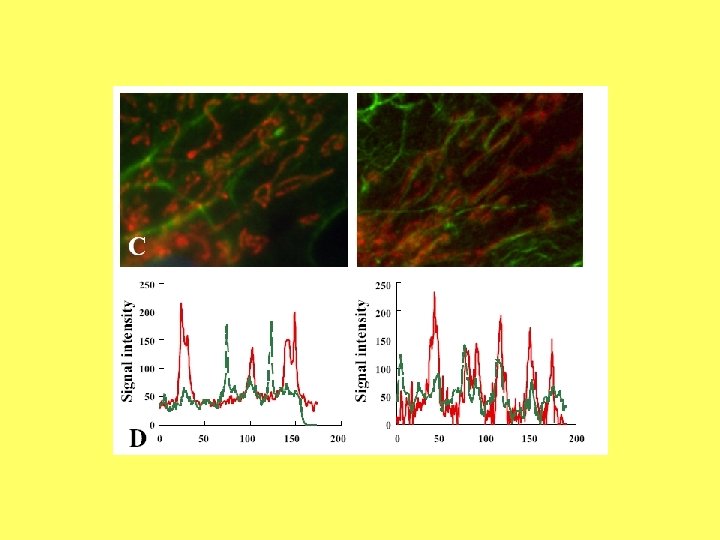
Aktīns un mitohondriji

Ieteicamās publikācijas • Mechanism of filopodia initiation by reorganization of a dendritic network. Svitkina TM, Bulanova EA, Chaga OY, Vignjevic DM, Kojima S, Vasiliev JM, Borisy GG J Cell Biol. 2003 Feb 3; 160(3): 409 -21. • Cellular motility driven by assembly and disassembly of actin filaments. Pollard TD, Borisy GG. Cell. 2003 Feb 21; 112(4): 453 -65. Review. Erratum in: Cell. 2003 May 16; 113(4): 549. • Formation of filopodia-like bundles in vitro from a dendritic network. Vignjevic D, Yarar D, Welch MD, Peloquin J, Svitkina T, Borisy GG. J Cell Biol. 2003 Mar 17; 160(6): 951 -62. • Microtubule dynamics in living cells: direct analysis in the internal cytoplasm. Vorobjev IA, Alieva IB, Grigoriev IS, Borisy GG. Cell Biology International Volume 27, Issue 3 , 2003, Pages 293 -294 • Analysis of Na+, K+-ATPase Motion and Incorporation into the Plasma Membrane in Response to G Protein–coupled Receptor Signals in Living Cells. Bertorello AM, Komarova Y, Smith K, Leibiger IB, Efendiev R, Pedemonte CH, Borisy G, Sznajder JI. Mol Biol Cell. 2003 March; 14 (3): 1149– 1157
- Slides: 75