La natura atomica della materia 4 Elemento specie















- Slides: 19

La natura atomica della materia 4

Elemento= specie atomica • • • Idrogeno, H Elio, He Litio, Li Berillio, Be Boro, B Carbonio, C Azoto, N Ossigeno, O Fluoro, F Neon, Ne • • • Sodio, Na Calcio, Ca Alluminio, Al Silicio, Si Fosforo, P Zolfo, S Cloro, Cl Argo, Ar Ferro, Fe Argento, Ag

Tavola Periodica

Cose da fare • Imparare i nomi e i simboli degli elementi più comuni

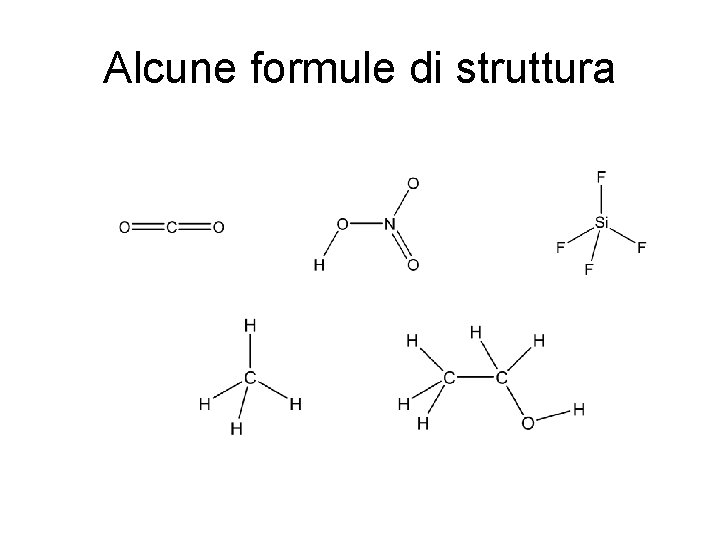
Formule chimiche • Danno la composizione atomica delle sostanze • Formula minima o stechiometrica o elementare: il semplice rapporto tra atomi. Na. Cl, P 2 O 5, Si. O 2, Ca 3 P 2 O 8 • Formula molecolare: specifica il numero di atomi che entra a far parte della “molecola”: H 2, O 2, N 2, H 2 O 2, C 6 H 6, Ca 3(PO 4)2 • Formula di struttura: fornisce la concatenazione molecolare

Alcune formule di struttura

La struttura dell’atomo Nucleo, caricato positivamente in cui è praticamente tutta la massa dell’atomo; neutroni n e protoni p+ Elettroni caricati negativamente e-

Isotopi Numero atomico= numero di protoni, Z Nell’atomo neutro Z elettroni Numero di neutroni, N Numero di massa A= N+ Z Le proprietà chimiche sono legate agli elettroni quindi a Z. Tutti gli atomi che hanno lo stesso Z corrispondono alla stessa specie chimica, o elemento. Atomo dello stesso elemento possono avere differente N: Isotopi

Simboli degli isotopi

Massa atomica relativa La massa atomica relativa di un nuclide indica il rapporto tra la massa del nuclide e la massa di 1/12 della massa del 12 C che è presa per convenzione uguale a 12 esatto Se si definisce una nuova unità di misura uguale a 1/12 della massa del nuclide 12 C, detta unità di massa atomica, uma, o Dalton, Da, lo stesso numero dà la massa relativa e la massa nella nuova unità di misura 1 uma= 1 Da= 1, 6605389(10). 10 -27 kg

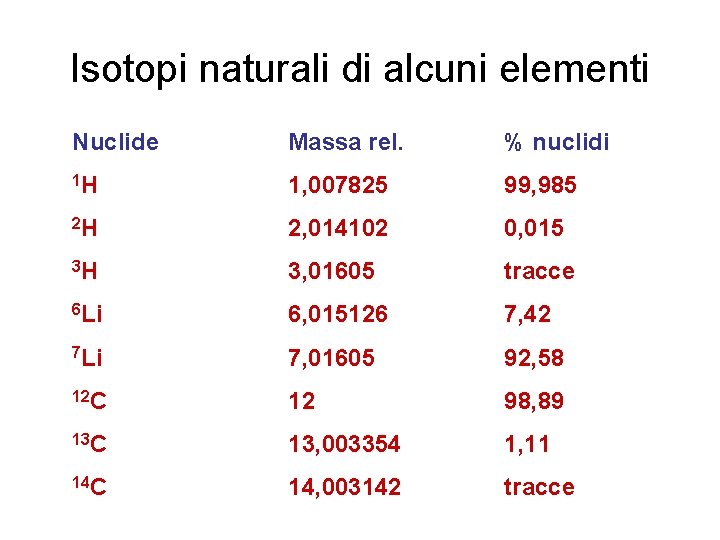
Isotopi naturali di alcuni elementi Nuclide Massa rel. % nuclidi 1 H 1, 007825 99, 985 2 H 2, 014102 0, 015 3 H 3, 01605 tracce 6 Li 6, 015126 7, 42 7 Li 7, 01605 92, 58 12 C 12 98, 89 13 C 13, 003354 1, 11 14 C 14, 003142 tracce

Peso atomico relativo e medio degli elementi La percentuale dei vari isotopi di un elemento è costante su tutta la terra. Si può quindi definire un peso atomico medio come la media pesata degli isotopi di un certo elemento. Il fattore di peso è la percentuale dell’isotopo nella miscela naturale 1 H 1, 007825 (99, 985%) 2 H 2, 014102 (0, 015%) (1, 007825 x 99, 985/100)+ (2, 014102 x 0, 015/100)= 1, 007976 12 C 13, 003354 (1, 11%) 12 (98. 89%) (12 x 0, 9889)+ (13, 0034 x 0, 0111)= 12, 0111


Peso molecolare e peso formula La somma dei pesi atomici di tutti gli elementi della molecola o della formula di una sostanza è detta peso molecolare Peso molecolare di I 2: 2 x 126, 9= 253, 8 Peso molecolare di H 2 SO 4: 2 x 1, 00798+ 32, 064+ 4 x 15, 999= 98, 076 Peso formula di K 2 Cr 2 O 7: 2 x 39, 10+ 2 x 51, 996+7 x 15, 999= 294, 2

La mole è la quantità di materia che contiene tante unità elementari (atomi, molecole, ioni, elettroni, ecc. ) quanti ne sono contenuti in 12 g del nuclide 12 C Numero o costante di Avogadro, NA NA= 6, 0221415(10). 1023 mol-1 La massa in g di una mole di sostanza è data dallo stesso numero che ne esprime il peso molecolare

Massa molare La massa molare è il rapporto tra massa e quantità di sostanza. E’ espressa dal simbolo M. Ha dimensioni: [M]= g mol-1

Qual’è la massa di una mole di: • • Idrogeno (sostanza elementare) Ossigeno (sostanza elementare) Cloruro di sodio Metano Biossido di carbonio Acido solforico Permanganato di potassio benzene

Quante moli ci sono in 100 g di: • • Azoto (sostanza elementare) Ossido di carbonio Ferro Biossido di silicio Alcool etilico Biossido di zolfo Fluoruro di potassio Tetrossido di osmio

Calcolare le percentuali in massa degli elementi in • • Cloruro di sodio Bromuro di magnesio Diossido di carbonio Carbonato ferrico Ossido di mercurio Acido solfidrico Cianuro di potassio Solfato di calcio biidrato