Kzs kincsnk fkuszban a gyermekgygyszati gygyszerek Iparjogvdelmi jutalmak

Közös kincsünk? – fókuszban a gyermekgyógyászati gyógyszerek Iparjogvédelmi jutalmak és ösztönzők Buzásné Nagy Zsuzsanna Magyar Szabadalmi Hivatal Medical. Tribune, Budapest, 2010. szeptember 21. 1

Bevezetés q Jutalmak és ösztönzők q Néhány szó a kiegészítő oltalmi tanúsítványról SPC bejelentések Európában és Magyarországon q Milyen feltételekkel adható 6 hónapos meghoszabbítás q Gyermekgyógyászati információ az EMEA honlapján q Trendelemzés q Az MSZH, mint eljáró iparjogvédelmi hatóság

Az 1901/2006/EK rendelet - Cél a gyermekgyógyászati kutatások ösztönzése. - A jóváhagyott gyermekgyógyászati vizsgálati terv(PIP) végrehajtása, az információ beépítése a betegtájékoztatóba. - A Gyermekgyógyászati Bizottság értékeli a vizsgálati tervet, dönt a mentességekről és halasztásokról, vagy véleményt ad más (nemzeti) hatóság kérésére. - Jutalmak és ösztönzők a költséges vizsgálatok elvégzéséért. - A jutalmat akkor is meg kell adni, ha a kutatás negatív eredménnyel zárul. 3

Jutalmak és ösztönzők -Szabadalommal vagy kiegészítő oltalmi tanúsítvánnyal(SPC) védett termék esetén az SPC oltalmi idejének 6 hónapos meghosszabbítása -Ritka betegségek gyógyszerei esetén a tíz éves piaci kizárólagosság tizenkét évre emelkedik -Szellemi tulajdonjog oltalma alatt (már) nem álló termékek, kizárólag gyermekgyógyászati célra kifejlesztett gyógyszerek esetén gyermekgyógyászati felhasználásra szolgáló forgalomba hozatali engedély (PUMA) adható +1 év adatkizárólagosság 4
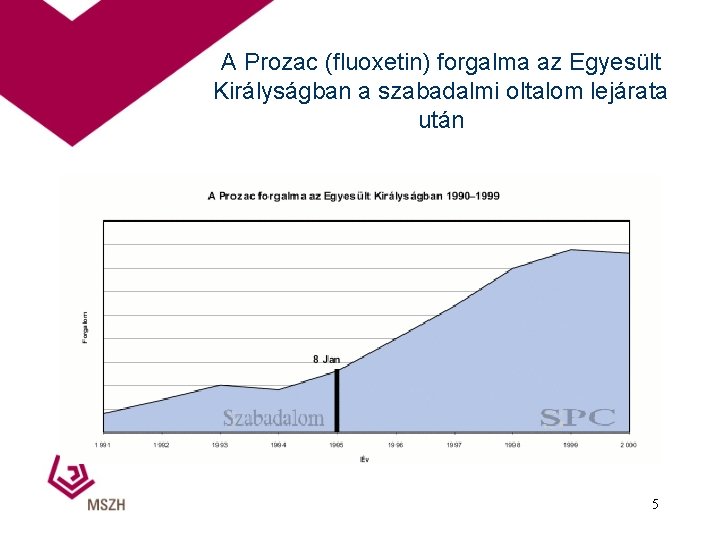
A Prozac (fluoxetin) forgalma az Egyesült Királyságban a szabadalmi oltalom lejárata után 5

AZ SPC oltalmi ideje 6

Néhány szó az SPC-ről A Tanács 1768/92/EGK rendelete (1992. június 18. ) a gyógyszerek kiegészítő oltalmi tanúsítványának bevezetéséről Magyarországon 2004. május 1 -től Az Európai Parlament és a Tanács 1610/96/EK rendelete (1996. július 23. ) a növényvédő szerek kiegészítő szabadalmi oltalmi tanúsítványának létrehozásáról 7

Az SPC megszerzésének feltételei Ha a bejelentés napján Magyarországon a. A termék hatályos alapszabadalom oltalma alatt áll b. a termék érvényes forgalomba hozatali engedéllyel rendelkezik Csak piacra került találmányokat helyez védelem alá! c. A termékre még nem adtak tanúsítványt ( egy termékre ugyannak a bejelentőnek csak egy SPC adható) 8

Az SPC oltalom az alapszabadalmon belül csak a forgalomba hozott termékre terjed ki Szabadalom: Az (I) általános képletű kinuklidin származékok 9
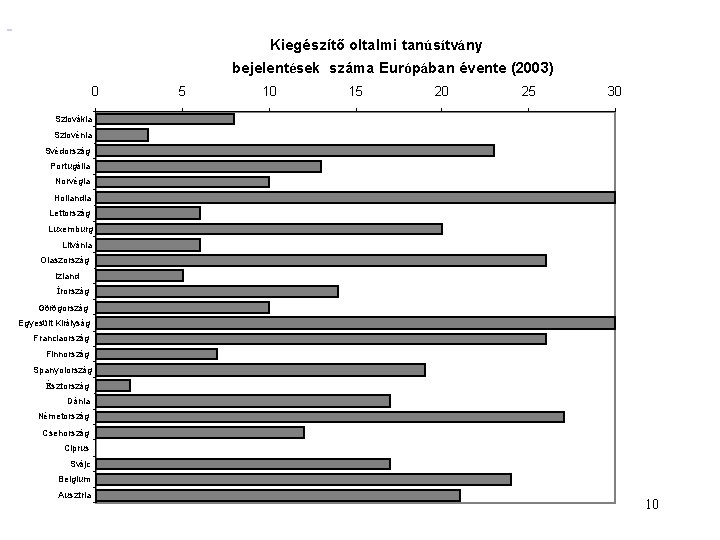
Kiegészítő oltalmi tanúsítvány bejelentések száma Európában évente (2003) 0 5 10 15 20 25 30 Szlovákia Szlovénia Svédország Portugália Norvégia Hollandia Lettország Luxemburg Litvánia Olaszország Izland Írország Görögország Egyesült Királyság Franciaország Finnország Spanyolország Észtország Dánia Németország Csehország Ciprus Svájc Belgium Ausztria 10
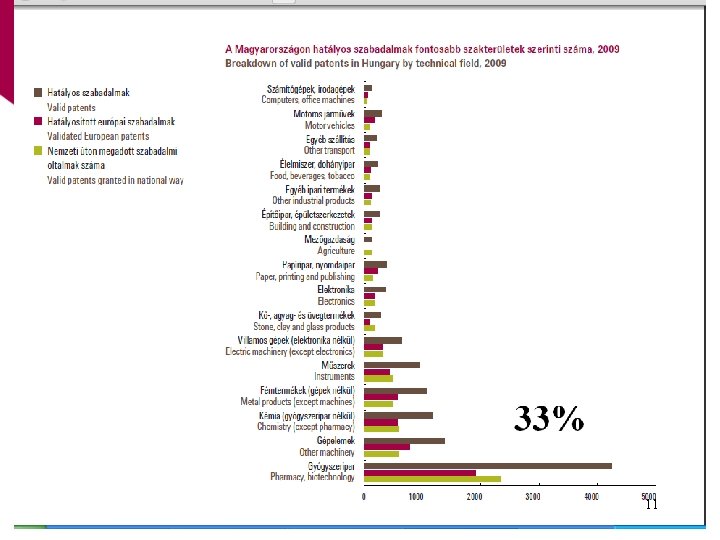
11
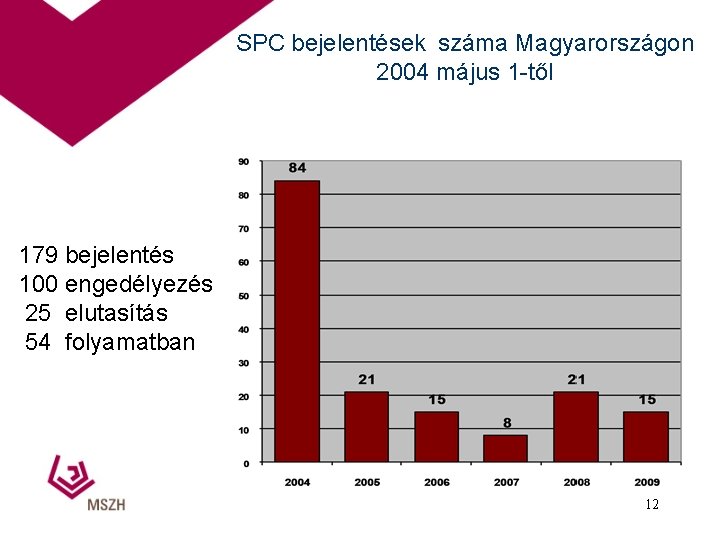
SPC bejelentések száma Magyarországon 2004 május 1 -től 179 bejelentés 100 engedélyezés 25 elutasítás 54 folyamatban 12
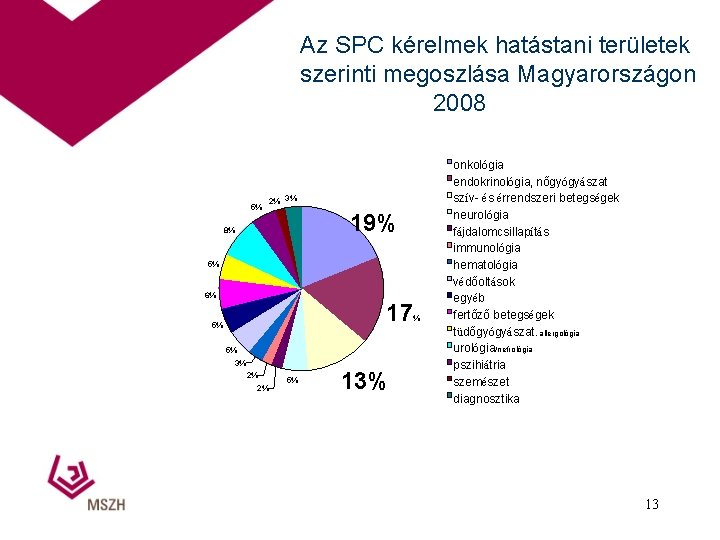
Az SPC kérelmek hatástani területek szerinti megoszlása Magyarországon 2008 5% 2% 3% 19% 8% 5% 6% 17 5% 5% 3% 2% 2% 5% 13% % onkológia endokrinológia, nőgyógyászat szív- és érrendszeri betegségek neurológia fájdalomcsillapítás immunológia hematológia védőoltások egyéb fertőző betegségek tüdőgyógyászat, allergológia urológia/nefrológia pszihiátria szemészet diagnosztika 13

A 6 hónapos meghosszabbítás feltételei • Gyermekgyógyászati kutatások elvégzése • Az eredmények beépítése a forgalomba hozatali engedélybe • A jutalmat akkor is meg kell adni, ha a kutatás negatív eredménnyel zárul. • A nemzeti szabadalmi hivatalnál kell kérelmezni az új SPC bejelentéssel vagy már megadott SPCbejelentésre alapozva és benyújtani a bizonyítékokat. 14

A 6 hónapos hosszabbítási kérelem benyújtásának határideje • 7 cikk (3) : Az időtartam meghosszabbítási kérelem legkésőbb az SPC lejárta előtt két évvel nyújtható be. Miért? A generikus gyártók még idejében értesülhetnek a piacra lépésüket késleltető meghosszabbításról. • Átmeneti időszakban, 2007 január 26 -tól kezdődő 5 évig: a bejelentési határidő az SPC lejárta előtt hat hónappal. Miért? A lejárathoz közeledő SPC –k oltalma alatt álló hatóanyagok is részesülhessenek az új jutalmakból . 15

Milyen bizonyítékokat kell benyújtani a 6 hónapos hosszabbítás elnyeréséhez? EMEA engedély. • kölcsönös elismerésen A forgalomba hozatali alapuló vagy nemzeti engedélyben az EMEA eljárás (OGYI) keretén elismeri, hogy az belül engedélyezett előzetesen jóváhagyott hatóanyag esetén: gyermekgyógyászati vizsgálati tervet + Bizonyítani kell, hogy a végrehajtották és az termék az összes tagállam vonatkozásában forgalomba eredményeket beépítették hozatali engedéllyel a betegtájékoztatóba. rendelkezik. 16

ZOMETA Súlyos osteogenesis imperfecta kezelésében – két klinikai vizsgálatban értékelték gyermekkorú betegek körében. A Zometa gyermekpopulációban nem alkalmazható, mert a biztonságosságot és hatásosságot gyermekekben nem igazolták Pozitív megfelelőségi nyilatkozat van: végrehajtották a gyermekgyógyászati vizsg tervet és a betegtájékoztatóban szerepel az eredmény! 17

SPC bejelentések megoszlása a hatóanyag forgalomba hozatali engedélyét kiadó hatóság szerint 18
19
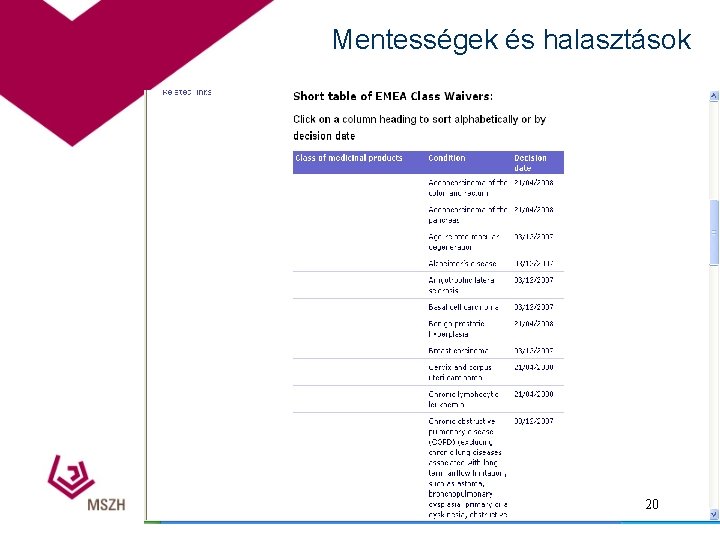
Mentességek és halasztások 20
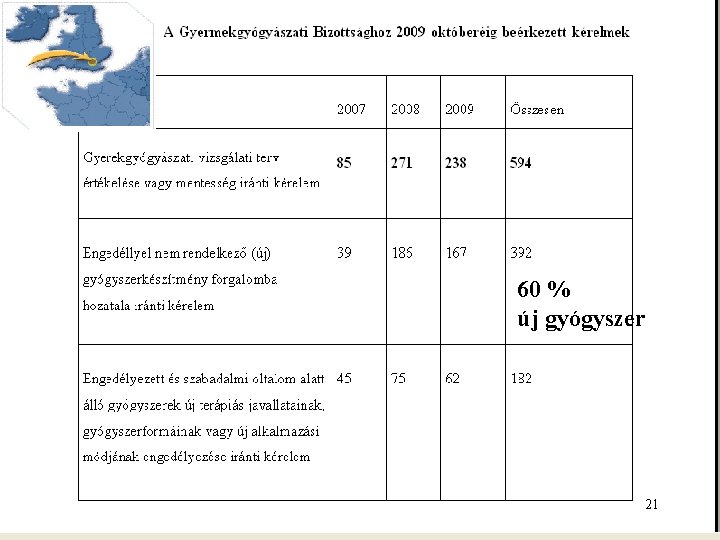
60 % új gyógyszer 21
A Gyermekgyógyászati Bizottság által 2009 októberéig kiadott vélemények száma 2007 2008 2009 Összesen Teljes mentesség 10 48 56 14 Vizsgálati terv elfogadás halasztással 2 81 110 193 Negatív vélemény 0 4 12 16 Pozitív vélemény a megfelelőségről 0 5 7 12 Negatív vélemény a megfelelőségről 0 0 1 1 22

Az EMEA Gyermekgyógyászati Bizottsága által kiadott pozitív megfelelőségi nyilatkozatok (2009 végéig): endokrinológia-nőgyógyászat: Anastrozole, Colesevelam hidroklorid, Dienogest, Nomegestrol acetát, 17 betaestradiol, onkológia: Aprepitant, Ipilimumab, Vandetanib kardiovaszkuláris betegségek: Losartan kálium, Valsartan, dermatológia: Ustekinumab, Nalfurafine hidroklorid, immunológia, reumatológia: Abatacept, Belatacept, hematológia: Eltrombopag láz- és fájdalomcsillapítás: Paracetamol, 23
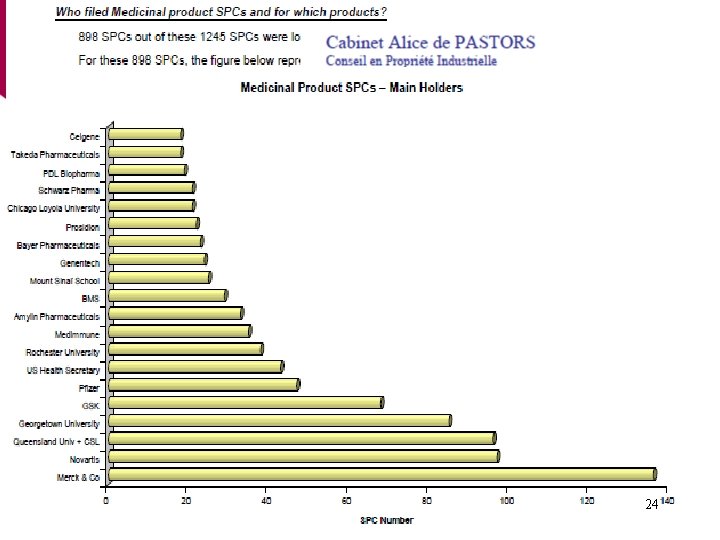
24

A következő hatóanyagok kiegészítő oltalma jár le 2012 -ig (HU): Dezloratadin és gyógyszerészetileg elfogadható sói (2010) Florfenikol (2011) Duloxetin és gyógyászatilag elfogadható savaddíciós sói, különösen hidrokloridja (2012) Pioglitazon és sói (2012) Zoledronsav, gyógyászatilag alkalmazható sói és hidrátjai (2 SPC, eltérő jogosultak) (2012)+ 6 hónap! Levodopa, carbidopa és entacapone valamint sóik kombinációja (2012) 25

26
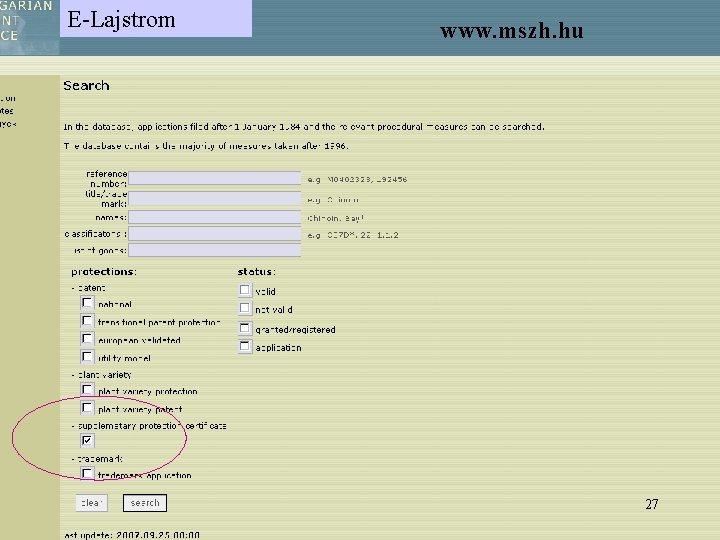
E-Lajstrom www. mszh. hu 27
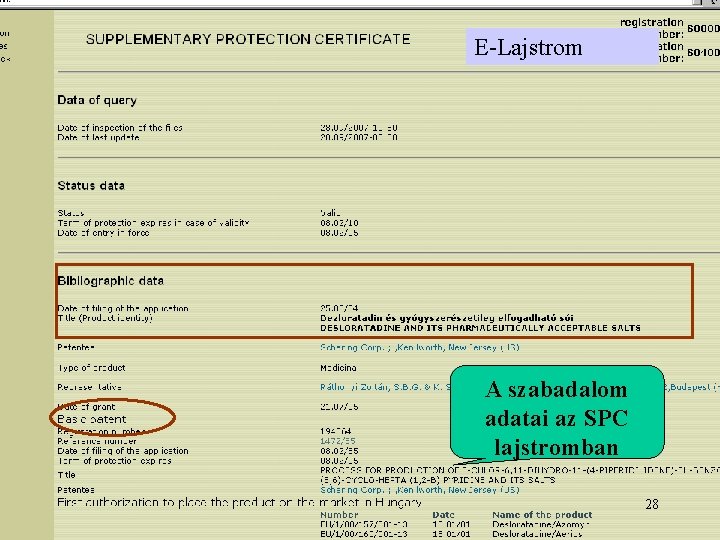
E-Lajstrom A szabadalom adatai az SPC lajstromban 28
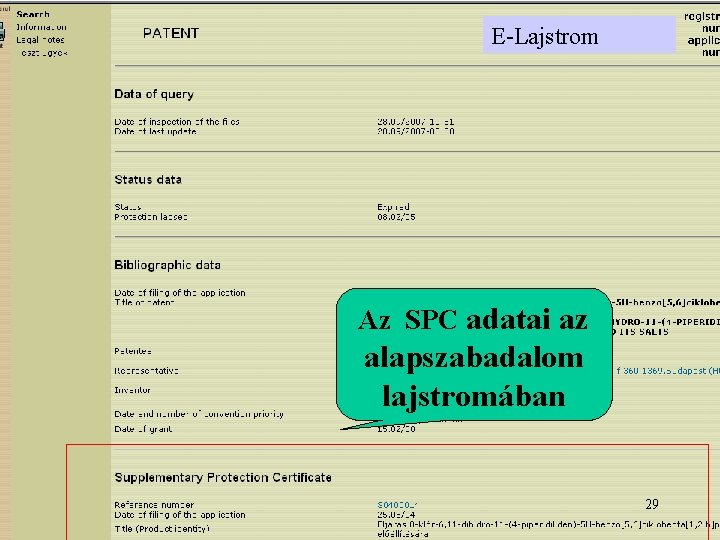
E-Lajstrom Az SPC adatai az alapszabadalom lajstromában 29

Viszontlátásra az MSZH-ban! www. mszh. hu Email: zsuzsanna. buzas@hpo. hu 30 30
- Slides: 30