INMOVILIZACIN POR ENTRECRUZAMIENTO CROSSLINKING Prof J M Snchez











- Slides: 30

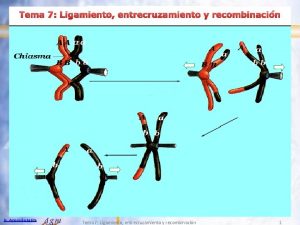
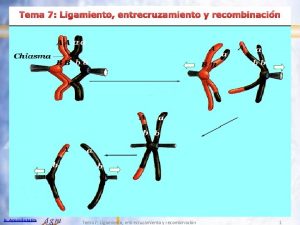
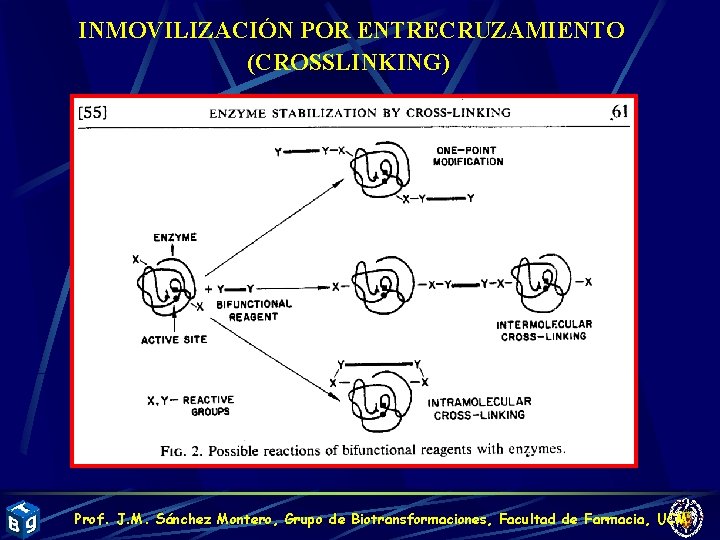
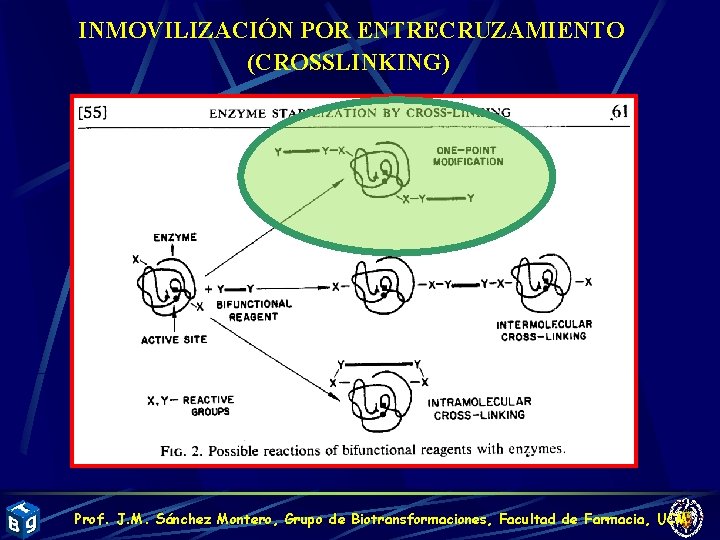
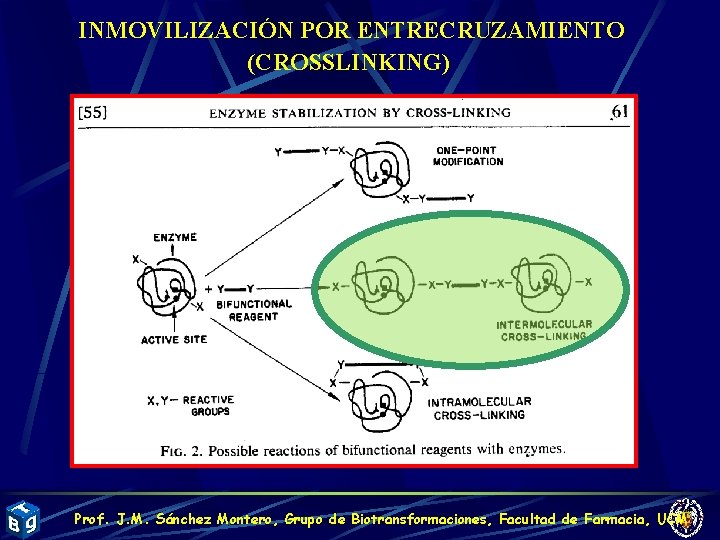
INMOVILIZACIÓN POR ENTRECRUZAMIENTO (CROSSLINKING) Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

INMOVILIZACIÓN POR ENTRECRUZAMIENTO (CROSSLINKING) Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

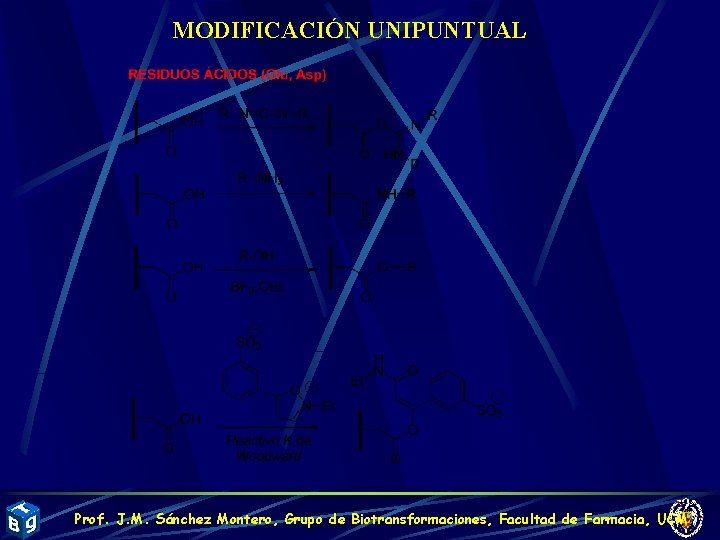
MODIFICACIÓN UNIPUNTUAL Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

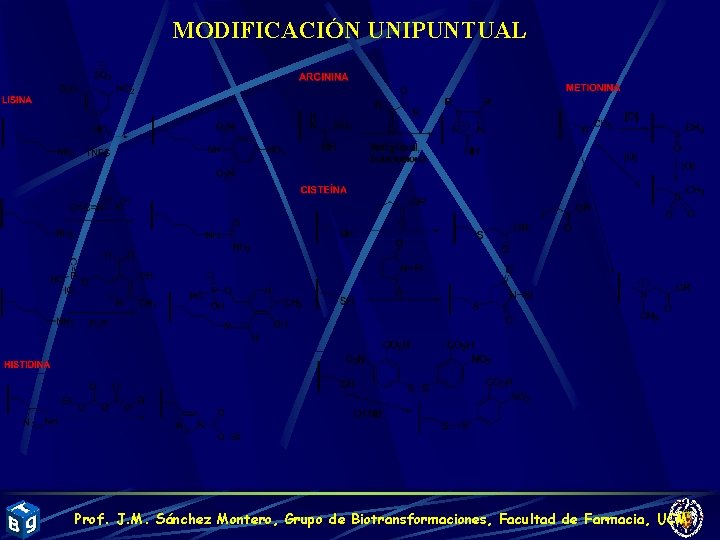
MODIFICACIÓN UNIPUNTUAL Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

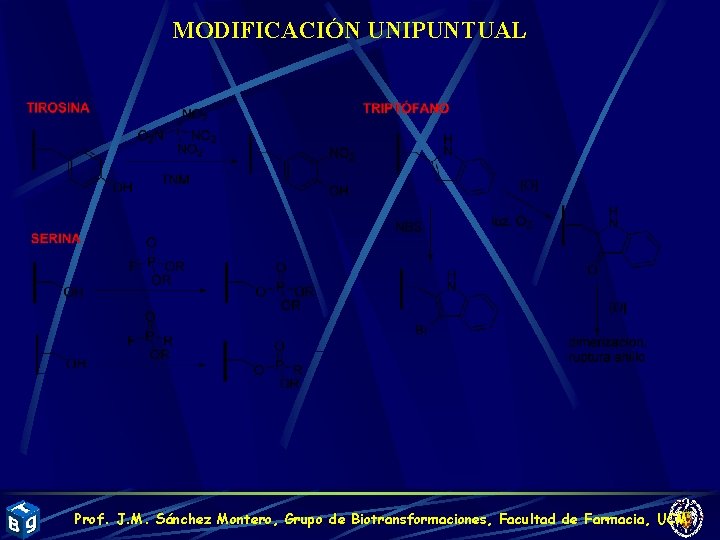
MODIFICACIÓN UNIPUNTUAL Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

üModificaciones unipuntuales de interés üObjetivo: hacer a la enzima insoluble en disoluciones acuosas. üUno de los métodos más tradicionales: ü UNIÓN COVALENTE DE UN POLÍMERO ANFIPÁTICO. üEl más habitual: monometoxipolietelienglicol (m. PEG) üPeso molecular variable. El mas usado: sobre 5 k. Da. üDependiendo del grado de modificación, se consigue la total insolubilidad en agua. üEste grado debe ser controlado cuidadosamente, pues puede conducir a la pérdida de actividad. üLa unión se suele hacer sobre lisinas. Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

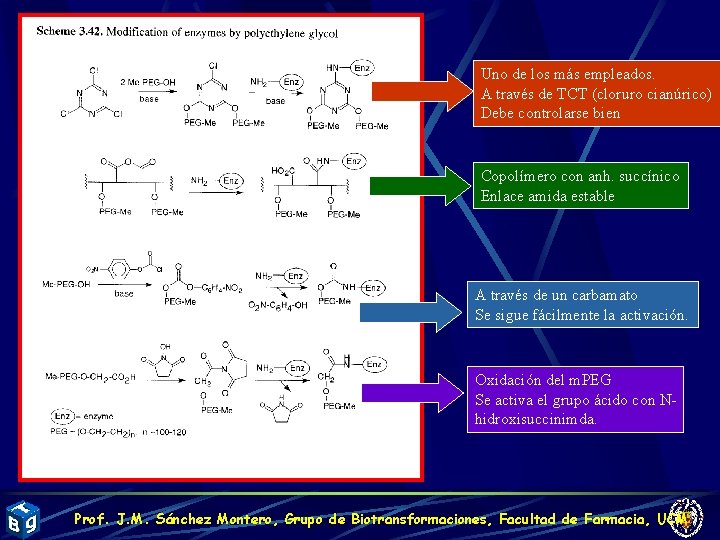
Uno de los más empleados. A través de TCT (cloruro cianúrico) Debe controlarse bien Copolímero con anh. succínico Enlace amida estable A través de un carbamato Se sigue fácilmente la activación. Oxidación del m. PEG Se activa el grupo ácido con Nhidroxisuccinimda. Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

üOtra característica interesante de esta metodología: SE OBTIENEN DERIVADOS SOLUBLES EN CIERTOS DISOLVENTES ORGÁNICOS: Benceno, tolueno y clorados (cloroformo, 1, 1, 1 -tricloroetano, tricloroetileno) LA CATÁLISIS SE HACE HOMOGÉNEA. üInmovilización en disolventes orgánicos? Siempre que se pueda recuperar el derivado. Recuperación: Añadiendo disolv. muy apolares (hexano, éter de petróleo) se produce la pptación. Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

INMOVILIZACIÓN POR ENTRECRUZAMIENTO (CROSSLINKING) Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

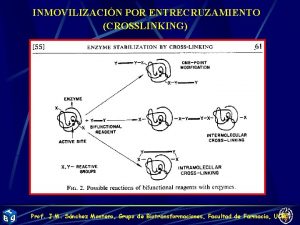
REACTIVOS ENTRECRUZANTES DIFUNCIONALES Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

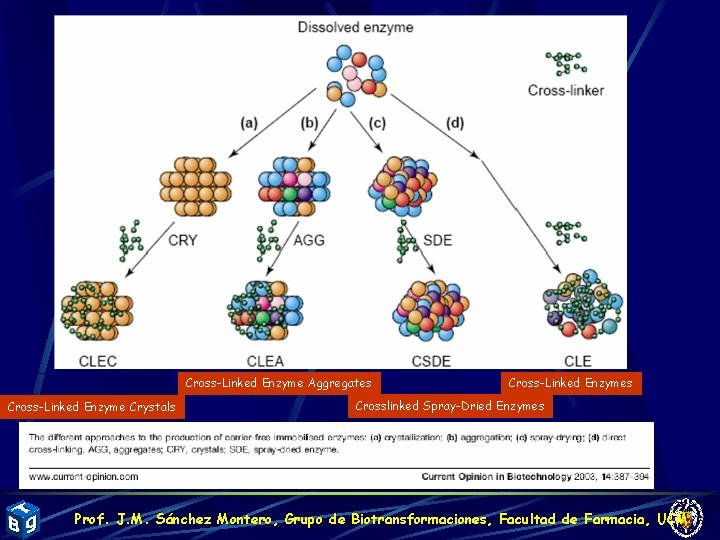
Cross-Linked Enzyme Aggregates Cross-Linked Enzyme Crystals Cross-Linked Enzymes Crosslinked Spray-Dried Enzymes Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

Cross Linked Enzymes (CLE) A comienzos de los años 60 se describe por primera vez que el tratamiento de enzimas con reactivos difuncionales (fundamentalmente glutaraldehído) originaba derivados insolubles con retención de actividad (CLEs) Al mismo tiempo, se aumentaba la termoestabilidad (sobre todo en enzimas multiméricas), pero se necesitan unas condiciones muy delicadas (cantidad crosslinker, T, p. H, fuerza iónica). El material obtenido era gelatinoso, y se intentó el entrecruzamiento con otras moléculas para aumentar propiedades mecánicas, Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

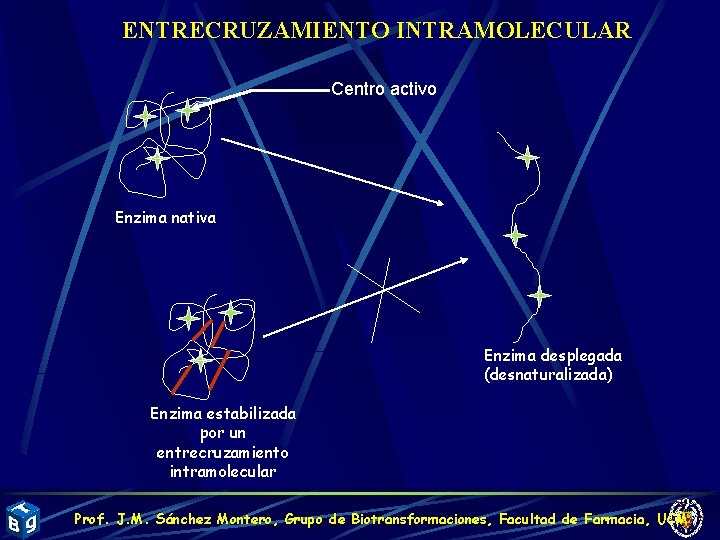
ENTRECRUZAMIENTO INTRAMOLECULAR Centro activo Enzima nativa Enzima desplegada (desnaturalizada) Enzima estabilizada por un entrecruzamiento intramolecular Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

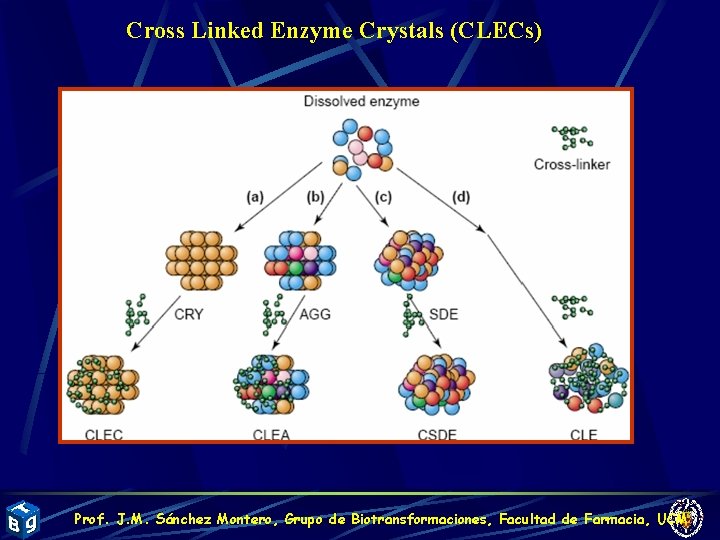
Cross Linked Enzyme Crystals (CLECs) Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

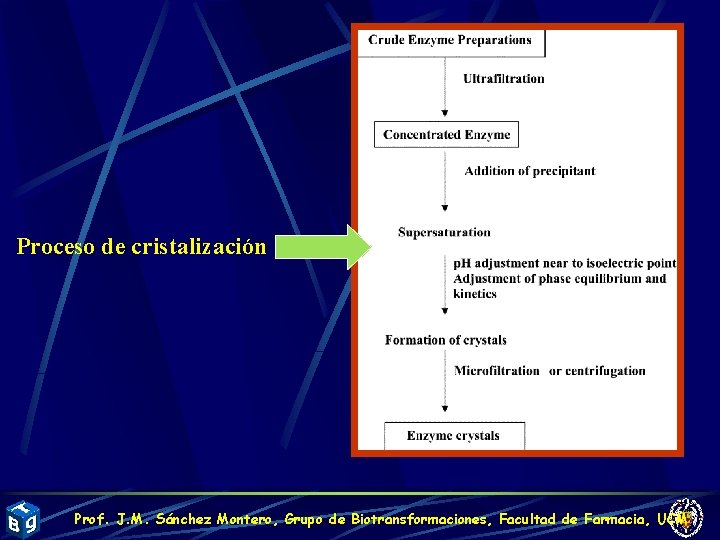
Proceso de cristalización Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

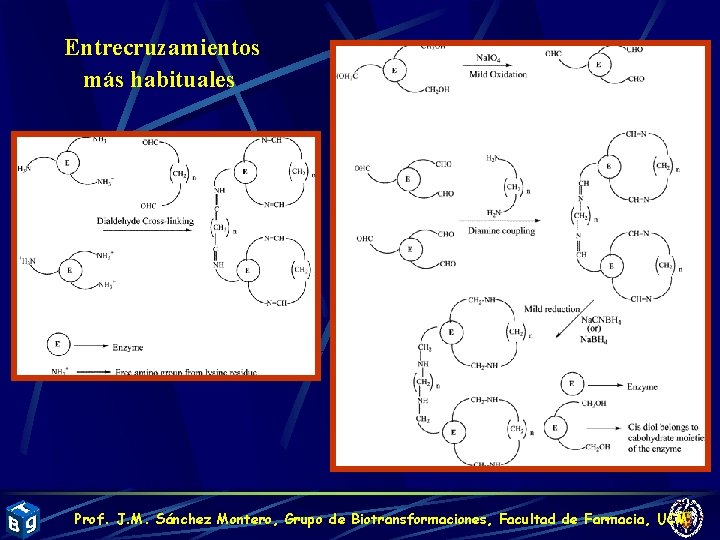
Entrecruzamientos más habituales Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

Ventajas 1. 2. 3. 4. 5. 6. 7. Mayor actividad por unidad de volúmen (partículas uniformes, microporosas, formadas por sólo moléculas de enzima pura, lo que implica la máxima posible concentración de enzima) Gran actividad específica Fácil separación del medio de reacción, lo que facilita su reutilización. Buenas propiedades mecánicas y termoestabilidad, así como resistencia a disolventes orgánicos. No producen contaminación medioambiental. No requieren soportes muy caros Resistentes a la proteolisis Desventajas 1. 2. 3. Dificultad de cristalización Problemas de difusión (debe miminizarse el tamaño del cristal) Alto precio Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

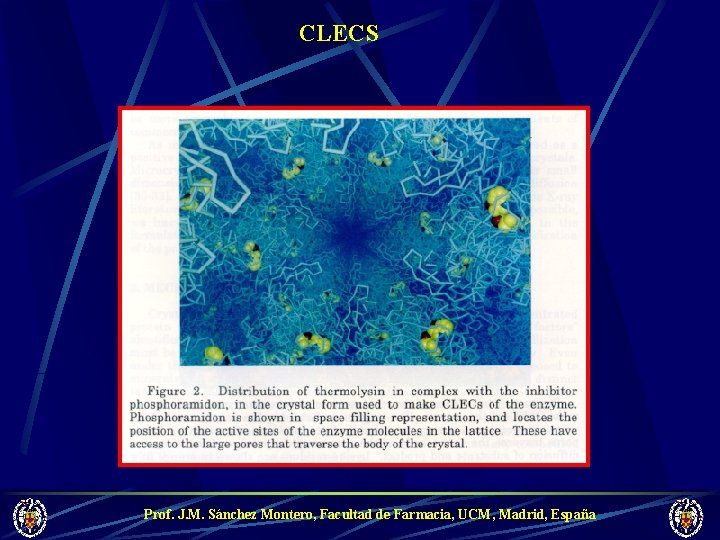
CLECS Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

CLECS Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

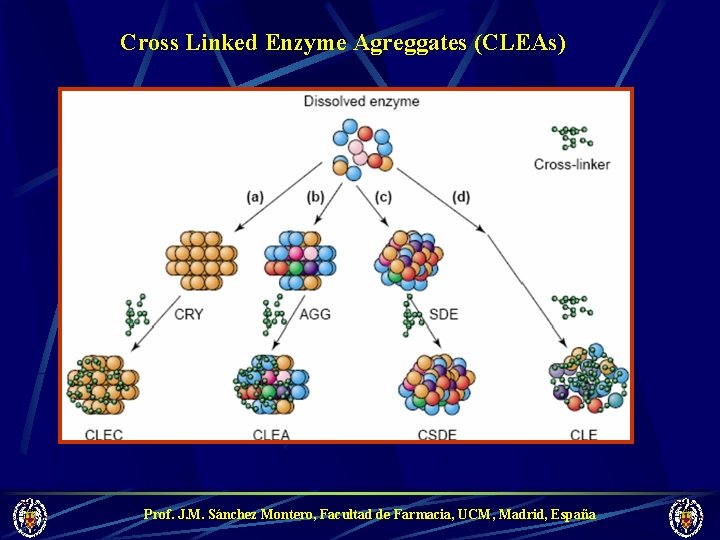
Cross Linked Enzyme Agreggates (CLEAs) Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

POSIBILIDADES Crosslinked Enzyme Crystals CLECs Crosslinked Enzyme Aggregates CLEAs Enzimas puras y cristalinas Enzimas con trazas de impurezas Necesidad de enzima pura Coagregación de enzimas Estabilización de proteinas multiméricas Agregación de enzima y polímero Estabilización de enzimas multiméricas Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

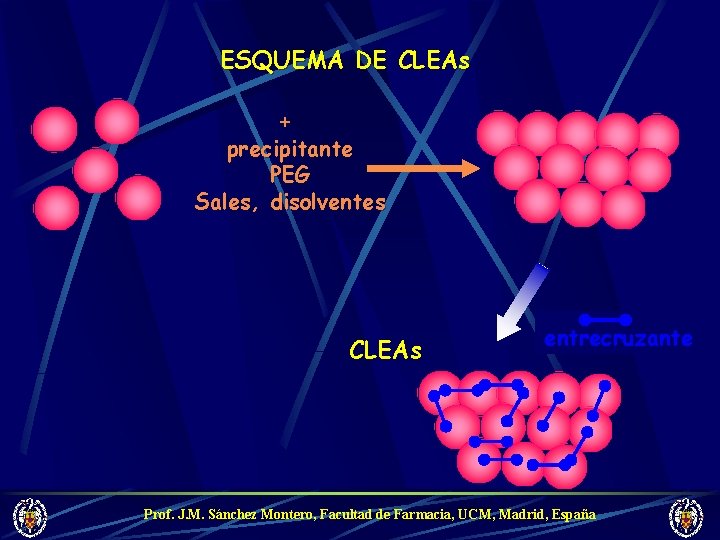
ESQUEMA DE CLEAs + precipitante PEG Sales, disolventes CLEAs entrecruzante Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

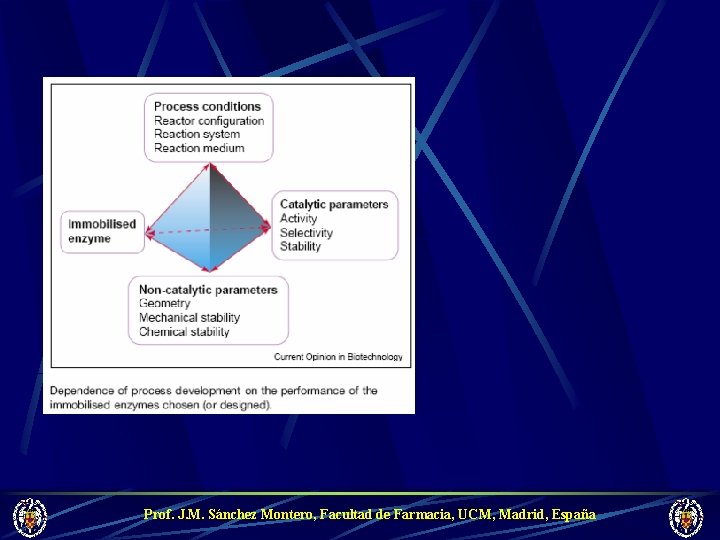
Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

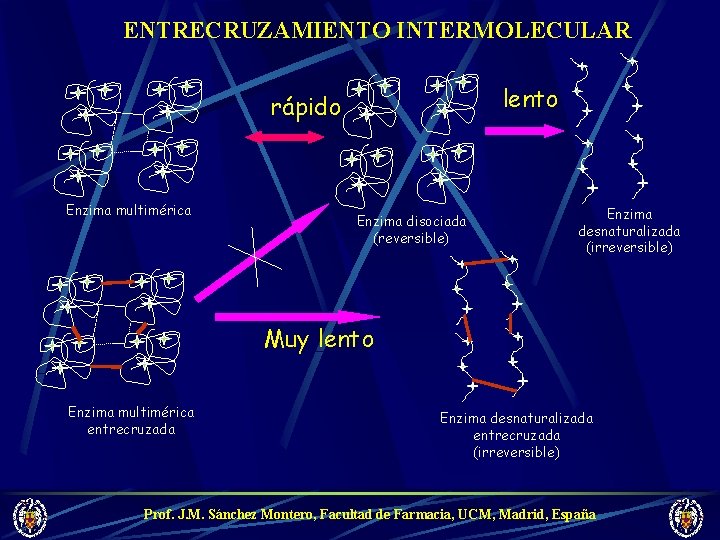
ENTRECRUZAMIENTO INTERMOLECULAR lento rápido Enzima multimérica Enzima disociada (reversible) Enzima desnaturalizada (irreversible) Muy lento Enzima multimérica entrecruzada Enzima desnaturalizada entrecruzada (irreversible) Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

INMOVILIZACIÓN POR ADSORCIÓN üEs el método más sencillo y antíguo (células de acetobacter adsorbidas sobre palos de madera para obtener vinagre por fermentación-1815) üSe puede emplear tanto para células como para enzimas. üLas fuerzas de unión son débiles: üVan der Waals üInteracciones iónicas üEnlaces de hidrógeno. üSe producen fácilmente desorciones debido a: üvariaciones concentración de sustrato. üCambios de p. H ücambios de T üalteración de la fuerza iónica. Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

INMOVILIZACIÓN POR ADSORCIÓN üSoportes típicos: ücarbón activo üsílice, alúmina, titania, . . . üTierra de diatomeas (Celite) ücelulosa üresinas sintéticas üCPG (controlled pore glasses). üLa mayoría de las enzimas se unen mejor a soportes polares üLas lipasas se unen mejor a superficies hidrofóbicas üMÉTODO MUY RECOMENDADO PARA ENZIMAS EN DISOLVENTES ORGÁNICOS (NO DESORCIÓN) Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

INMOVILIZACIÓN POR ADSORCIÓN üUnión iónica es bastante habitual. üSe usan a nivel industrial resinas intercambiadoras : ücatiónicas ücarboximetilcelulosa üamberlite IRA üaniónicas üdietilaminoetilcelulosa (DEAE-celulosas) üresinas Sephadex üSe precisa un exquisito control del p. H de la inmovilización : Coherencia con la carga neta enzimática como consecuencia del p. Ka. Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

INMOVILIZACIÓN POR ADSORCIÓN üMetodologías empleadas: ümétodos en batch üayuda de precipitación (ej acetona, isopropanol) ümétodos en columna üplug flow ülecho fluidizado üREGLA DEL DIÁMETRO DE GIRO (spin diameter) Prof. J. M. Sánchez Montero, Facultad de Farmacia, UCM, Madrid, España

Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM

Prof. J. M. Sánchez Montero, Grupo de Biotransformaciones, Facultad de Farmacia, UCM
 Dr. alireza peyman
Dr. alireza peyman Mezkalitos
Mezkalitos Elisa snchez
Elisa snchez Nombres de unicornios
Nombres de unicornios Elisa snchez
Elisa snchez Genes ligados
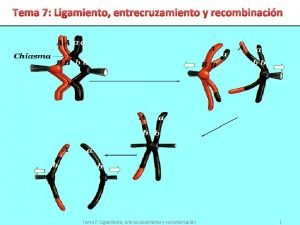
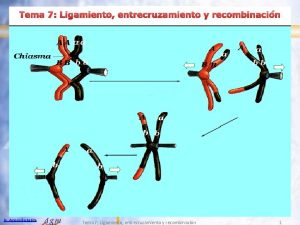
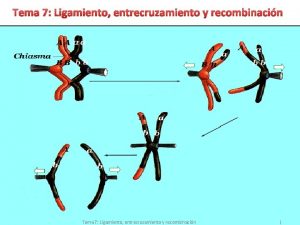
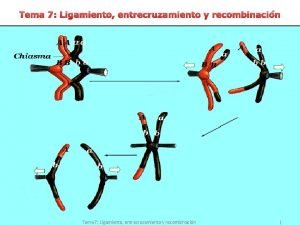
Genes ligados Entrecruzamiento cromosomas
Entrecruzamiento cromosomas Entrecruzamiento dibujo
Entrecruzamiento dibujo Quiasmas
Quiasmas Zigonema
Zigonema Cromosomas entrecruzamiento
Cromosomas entrecruzamiento Ligamiento y entrecruzamiento
Ligamiento y entrecruzamiento Recombinación del adn en la reproducción asexual
Recombinación del adn en la reproducción asexual Hoy rezo por ti
Hoy rezo por ti La banderita española letra
La banderita española letra Por fuera muy colorido por dentro una sorpresa
Por fuera muy colorido por dentro una sorpresa Esforzaos entrar por la puerta estrecha
Esforzaos entrar por la puerta estrecha Campanita campanera blanca por dentro y verde por fuera
Campanita campanera blanca por dentro y verde por fuera Frases de los libros sapienciales
Frases de los libros sapienciales Aqui esta la paciencia de los santos
Aqui esta la paciencia de los santos Porque este hombre caminaba por el bosque
Porque este hombre caminaba por el bosque Las personas valen por lo que son y no por lo que tienen
Las personas valen por lo que son y no por lo que tienen Por que o entrevistado não vai agradecer por ele ter vindo
Por que o entrevistado não vai agradecer por ele ter vindo Por el amor brindo por la familia
Por el amor brindo por la familia Adonde vas ahora a la clase de matematicas
Adonde vas ahora a la clase de matematicas Brindo por el amor brindo por la familia
Brindo por el amor brindo por la familia Indice de canciones
Indice de canciones Simetria de conjuntos ejemplos
Simetria de conjuntos ejemplos Estudio bíblico sobre el infierno y el lago de fuego
Estudio bíblico sobre el infierno y el lago de fuego Representacion sucesoria
Representacion sucesoria Solo quiero orar un momento mas
Solo quiero orar un momento mas