HaberBoschVerfahren Ammoniaksynthese Durch das HaberBoschVerfahren war es zu

Haber-Bosch-Verfahren Ammoniaksynthese Durch das Haber-Bosch-Verfahren war es zu Beginn des 20. Jahrhunderts möglich, große Mengen Ammoniak herzustellen. H H H H H N N H H H N N N H H H H N H H N H H H Entwickelt wurde das Verfahren von deutschen Chemikern Fritz Haber und Carl Bosch. H N
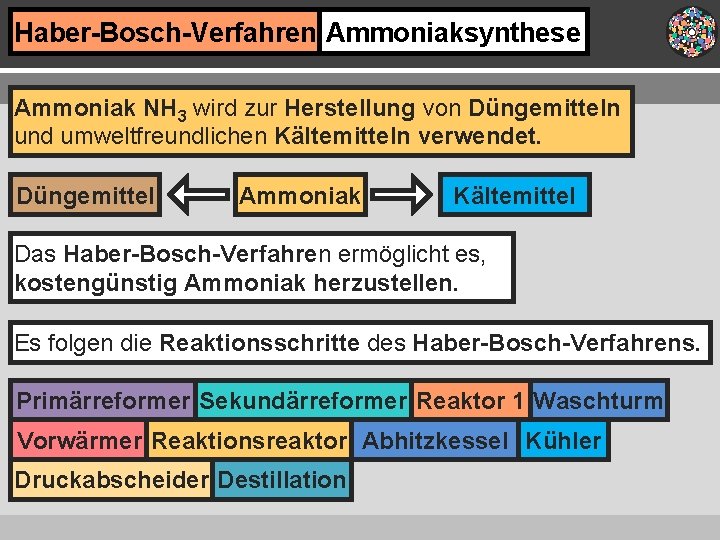
Haber-Bosch-Verfahren Ammoniaksynthese Ammoniak NH 3 wird zur Herstellung von Düngemitteln und umweltfreundlichen Kältemitteln verwendet. Düngemittel Ammoniak Kältemittel Das Haber-Bosch-Verfahren ermöglicht es, kostengünstig Ammoniak herzustellen. Es folgen die Reaktionsschritte des Haber-Bosch-Verfahrens. Primärreformer Sekundärreformer Reaktor 1 Waschturm Vorwärmer Reaktionsreaktor Abhitzkessel Kühler Druckabscheider Destillation
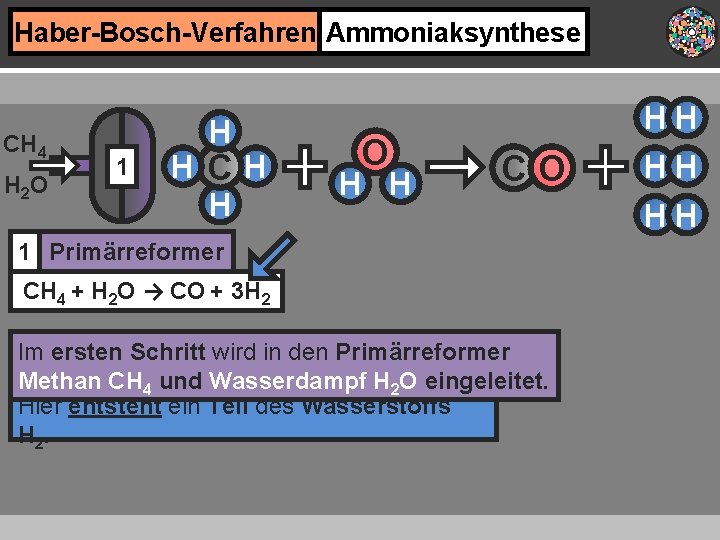
Haber-Bosch-Verfahren Ammoniaksynthese CH 4 H 2 O H 1 HCH H O H H HH CO 1 Primärreformer CH 4 + H 2 O → CO + 3 H 2 Im ersten Schritt wird in den Primärreformer Methan CH 4 und Wasserdampf H 2 O eingeleitet. Hier entsteht ein Teil des Wasserstoffs H 2. HH HH
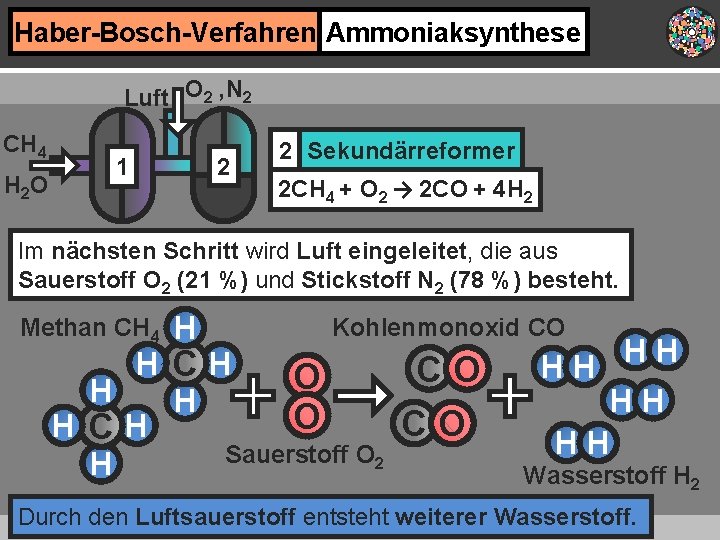
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 2 1 2 Sekundärreformer 2 CH 4 + O 2 → 2 CO + 4 H 2 Im nächsten Schritt wird Luft eingeleitet, die aus Sauerstoff O 2 (21 %) und Stickstoff N 2 (78 %) besteht. Methan CH 4 H Kohlenmonoxid CO HCH CO O H H O CO HCH Sauerstoff O 2 H HH HH Wasserstoff H 2 Durch den Luftsauerstoff entsteht weiterer Wasserstoff.
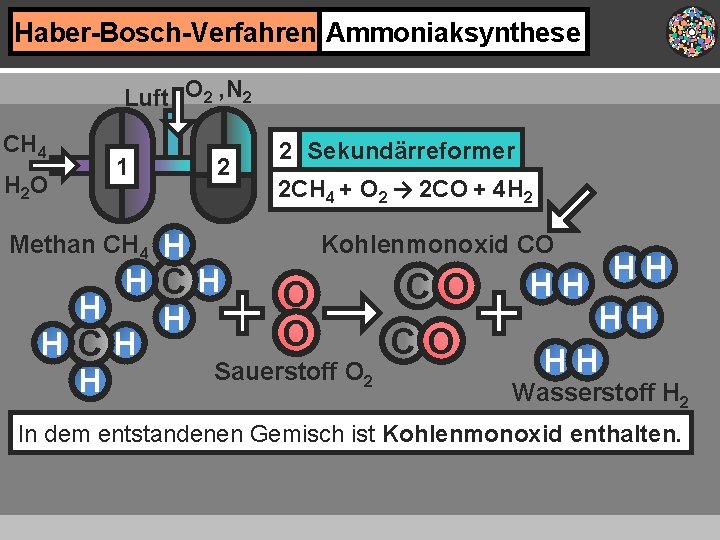
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 2 1 Methan CH 4 H 2 Sekundärreformer 2 CH 4 + O 2 → 2 CO + 4 H 2 Kohlenmonoxid CO HCH CO O H H O CO HCH Sauerstoff O 2 H HH HH Wasserstoff H 2 In dem entstandenen Gemisch ist Kohlenmonoxid enthalten.
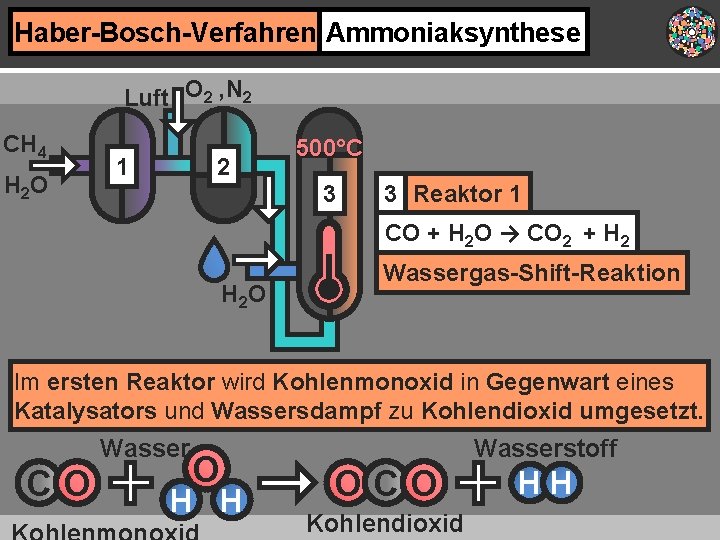
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 2 1 500°C 3 3 Reaktor 1 CO + H 2 O → CO 2 + H 2 O Wassergas-Shift-Reaktion Im ersten Reaktor wird Kohlenmonoxid in Gegenwart eines Katalysators und Wassersdampf zu Kohlendioxid umgesetzt. Wasser CO O H H Wasserstoff OCO Kohlendioxid HH
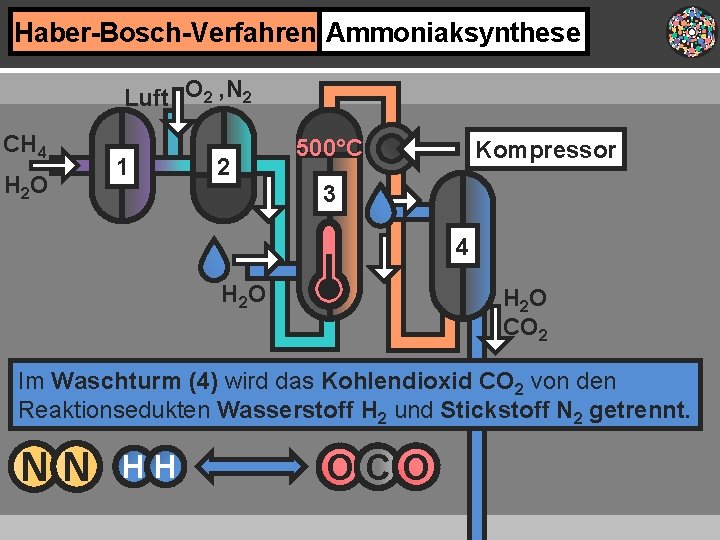
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C Kompressor 3 4 H 2 O CO 2 Im Waschturm (4) wird das Kohlendioxid CO 2 von den Reaktionsedukten Wasserstoff H 2 und Stickstoff N 2 getrennt. HH OCO NN
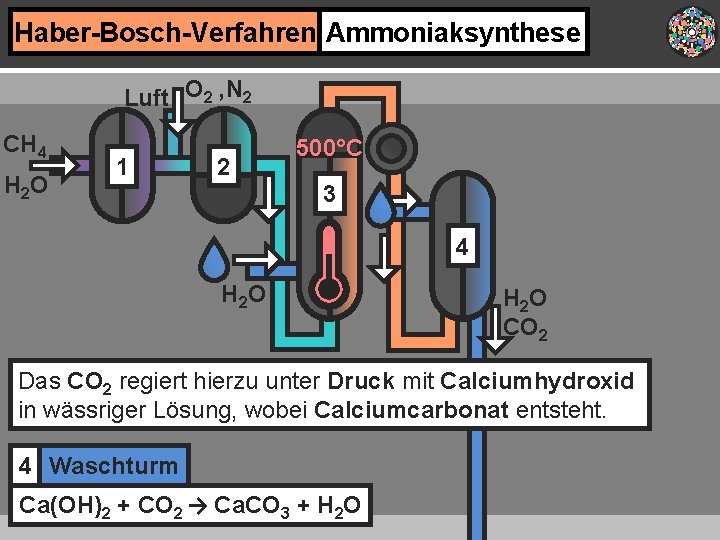
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C 3 4 H 2 O CO 2 Das CO 2 regiert hierzu unter Druck mit Calciumhydroxid in wässriger Lösung, wobei Calciumcarbonat entsteht. 4 Waschturm Ca(OH)2 + CO 2 → Ca. CO 3 + H 2 O
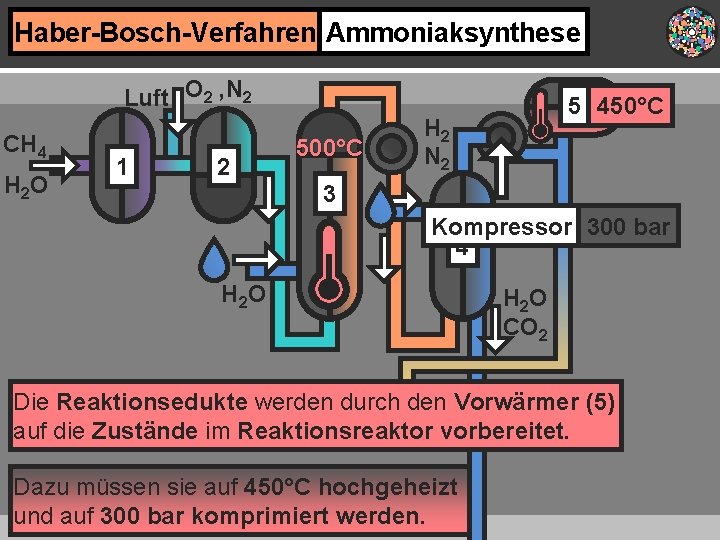
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C 5 450°C H 2 N 2 3 Kompressor 300 bar 4 H 2 O CO 2 Die Reaktionsedukte werden durch den Vorwärmer (5) auf die Zustände im Reaktionsreaktor vorbereitet. Dazu müssen sie auf 450°C hochgeheizt und auf 300 bar komprimiert werden.
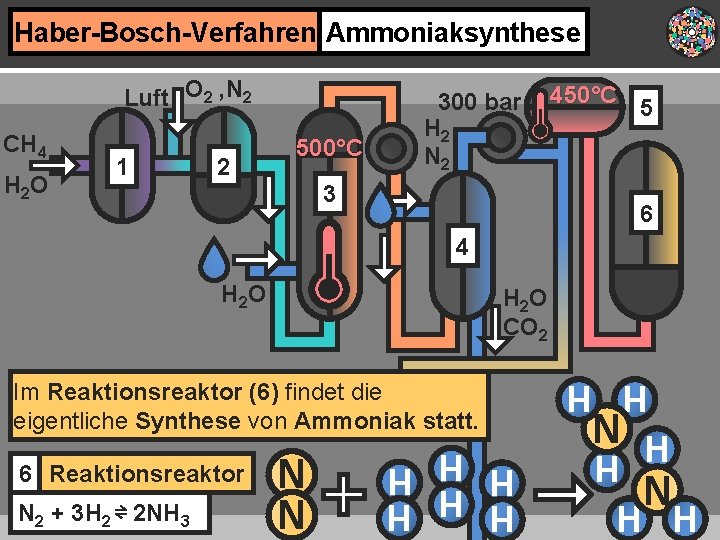
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C 300 bar H 2 N 2 450°C 3 5 6 4 H 2 O CO 2 H H H H N N N 2 + 3 H 2 ⇌ 2 NH 3 N 6 Reaktionsreaktor H H Im Reaktionsreaktor (6) findet die eigentliche Synthese von Ammoniak statt. H N H H
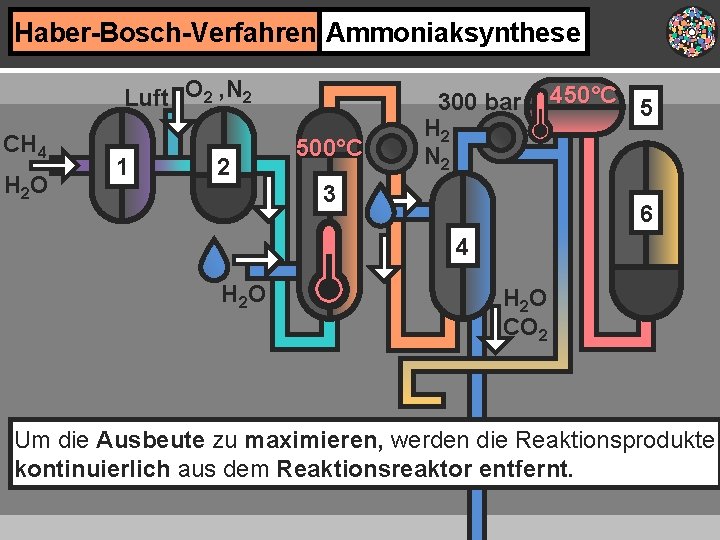
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C 300 bar H 2 N 2 3 450°C 5 6 4 H 2 O CO 2 Um die Ausbeute zu maximieren, werden die Reaktionsprodukte kontinuierlich aus dem Reaktionsreaktor entfernt.
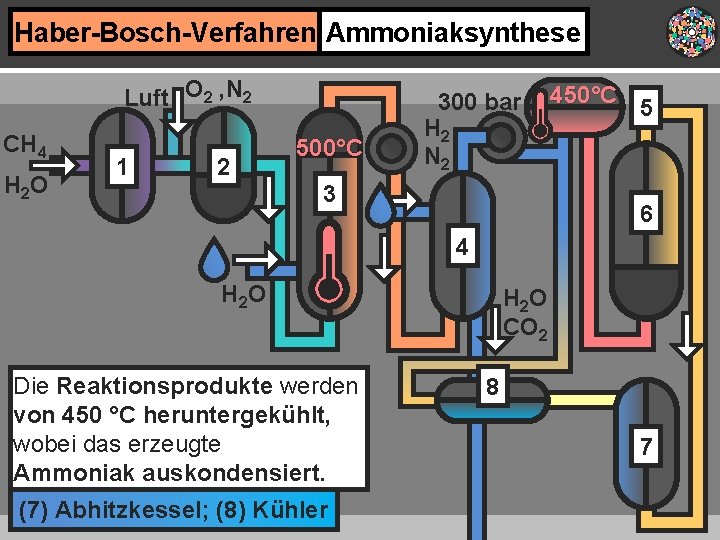
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C 300 bar H 2 N 2 3 450°C 5 6 4 H 2 O Die Reaktionsprodukte werden von 450 °C heruntergekühlt, wobei das erzeugte Ammoniak auskondensiert. (7) Abhitzkessel; (8) Kühler H 2 O CO 2 8 7
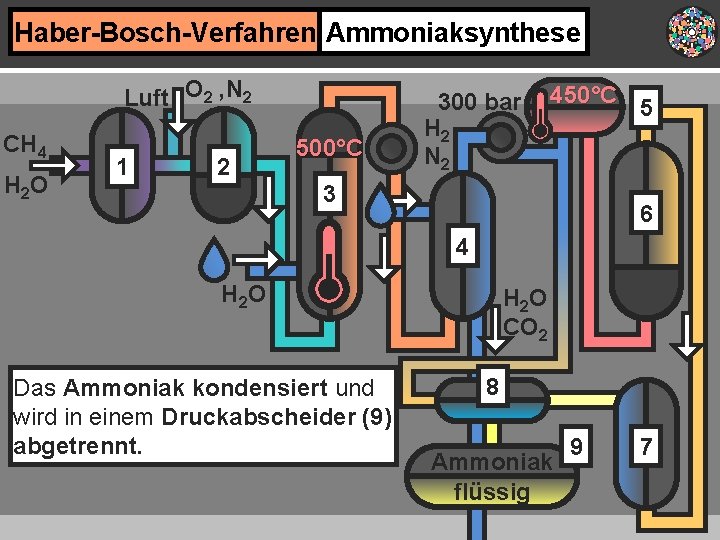
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C 300 bar H 2 N 2 450°C 3 5 6 4 H 2 O Das Ammoniak kondensiert und wird in einem Druckabscheider (9) abgetrennt. H 2 O CO 2 8 Ammoniak flüssig 9 7
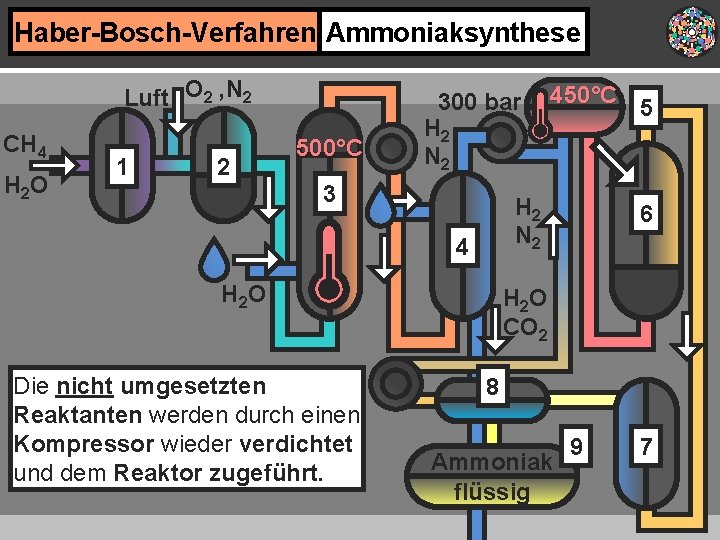
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C 300 bar H 2 N 2 3 H 2 N 2 4 H 2 O Die nicht umgesetzten Reaktanten werden durch einen Kompressor wieder verdichtet und dem Reaktor zugeführt. 450°C 5 6 H 2 O CO 2 8 Ammoniak flüssig 9 7
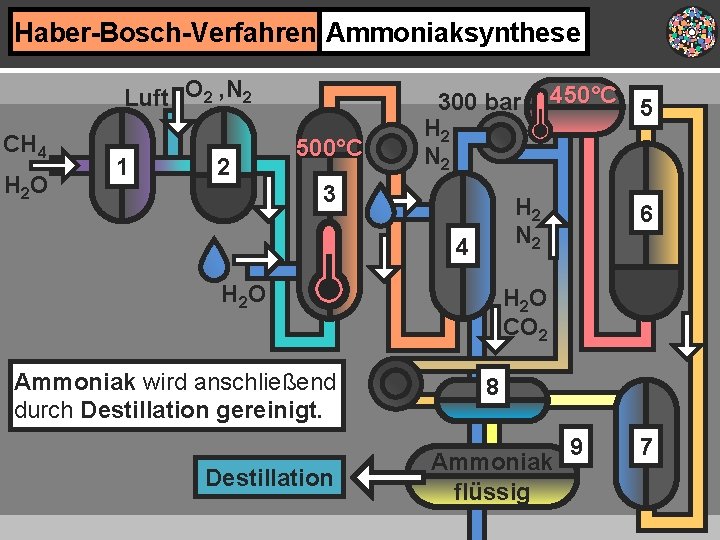
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O 1 2 500°C 300 bar H 2 N 2 3 H 2 N 2 4 H 2 O Ammoniak wird anschließend durch Destillation gereinigt. Destillation 450°C 5 6 H 2 O CO 2 8 Ammoniak flüssig 9 7
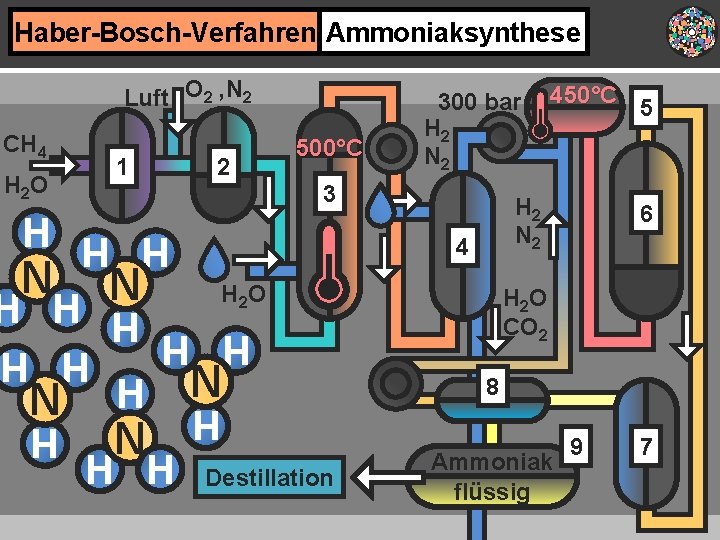
Haber-Bosch-Verfahren Ammoniaksynthese Luft O 2 , N 2 CH 4 H 2 O H H Destillation 6 8 H N N H 5 H 2 O CO 2 H H H 450°C H 2 N 2 4 N N 3 H H H 2 1 500°C 300 bar H 2 N 2 Ammoniak flüssig 9 7 N H

Haber-Bosch-Verfahren Ammoniaksynthese Im Jahr 1913 nahm die BASF erstmals eine Anlage nach dem Haber-Bosch-Verfahren in Betrieb. Fritz Haber und Carl Bosch erhielten für die Entwicklung des Haber-Bosch-Verfahrens den Nobelpreis für Chemie.

Haber-Bosch-Verfahren Ammoniaksynthese Zusammenfassung: Durch das Haber-Bosch-Verfahren wird aus Stickstoff N 2 und Wasserstoff H 2, Ammoniak NH 3 hergestellt. Die Ausbeute von Ammoniak ist von vier Reaktionsbedingungen abhängig. Temperatur 450°C, einen Druck von 250 -300 bar, eine hohe N 2 Konzentration und einen Katalysator.
- Slides: 18