Die Ammoniaksynthese Das HaberBoschVerfahren Ammoniak NH 3 Siedepunkt

Die Ammoniaksynthese Das Haber-Bosch-Verfahren

Ammoniak § § § § NH 3 Siedepunkt: -33°C Stark riechendes, giftiges Gas Leichter als Luft Sehr gut wasserlöslich Reagiert alkalisch Jährliche Produktion: 120 Mio Tonnen

Anwendungen von Ammoniak § Hohe Verdampfungswärme: Kühlschrank § Ausgangsstoff für Synthese von: – Salpetersäure – Sprengstoffe – Medikamente – Düngemittel – Harnstoff –…

Synthese von Ammoniak § Aber wie stellt man Ammoniak her ? ? / Fritz Haber Carl Bosch

Synthese von Ammoniak Aus den Elementen Stickstoff und Wasserstoff: N 2 + 3 H 2 2 NH 3 DH=-92, 5 k. J/mol Hin-Reaktion: exotherm Erhöhung der Temperatur: Beschleunigung des Erreichens des GGW‘s aber: GGW verschiebt sich nach links Also: bei möglichst tiefer Temperatur arbeiten

Synthese von Ammoniak N 2 + 3 H 2 2 NH 3 DH=-92, 5 k. J/mol Die Zugabe eines Katalysators erhöht die Geschwindigkeit ohne das GGW zu Verschieben.

Synthese von Ammoniak N 2 + 3 H 2 2 NH 3 DH=-92, 5 k. J/mol Erhöhung des Drucks: Verschiebung des GGW nach rechts Also: Die besten Bedingungen sind: möglichst tiefe Temperatur (immerhin 500°C) Hoher Druck Geeigneter Katalysator

Die industrielle Herstellung § 1913 in Ludwigshafen an der BASF Experimentalaufbau zur Synthese von Ammoniak Heute arbeiten allein in Ludwigshafen 34 150 Mitarbeiter der BASF

Die industrielle Herstellung § Erzeugung des Synthesegasgemischs: N 2 + 3 H 2 2 NH 3 § Stickstoff ist der Hauptbestandteil der Luft, der Sauerstoff muss noch entfernt werden § Wasserstoff muss durch Dampfspaltung von Methan gewonnen werden
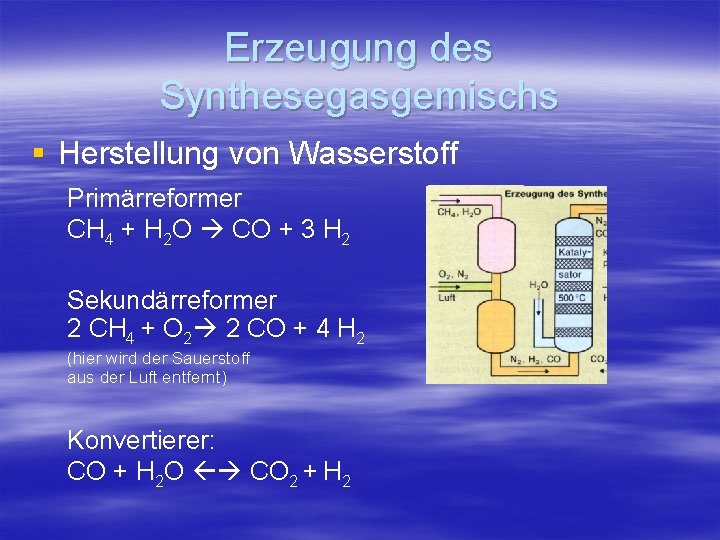
Erzeugung des Synthesegasgemischs § Herstellung von Wasserstoff Primärreformer CH 4 + H 2 O CO + 3 H 2 Sekundärreformer 2 CH 4 + O 2 2 CO + 4 H 2 (hier wird der Sauerstoff aus der Luft entfernt) Konvertierer: CO + H 2 O CO 2 + H 2

Erzeugung des Synthesegasgemischs § Am Ende dieses Prozesses ist also der Sauerstoff aus der Luft entfernt worden und es liegt folgendes Gasgemisch vor: – Stickstoff – Wasserstoff – Kohlenstoffdioxid
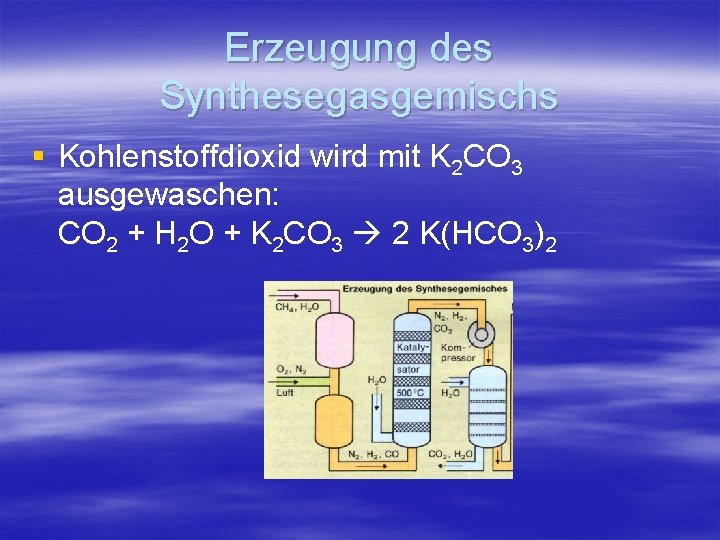
Erzeugung des Synthesegasgemischs § Kohlenstoffdioxid wird mit K 2 CO 3 ausgewaschen: CO 2 + H 2 O + K 2 CO 3 2 K(HCO 3)2

Synthese von Ammoniak § Nun liegt das Synthesegasgemisch vor: – 1 Teil Stickstoff – 3 Teile Wasserstoff N 2 + 3 H 2 2 NH 3 DH=-92, 5 k. J/mol

Synthese von Ammoniak § Das kalte Synthesegas wird durch Kompressoren auf den Reaktionsdruck gebracht. § Die Reaktion ist exotherm: es wird Wärme freigesetzt. N 2 + 3 H 2 2 NH 3 DH=-92, 5 k. J/mol § Das heiße Gasgemisch erhitzt das Synthesegas auf 500°C.

Synthese von Ammoniak Die Synthese wird im Kreislauf betrieben, das gebildete Ammoniak wird abgekühlt, verflüssigt und abgetrennt die Stoffe die nicht reagiert haben werden erneut eingespeist.

Synthese von Ammoniak § Der Reaktor, in dem die Reaktion abläuft produziert täglich 1500 Tonnen Ammoniak und ist 30 m hoch. § Moderne Reaktoren enthalten bis zu 100 Tonnen Katalysator.
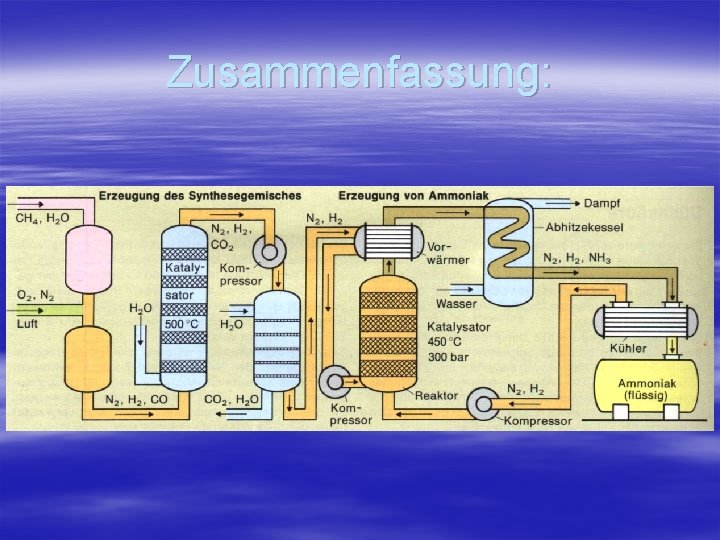
Zusammenfassung:
- Slides: 17