EXERCCIOS DA LISTA TERMODIN MICA APOSTILA 1 PGINA







- Slides: 8

EXERCÍCIOS DA LISTA “TERMODIN MICA” APOSTILA 1 PÁGINA 78

ENERGIA INTERNA DE UM GÁS

pp 78 #08 Duas amostras de massas iguais de um mesmo gás perfeito são colocadas em dois recipientes, A e B. As temperaturas são diferentes, sendo TA > TB. Podemos afirmar que: a) o gás em A possui mais calor que em B; b) o gás em A possui menor velocidade que em B; c) a energia cinética das moléculas é menor no gás em A que em B; d) a energia cinética média das moléculas do gás é maior em A que em B; e) a temperatura não influencia a energia de movimento das partículas de um gás.

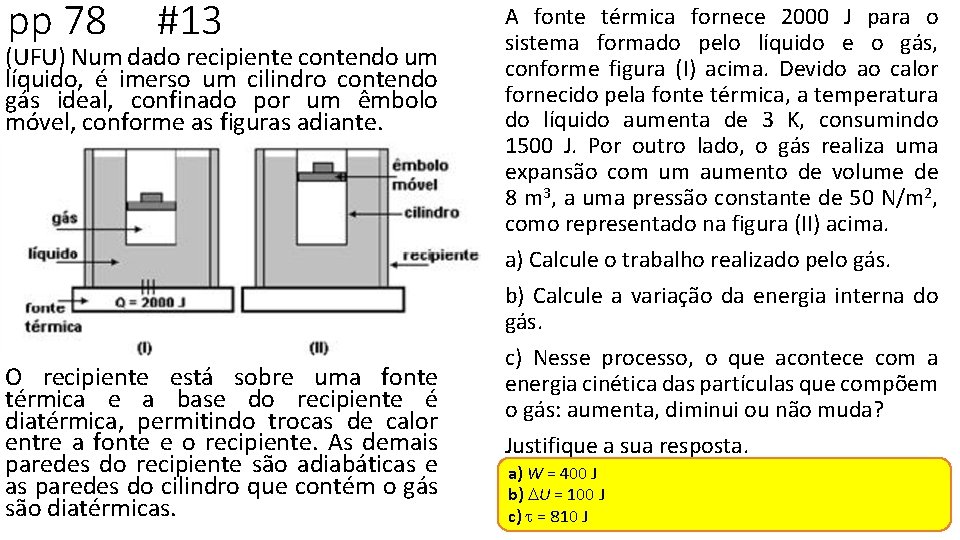
pp 78 #13 (UFU) Num dado recipiente contendo um líquido, é imerso um cilindro contendo gás ideal, confinado por um êmbolo móvel, conforme as figuras adiante. O recipiente está sobre uma fonte térmica e a base do recipiente é diatérmica, permitindo trocas de calor entre a fonte e o recipiente. As demais paredes do recipiente são adiabáticas e as paredes do cilindro que contém o gás são diatérmicas. A fonte térmica fornece 2000 J para o sistema formado pelo líquido e o gás, conforme figura (I) acima. Devido ao calor fornecido pela fonte térmica, a temperatura do líquido aumenta de 3 K, consumindo 1500 J. Por outro lado, o gás realiza uma expansão com um aumento de volume de 8 m 3, a uma pressão constante de 50 N/m 2, como representado na figura (II) acima. a) Calcule o trabalho realizado pelo gás. b) Calcule a variação da energia interna do gás. c) Nesse processo, o que acontece com a energia cinética das partículas que compõem o gás: aumenta, diminui ou não muda? Justifique a sua resposta. a) W = 400 J b) DU = 100 J c) t = 810 J

pp 78 #14 Num recipiente hermeticamente fechado, encontramos nitrogênio à temperatura de 0 °C, Como o mol do referido gás é igual a 28 g, qual o valor da velocidade média quadrática das suas partículas? Dado: R= 8, 31 J/mol K 493 m/s

PRIMEIRA LEI DA TERMODIN MICA

pp 79 #16 (UNIFESP) A figura representa uma amostra de um gás, suposto ideal, contida dentro de um cilindro. As paredes laterais e o êmbolo são adiabáticos; a base é diatérmica e está apoiada em uma fonte de calor. Considere duas situações: I. o êmbolo pode mover-se livremente, permitindo que o gás se expanda à pressão constante; II. o êmbolo é fixo, mantendo o gás a volume constante. Suponha que nas duas situações a mesma quantidade de calor é fornecida a esse gás, por meio dessa fonte. Pode-se afirmar que a temperatura desse gás vai aumentar a) igualmente em ambas as situações. b) mais em I do que em II. c) mais em II do que em I. d) em I, mas se mantém constante em II. e) em II, mas se mantém constante em I.

pp 79 #17 (UNESP) Um pistão com êmbolo móvel contém 2 mols de O 2 e recebe 581 J de calor. O gás sofre uma expansão isobárica na qual seu volume aumentou de 1, 66 L, a uma pressão constante de 105 N/m 2. Considerando que nessas condições o gás se comporta como gás ideal, utilize R = 8, 3 J/(mol. K) e calcule a) a variação de energia interna do gás. b) a variação de temperatura do gás. a) DU = 415 J b) DT = 10 K