Dal modellino dei Gas perfetti alla Tecnologia del


















- Slides: 23

Dal modellino dei Gas perfetti alla Tecnologia del vuoto �Il gas perfetto è un “modellino” teorico che permette di “progettare e dimensionare i sistemi da vuoto”, parte tutto da PV= Nk. T (*) �L’equazione (*) contiene tutte le informazioni necessarie per qualsiasi tipo di gas. �Ed è impressionante: �P pressione del gas, mette in relazione grandezze �V Volume che lo contiene, MACROSCOPICHE �N numero di molecole, (P, V e T) �k costante dei Boltzmann e con la grandezze microscopica N �T temperatura del gas (K) ( numero di atomi, molecole) Vuoto e Spettrometria di Massa

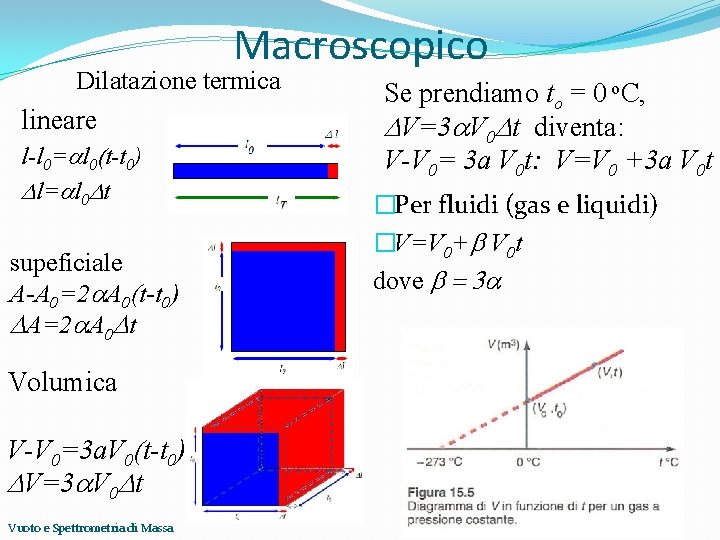
Macroscopico Dilatazione termica lineare l-l 0=al 0(t-t 0) Dl=al 0 Dt supeficiale A-A 0=2 a. A 0(t-t 0) DA=2 a. A 0 Dt Volumica V-V 0=3 a. V 0(t-t 0) DV=3 a. V 0 Dt Vuoto e Spettrometria di Massa Se prendiamo to = 0 o. C, DV=3 a. V 0 Dt diventa: V-V 0= 3 a V 0 t: V=V 0 +3 a V 0 t �Per fluidi (gas e liquidi) �V=V 0+b V 0 t dove b = 3 a

Dilatazione dei gas Dati sperimentali DV =V-V 0 =m ∙ t, da V=V 0 + b ∙ Vo t si ha: m = b ∙ Vo Per tutti i gas che non condensano, a pressione costante si ha che b è lo stesso. Ad un gas rarefatto (vuoto) questo modellino si adatta molto bene. Vuoto e Spettrometria di Massa

Scala termometrica dei Kelvin Riscriviamo DV= b ∙ Vo ∙ Dt , dato che to = 0 Conversione della scala termometrica da ° Celsius a gradi Kelvin o. C, si ha V= Vo (1+ b ∙ t) tk = T = tc + 273. 15 V= Vo (1+ b ∙ t) 1ª legge di Gay-Lussac o (Volta Gay-Lussac) Vuoto e Spettrometria di Massa

V constante 2 a legge di Gay-Lussac Dp = m’ ∙ Dt, Anche in questo caso si ha m’ = b ∙ po, come per la variazione di volume si aveva m = b ∙ Vo e b vale sempre Quindi allo stesso modo con la scala assoluta si ha: 2ª legge di Gay-Lussac o (Volta Gay-Lussac) Vuoto e Spettrometria di Massa

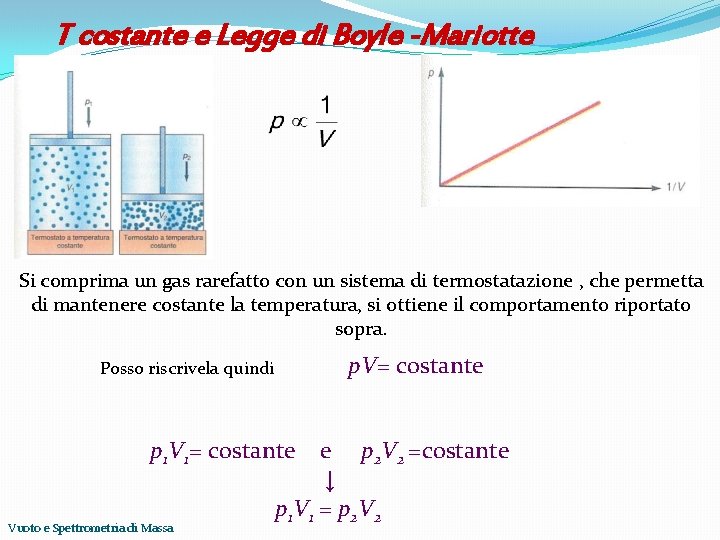
T costante e Legge di Boyle -Mariotte Si comprima un gas rarefatto con un sistema di termostatazione , che permetta di mantenere costante la temperatura, si ottiene il comportamento riportato sopra. p. V= costante Posso riscrivela quindi p 1 V 1= costante Vuoto e Spettrometria di Massa e p 2 V 2 =costante ↓ p 1 V 1 = p 2 V 2

Partiamo dalla relazione p 1 V 1 = p 2 V 2 (§) Prendiamo la 1 a legge di Gay-Lussac: Moltiplichiamo 1 o e 2 o membro dell’equazione (§) per questa quantità uguale: p 1 V 1 = p 2 V 2 (#) Prendiamo la 2 a legge di Gay-Lussac: Moltiplichiamo 1 o e 2 o membro dell’equazione (#) per una quantità uguale p 1 V 1 = p 2 Vuoto e Spettrometria di Massa

Si ricava ($) Cerco di ordinare a 1 o membro tutto con il pedice 1 ed al 2 o membro con il pedice 2, moltiplicando 1 o e 2 o membro dell’equazione ($) per una quantità uguale Semplifico; Vuoto e Spettrometria di Massa Si ha quindi;

Equazione di Stato dei Gas perfetti Tutti i tipi di gas in condizioni rarefatte (pressioni basse alto vuoto, quello che interessa a noi) soddisfano la seguente legge: Vuoto e Spettrometria di Massa

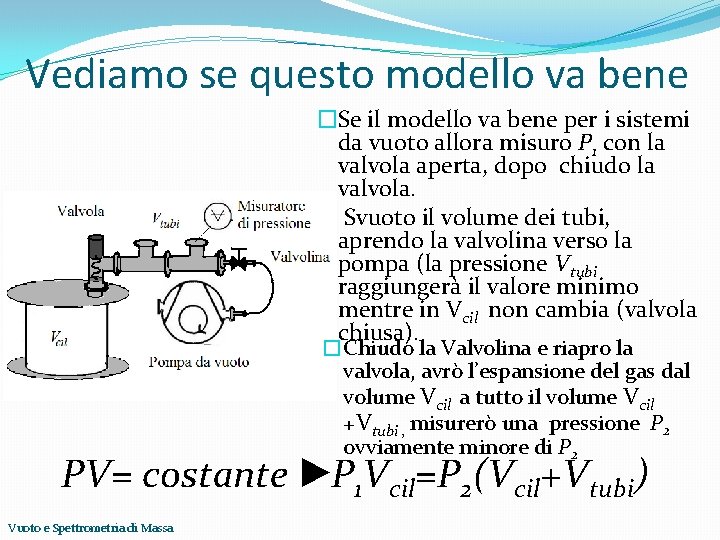
Vediamo se questo modello va bene �Se il modello va bene per i sistemi da vuoto allora misuro P 1 con la valvola aperta, dopo chiudo la valvola. � Svuoto il volume dei tubi, aprendo la valvolina verso la pompa (la pressione Vtubi raggiungerà il valore minimo mentre in Vcil non cambia (valvola chiusa). �Chiudo la Valvolina e riapro la valvola, avrò l’espansione del gas dal volume Vcil a tutto il volume Vcil +Vtubi , misurerò una pressione P 2 ovviamente minore di P 2 PV= costante ►P 1 Vcil=P 2(Vcil+Vtubi) Vuoto e Spettrometria di Massa

Questo vale per ogni successiva operazione � P 1 Vcil = P 2(Vcil+Vtubi) (a) �P 2 Vcil = P 3(Vcil+Vtubi) (b) �P 3. . . = P 4. . ecc. Se divido il primo membro di (a) per il primo membro di (b) , se uso la stessa quantità (secondi membri) l’uguaglianza non cambia. Il rapporto tra le pressioni rimane sempre lo stesso. Vuoto e Spettrometria di Massa

Misura dei rapporti tra le pressione, nel caso dell’espansione Pressione misurata nel volume Vtubi in espansioni successive P 1 P 2 P 3 P 4 P 5 P 6 P 7 P 8 P 9 P 10 P 1/P 2 P 2/P 3 P 3/P 4 P 4/P 5 P 5/P 6 P 6/P 7 P 7/P 8 P 8/P 9 P 9/P 10 media dei rapporti deviazione standard errore percentuale Vuoto e Spettrometria di Massa �La legge che abbiamo introdotto descrive bene il sistema per l’aria, anche in condizioni non rarefatte.

Misura dei rapporti tra P T, nel caso del riscaldamento dell’aria Pressione misurata nel volume Vtubi in espansioni successive P 1 P 2 P 3 P 4 P 5 P 6. . . Pn-1 Pn P 1 P 2 P 3 P 4 P 5 P 6. . . Tn-1 Tn Vuoto e Spettrometria di Massa P 2/P 1 P 3/P 2 P 4/P 3 P 5/P 4 P 6/P 5 Pn/Pn-1 = = =. . . = T 2/T 1 T 3/T 2 T 4/T 3 T 5/T 4 T 6/T 5 Tn/Tn-1 �La legge che abbiamo introdotto descrive bene il sistema per l’aria, anche in condizioni non rarefatte. �Si osservano che i rapporti, rimangono costanti e il rapporto delle pressioni è uguale al rapporto delle temperature.

Equazione di Stato dei Gas perfetti Tutti i tipi di gas in condizioni rarefatte (pressioni basse alto vuoto, quello che interessa a noi) soddisfano la seguente legge: Cos’è questa “costante” ? Vuoto e Spettrometria di Massa Continua

Numero di molecole, massa. . . �Quando gonfiamo un palloncino. = Immettiamo aria. . �Quando evacuiamo una camera. = Togliamo aria. Consideriamo quanto segue, conoscete il significato di queste uguaglianze “chimiche”: Vuoto e Spettrometria di Massa

Legge di Avogado 1811 �Nelle stesso condizioni di pressione e temperatura, stessi volumi di gas diversi contengono lo stesso numero di “particelle”, atomi, molecole … �Per i chimici questo numero è espresso per una mole alla pressione di una atmosfera ed alla temperatura di 0 °C, risultando in V= 22. 4 l. Numero di Avogadro Magari risulta più comprensibile per un volume delle dimensioni di un dado un cc (cm 3) Numero di Loschmidt Vuoto e Spettrometria di Massa

Ora possiamo riscrivere �P pressione, V volume T temperatura espressa in Kelvin, k costante di Boltzmann N numero di molecole. �Questa formula mette in relazione proprietà MACROSCOPICHE (P, V, T) e microscopiche il numero N di molecole. �È stato il cavallo di battaglia della prima teoria fisica: la teoria cinetica dei gas. Vuoto e Spettrometria di Massa

Le grandezze macroscopiche sono misurabili (comprensibili) in modo immediato Unità di misura e simboli utili PRESSIONE P � Dyne/cm 2 = mbar CGS � Newton/m 2 = Pascal � 1 Pa = 1. 0 10 -5 bar �Volumi � 1 m 3= 1 000 l �Litro = l = dm 3 = 1 000 cm 3 �m 3 = 1 000 cm 3 = = 106 cm 3 � 1 atm = 760 Torr (mm Hg) PRESSIONE P 1 atm = 1 013 mbar 1 mbar = 0. 75 Torr Vuoto e Spettrometria di Massa Potenze di 10 10 -12, 10 -9, 10 -6, 10 -3, 1, 103, 106, 109, 1012 pico, nano, micro, milli, . . . , chilo, mega, giga, tera. p, n, m, m, . . . , k, M, G, T

Condizioni stazionarie � Dopo l’evacuazione il sistema rimare ad una pressione costante � Ma la pompa sta asportando volume di gas nell’unità di tempo, ovvero asporta molecole, ci sarà una variazione di molecole nel tempo: (DN/Dt) � ma se moltiplichiamo per k. T: � : (DN/Dt)k. T= D(PV/Dt) che chiamiamo portata Q � Q= D(PV/Dt) � per P costante = P(DV/Dt) e T � dove DV/Dt volume di gas asportato Se guardiamo variazioni per intervalli di tempi infinitesimali Q= P(d. V/dt)=(d. N/dt)k. T d. V/dt= volume di gas evacuato detto: S velocità di pompaggio (l/s) Vuoto e Spettrometria di Massa

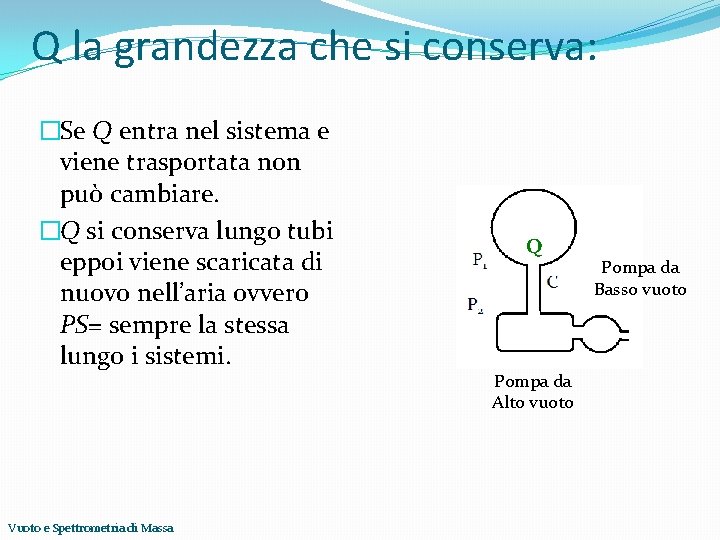
Q la grandezza che si conserva: �Se Q entra nel sistema e viene trasportata non può cambiare. �Q si conserva lungo tubi eppoi viene scaricata di nuovo nell’aria ovvero PS= sempre la stessa lungo i sistemi. Vuoto e Spettrometria di Massa Q Pompa da Alto vuoto Pompa da Basso vuoto

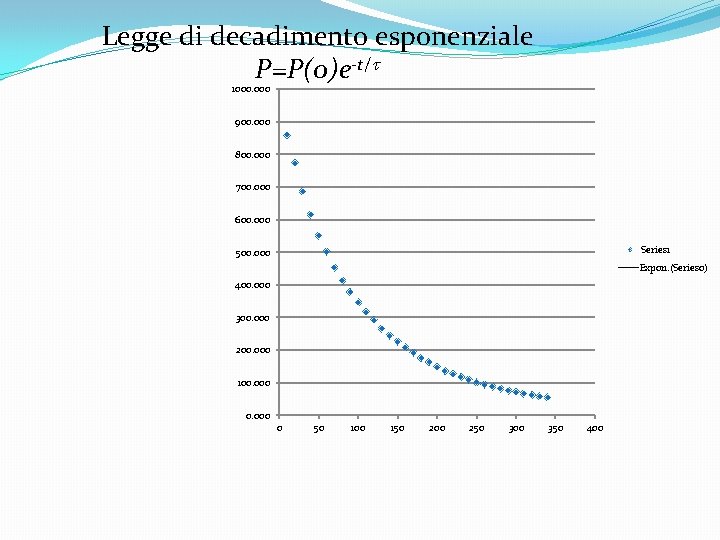
Condizioni non stazionarie: la pressione varia nel tempo. �P varia, consideriamo il volume del contenitore Vcil volume �(Pf-Pi)Vcil =Q=PS �=-d. P/dt=S/Vcil P �P=P(0)e-S/Vcil t = P=P(0)e-t/t �t detta costante di tempo t=Vcil / S �In un tempo t= t la pressione si riduce rispetto al valore iniziale a P=P(0)/e. �Vediamo sperimentalmente se è così. Vuoto e Spettrometria di Massa

Legge di decadimento esponenziale P=P(0)e-t/t 1000. 000 900. 000 800. 000 700. 000 600. 000 Series 1 500. 000 Expon. (Series 0) 400. 000 300. 000 200. 000 100. 000 0 50 100 150 200 250 300 350 400

Legge di decadimento esponenziale Decadimenti radioattivi : numero di atomi radioattivi che decadono nel tempo proporzionale al N Decadimento dell’intensità di particelle negli acceleratori :