Chimica Fisica Canale MZ Aula T 8 Gio
















- Slides: 22

Chimica Fisica Canale M-Z Aula T 8, Gio. 9 -11 Ven. 14 -16 Fino al 30 aprile Prof. Lorenzo Stella Sett. 5 Liv. 1 (Chimica Fisica) Stanza 4 0672594463 stella@stc. uniroma 2. it

Libri di testo • R. Chang Chimica Fisica (Vol. 1). Zanichelli 2003. • M. Venanzi Appunti di chimica fisica per scienze biologiche. Universitalia 2010. (via di Passolombardo 421) Modalità d’esame • Scritto (esercizi) • Voto finale unico con Chimica Organica (media pesata)

Esercitazioni Lunedì: – 12/4 – 19/4 – 3/5 – 10/5 Aula T 8, ore 14: 30 -16: 30 OPZIONALI

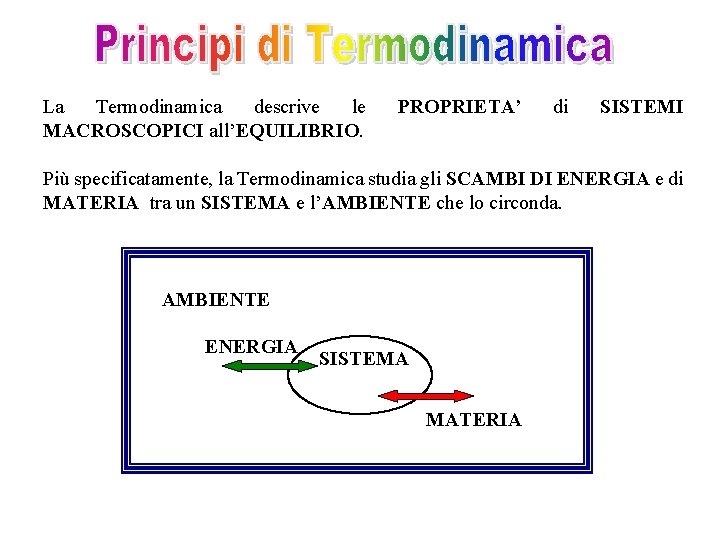
La Termodinamica descrive le MACROSCOPICI all’EQUILIBRIO. PROPRIETA’ di SISTEMI Più specificatamente, la Termodinamica studia gli SCAMBI DI ENERGIA e di MATERIA tra un SISTEMA e l’AMBIENTE che lo circonda. AMBIENTE ENERGIA SISTEMA MATERIA

SISTEMA - Un insieme costituito da un numero macroscopico di molecole, dell’ordine del numero di Avogadro, NA=6. 023 1023. Rappresenta una piccola parte di un sistema molto più grande (AMBIENTE) che lo racchiude interamente. AMBIENTE – Un sistema molto più grande del sistema in esame. Temperatura, volume e pressione dell’ambiente rimangono costanti qualunque siano i cambiamenti del sistema. In particolare, la sua temperatura non cambia qualunque sia l’energia scambiata tra sistema e ambiente.

U = energia scambiata tra sistema e ambiente n = materia scambiata tra sistema e ambiente SISTEMA ISOLATO: ISOLATO non ci sono né scambi di energia, né di materia U = 0 n = 0 SISTEMA CHIUSO: CHIUSO scambia energia, ma non materia U 0 n = 0 SISTEMA APERTO: APERTO scambia energia e materia U 0 n 0

EQUILIBRIO = uno stato durante il quale le proprietà del sistema non cambiano nel tempo. L’equilibrio è sempre di tipo dinamico. Esempio: Liquido puro in equilibrio con la sua fase vapore All’equilibrio: Gas n(gas)=costante n(g→l) n(liq)=costante dn(gas o liq) = dn(g→l) + dn(l→g) = 0 n(l→g) Liquido dn(g→l) = - dn(l→g)

D = rappresenta una variazione finita Ex. T = 10°C, p = 2 atm d = rappresenta una variazione infinitesima (differenziale) Ex. d. T, dp, d. V sono variazioni infinitesime di temperatura, pressione, volume.

Lo stato di equilibrio di un sistema è definito da poche variabili, dette VARIABILI DI STATO ESTENSIVE: DIPENDONO DAL NUMERO DI MOLECOLE CHE COMPONGONO IL SISTEMA. Ex. N = numero di molecole, V = Volume U = Energia interna H = Entalpia S = Entropia G = Energia libera Sono tutte grandezze estensive

VARIABILI DI STATO INTENSIVE NON DIPENDONO DAL NUMERO DI MOLECOLE CHE COMPONGONO IL SISTEMA. p = Pressione, T = Temperatura, = Potenziale chimico Le variabili di stato sono legate tra loro da equazioni dette EQUAZIONI DI STATO Ex. Equazione di stato dei gas ideali p. V=n. RT

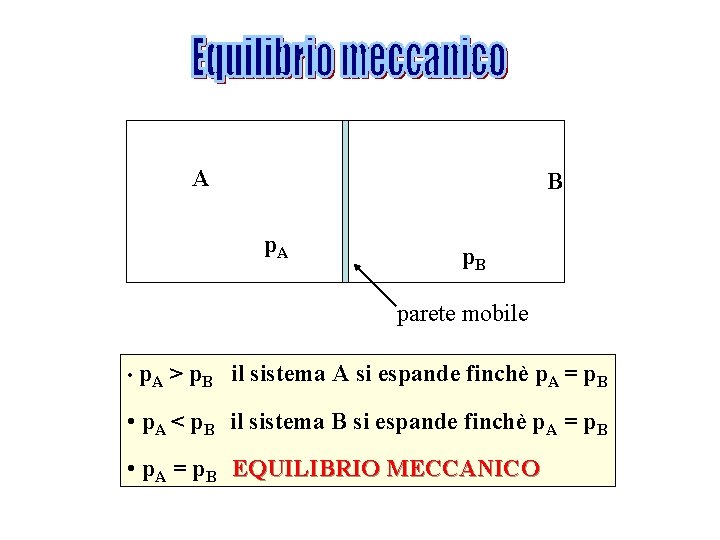
A B p. A p. B parete mobile • p. A > p. B il sistema A si espande finchè p. A = p. B • p. A < p. B il sistema B si espande finchè p. A = p. B • p. A = p. B EQUILIBRIO MECCANICO

1 atm = 760 torr (o mm. Hg) = la pressione esercitata da una colonna riempita di mercurio dell’altezza di 76 cm.

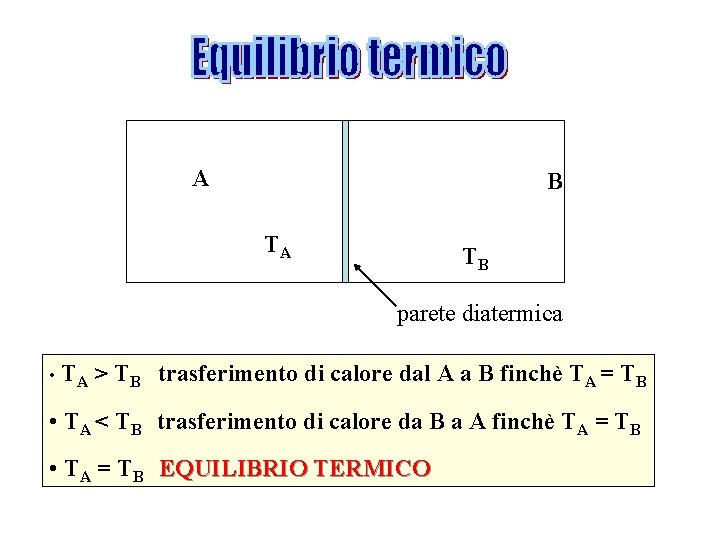
A B TA TB parete diatermica • TA > TB trasferimento di calore dal A a B finchè TA = TB • TA < TB trasferimento di calore da B a A finchè TA = TB • TA = TB EQUILIBRIO TERMICO

GAS IDEALE: un gas di molecole non interagenti e di volume trascurabile Equazione di stato dei gas ideali: p. V=n. RT n = numero di moli p = pressione V = volume T = temperatura R = costante universale dei gas

1. Legge di Boyle: p. V = costante per n e T costanti 2. Legge di Charles: V = cost T per n e p costanti Principio di Avogadro: V = cost n per p e Tcostanti Combinando questi leggi si ottiene l’equazione di stato dei gas ideali. Sono dette leggi limite perché valgono per tutti i gas reali allorchè la pressione è sufficientemente bassa da poter trascurare le interazioni tra le molecole (al limite per p che tende a zero).

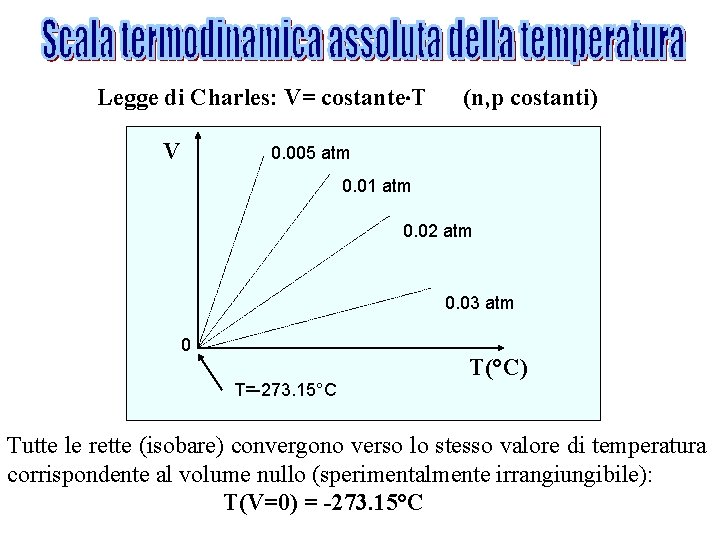
Legge di Charles: V= costante T V (n, p costanti) 0. 005 atm 0. 01 atm 0. 02 atm 0. 03 atm 0 T=-273. 15°C T(°C) Tutte le rette (isobare) convergono verso lo stesso valore di temperatura corrispondente al volume nullo (sperimentalmente irrangiungibile): T(V=0) = -273. 15°C

La scala Kelvin assume una scala lineare di temperature tra T = 0 K (zero assoluto -273. 15 °C) e T=273. 16 K (punto triplo del diagramma di fase dell’acqua 0. 01 °C). T(K) = T(°C) + 273. 15 Punto triplo = unico punto in cui coesistono le fasi solida, liquida e gassosa per l’H 2 O (T=273. 16 K, P=0. 0061173 bar). E’ detta scala assoluta delle temperature poiché tutte le sostanze si comportano come gas ideali al tendere a zero della pressione. In termodinamica si usa esclusivamente la scala assoluta delle temperature.

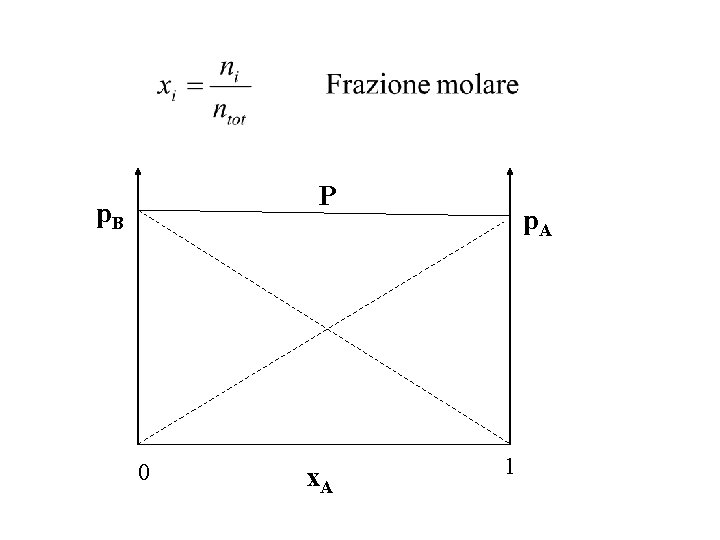
La pressione esercitata da una miscela di gas è data dalla somma delle pressioni parziali dei singoli componenti.

P p. B 0 x. A p. A 1

Condizioni normali: n = 1, p= 1 atm, T = 273. 16 K, V=22. 414 litri Equivalenza meccanica del calore (Mayer-Joule): 1 cal = 4. 184 J

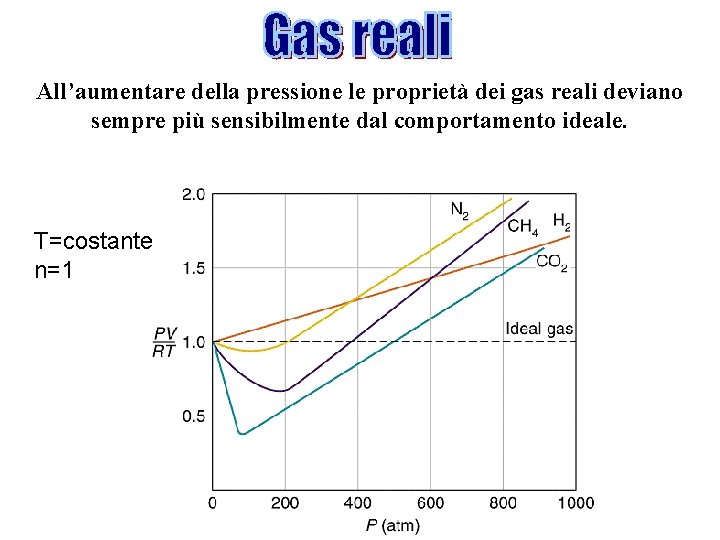
All’aumentare della pressione le proprietà dei gas reali deviano sempre più sensibilmente dal comportamento ideale. T=costante n=1

• Convertire 5 atm in Pa, bar, torr. • Un gas perfetto, in un recipiente a volume costante, ha pressione di 50. 2 torr alla temperatura di 273. 16 K. • Quale variazione di pressione è associata all’aumento di 1 K da questa temperatura? • Quale pressione corrisponde alla temperatura di 100 °C? • Quale variazione di pressione è associata all’aumento di 1 K da questa seconda temperatura? • Un recipiente di 22. 4 L contiene inizialmente 2 moli di idrogeno e 1 mole di azoto, a 273. 15 K. L’idrogeno reagisce completamente con l’azoto per dare ammoniaca. Calcolare la pressione parziale delle specie gassose presenti alla fine della reazione e la pressione totale della miscela finale.