CHEMICK vzba Kovalentn vzba Vzbu medzi atmami tvor

CHEMICKÁ väzba

Kovalentná väzba § Väzbu medzi atómami tvorí spoločný elektrónový pár H. +. H l. Cl. +. Cll H–H l. Cl – Cll H – Cll

Môže byť nepolárna - ak väzbové elektróny patria obidvom zlúčeným atómom rovnako.

Alebo polárna - ak väzbové elektróny nepatria obidvom atómom rovnako.

Elektronegativita § Sila , ktorou atóm priťahuje elektróny chemickej väzby, sa volá elektronegativita. § Elektronegativitu každého prvku nájdeme v periodickej sústave prvkov.
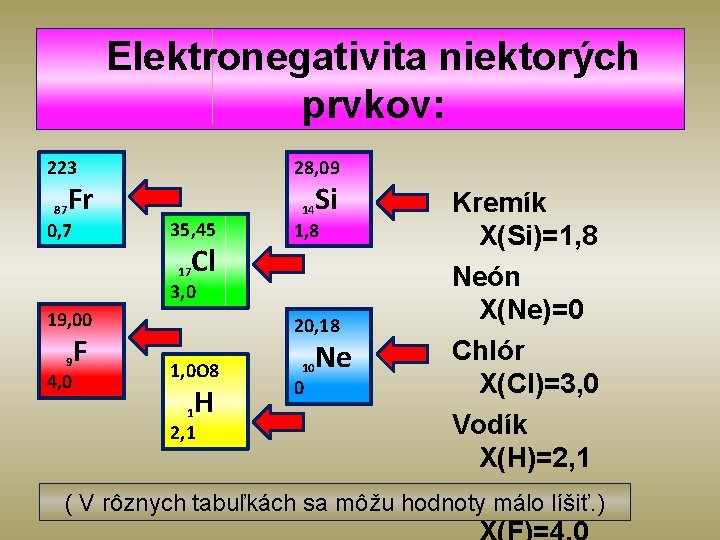
Elektronegativita niektorých prvkov: 223 Fr 28, 09 Si Kremík 35, 45 0, 7 1, 8 X(Si)=1, 8 17 Cl Neón 3, 0 X(Ne)=0 19, 00 20, 18 Chlór 9 F Ne 10 1, 0 O 8 4, 0 X(Cl)=3, 0 0 1 H Vodík 2, 1 X(H)=2, 1 Fluor ( V rôznych tabuľkách sa môžu hodnoty málo líšiť. ) 87 14

Ako zistíme, o aký typ kovalentnej väzby v danej molekule ide? Napríklad: H 2 Ak je rozdiel elektronegativít X(H) = 2, 1 zlúčených atómov od 0 až do 0, 4, X(H) – X(H) = potom je väzba =2, 1 – 2, 1 = nepolárna. 0

Molekula HCl: X(H) = 2, 1 X(Cl) = 3, 0 X(Cl) – X(H) = 3, 0 – 2, 1 = 0, 9 Ak je rozdiel elektronegativít zlúčených atómov väčší ako 0, 4 ale menší ako 1, 7, potom je väzba málo polárna.

Iónová väzba ( silne polárna) • tvoria ju opačne nabité Ak je rozdiel ióny elektronegativít Chlorid sodný zlúčených atómov Na. Cl: väčší ako 1, 7. X(Na) = 0, 9 X(Cl) = 3, 0 X(Cl) – X(Na)=
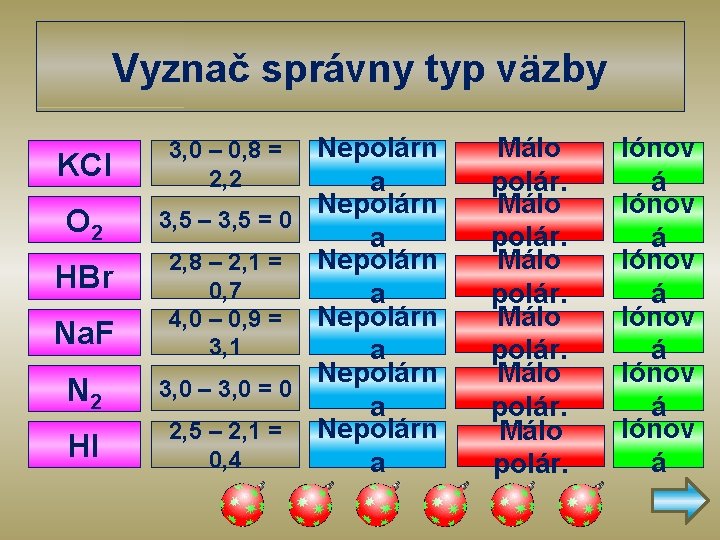
Vyznač správny typ väzby KCl O 2 HBr Na. F N 2 HI Nepolárn a Nepolárn 3, 5 – 3, 5 = 0 a 2, 8 – 2, 1 = Nepolárn 0, 7 a 4, 0 – 0, 9 = Nepolárn 3, 1 a Nepolárn 3, 0 – 3, 0 = 0 a 2, 5 – 2, 1 = Nepolárn 0, 4 a 3, 0 – 0, 8 = 2, 2 Málo polár. Iónov á Iónov á

Ďakujem za pozornosť
- Slides: 11