Chemick vzba Chemick vzba sdrn psobenie medzi dvoma

Chemická väzba

Chemická väzba -súdržné pôsobenie medzi dvoma alebo viacerými atómami sprostredkované elektrónmi

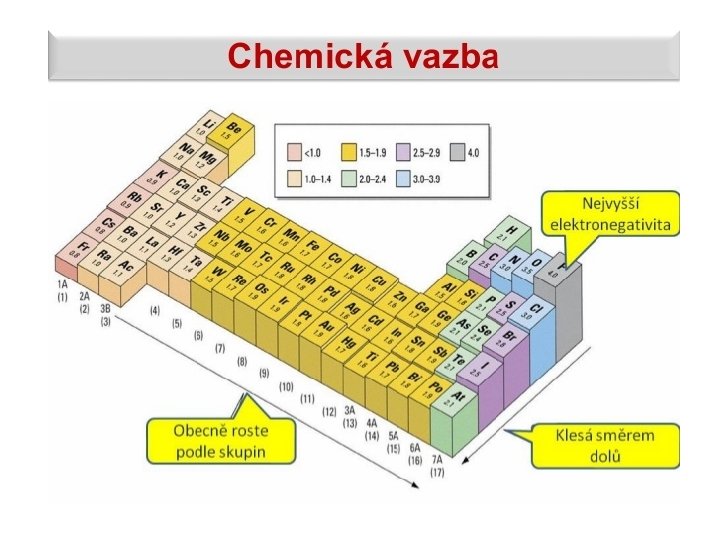
Elektronegativita (x) - sila, akou atóm priťahuje elektróny chemickej väzby -hodnoty elektronegativít chemických prvkov nájdeš v PSP -z rozdielu hodnôt elektronegativít zlúčených atómov zistíme o aký typ väzby sa jedná
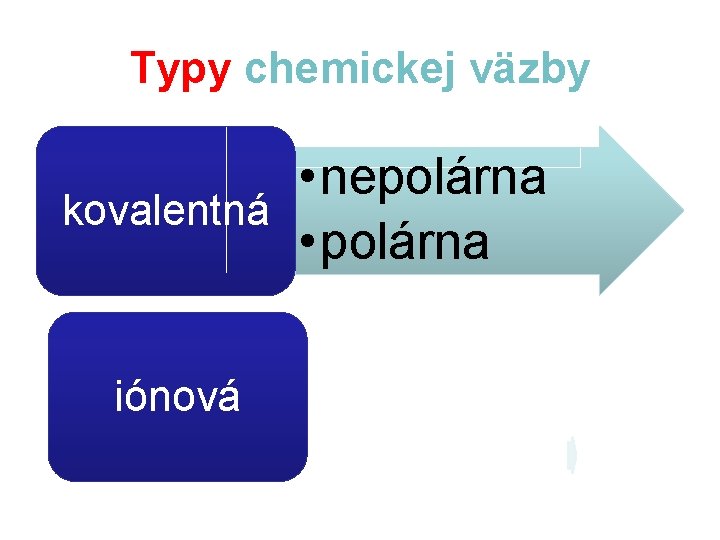
Typy chemickej väzby • nepolárna kovalentná • polárna iónová
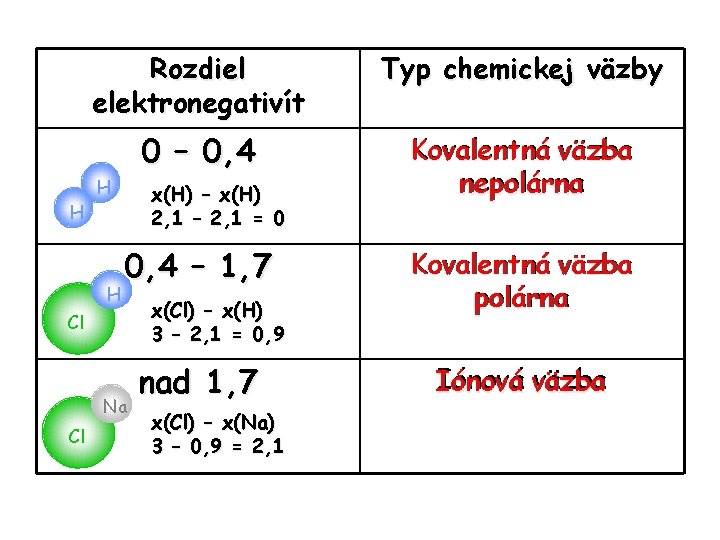
Rozdiel elektronegativít Typ chemickej väzby 0 – 0, 4 Kovalentná väzba nepolárna H x(H) – x(H) 2, 1 – 2, 1 = 0 H H 0, 4 – 1, 7 Cl Na Cl x(Cl) – x(H) 3 – 2, 1 = 0, 9 nad 1, 7 x(Cl) – x(Na) 3 – 0, 9 = 2, 1 Kovalentná väzba polárna Iónová väzba
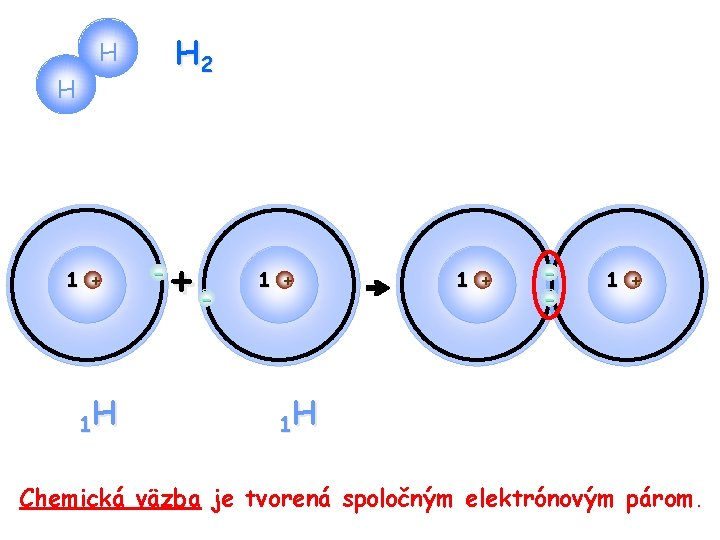
H 2 H H 1 + 1 H - +- 1 + 1 H Chemická väzba je tvorená spoločným elektrónovým párom.
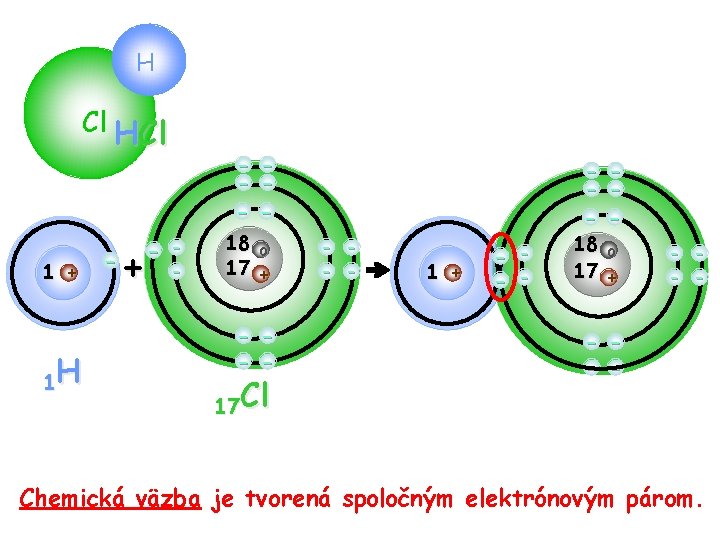
H Cl HCl 1 + 1 H - - - + - - 18 o 17 + - - - 17 Cl - - - 1 + - - 18 17 o + - - - Chemická väzba je tvorená spoločným elektrónovým párom.
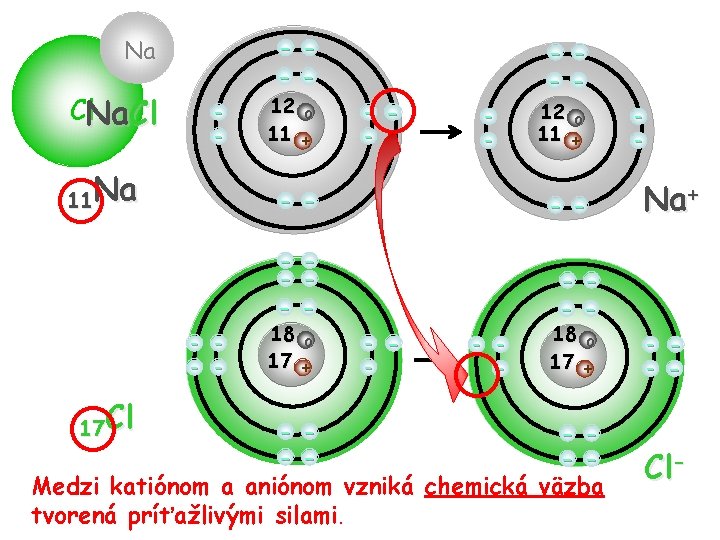
Na Cl. Na. Cl - 11 Na - - - - - 17 Cl - - 12 o 11 + - - - 18 o 17 + - - - - 12 o 11 + - - - Na+ - - 18 o 17 + - - Medzi katiónom a aniónom vzniká chemická väzba tvorená príťažlivými silami. - Cl-
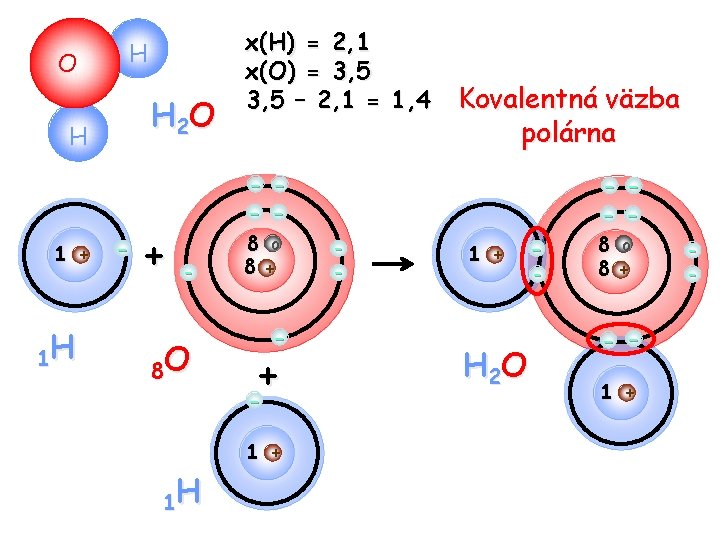
O H H 2 O H 1 + 1 H - + - 8 O x(H) = 2, 1 x(O) = 3, 5 – 2, 1 = 1, 4 - - 8 o 8 + - + 1 H - Kovalentná väzba polárna 1 + H 2 O - - - 8 o 8 + - 1 + -
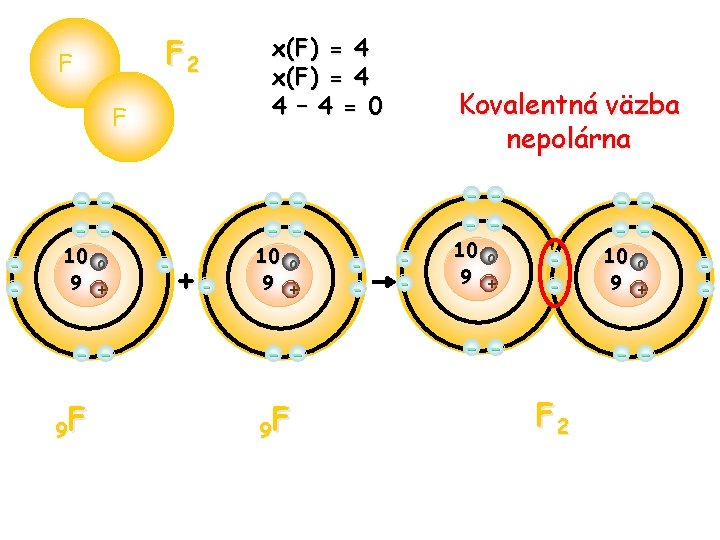
F 2 F F - 10 9 o + - - 9 F - +- x(F) = 4 4 – 4 = 0 10 9 Kovalentná väzba nepolárna o + - - 9 F - - 10 9 o + - - F 2 -
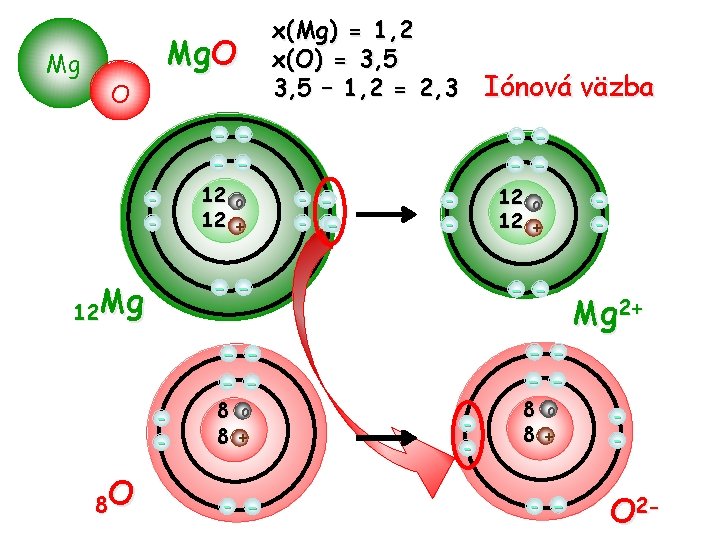
Mg Mg. O O x(Mg) = 1, 2 x(O) = 3, 5 – 1, 2 = 2, 3 Iónová väzba - - --- 12 o 12 + - - - 12 Mg - 8 O 12 o 12 + - - - - - 8 o 8 + - - - Mg 2+ - O 2 -
Vypracovala: Ing. Lucia Dovalová ZŠ s MŠ Badín Upravila: Mgr. Jana Sabolová
- Slides: 13