CHEMICK REAKCE Mgr Petra Vojtkov Mgr Irena Pluckov








- Slides: 17

CHEMICKÉ REAKCE © Mgr. Petra Vojtěšková, Mgr. Irena Plucková, Ph. D.

CHEMICKÁ REAKCE �Je děj, při kterém z výchozích chemických látek (reaktantů) vznikají jiné chemické látky (produkty).

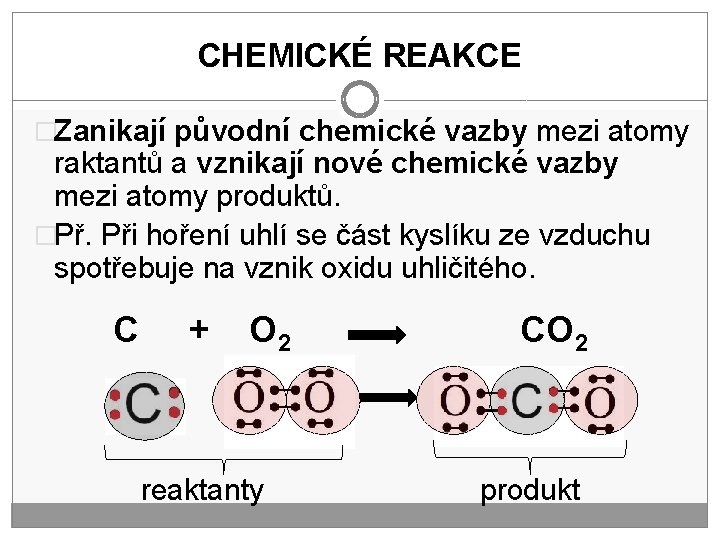
CHEMICKÉ REAKCE �Zanikají původní chemické vazby mezi atomy raktantů a vznikají nové chemické vazby mezi atomy produktů. �Př. Při hoření uhlí se část kyslíku ze vzduchu spotřebuje na vznik oxidu uhličitého. C + O 2 reaktanty CO 2 produkt

CHEMICKÉ REAKCE � � Hoření je děj, při kterém se uvolňuje světelná a tepelná energie. �Reakce tedy můžeme rozdělit na: 1) exotermické – reakce, při které se teplo uvolňuje (např. hoření) 2) endotermické – reakce, při které se teplo spotřebovává (např. tepelnýrozklad vápence)

CHEMICKÉ REAKCE Průběh chemických reakcí ovlivňují reakční podmínky: teplota tlak katalyzátor

ZÁKON ZACHOVÁNÍ HMOTNOSTI Objeven v 18. století ruským přírodovědcem M. V. Lomonosovem a francouzským vědcem A. L. Lavoisierem. �Při chemických reakcích vznikají z výchozích látek látky jiné. �Pro hmotnost chemických látek před reakcí a po ní platí zákon zachování hmotnosti.

ZÁKON ZACHOVÁNÍ HMOTNOSTI Hmotnost chemických látek před reakcí je stejná jako hmotnost chemických látek po reakci. Platí v uzavřené soustavě.

CHEMICKÁ ROVNICE �Používá se pro zápis chemické reakce. �Je vyjádřená značkami a vzorci chemických látek. �Rovnice jsou zapisovány ustáleným zápisem: reaktanty uhlík + kyslík C + O 2 produkty oxid uhličitý CO 2

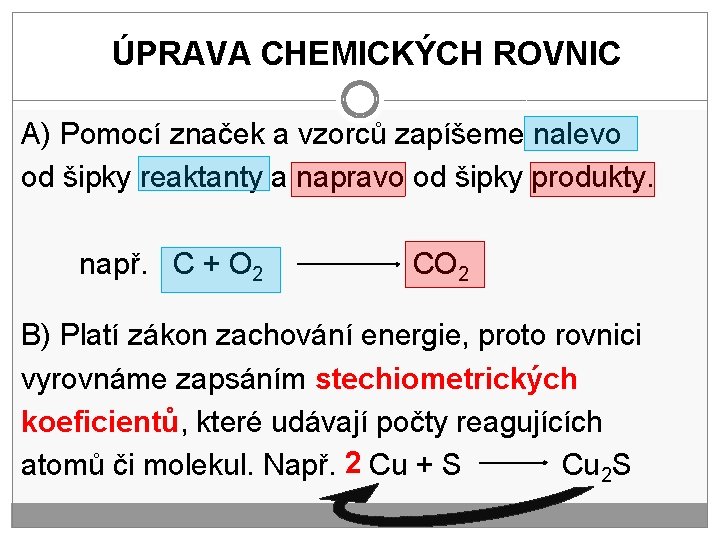
ÚPRAVA CHEMICKÝCH ROVNIC A) Pomocí značek a vzorců zapíšeme nalevo od šipky reaktanty a napravo od šipky produkty. např. C + O 2 CO 2 B) Platí zákon zachování energie, proto rovnici vyrovnáme zapsáním stechiometrických koeficientů, které udávají počty reagujících atomů či molekul. Např. 2 Cu + S Cu 2 S

ÚPRAVA CHEMICKÝCH ROVNIC �Příklad: Zapište chemickou rovnicí rozklad vody, jejímiž produkty jsou vodík a kyslík, které tvoří dvouatomové molekuly. � 1) Zapíšeme reaktanty a produkty. H 2 O H 2 + O 2

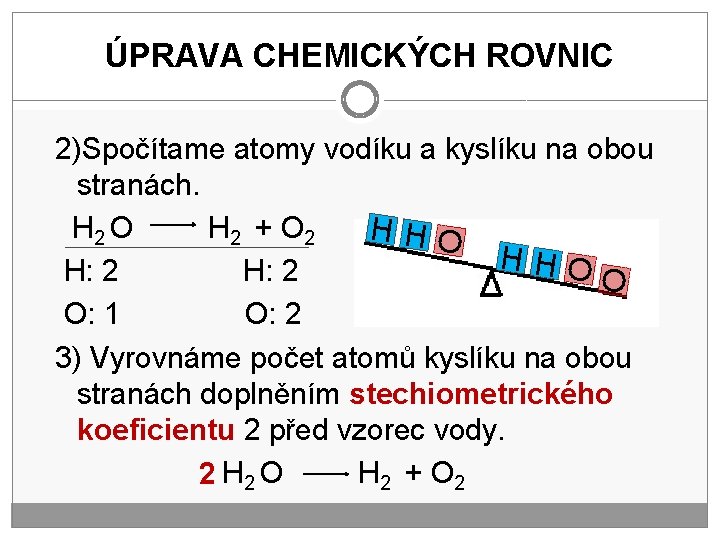
ÚPRAVA CHEMICKÝCH ROVNIC 2)Spočítame atomy vodíku a kyslíku na obou stranách. H 2 O H 2 + O 2 HHO H: 2 O O: 1 O: 2 3) Vyrovnáme počet atomů kyslíku na obou stranách doplněním stechiometrického koeficientu 2 před vzorec vody. H 2 + O 2 2 H 2 O

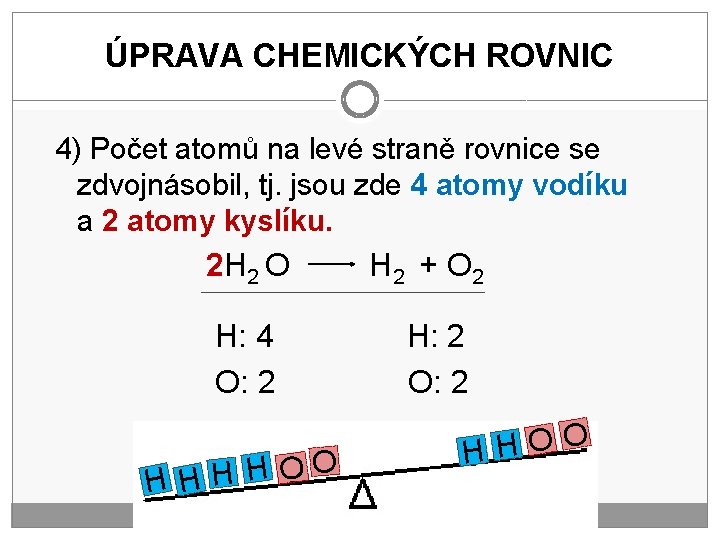
ÚPRAVA CHEMICKÝCH ROVNIC 4) Počet atomů na levé straně rovnice se zdvojnásobil, tj. jsou zde 4 atomy vodíku a 2 atomy kyslíku. 2 H 2 O H: 4 O: 2 O H HH H 2 + O 2 H: 2 O O H H

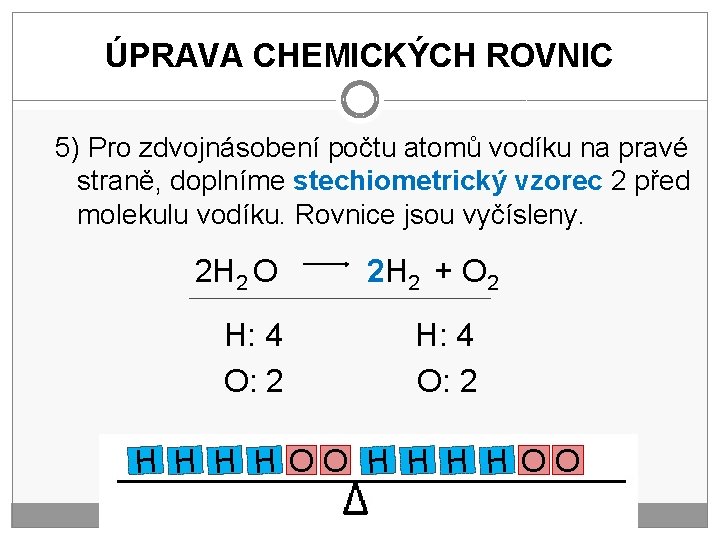
ÚPRAVA CHEMICKÝCH ROVNIC 5) Pro zdvojnásobení počtu atomů vodíku na pravé straně, doplníme stechiometrický vzorec 2 před molekulu vodíku. Rovnice jsou vyčísleny. 2 H 2 O H: 4 O: 2 2 H 2 + O 2 H: 4 O: 2 H H H H OO

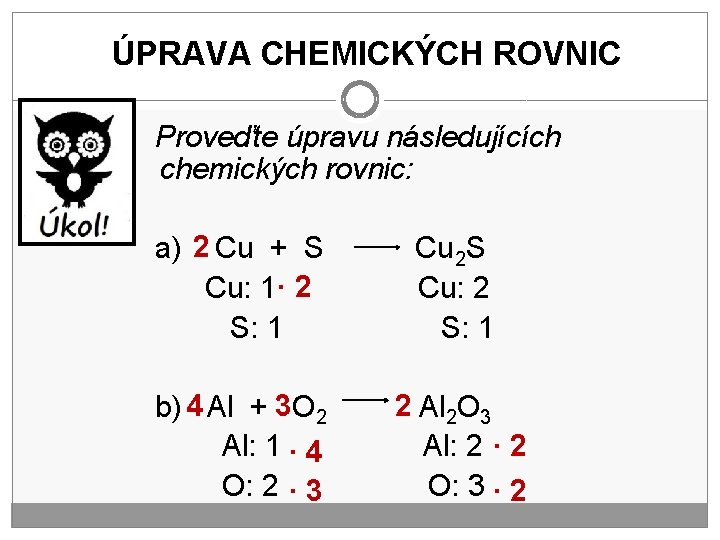
ÚPRAVA CHEMICKÝCH ROVNIC Proveďte úpravu následujících chemických rovnic: a) 2 Cu + S Cu: 1· 2 S: 1 Cu 2 S Cu: 2 S: 1 b) 4 Al + 3 O 2 Al: 1 · 4 O: 2 · 3 2 Al 2 O 3 Al: 2 · 2 O: 3 · 2

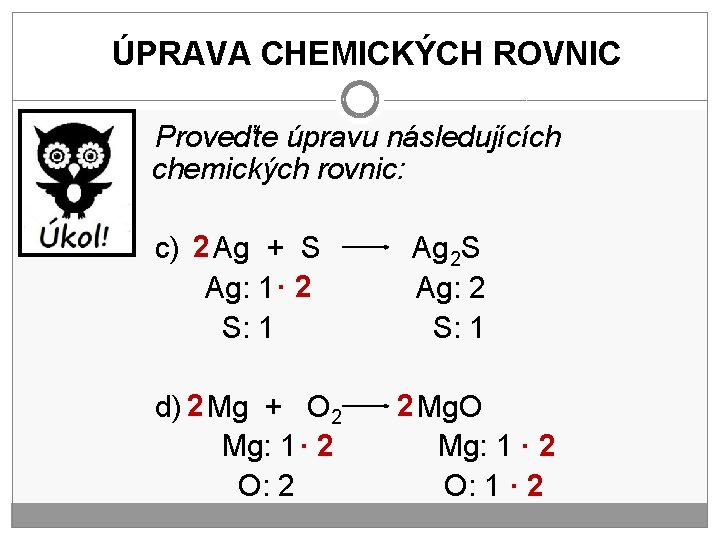
ÚPRAVA CHEMICKÝCH ROVNIC Proveďte úpravu následujících chemických rovnic: c) 2 Ag + S Ag: 1 · 2 S: 1 d) 2 Mg + O 2 Mg: 1 · 2 O: 2 Ag 2 S Ag: 2 S: 1 2 Mg. O Mg: 1 · 2 O: 1 · 2

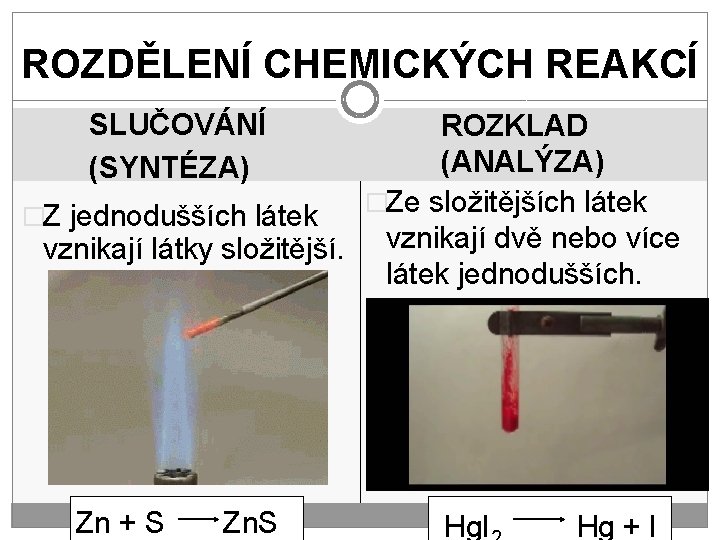
ROZDĚLENÍ CHEMICKÝCH REAKCÍ SLUČOVÁNÍ (SYNTÉZA) ROZKLAD (ANALÝZA) �Ze složitějších látek �Z jednodušších látek vznikají látky složitější. vznikají dvě nebo více látek jednodušších. Zn + S Zn. S Hg. I Hg + I

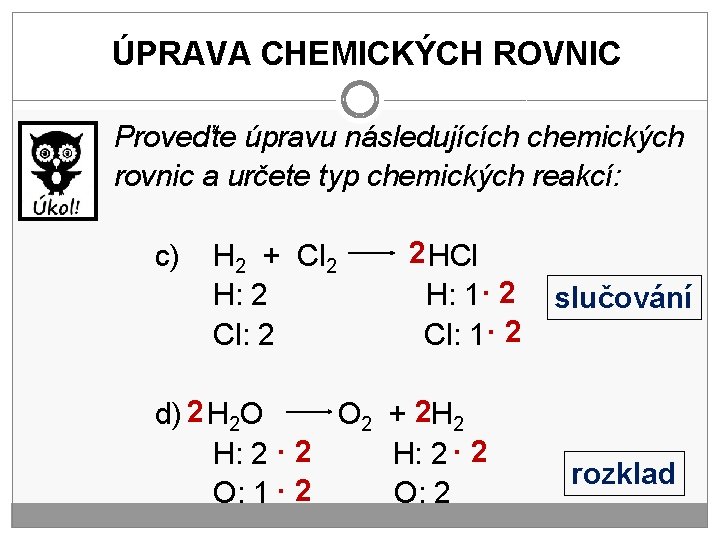
ÚPRAVA CHEMICKÝCH ROVNIC Proveďte úpravu následujících chemických rovnic a určete typ chemických reakcí: c) H 2 + Cl 2 H: 2 Cl: 2 2 HCl H: 1· 2 Cl: 1· 2 d) 2 H 2 O O 2 + 2 H 2 H: 2 · 2 O: 1 · 2 O: 2 slučování rozklad